Administración Nacional de Medicamentos, Alimentos y Tecnología Médica
PRODUCTOS PARA DIAGNOSTICO
Disposición 4043/2005
Acéptase el uso de determinados símbolos en reemplazo del texto de la información requerida en la Disposición Nº 2674/99 para los rótulos de los productos para diagnóstico de uso in vitro. Exclusiones.
Bs. As., 14/7/2005
VISTO el Expediente N° 1-47-1110-4412-04-2 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica; y
CONSIDERANDO:
Que los requisitos para la autorización de productos para diagnóstico de uso in vitro, en la República Argentina se encuentran establecidos en la Disposición ANMAT 2674/99.
Que los miembros de la Unión Europea han realizado esfuerzos para armonizar sus legislaciones nacionales relacionadas con estos productos a través de la Directiva de la Unión Europea sobre productos para diagnóstico de uso in vitro confirmada como Directriz 98/79/ EC (IVD Directive).
Que de la evaluación de dicha reglamentación así como de la establecida por la Food and Drug Administration de los Estados Unidos de Norteamérica se ha constatado que la información requerida en las mismas para el rotulado e instrucciones de uso de productos para diagnóstico de uso in vitro resultan substancialmente equivalentes a la requerida por esta Administración.
Que no obstante, ello la Directriz 98/79/EC al autorizar específicamente a cada Estado miembro de la Unión Europea a requerir que dicha información se encuentre en su idioma nacional, ha promovido la utilización de símbolos establecidos en dos Normas Internacionales armonizadas como alternativa a la utilización de texto que debería estar expresado de lo contrario en múltiples idiomas.
Que habiéndose evaluado las dos Normas armonizados a nivel Internacional: ISO 15.223 y EN 980 relativas a la utilización de símbolos específicos aplicables al rotulado de productos para diagnóstico de uso in vitro, se ha concluido que las mismas satisfacen los requerimientos de rotulado exigidos en la Disposición (ANMAT) N° 2674/99.
Que a los efectos de facilitar la importación y exportación de productos para diagnóstico de uso in vitro se hace necesario aceptar el uso de estos símbolos en lugar de texto para cierta información contenida en el rotulado de los productos en cuestión.
Que el Instituto Nacional de Medicamentos y la Dirección de Asuntos Jurídicos han tomado la intervención de su competencia
Que se actúa en virtud de las facultades conferidas por el Decreto 1490/92 y la Resolución M.S. y A.S. N° 145/99.
Por ello;
EL INTERVENTOR DE LA ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
DISPONE:
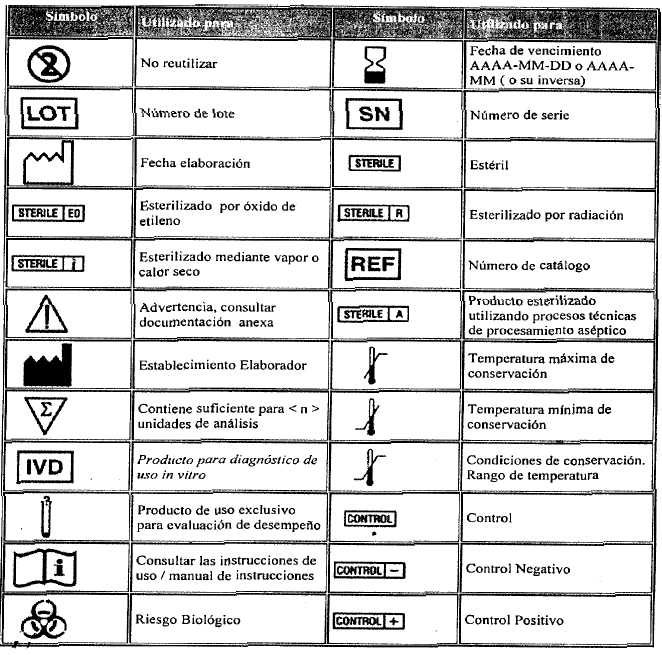
Artículo 1º — Acéptase el uso de los 24 (veinticuatro) símbolos descriptos y definidos en el Anexo de la presente disposición, en reemplazo del texto de la información requerida en la Disposición A.N.M.A.T. N° 2674/99 en los rótulos de los productos para diagnóstico de uso in vitro.
Art. 2º — La utilización de símbolos en remplazo de texto sólo será de aplicación en el rótulo de productos para diagnóstico de uso in vitro de uso profesional exclusivo, quedando totalmente excluidos los clasificados como de "Autoevaluación".
Art. 3º — Cuando sean utilizados símbolos en el rotulado de productos para diagnóstico de uso in vitro en reemplazo de texto, los establecimientos elaboradores y/o importadores deberán acompañar en el manual de instrucciones o en inserto anexo el glosario de términos que definan los símbolos.
Art. 4º — El glosario al que refieren los Artículos 1° y 3° deberá permitir al usuario familiarizarse con el significado de los símbolos, constituyendo una referencia a consultar en caso de no recordar los mismos.
Art. 5º — Los establecimientos elaboradores y/o importadores de productos para diagnóstico de uso in vitro que pretendan modificar los rótulos de sus productos de conformidad con la presente disposición deberán comunicar por nota dichas modificaciones detallando todos los símbolos a utilizar y los productos con dicha modificación. Asimismo, y con carácter de declaración jurada informará que una vez introducido el uso de símbolos en el rotulado de productos incluirá en el manual de instrucciones el glosario requerido en el artículo 3° de la presente Disposición.
Art. 6º — El establecimiento solicitante y su Director Técnico son responsables de la exactitud de las declaraciones presentadas en la comunicación.
Art. 7º — La Autoridad de Aplicación se reserva el derecho de verificar en cualquier momento la veracidad y exactitud de la información inserta en la declaración jurada, pudiendo dejar sin efecto la ejecución de lo solicitado mediante Disposición fundada, todo ello sin perjuicio de las sanciones que pudieran corresponder por aplicación de la normativa vigente.
Art. 8º — Comuníquese a la Cámara Argentina de Reactivos para Diagnóstico (CAPRODI) y demás entidades profesionales.
Art. 9º — Anótese; comuníquese. Publíquese, dése a la Dirección Nacional de Registro Oficial, cumplido, archívese PERMANENTE. — Manuel R. Limeres.
ANEXO - Disposición A.N.M.A.T. Nº: 4043