Servicio Nacional de Sanidad y Calidad Agroalimentaria
SANIDAD ANIMAL
Resolución 520/2010
Modificación de la Resolución Nº 446/10 en relación con los requisitos para la distribución, aplicación y certificación de la vacunación contra Arteritis Viral Equina.
Bs. As., 6/8/2010
VISTO el Expediente Nº S01:0235927/2010 del Registro del MINISTERIO DE AGRICULTURA, GANADERIA Y PESCA, la Ley Nº 3959 de Policía Sanitaria de los Animales, las Resoluciones Nros. 617 del 12 de agosto de 2005 de la ex SECRETARIA DE AGRICULTURA, GANADERIA, PESCA Y ALIMENTOS, 422 del 20 de agosto de 2003, 265 del 6 de mayo de 2010, 342 del 20 de mayo de 2010, 360 del 4 de junio de 2010 y 446 del 8 de julio de 2010, todas del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, la Disposición Nº 2 del 5 de febrero de 2009 de la Dirección Nacional de Sanidad Animal del citado Servicio Nacional, y
CONSIDERANDO:
Que por la Resolución Nº 617 del 12 de agosto de 2005 de la ex SECRETARIA DE AGRICULTURA, GANADERIA, PESCA Y ALIMENTOS, se aprobó el "Programa de Control y Erradicación de las Enfermedades Equinas" y su "Reglamento de Control Sanitario".
Que ante la presencia de focos de Arteritis Viral Equina se declaró el Estado de Alerta Sanitario por la Resolución Nº 265 de fecha 6 de mayo de 2010 del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA.
Que no obstante ello, la evaluación epidemiológica sobre la difusión, distribución y evolución de la enfermedad, evidencian resultados satisfactorios respecto a la superación del brote.
Que resulta necesario establecer medidas tendientes a mitigar los riesgos de reintroducción y difusión del agente infeccioso de Arteritis Viral Equina en la población equina.
Que el único laboratorio comercial elaborador de vacuna contra la Arteritis Viral Equina en sus DOS (2) presentaciones inactivada y atenuada, declara no tener existencias de la primera hasta fines del presente año.
Que por la Resolución Nº 446 del 8 de julio de 2010 del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, se autorizó con carácter de excepción la importación y uso de QUINIENTAS (500) dosis de vacuna atenuada contra la Arteritis Viral Equina, ARVAC elaborada por la firma FORT DODGE e importada y comercializada por LABORATORIOS PFIZER S.R.L.
Que en el Anexo de la citada Resolución SENASA Nº 446/2010, se limitan los alcances del procedimiento aprobado por dicha norma, a los equinos propiedad de los socios de la Asociación Criadores de Sangre Pura de Carrera.
Que la Asociación Argentina de Fomento Equino, Asociación Argentina de Criadores de Caballos Arabes y Asociación Argentina de Criadores de Caballos de Polo, constituyeron formalmente una solicitud expresa, para autorizar la práctica de la vacunación contra arteritis viral equina, en los equinos que son propiedad de sus asociados, argumentando la necesidad de proteger a sus padrillos de alto valor económico, genético y/o deportivo, como medida de prevención con motivo del inicio de la actividad de reproducción.
Que tales solicitudes de las asociaciones precitadas, a juicio de la Dirección Nacional de Sanidad Animal, constituyen una circunstancia de carácter especial y homologable al escenario presentado para con la Asociación Criadores de Sangre Pura de Carrera para la cual rige la mencionada Resolución SENASA Nº 446/2010, en torno a la aplicación de medidas de prevención inmunológicas contra la Arteritis Viral Equina.
Que en virtud de lo expuesto, resulta necesario ampliar los requisitos establecidos por dicha norma a los propietarios de equinos de las distintas razas.
Que dada la falta de vacuna inactivada en el mercado internacional y la necesidad de salvaguardar el patrimonio de alto valor genético y comercial de los padrillos registrados en la Asociación Argentina de Fomento Equino, en la Asociación Argentina de Criadores de Caballos Arabes y en la Asociación Argentina de Criadores de Caballos de Polo, resulta necesario adoptar medidas excepcionales de prevención como, autorizar la importación y el uso de vacuna atenuada, previo al momento del inicio de la temporada de servicio de la población equina de las citadas razas.
Que la Dirección de Asuntos Jurídicos ha tomado la intervención que le compete.
Que el suscripto es competente para dictar la presente medida en virtud de las atribuciones conferidas por el Artículo 5º del Decreto Nº 583 del 31 de enero de 1967, modificado por sus similares Nros. 3899 del 2 de junio de 1972 y 35 del 11 de enero de 1988 reglamentario de la Ley Nº 13.636 y por los Artículos 8º, incisos h) y k) y 9º, inciso a) del Decreto Nº 1585 del 19 diciembre de 1996, sustituido por su similar Nº 825 del 10 de junio de 2010.
Por ello,
EL VICEPRESIDENTE DEL SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
RESUELVE:
Artículo 1º — Se sustituyen los requisitos para la distribución, aplicación y certificación de la vacunación contra Arteritis Viral Equina, establecidos en el Anexo de la Resolución Nº 446 de fecha 8 de julio de 2010 del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, por los previstos Anexos I, II y III que forman parte de la presente resolución, a fin de ser ampliado a los propietarios de equinos de las distintas razas.
Art. 2º — La presente resolución entrará en vigencia a partir de la fecha de su firma.
Art. 3º — Comuníquese, publíquese, dése a la Dirección Nacional del Registro Oficial y archívese. — Carlos A. Paz.
ANEXO I
Solicitud de vacunación contra Arteritis Viral Equina
En mi carácter de Propietario o Tenedor Responsable de los padrillos que a continuación se detallan, solicito dar curso, ante el SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, al presente documento para la vacuna contra Arteritis Viral Equina (AVE) con la vacunación a virus vivo modificada ARVAC.
Datos del Establecimiento:
|
Nombre del Establecimiento |
|
|
Nº de RENSPA |
|
|
Partido o Departamento |
Veterinario a cargo del Establecimiento:
|
Nombre de Veterinario Acreditado |
|
|
Nº de Acreditación |
Listado de padrillos a Vacunar:
|
Nombre de los Padrillos |
Raza |
|
|
1 |
||
|
2 |
||
|
3 |
||
|
4 |
||
|
5 |
||
|
6 |
||
|
7 |
||
|
8 |
||
Nota: en caso de solicitar vacunar más de OCHO (8) padrillos, completar otra solicitud.
Declaro bajo juramento conocer y aceptar las condiciones establecidas por el SENASA y me comprometo a cumplirlas asumiendo la responsabilidad por el uso de la vacuna.
Asimismo, me comprometo:
1) Al aislamiento por un período mínimo de TRES (3) semanas del padrillo vacunado, el cual debe permanecer a una distancia no menor a los CINCUENTA (50) metros de otros animales susceptibles a la AVE.
2) A la remisión al SENASA en forma fehaciente de toda la información pertinente al caso, haciéndome responsable por las consecuencias que pudieran derivar del incumplimiento de las obligaciones a mi cargo.
Propietario o Tenedor Responsable:
Apellido y Nombre: ……………………………………………………..
D.N.I. Nº: ………………………………………………………………..
Firma: ……………………………………………………………………
ANEXO II
PROCEDIMIENTO PARA IMPLEMENTAR LA VACUNACION
CONTRA ARTERITIS VIRAL EQUINA
Por intermedio del Veterinario Acreditado que figura en la solicitud de vacunación el Propietario o Tenedor Responsable se compromete a cumplimentar el siguiente procedimiento:
Documentación a presentar en Lazareto Cuarentenario Capital
• El Veterinario Acreditado que figura en la "Solicitud de Vacunación contra Arteritis Viral Equina", o quien él designe mediante una autorización por escrito, será el encargado de presentar la siguiente documentación:
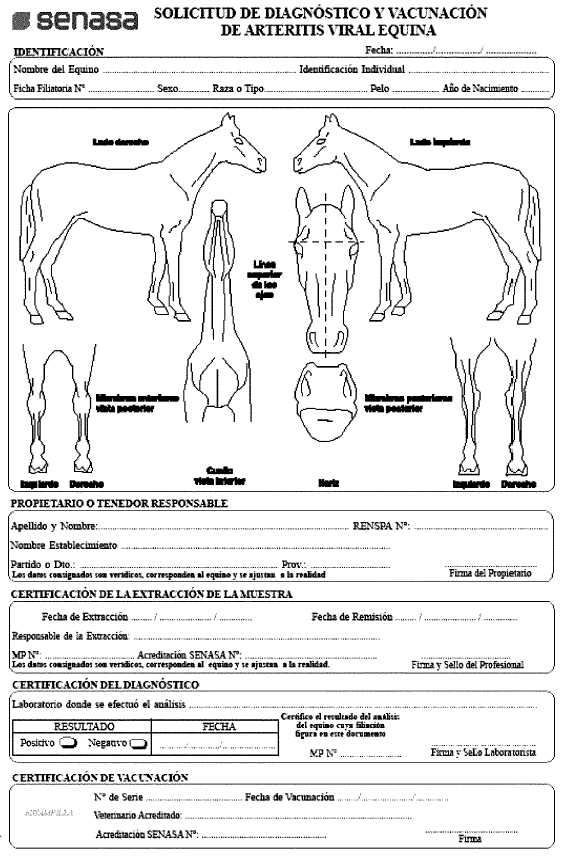
1. El Certificado "Solicitud de Diagnóstico y Vacunación de Arteritis Viral Equina" con el resultado negativo contra AVE y que no tenga una antigüedad mayor a DIEZ (10) días. Dicho certificado se encuentra en la página web del SENASA.
2. La "Solicitud de Vacunación contra AVE" correctamente confeccionada, que se encuentra en la página web del SENASA.
• El Nombre y la Raza del equino que figura en los documentos antes mencionados deben estar escritos claramente en imprenta mayúscula y corresponderse.
• En el Lazareto Cuarentenario Capital, personal del SENASA asignado debe confeccionar un Acta por triplicado por cada "Solicitud de Vacunación contra AVE" presentada.
• Al solicitante se le entregará como una unidad, los siguientes documentos:
1. Solicitud de Diagnóstico y Vacunación de AVE.
2. Solicitud de vacunación contra AVE.
3. Original y duplicado del Acta.
Retiro y conservación de las vacunas
• Para el retiro de las vacunas debe dirigirse a la oficina de Criadores Argentinos de Sangre Pura de Carrera (CASPC) con la documentación recibida en el Lazareto Cuarentenario Capital.
• La persona encargada de retirar las vacunas, presentará la documentación en Criadores Argentinos de Sangre Pura de Carrera (CASPC), donde a contra entrega del duplicado del Acta contenida en la documentación, y previa acreditación de identidad mediante el Documento Nacional de Identidad o Cédula de Identidad, se le entregará las vacunas solicitadas.
• La persona encargada de retirar las vacunas deberá concurrir provista con los materiales necesarios para el transporte y conservación de las mismas, a efecto de asegurar la cadena de frío.
Aplicación de la Vacuna
• El encargado de aplicar la vacuna será el Veterinario Acreditado a cargo del establecimiento que figura en la "Solicitud de Vacunación contra AVE".
Certificación de Vacunación
• El Veterinario Acreditado, deberá certificar la vacunación en la "Solicitud de Diagnóstico y Vacunación de Arteritis Viral Equina".
Aislamiento del padrillo vacunado
• Debido a que luego de aplicada la vacuna a virus vivo modificado ARVAC, el padrillo debe quedar aislado por un período mínimo de TRES (3) semanas, el propietario o tenedor responsable de los padrillos a vacunar debe dejar constancia de dicha situación firmando la "Solicitud para la Vacunación contra AVE", aceptando las condiciones establecidas por el SENASA y su responsabilidad en cuanto al aislamiento del animal vacunado y consecuencias que pudieran derivar de su incumplimiento y del uso de la vacuna.
• Durante el período de aislamiento del padrillo vacunado, no podrá haber animales susceptibles a AVE a una distancia menor a los CINCUENTA (50) metros.
Documentación respaldatoria para registrar la vacunación e identificación del padrillo en SENASA
• Los propietarios o tenedores responsables de los padrillos, deben dirigirse a la Oficina Local del SENASA de la jurisdicción donde se encuentra el padrillo vacunado, a los efectos de registrar la vacunación contra AVE e identificación.
• El registro mencionado en el párrafo anterior debe realizarse antes de la finalización del período de aislamiento posterior a la vacunación [plazo mínimo TRES (3) semanas].
La documentación a presentar en la Oficina Local de SENASA es la siguiente:
• Original y copia de la documentación recibida al momento del retiro de la vacuna (la copia se entrega y queda en poder el SENASA) con las siguientes certificaciones realizadas:
1. Certificación de la aplicación de la vacuna, que debe constar en la "Solicitud de Diagnóstico y Vacunación para AVE".
2. Certificación de la aplicación de un microchip al padrillo vacunado, mediante la oblea con el número impreso pegada en la "Solicitud de Diagnóstico y Vacunación para AVE".
• La Libreta Sanitaria Equina (LSE) del padrillo vacunado correctamente confeccionada incluyendo:
1. La transcripción de los datos de la "Solicitud de Diagnóstico y Vacunación para AVE" a los apartados correspondientes a otras pruebas de laboratorio y otras vacunaciones preventivas.
2. La certificación de la aplicación de un microchip al padrillo vacunado, mediante la oblea con el número impreso pegada en la LSE.
ANEXO III