Ministerio
de Salud
SALUD PUBLICA
Resolución 1472/2011
Apruébase el “Proyecto Demostración
para la incorporación de la Prueba de HPV como Tamizaje Primario”.
Bs. As., 12/9/2011
VISTO el expediente Nº 2002-22108-10-9 del registro del MINISTERIO DE
SALUD, y
CONSIDERANDO:
Que en el marco del PROGRAMA NACIONAL DE PREVENCION DE CANCER
CERVICO-UTERINO, este Ministerio, oportunamente, suscribió con la
PROVINCIA DE JUJUY, un Acta Acuerdo para el fortalecimiento del
PROGRAMA PROVINCIAL DE PREVENCION DE CANCER CERVICO-UTERINO en dicha
jurisdicción considerada prioritaria.
Que en tal acuerdo, las partes previeron como uno de los objetivos
específicos, para desarrollar conjuntamente, lograr la alta calidad de
los servicios diagnósticos (toma y lectura de la citología).
Que el cáncer cérvico-uterino es la segunda causa de muerte por cáncer
en mujeres entre TREINTA Y CINCO Y SESENTA Y CUATRO (35 y 64) años.
Que en la Argentina se diagnostican alrededor de TRES MIL (3000) casos
nuevos por año de cáncer cérvico-uterino, muriendo DOS MIL (2000)
mujeres por año por esta enfermedad.
Que existen limitaciones para reducir la incidencia y mortalidad por
cáncer cérvico-uterino, inherentes al tamizaje basado en la citología
convencional (Prueba de Papanicolaou —Pap—).
Que estas limitaciones están generalmente asociadas a la baja cobertura
de mujeres tamizadas, el bajo porcentaje de adhesión al seguimiento y
tratamiento de lesiones, y a las dificultades operativas derivadas de
la sensibilidad moderada de la prueba del Pap para la detección de
lesiones de alto grado, que es de entre el CINCUENTA y SESENTA POR
CIENTO (50% y 60%), y de su limitado valor predictivo negativo.
Que en Latinoamérica se están desarrollando con éxito experiencias de
incorporación de nuevas tecnologías para el tamizaje, como la prueba de
HPV-CH2.
Que a diferencia de la prueba del Pap, la prueba de HPV-CH2 tiene una
sensibilidad mayor al NOVENTA Y CINCO POR CIENTO (95%) para la
detección de lesiones de alto grado y un alto valor predictivo negativo.
Que la recomendación científica y de los organismos internacionales de
salud pública, es la implementación de proyectos de demostración para
cambiar los programas al nuevo paradigma de la prevención del cáncer
cérvico-uterino basado en la prueba de HPV como tamizaje primario.
Que desde el MINISTERIO DE SALUD, resulta ineludible coordinar con las
jurisdicciones provinciales, las acciones conducentes a la obtención de
estrategias que optimicen la prevención del cáncer cérvico-uterino en
el marco de programas organizados.
Que uno de los objetivos específicos del INSTITUTO NACIONAL DEL CANCER,
es la implementación de estrategias de detección temprana promoviendo
la inclusión de programas de prevención y control de dicha enfermedad
en las diferentes jurisdicciones, con el objeto principal de disminuir
la incidencia y mortalidad por cáncer.
Que la PROVINCIA DE JUJUY es una de las provincias con mayores tasas de
mortalidad por cáncer cérvico-uterino.
Que la DIRECCION DE PROGRAMACION Y CONTROL PRESUPUESTARIO de la
DIRECCION GENERAL DE ADMINISTRACION de la SECRETARIA DE COORDINACION de
este Ministerio ha tomado la intervención que le compete.
Que la SUBSECRETARIA DE SALUD COMUNITARIA y la SECRETARIA DE PROMOCION
Y PROGRAMAS SANITARIOS han tomado la intervención de su competencia y
propician la aprobación del “PROYECTO PARA LA INCORPORACION DE LA
PRUEBA DE HPV-CH2 COMO TAMIZAJE PRIMARIO”.
Que la DIRECCION GENERAL DE ASUNTOS JURIDICOS ha tomado la intervención
de su competencia.
Que la presente medida se dicta en ejercicio de las facultades
conferidas por la Ley de Ministerios - T.O. 1992, modificada por su
similar Ley 26.338, y por el Artículo 2º del “Reglamento de
Procedimientos Administrativos, Decreto 1759/72 t.o. 1991”.
Por ello,
EL MINISTRO DE SALUD
RESUELVE:
Artículo 1º — Apuébase el
“PROYECTO DEMOSTRACION PARA LA INCORPORACION DE LA PRUEBA DE HPV COMO
TAMIZAJE PRIMARIO”, que como ANEXO I forma parte integrante de la
presente medida, en el ámbito de la SUSBSECRETARIA DE SALUD COMUNITARIA
de la SECRETARIA DE PROMOCION Y PROGRAMAS SANITARIOS del MINISTERIO DE
SALUD, a fin de coordinar las acciones para desarrollar una estrategia
de prevención basada en la prueba de HPV como método primario de
tamizaje.
Art. 2º — Apruébase el texto
del convenio a suscribirse entre este Ministerio y la PROVINCIA DE
JUJUY, para la puesta en marcha del Proyecto que se aprueba por el
Artículo 1º, que como ANEXO II forma parte integrante de la presente
resolución.
Art. 3º — El “PROYECTO
DEMOSTRACION PARA LA INCORPORACION DE LA PRUEBA HPV COMO TAMIZAJE
PRIMARIO”, se ejecutará en forma articulada con el INSTITUTO NACIONAL
DEL CANCER, organismo dependiente del MINISTERIO DE SALUD, referente
nacional rector de las acciones en materia de cáncer, el que tendrá a
su cargo la coordinación de las acciones que demande el cumplimiento de
los objetivos del referido Proyecto.
Art. 4º — El INSTITUTO NACIONAL
DEL CANCER, en el ámbito de su competencia, deberá articular con la
SUBSECRETARIA DE SALUD COMUNITARIA de la SECRETARIA DE PROMOCION Y
PROGRAMAS SANITARIOS del MINISTERIO DE SALUD, las acciones que resulten
necesarias a fin de contribuir al cumplimiento de los objetivos
propuestos.
Art. 5º — El “PROYECTO
DEMOSTRACION PARA LA INCORPORACION DE LA PRUEBA DE HPV COMO TAMIZAJE
PRIMARIO”, estará a cargo de UN (1) Director de Proyecto, que dependerá
directamente de la SUBSECRETARIA DE SALUD COMUNITARIA de la SECRETARIA
DE PROMOCION Y PROGRAMAS SANITARIOS de este Ministerio.
Art. 6º — Autorízase a la
SUBSECRETARIA DE SALUD COMUNITARIA de la SECRETARIA DE PROMOCION Y
PROGRAMAS SANITARIOS de este Ministerio, a suscribir los convenios,
documentos e instrumentos que resulten necesarios para la adecuada
ejecución e implementación del Proyecto que se aprueba por el Artículo
1º de la presente Resolución.
Art. 7º — Delégase en la
SUBSECRETARIA DE SALUD COMUNITARIA de la SECRETARIA DE PROMOCION Y
PROGRAMAS SANITARIOS de este Ministerio, la facultad de autorizar las
transferencias de fondos a que hubiere lugar, imprescindibles para el
correcto cumplimiento del “PROYECTO DEMOSTRACION PARA LA INCORPORACION
DE LA PRUEBA DE HPV COMO TAMIZAJE PRIMARIO”, así como, la atribución de
aprobar las rendiciones de cuentas del gasto de las transferencias que
se efectúen.
Art. 8º — Facúltase a la
SECRETARIA DE PROMOCION Y PROGRAMAS SANITARIOS de este Ministerio a
dictar las normas complementarias, interpretativas y aclaratorias de la
presente Resolución.
Art. 9º — El gasto que demande
la ejecución efectiva del “PROYECTO PARA LA INCORPORACION DE LA PRUEBA
DE HPV-CH2 COMO TAMIZAJE PRIMARIO”, será atendido con cargo a los
créditos presupuestarios de la SUSBSECRETARIA DE SALUD COMUNITARIA de
la Secretaría de Estado mencionada de este Ministerio.
Art. 10. — Regístrese,
comuníquese, publíquese, dése a la Dirección Nacional del Registro
Oficial a sus efectos y archívese. — Juan L. Manzur.
ANEXO I
“Proyecto para la incorporación del la
prueba de HPV-HC21 como tamizaje primario”
Presentado por la Coordinación de Detección Temprana del Instituto
Nacional Del Cáncer y el Programa Nacional de Prevención de Cáncer
Cérvico-uterino
Año 2011
FUNDAMENTACION
El cáncer cérvico-uterino es la segunda causa de muerte por cáncer en
mujeres entre 35 y 64 años. En la Argentina se diagnostican alrededor
de 3000 casos nuevos por año, y mueren 2000 mujeres por esta enfermedad.
Se ha comprobado que la causa necesaria del cáncer cérvico-uterino es
la infección por el Virus Papiloma Humano (HPV), cuya principal vía de
transmisión es la vía sexual (Bosch FX., 2002). Existe una asociación
de más del 99% entre el HPV y el cáncer de cuello de útero
(Castellsagué X., 2006). Se han encontrado más de 100 tipos de HPV, de
los cuales alrededor de 15 son considerados de alto riesgo oncogénico
(los más comunes son el 16 y el 18, responsables de aproximadamente el
70% de los casos de cáncer cérvico-uterino, seguidos por el 31 y el 45).
A diferencia de los países desarrollados, los países latinoamericanos
que han implementado programas organizados de prevención basados en la
citología convencional se han encontrado con limitaciones para alcanzar
el impacto deseado en la reducción de la incidencia y mortalidad. Las
principales limitaciones se asocian con:
- la baja cobertura de mujeres tamizadas,
- el bajo porcentaje de mujeres con Pap anormal que son efectivamente
seguidas y tratadas,
- la sensibilidad de la prueba que es entre moderada y baja, lo que
obliga a repeticiones frecuentes del tamizaje para reducir el
porcentaje de falsos positivos, y
- las numerosas instancias que pueden afectar la calidad de la lectura
(toma, transporte, coloración, calidad de la muestra, etc.).
La sensibilidad de la prueba del Pap se estima entre el 50 y 60%. Esto
resulta de la multiplicidad de instancias que deben asegurarse para la
adecuada toma y lectura de la muestra. De hecho, el Pap es una prueba
altamente operador-dependiente, sujeta a interpretaciones subjetivas,
tanto en lo que refiere a quien toma la muestra como a quien la procesa.
En la siguiente tabla se resumen las ventajas de la prueba de HPV-HC2
en relación con la citología:
Tabla I: Cuadro comparativo. Características principales de la prueba
de HPV-HC2 y la citología como métodos de tamizaje.
|
Citología |
Prueba
de HPV-HC2 |
| Sensibilidad
de la técnica |
Entre
moderada y baja (40%-50%): requiere repetir la prueba durante varios
años para compensar la baja sensibilidad (1-1-3). |
Alta
(mayor al 90%) para lesiones de alto grado. |
| Valor
predictivo negativo |
Bajo. |
Alto.
Esto permite espaciar el intervalo de tamizaje a 3 ó 5 años para las
mujeres negativas para HPV. |
| Toma
de la muestra |
Altamente
operador-dependiente. |
Menos
dependiente de la pericia del tomador de la muestra. |
| Traslado
de la muestras |
Alto
riesgo de disecación y contaminación debido a la falta de cuidado en
los traslados. |
Colector
estandarizado. Alta calidad de preservación. |
| Procesamiento
de las muestras |
Altamente
dependiente del operador. Requiere personal especializado para la
lectura de una gran cantidad de Paps de los cuales sólo una minoría son
positivos (5%). |
Procesamiento
automático. Analiza automáticamente 88 muestras a la vez. |
Para
compensar estas deficiencias y asegurar la calidad de la citología, es
necesaria la repetición de la prueba y la implementación de estrictos
controles
de calidad. Por ello, a pesar de los costos reducidos de los insumos,
la
citología no es necesariamente la opción más costo-efectiva para el
tamizaje,
en la medida que aumentan los costos y el número de veces que las
mujeres deben
concurrir a la consulta, con el riesgo de abandono que eso implica.
Estas
dificultades en la implementación de programas de tamizaje basados en
la
citología en los países latinoamericanos, plantea la necesidad de un
cambio de
paradigma que incorpore los nuevos avances tecnológicos para la
prevención del
cáncer cérvico-uterino.
Tamizaje
basado en la prueba de Virus del Papiloma Humano (Prueba de HPV)
A
partir de la década del 90, se comenzó a desarrollar un método que
permite
detectar la presencia de ADN de HPV de alto riesgo oncogénico en las
células
del cuello del útero. Actualmente, existen en el mercado, aprobados por
la FDA
(Food And Drug
Administration), tres pruebas para la detección de ADN de HPV en
contextos de
tamizaje poblacional. Sin embargo, la única prueba utilizada en los
países de
Latinoamérica que ya han iniciado experiencias de incorporación del la
prueba
de HPV como tamizaje primario es la prueba de HPV por captura de
híbridos
(HPV-HC2).
1) El
test de HPV basado en la captura de híbridos es el único en el mundo
para el
cuál su efectividad para reducir la incidencia y mortalidad por cáncer
de
cuello de útero ha sido demostrada científicamente. En efecto, el único
estudio
publicado hasta el momento que se propuso medir el impacto de tres
diferentes
métodos de tamizaje en la reducción de la incidencia y mortalidad por
cáncer
cérvico-uterino fue realizado en India (Sankaranarayanan et al., 2009).
En
dicho estudio se concluyó que las tasas de incidencia y mortalidad
fueron
significativamente mayores para los grupos que fueron tamizados con
citología o
Inspección Visual con ácido acético (VIA) que en el caso del grupo al
que se le
aplicó la prueba de HPV-HC2. El tamizaje mediante la prueba de HPV-HC2
contribuyó a alcanzar una reducción de casi el 50% en la tasa de
mortalidad.
2)
Existe amplia evidencia científica sobre la alta eficacia de la prueba
de
HPV-HC2 como método primario para la detección de lesiones de alto
grado y
cáncer (Tabla 1). No existe el mismo nivel de evidencia sobre la
eficacia de
las otras pruebas aprobadas por la FDA.
En la
tabla 1 se presenta un listado de estudios que comparan la sensibilidad
de la
prueba de HPV-HC2 con la de la citología.
Tabla
I: Sensibilidad relativa de la prueba de HPV-HC2 comparada con la
citología en
diferentes estudios. Años 1999 a 2004.
|
Citología
(LSIL+)% |
HPV
+% |
| Clavel
et al. (1999) |
85
(CIN2+) |
100 |
| Cuzick
et al. (1999a) |
79
(CIN2+) |
95 |
| Schiffman
et al. (2000) |
78
(CIN2+) |
88 |
| Ratnam
et al. (2000) |
40
(CIN2+) |
90 |
| Denny
et al. (2000a) |
78
(CIN2+) |
73 |
| Denny
et al. (2000b) |
82
(CIN2+) |
72 |
| Schneider
et al. (2000) |
20
(CIN2+) |
89 |
| Womack
et al. (2000) |
44
(CIN2+) |
81 |
| Clavel
et al. (2001) |
68
(CIN2+) |
100 |
| Petry
et al. (2003) |
37
(CIN2+) |
98 |
| Kulasingam
et al. (2002) |
36
(CIN2+) |
63 |
| Cuzick
et al. (2003) |
70
(CIN2+) |
97 |
| Sankaranarayanan
et al. (2004b) |
37-72
(CIN2+) |
46-81 |
| Salmeron
et al. (2003) |
59
(CIN2+) |
93 |
| Nieminen
et al. (2004) |
83
(CIN2+) |
98 |
LSIL= lesión escamosa intraepitelial de
bajo grado *Fuente: IARC Handbook 2005:187
CIN= neoplasia cervical intraepitelial
A su
vez, un meta-análisis publicado en 2008 (Cuzick 2008) presenta una
revisión de
31 estudios llevados a cabo entre los años 1995 y 2007 en diferentes
países del
mundo, que han evaluado la sensibilidad de la prueba de HPV-HC2
utilizado como
método de tamizaje primario. En promedio, la sensibilidad de la prueba
de
HPV-HC2 fue del 89.7%. A continuación se presenta el listado de
investigaciones
revisadas entre los años 2005 y 2007:
-
Agorasros T et al., 2005
-
Bigras G et al., 2005
-
Kotaniemi-Talonen L et al., 2005
-
Sankaranarayanan R et al., 2005
-
Sarian LO et al., 2005 - Ronco G et al., 2006
-
Ronco G et al., 2006
-
Almonte M et al., 2007
-
Bulkmans NW et al., 2007
- Naucler P et al., 2007
-
Mayrand MH et al., 2007
*Fuente:
Cuzick, et al., 2008.
Existen
también estudios en Latinoamérica que dan cuenta de esta ventaja de la
prueba
de HPV-HC2. Un estudio publicado en 2008 (Herrero et al., 2008) analiza
diversos estudios de investigación sobre nuevas tecnologías aplicadas
al
tamizaje para la prevención del cáncer cérvico-uterino. La siguiente
tabla
resume algunos de esos proyectos, destacando la sensibilidad obtenida
para la
prueba HPV-HC2 en cada caso.
Tabla
II: Proyectos de Investigación en Latinoamérica sobre evaluación de la
inclusión de nuevas tecnologías al tamizaje del cáncer cérvico-uterino.
| Proyecto |
Autor
y año de publicación |
País |
Cantidad
de población incluida en la muestra |
Sensibilidad
de la prueba de HPV |
| Proyecto
Guanacaste |
Shifman
et al., 2000 |
Costa
Rica |
8500 |
88.4
(Cin3+) |
| Proyecto
TATI |
Almonte
et al., 2007 |
Perú |
5435 |
89.4
(Cin3+) |
| IMSS |
Salmeron
et al., 2003 |
México
(Morelos) |
7868 |
93.1
(Cin 2+) |
| IMSS |
Lascano-Ponce
et al., 2010 |
México |
51168 |
93.3 |
| CIN=
neoplasia cervical intraepitelial |
*Fuente:
Herrero et al., 2008 |
Programas de
tamizaje basados en la prueba de HPV como tamizaje primario: el
contexto latinoamericano
Tomando en cuenta
esta evidencia sobre la aplicación de nuevas tecnologías en los
programas de tamizaje de cáncer cérvico-uterino, la OPS elaboró en 2008
una Estrategia Regional y Plan de Acción para la Prevención y Control
del cáncer cérvico-uterino, que fue aprobada por los Ministros de Salud
de América Latina durante el Consejo Directivo de la OPS de ese año.
Como parte de esta estrategia, en junio de 2010 se llevó a cabo en
Panamá el encuentro “Nuevas Tecnologías para la prevención del cáncer
cérvico-uterino: de la evidencia científica a la planificación de
programas”. Las principales conclusiones del encuentro apuntan a que la
implementación de estas nuevas tecnologías, respaldadas por evidencia
científica clara y bien establecida, resulta factible. La Región se
encuentra en un punto de inflexión en el que se reúnen las condiciones
oportunas para lograr la incorporación de cambios en los programas que
permitan lograr un impacto mayor en la reducción de las tasas de
incidencia y mortalidad por esta enfermedad.
LA RECOMENDACION
CIENTIFICA Y DE SALUD PUBLICA INTERNACIONAL ES LA IMPLEMENTACION DE
PROYECTOS DE DEMOSTRACION PARA CAMBIAR LOS PROGRAMAS AL NUEVO PARADIGMA
DE LA PREVENCION DEL CANCER CERVICO-UTERINO BASADO EN LA PRUEBA DE
HPV-HC2 COMO TAMIZAJE PRIMARIO.
En algunos países
latinoamericanos ya se han desarrollado experiencias de incorporación
de la prueba de HPV-HC2 como método de tamizaje, buscando superar las
limitaciones propias de la citología y contribuir a alcanzar la meta de
reducción de la mortalidad. Es el caso de México, que desde el año 2007
ha establecido un esquema de tamizaje basado en la prueba de HPV-HC2
como tamizaje primario, seguido del Pap para las mujeres HPV positivas.
PROPUESTA DE
INCORPORACION DE LA PRUEBA DE HPV-CH2 COMO TAMIZAJE PRIMARIO EN LA
PROVINCIA DE JUJUY.
Se propone la
implementación de un proyecto en la Provincia de Jujuy para incorporar
la prueba de HPV-HC2 como tamizaje primario en mujeres entre 30 y 65
años, seguido de citología para aquellas mujeres con prueba de HPV
positiva.
Se ha seleccionado
la Provincia de Jujuy porque es una de las provincias con mayores tasas
de mortalidad por cáncer cérvico-uterino, y tiene una capacidad
organizativa del sistema de salud adecuada para la implementación del
proyecto.
POBLACION OBJETIVO
Mujeres entre 30 y
65 años sin cobertura de salud de la provincia de Jujuy.
OBJETIVO GENERAL
Desarrollar una
estrategia de prevención basada en la prueba de HPV-HC2 como método de
tamizaje primario con el objetivo de reducir la incidencia y mortalidad
por cáncer de cuello uterino en el país.
OBJETIVOS
ESPECIFICOS
a) Implementar un
proyecto de introducción de la prueba de HPV-HC2 en una provincia
seleccionada.
b) Desarrollar,
monitorear y evaluar los distintos componentes que deben articularse en
un programa de prevención de cáncer cérvico-uterino basado en la prueba
de HPV-HC2:
- b1) la estrategia
de comunicación dirigida a la población y a los profesionales de la
salud.
- b2) la estrategia
de capacitación de los equipos de salud.
- b3) las
estrategias de búsqueda activa de mujeres en edad objetivo.
- b4) la capacidad
operativa del laboratorio de citología en el marco de una estrategia de
doble toma (Prueba de HPV/citología): dispositivo de almacenamiento
(espacio, tiempos), recursos humanos, identificación de muestras, carga
de trabajo, etc.
- b5) un sistema de
controles negativos de la prueba de HPV, que incluya la realización del
Pap y colposcopia a una muestra de mujeres con prueba de HPV negativa.
- b6) un sistema de
calidad para el seguimiento y tratamiento de las mujeres.
c) Evaluar en una
muestra de mujeres la eficacia de la prueba de HPV-HC2 para
detectar HSIL y cáncer en una población con alta mortalidad por
cáncer cérvico-uterino.
d) Evaluar la
aceptabilidad y la eficacia de la autotoma de la prueba de HPV-HC2 como
estrategia para asegurar la cobertura del tamizaje.
e) Evaluar un
algoritmo alternativo de seguimiento para las mujeres con prueba de HPV
positiva y citología negativa.
METAS
Alcanzar un 80% de
cobertura del tamizaje por medio de la prueba de HPV-HC2, en mujeres
entre 30 y 65 años sin cobertura de salud.
Asegurar la calidad
de la toma de la prueba de HPV-HC2 y su procesamiento en el laboratorio
de HPV.
Lograr que el 100%
de las mujeres con diagnóstico de HSIL+ accedan al tratamiento
efectivo dentro de los 6 meses después del diagnóstico.
ACTIVIDADES
A. FIRMA DE
CONTRATO CON EMPRESA PRODUCTORA (Qiagen)
1. CONSTITUCION DE
CONSEJO ASESOR
Integrado por:
Programa Nacional de Salud Sexual y Procreación Responsable, Sociedad
Argentina de Citología, Sociedad de Ginecología de Buenos Aires,
Sociedad Argentina del Tracto Genital Inferior y Colposcopía, Instituto
Malbrán, Hospital de Clínicas San Martín, Organización Panamericana de
la Salud, Fondo de Población de las Naciones Unidas, Centro de Estudios
de Estado y Sociedad, Instituto Gino Germani, Consejo Nacional de la
Mujer, Secretaría de Derechos Humanos, y expertos nacionales e
internacionales invitados (Dr. Eduardo Lazcano-Ponce, Dr. Rolando
Herrero, Dra. Lucrecia Illescas).
- Elaboración de
Resolución de creación del Consejo Asesor.
2. FIRMA DE ACTA
ACUERDO CON EL MINISTERIO DE SALUD DE LA PROVINCIA SELECCIONADA
- Reunión de
presentación del proyecto con el Ministro de Salud de la Provincia
seleccionada.
- Reunión de
presentación del proyecto con directores provinciales y jefes de
servicio involucrados en la implementación del proyecto.
- Elaboración de
Acta Acuerdo: definición de compromisos del Ministerio de Salud de la
Nación y del Ministerio de Salud de la Provincia.
- Firma de Acta
Acuerdo.
3.
REORGANIZACION DE LA RED DE LABORATORIOS DE CITOLOGIA DE LA PROVINCIA
-
Reacondicionamiento del laboratorio de citología del Hospital Soria
para el almacenamiento de las muestras citológicas de las mujeres entre
30 y 65 años (en el marco de la estrategia de doble toma —Prueba de
HPV/citología—).
4. INSTALACION DEL
LABORATORIO DE HPV EN EL HOSPITAL DE MAYOR COMPLEJIDAD DE LA PROVINCIA
- Creación de un
espacio físico para su funcionamiento (requerimientos de espacio,
teléfono, refrigeración y equipamiento).
- Montaje del
laboratorio de HPV (instalación de equipos).
- Elaboración de
guías y normas de procedimiento para el laboratorio y su articulación
con el laboratorio de citología del Hospital.
- Designación y
contratación del personal a cargo del laboratorio: Jefe de laboratorio,
técnico de laboratorio, administrativo (a cargo del Ministerio de Salud
Provincial).
- Capacitación del
personal que estará a cargo del laboratorio: provista por Qiagen en
Brasil (incluye vuelo, hotel, comida y transporte).
5. ARMADO DE LA RED
DE REFERENCIA, DEFINICION DE SISTEMAS DE TRANSPORTE DE LAS MUESTRAS
- Diseño de la red
de referencia.
- Definición e
implementación de sistemas de transporte de muestras.
6. DISEÑO DEL
PROTOCOLO DE TOMA, LECTURA, SEGUIMIENTO Y TRATAMIENTO DE MUJERES
TAMIZADAS
- Armado de
protocolo de toma, seguimiento y tratamiento.
- Elaboración de
manuales y guías para los equipos de salud.
7. TOMA DE MUESTRAS.
- Definición de
efectores y personal a cargo de la toma.
- Capacitación de
los efectores a cargo de la toma sobre la toma de la muestra en un
contexto de tamizaje basado en la prueba de HPV-HC2.
8. SISTEMA DE
INFORMACION PARA EL MONITOREO Y EVALUACION
- Contratación del
informático a cargo del SITAM para el diseño del nodo Laboratorio de
HPV.
- Capacitación a
usuarios del SITAM.
9. INVESTIGACION
FORMATIVA PARA INDAGAR CONOCIMIENTOS Y PERCEPCIONES DE LA POBLACION
SOBRE EL HPV (Grupos focales; Entrevistas cualitativas a equipos de
salud)
- Contratación de
investigadores.
- Realización de
investigación cualitativa
- Análisis de
resultados y preparación de informe.
10. ELABORACION DE
MATERIALES EDUCATIVOS PARA LA POBLACION SOBRE EL TAMIZAJE BASADO EN LA
PRUEBA DE HPV (folletos, afiches, spots radiales y televisivos).
- Diseño de
materiales.
- Impresión/grabación.
- Difusión en los medios.
11. ELABORACION DE
UNA ESTRATEGIA DE COMUNICACION EN MEDIOS
12. FORMACION DE
RECURSOS HUMANOS
- Seminario sobre
Epidemiología del HPV y cáncer de cuello de útero, y evidencia
científica sobre estrategias de tamizaje basadas en la prueba de
HPV-HC2:
Destinatarios:
profesionales de la salud de la provincia: APS, servicios de
ginecología, servicios de patología cervical, servicios de anatomía
patológica, oncología.
Duración: 3-4 días.
Fecha: Semana del 16
de mayo 2011.
Financiamiento:
Ministerio de Salud de la Nación/organismos internacionales.
Se ha solicitado
apoyo a la UICC para el financiamiento de los invitados internacionales
(Dr. Eduardo Lazcano-Ponce - México; Dr. Rolando Herrero - Costa Rica;
Dr. R Rengaswamy Sankaranarayanan - Francia).
-Taller de
capacitación a los equipos de APS.
-Taller de
actualización en la técnica de la Colposcopía para servicios de
ginecología.
- Capacitaciones
específicas
13. LANZAMIENTO DE
PROMOCION, TAMIZAJE, SEGUIMIENTO Y TRATAMIENTO
- Búsqueda activa de
mujeres en edad objetivo para la realización de la prueba de HPV.
- Tamizaje de las
mujeres en edad objetivo.
- Implementación del
protocolo de seguimiento y tratamiento establecido
14. VISITAS DE
MONITOREO A LA PROVINCIA
15. IMPLEMENTACION
DE UN SISTEMA DE CONTROLES NEGATIVOS DE LA PRUEBA DE HPV
- Diseño e
implementación del sistema de controles negativos.
16. EVALUACION DE LA
EFICACIA DE LA PRUEBA DE HPV-CH2 PARA DETECTAR HSIL Y CANCER
- Diseño e
implementación del estudio.
17. EVALUAR LA
ACEPTABILIDAD Y LA EFICACIA DE LA AUTOTOMA DE LA PRUEBA DE HPV-HC2 COMO
ESTRATEGIA PARA ASEGURAR LA COBERTURA DEL TAMIZAJE
- Diseño e
implementación de la evaluación.
18. IMPLEMENTACION
DE UN ALGORITMO ALTERNATIVO DE SEGUIMIENTO PARA LAS MUJERES CON PRUEBA
DE HPV POSITIVA Y CITOLOGIA NEGATIVA
- Diseño e
implementación del estudio
*Cálculo de
población estimada a tamizar en la Provincia de Jujuy
Total mujeres entre
30 y 64 años sin obra social: 70.000
Cobertura estimada:
80%
Total mujeres a
tamizar para alcanzar meta de cobertura en 3 años: 56.000
Total mujeres a
tamizar por año: 20.000
Cantidad esperada de
mujeres con HPV positivo: 1800 (9%)
Cantidad esperada de
mujeres con HPV positivo y Pap negativo: 1400
Cantidad esperada de mujeres con HPV positivo y Pap positivo: 400 (2%
del total mujeres)
Cantidad esperada de
mujeres con HPV positivo y Pap positivo pero ASCUS o Bajo Grado: 229
mujeres
Cantidad esperada de
mujeres con HPV positivo y HSIL +: 171 (43% de mujeres con HPV
positivo y Pap positivo).
Estas son las
mujeres que luego de la confirmación histológica deberán ser tratadas.
Cantidad esperada de
mujeres a seguir el año siguiente con repetición de la prueba de
HPV-HC2 y Pap: 1629.
Proporción esperada
de mujeres con persistencia de HPV+: 40%, 650 mujeres a las que deberá
hacerse una colposcopía y biopsia. De estas mujeres, se espera que un
15% tengan hsIL+, es decir, aproximadamente 100 mujeres que
deberán tratarse en el año 2 y 3.
En total, en el año
2, deberán tratarse 271 mujeres con HSIL+.
Fuente:
Lazcano-Ponce et al, 2010.
CRONOGRAMA
DE ACTIVIDADES PARA EL PRIMER AÑO
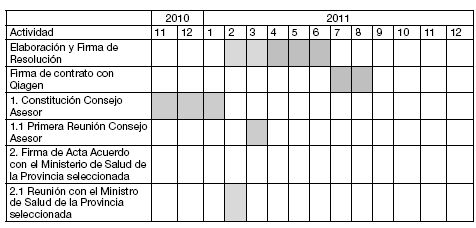
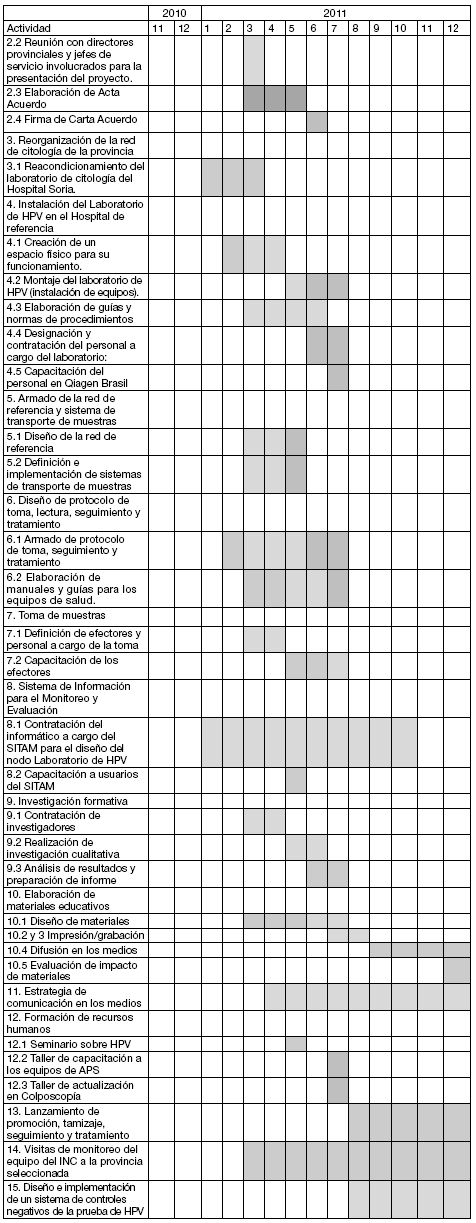
PRESUPUESTO ESTIMADO
| Actividad |
Costo
unitario |
Total |
| 1.
Constitución Consejo Asesor |
|
|
| 1.1
Viajes 2 miembros internacionales |
9000 |
18000 |
| 2.
Firma de Acta Acuerdo con el Ministerio de Salud de la Provincia |
|
|
| 2.1
Reunión con el Ministro de Salud de la Provincia de Jujuy (viaje a la
provincia, pasajes y viáticos) |
2000 |
4000 |
| 2.2
Reunión con directores provinciales y jefes de servicio involucrados
para la presentación del proyecto (viaje a la provincia, pasajes y
viáticos) |
2000 |
4000 |
| 2.3
Elaboración de Acta Acuerdo |
|
|
| 2.4
Firma de Acta Acuerdo |
|
|
| 3.
Reorganización de la red de citología de la provincia |
|
|
| 4.
Instalación del Laboratorio de HPV en el Hospital Soria |
|
|
| 4.1
Creación de un espacio físico para su funcionamiento |
|
|
| 4.2
Montaje del laboratorio de HPV (instalación de equipos) |
|
|
| 4.3
Elaboración y publicación de guías y normas de procedimientos |
40 |
800 |
| 4.4
Designación y contratación del personal a cargo del laboratorio |
|
|
| 4.5
Capacitación del personal en Qiagen Brasil |
|
|
| 5.
Armado de la red de referencia y sistema de transporte de muestras |
|
|
| 5.1
Diseño de la red de referencia |
|
|
| 5.2
Definición e implementación de sistemas de transporte de muestras |
|
|
| 6.
Diseño de protocolo de toma, lectura, seguimiento y tratamiento |
|
|
| 6.1
Armado de protocolo de toma, seguimiento y tratamiento |
|
|
| 6.2
Elaboración y publicación de manuales y guías para los equipos de salud |
40 |
4000 |
| 7.
Toma de muestras |
|
|
| 7.1
Definición de efectores y personal a cargo de la toma |
|
|
| 7.2
Capacitación de tomadores de muestra |
10000 |
30000 |
| 8.
Sistema de Información para el Monitoreo y Evaluación |
|
|
| 8.1
Contratación del informático a cargo del SITAM para el diseño del nodo
Laboratorio de HPV |
3000 |
36000 |
| 8.2
Capacitación a usuarios del SITAM (2) |
5000 |
10000 |
| 9.
Investigación formativa |
|
|
| 9.1
Realización de investigación cualitativa |
|
60000 |
| 9.2
Análisis de resultados y preparación de informe |
|
|
| 10.
Elaboración de materiales educativos |
|
|
| 10.1
Diseño de materiales |
|
|
| 10.2
Impresión de folletos/afiches |
8 |
160000 |
| 10.3
Grabación de spots |
3000 |
3000 |
| 10.4
Difusión en los medios |
|
|
| 10.5
Evaluación de impacto de materiales |
|
80000 |
| 11.
Estrategia de comunicación en los medios |
|
|
| 12.
Formación de recursos humanos |
|
|
| 12.1
Seminario sobre HPV |
|
300000 |
| 12.2
Talleres de capacitación a los equipos de APS |
|
50000 |
| 12.3
Talleres de actualización en colposcopía |
|
50000 |
| 13.
Lanzamiento de promoción, tamizaje, seguimiento y tratamiento |
|
60000 |
| 14.
Visitas de Monitoreo a la Provincia (2 viajes x mes, pasaje y viáticos) |
5000 |
60000 |
| 15.
Diseño e implementación de un sistema de controles negativos de la
prueba de HPV |
|
|
| 16.
Diseño e implementación de la evaluación de la eficacia de la prueba de
HPV-CH2 para detectar hsIL y cáncer |
|
65000 |
| 17.
Diseño e implementación de la evaluación de la aceptabilidad y la
eficacia de la autotoma de la prueba de HPV-HC2 |
|
160000 |
| 18.
Diseño e implementación de un algoritmo alternativo de seguimiento para
las mujeres con prueba de HPV positiva y citología negativa |
|
25000 |
| 19.
Prueba de HPV (30000 por año) |
68 |
2040000 |
| TOTAL |
|
3219800 |
ANEXO II
CONVENIO ESPECIFICIO
MINISTERIO DE SALUD DE LA NACION - PROVINCIA DE JUJUY
PROGRAMA NACIONAL DE PREVENCION DE CANCER CERVICO-UTERINO
INSTITUTO NACIONAL DEL CANCER
“PROYECTO PARA LA INCORPORACION DE LA
PRUEBA DE HPV-HC2 COMO TAMIZAJE PRIMARIO”
Entre el ESTADO NACIONAL - MINISTERIO
DE SALUD, representado en este acto por el Subsecretario de Salud
Comunitaria del MINISTERIO DE SALUD DE LA NACION, doctor Guillermo
González Prieto, con domicilio en Av. 9 de Julio 1925 de la Ciudad
Autónoma de Buenos Aires, en adelante “EL MINISTERIO”; y por la otra,
EL MINISTERIO DE SALUD DE LA PROVINCIA DE JUJUY, representado por el
Ministro de Salud, doctor Víctor Alberto Urbani, con domicilio en San
Martín 61 de la Ciudad de San Salvador de Jujuy, Provincia de Jujuy, en
adelante “LA PROVINCIA”, DECLARAN lo siguiente:
1º) Que con fecha 22/10/2008 en el marco del Programa Nacional de
Prevención de Cáncer Cérvico-Uterino, ambas partes suscribieron una
Carta Acuerdo para el fortalecimiento del Programa de Prevención de
Cáncer Cérvico-uterino de “LA PROVINCIA”.
2º) Que de acuerdo con el Artículo SEGUNDO de dicha Carta Acuerdo,
ambas partes previeron como uno de los objetivos específicos para
desarrollar conjuntamente, lograr la alta calidad de los servicios
diagnósticos (toma y lectura de la citología).
3º) Que a los fines de la consecución de la finalidad y objetivos
específicos establecidos en el Acuerdo mencionado, “EL MINISTERIO” y
“LA PROVINCIA” asumieron las obligaciones previstas en los Artículos
TERCERO y CUARTO, respectivamente.
Y por ello, en el marco de la Carta Acuerdo de fecha 22/10/2008 ambas
partes ACUERDAN en celebrar el presente Convenio Específico de
cooperación para el fortalecimiento del Programa Provincial de
Prevención de Cáncer Cérvico-Uterino, el que se regirá de acuerdo a las
siguientes cláusulas y condiciones:
PRIMERA: FINALIDAD
El presente convenio tiene como propósito establecer los términos y
condiciones bajo los cuales el “EL MINISTERIO” y “LA PROVINCIA”,
trabajarán en conjunto para la implementación del Proyecto de
Incorporación de la prueba de detección de ADN del virus de Papiloma
Humano (prueba de HPV-CH2) como tamizaje primario, cuyos fundamentos y
descripción se detallan en el Anexo I del presente acuerdo, el cual
forma parte integrante del mismo.
SEGUNDA: OBJETIVOS
Las partes declaran el siguiente objetivo para desarrollar
conjuntamente: Desarrollar una estrategia de prevención basada en la
prueba de HPV-HC2 como método de tamizaje primario con el objetivo de
reducir la incidencia y mortalidad por cáncer de cuello uterino en la
provincia de Jujuy.
TERCERA: OBLIGACIONES DE “EL MINISTERIO”
De conformidad con sus reglas, reglamentos, políticas y procedimientos,
EL MINISTERIO, a los fines del cumplimiento de los objetivos
establecido en la cláusula PRIMERA, se compromete a:
1. Proveer a LA PROVINCIA los insumos para la toma de las pruebas de
HPV-CH2, así como el equipamiento necesario para la instalación del
laboratorio de HPV, según se especifica en el Anexo II del presente
convenio.
2. Capacitar a los equipos de salud de la provincia involucrados en el
desarrollo del proyecto, a saber:
- capacitación para los profesionales del Laboratorio de HPV
- capacitación para la toma del test de HPV
- capacitación para la búsqueda activa de mujeres
- formación científica sobre epidemiología del HPV y nuevas tecnologías
en prevención de cáncer cérvico-uterino.
3. Proveer materiales de comunicación destinados a la promoción del
tamizaje con el test de HPV en la población objetivo.
4. Brindar asistencia técnica continua al Programa Provincial de
Prevención de Cáncer Cérvico-uterino y a los efectores y servicios
involucrados en la implementación del Proyecto.
CUARTA: OBLIGACIONES DE “LA PROVINCIA”
De conformidad con sus reglas, reglamentos, políticas y procedimientos,
LA PROVINCIA, a los fines del cumplimiento de los objetivos establecido
en la cláusula PRIMERA del presente convenio, se compromete a:
1. Instalar el Laboratorio de HPV en el Hospital Soria, adecuar el
espacio físico e instalar el equipamiento provisto por EL MINISTERIO.
2. Contratar un profesional capacitado para dirigir el Laboratorio de
HPV, que dependerá del Jefe del Laboratorio de Anatomía Patológica del
Hospital Pablo Soria.
3. Asegurar el adecuado funcionamiento de todos los componentes de la
prevención del cáncer cérvico-uterino. A tal efecto, deberá:
- implementar estrategias de búsqueda activa para la realización del
test de HPV en la población objetivo.
- asegurar la toma de la muestra en la población objetivo.
- implementar un adecuado mecanismo de traslado de las muestras.
- asegurar la calidad en el procesamiento de las muestras en el
laboratorio de HPV.
- asegurar el adecuado seguimiento y tratamiento de mujeres con
diagnóstico anormal.
QUINTA: RESPONSABLES DEL PROYECTO
La coordinación de la ejecución del presente convenio estará a cargo de
las siguientes personas:
a) Por “EL MINISTERIO”: la Coordinadora Científica del Programa
Nacional de Prevención de Cáncer Cérvico-uterino y la Coordinadora del
Area de Detección Temprana del INSTITUTO NACIONAL DEL CANCER.
b) Por “LA PROVINCIA”: la Coordinadora del Programa Provincial de
Prevención de Cáncer Cérvico- uterino.
SEXTA: INFORMES
“LA PROVINCIA” preparará y presentará a “EL MINISTERIO” un informe
trimestral del desarrollo de Proyecto. “EL MINISTERIO” por medio de la
SUBSECRETARIA DE SALUD COMUNITARIA y el INSTITUTO NACIONAL DEL CANCER,
se reservan el derecho de solicitar a “LA PROVINCIA” la ampliación de
la información suministrada.
SEPTIMA: CONTROL DE GESTION
“EL MINISTERIO”, a través de la Subsecretaría de Salud Comunitaria y el
INSTITUTO NACIONAL DEL CANCER, sin perjuicio de la auditoría que
realice la Unidad de Auditoria Interna de “EL MINISTERIO” en el ámbito
de su competencia, se encuentran facultados a efectuar el seguimiento y
evaluación de la ejecución de la ejecución del presente convenio. A tal
efecto, cada vez que lo consideren oportuno, podrán disponer el
traslado de personal especializado al ámbito provincial, a fin de
realizar las verificaciones y/o análisis de gestión que estimen
conducentes sobre el cumplimiento del presente acuerdo.
“La PROVINCIA” se compromete a poner a disposición de “EL MINISTERIO”
todos los elementos de juicio, documentación respaldatoria, personal de
apoyo, vehículos de transporte y todo instrumento que resulten
necesarios para las evaluaciones que se efectúen en el ámbito
provincial.
OCTAVA: RELACION Y RESPONSABILIDAD DE LAS PARTES
La ejecución del presente convenio no crea ningún tipo de relación
laboral entre “EL MINISTERIO” y los agentes provinciales que se
desempeñen en el marco de este Acuerdo “EL MINISTERIO” no será
responsable de ninguna pérdida, daño o perjuicio sufrido por “LA
PROVINCIA” o por cualquier persona que reclame en nombre de la
PROVINCIA o contra ella, que sea consecuencia o esté vinculada en
cualquier forma con la ejecución del presente convenio. “LA PROVINCIA”
asume el compromiso de reparar o sustituir, a su costa, el equipamiento
provisto por “EL MINISTERIO”, en caso de roturas del mismo, haciéndose
cargo, asimismo, de la reposición de insumos o arreglos de
funcionamiento del mismo. “LA PROVINCIA se compromete a mantener
indemne al Ministerio ante cualquier reclamo de cualquier índole que
realice cualquier persona física o ideal contra el Ministerio en virtud
de la ejecución del presente Acuerdo.
NOVENA: PROPIEDAD, DERECHOS DE AUTOR, DERECHOS DE PATENTES Y OTROS
Todos los derechos, incluidos los de propiedad, derechos de autor y
derechos de patentes, correspondientes a todo material producido bajo
el presente convenio, pertenecerán a “EL MINISTERIO”, quien tendrá
derecho a hacer los cambios o eliminaciones de las partes del material
que considere necesario o conveniente. La PROVINCIA y sus empleados
podrán utilizar una copia del material para fines educativos y de
investigación, sin fines de lucro, y siempre y cuando los derechos de
“EL MINISTERIO” sean reconocidos adecuadamente en el material.
DECIMA: PLAZO
El presente acuerdo regirá por el plazo de TRES (3) años, contado a
partir del refrendo del mismo, previsto en la cláusula DECIMA QUINTA.
Dicho plazo se prorrogará automáticamente por períodos iguales
sucesivos, salvo manifestación en contrario de cualquiera de los
partes. La voluntad de no prorrogar el plazo del presente convenio,
deberá ser notificada fehacientemente a la otra parte con no menos de
SESENTA (60) días de anticipación a su vencimiento.
DECIMOPRIMERA: RESOLUCION DEL CONVENIO
Ante el incumplimiento por alguna de las partes de cualquiera de las
obligaciones establecidas en el presente convenio, la parte cumplidora
se reserva el derecho de resolverlo, previa interpelación por medio
fehaciente, y sin perjuicio de las indemnizaciones por daños y
perjuicios a que hubiere lugar conforme la legislación de fondo
aplicable.
DECIMOSEGUNDA: RESCISION
Sin perjuicio de lo pactado en la cláusula DECIMA, el presente convenio
podrá ser rescindido por voluntad de una de las partes, sin expresión
de causa, debiendo para ello, dar previo aviso a la otra parte mediante
notificación fehaciente y con una antelación no menor a SESENTA (60)
días.
DECIMOTERCERA: JURISDICCION
Para el hipotético caso de suscitarse alguna controversia respecto de
la interpretación y/o ejecución del presente convenio, ambas partes se
someten a la jurisdicción originaria de la Corte Suprema de Justicia de
la Nación.
DECIMOCUARTA: DOMICILIOS
A todos los efectos del presente convenio, las partes constituyen
domicilio en los indicados en el encabezamiento, donde serán válidas
todas las notificaciones que se practiquen. Los domicilios constituidos
subsistirán para los efectos del presente, mientras no se constituyan
otros y sean fehacientemente notificados a la otra parte.
DECIMOQUINTA: ENTRADA EN VIGOR, REFRENDO POR PARTE DEL SEÑOR GOBERNADOR
DE LA PROVINCIA DE JUJUY
El presente convenio se suscribre ad referéndum del señor Gobernador de
la Provincia de Jujuy. En consecuencia, para tener plena eficacia, este
acuerdo deberá ser refrendado por dicha autoridad provincial, dentro
del plazo de NOVENTA (90) días contados desde la fecha de su
suscripción.
En prueba de conformidad se firman dos (2) ejemplares de un mismo tenor
y a un solo efecto, en la Ciudad Autónoma de Buenos Aires, a
los días del mes
de
del año 2011.
|
Por
la
PROVINCIA DE JUJUY
|
Por
EL MINISTERIO DE SALUD DE LA NACION
|
|
Firma
|
Firma
|
|
Aclaración
|
Aclaración
|
|
Lugar y fecha
|
Lugar y fecha
|
ANEXO I AL CONVENIO ESPECIFICO
“Proyecto para la incorporación del la
prueba de HPV-HC21 (1) como tamizaje primario”
Presentado por la Coordinación de
Detección Temprana del Instituto Nacional del Cáncer y el
Programa Nacional de Prevención de Cáncer Cérvico-uterino
Año 2011
FUNDAMENTACION
El cáncer cérvico-uterino es la segunda causa de muerte por cáncer en
mujeres entre 35 y 64 años. En la Argentina, se diagnostican alrededor
de 3000 casos nuevos por año, y mueren 2000 mujeres por esta enfermedad.
Se ha comprobado que la causa necesaria del cáncer cérvico-uterino es
la infección por el Virus Papiloma Humano (HPV), cuya principal vía de
transmisión es la vía sexual (Bosch FX., 2002). Existe una asociación
de más del 99% entre el HPV y el cáncer de cuello de útero
(Castellsagué X., 2006). Se han encontrado más de 100 tipos de HPV, de
los cuales alrededor de 15 son considerados de alto riesgo oncogénico
(los más comunes son el 16 y el 18, responsables de aproximadamente el
70% de los casos de cáncer cérvico-uterino, seguidos por el 31 y el 45).
A diferencia de los países desarrollados, los países latinoamericanos
que han implementado programas organizados de prevención basados en la
citología convencional se han encontrado con limitaciones para alcanzar
el impacto deseado en la reducción de la incidencia y mortalidad. Las
principales limitaciones se asocian con:
- la baja cobertura de mujeres tamizadas,
- el bajo porcentaje de mujeres con Pap anormal que son efectivamente
seguidas y tratadas,
- la sensibilidad de la prueba que es entre moderada y baja, lo que
obliga a repeticiones frecuentes del tamizaje para reducir el
porcentaje de falsos positivos, y
- las numerosas instancias que pueden afectar la calidad de la lectura
(toma, transporte, coloración, calidad de la muestra, etc.).
La sensibilidad de la prueba del Pap se estima entre el 50 y 60%. Esto
resulta de la multiplicidad de instancias que deben asegurarse para la
adecuada toma y lectura de la muestra. De hecho, el Pap es una prueba
altamente operador-dependiente, sujeta a interpretaciones subjetivas,
tanto en lo que refiere a quien toma la muestra como a quien la procesa.
En la siguiente tabla se resumen las ventajas de la prueba de HPV-HC2
en relación con la citología:
Tabla I: Cuadro comparativo. Características principales de la prueba
de HPV-HC2 y la citología como métodos de tamizaje.
|
Citología |
Prueba
de HPV-HC2 |
| Sensibilidad
de la técnica |
Entre
moderada y baja (40%-50%): requiere repetir la prueba durante varios
años para compensar la baja sensibilidad (1-1-3). |
Alta
(mayor al 90%) para lesiones de alto grado. |
| Valor
predictivo negativo |
Bajo. |
Alto.
Esto permite espaciar el intervalo de tamizaje a 3 ó 5 años para las
mujeres negativas para HPV. |
| Toma
de la muestra |
Altamente
operador-dependiente. |
Menos
dependiente de la pericia del tomador de la muestra. |
| Traslado
de las muestras |
Alto
riesgo de disecación y contaminación debido a la falta de cuidado en
los traslados. |
Colector
estandarizado. Alta calidad de preservación. |
| Procesamiento
de las muestras |
Altamente
dependiente del operador. Requiere personal especializado para la
lectura de una gran cantidad de Paps de los cuales sólo una minoría son
positivos (5%). |
Procesamiento
automático. Analiza automáticamente 88 muestras a la vez. |
Para compensar estas deficiencias y
asegurar la calidad de la citología, es necesaria la repetición de la
prueba y la implementación de estrictos controles de calidad. Por ello,
a pesar de los costos reducidos de los insumos, la citología no es
necesariamente la opción más costo-efectiva para el tamizaje, en la
medida que aumentan los costos y el número de veces que las mujeres
deben concurrir a la consulta, con el riesgo de abandono que eso
implica.
Estas dificultades
en la implementación de programas de tamizaje basados en la citología
en los países latinoamericanos, plantea la necesidad de un cambio de
paradigma que incorpore los nuevos avances tecnológicos para la
prevención del cáncer cérvico-uterino.
Tamizaje basado en
la prueba de Virus del Papiloma Humano (Prueba de HPV)
A partir de la
década del 90, se comenzó a desarrollar un método que permite detectar
la presencia de ADN de HPV de alto riesgo oncogénico en las células del
cuello del útero. Actualmente, existen en el mercado, aprobados por la
FDA (Food And Drug Administration), tres pruebas para la detección de
ADN de HPV en contextos de tamizaje poblacional. Sin embargo, la única
prueba utilizada en los países de Latinoamérica que ya han iniciado
experiencias de incorporación de la prueba de HPV como tamizaje
primario es la prueba de HPV por captura de híbridos (HPV-HC2).
1) El test de HPV
basado en la captura de híbridos es el único en el mundo para el cual
su efectividad para reducir la incidencia y mortalidad por cáncer de
cuello de útero ha sido demostrada científicamente. En efecto, el único
estudio publicado hasta el momento que se propuso medir el impacto de
tres diferentes métodos de tamizaje en la reducción de la incidencia y
mortalidad por cáncer cérvico-uterino fue realizado en India
(Sankaranarayanan et al., 2009). En dicho estudio se concluyó que las
tasas de incidencia y mortalidad fueron significativamente mayores para
los grupos que fueron tamizados con citología o Inspección Visual con
ácido acético (VIA) que en el caso del grupo al que se le aplicó la
prueba de HPV-HC2. El tamizaje mediante la prueba de HPV-HC2 contribuyó
a alcanzar una reducción de casi el 50% en la tasa de mortalidad.
2) Existe
amplia evidencia científica sobre la alta eficacia de la prueba de
HPV-HC2 como método primario para la detección de lesiones de alto
grado y cáncer (Tabla 1). No existe el mismo nivel de evidencia sobre
la eficacia de las otras pruebas aprobadas por la FDA.
En la tabla 1 se presenta un listado de estudios que comparan la
sensibilidad de la prueba de HPV-HC2 con la de la citología.
Tabla I: Sensibilidad relativa de la prueba de HPV-HC2 comparada con la
citología en diferentes estudios. Años 1999 a 2004.
|
Citología
(LSIL+)% |
HPV
+% |
| Clavel
et al. (1999) |
85
(CIN2+) |
100 |
| Cuzick
et al. (1999a) |
79
(CIN2+) |
95 |
| Schiffman
et al. (2000) |
78
(CIN2+) |
88 |
| Ratnam
et al. (2000) |
40
(CIN2+) |
90 |
| Denny
et al. (2000a) |
78
(CIN2+) |
73 |
| Denny
et al. (2000b) |
82
(CIN2+) |
72 |
| Schneider
et al. (2000) |
20
(CIN2+) |
89 |
| Womack
et al. (2000) |
44
(CIN2+) |
81 |
| Clavel
et al. (2001) |
68
(CIN2+) |
100 |
| Petry
et al. (2003) |
37
(CIN2+) |
98 |
| Kulasingam
et al. (2002) |
36
(CIN2+) |
63 |
| Cuzick
et al. (2003) |
70
(CIN2+) |
97 |
| Sankaranarayanan
et al. (2004b) |
37-72
(CIN2+) |
46-81 |
| Salmeron
et al. (2003) |
59
(CIN2+) |
93 |
| Nieminen
et al. (2004) |
83
(CIN2+) |
98 |
| LSIL=
lesión escamosa intraepitelial de bajo grado |
Fuente:
IARC Handbook 2005:187. |
| CIN=
neoplasia cervical intraepitelial |
A su vez, un meta-análisis publicado en
2008 (Cuzick 2008) presenta una revisión de 31 estudios llevados a cabo
entre los años 1995 y 2007 en diferentes países del mundo, que han
evaluado la sensibilidad de la prueba de HPV-HC2 utilizado como método
de tamizaje primario. En promedio, la sensibilidad de la prueba de
HPV-HC2 fue del 89.7%. A continuación se presenta el listado de
investigaciones revisadas entre los años 2005 y 2007:
- Agorasros T et
al., 2005
- Bigras G et al., 2005
- Kotaniemi-Talonen
L et al., 2005
- Sankaranarayanan R
et al., 2005
- Sarian LO et al.,
2005
- Ronco G et al.,
2006
- Ronco G et al.,
2006
- Almonte M et al.,
2007
- Bulkmans NW et
al., 2007
- Naucler P et al.,
2007
- Mayrand MH et al.,
2007
*Fuente: Cuzick, et
al., 2008.
Existen también
estudios en Latinoamérica que dan cuenta de esta ventaja de la prueba
de HPV-HC2. Un estudio publicado en 2008 (Herrero et al., 2008) analiza
diversos estudios de investigación sobre nuevas tecnologías aplicadas
al tamizaje para la prevención del cáncer cérvico-uterino. La siguiente
tabla resume algunos de esos proyectos, destacando la sensibilidad
obtenida para la prueba HPV-HC2 en cada caso.
Tabla II: Proyectos
de Investigación en Latinoamérica sobre evaluación de la inclusión de
nuevas tecnologías al tamizaje del cáncer cérvico-uterino.
| Proyecto |
Autor
y año de publicación |
País |
Cantidad
de población incluida en la muestra |
Sensibilidad
de la prueba de HPV |
| Proyecto
Guanacaste |
Shifman
et al., 2000 |
Costa
Rica |
8500 |
88.4
(Cin3+) |
| Proyecto
TATI |
Almonte
et al., 2007 |
Perú |
5435 |
89.4
(Cin3+) |
| IMSS |
Salmeron
et al., 2003 |
México
(Morelos) |
7868 |
93.1
(Cin 2+) |
| IMSS |
Lascano-Ponce
et al., 2010 |
México |
51168 |
93.3 |
| CIN=
neoplasia cervical intraepitelial |
Fuente:
Herrero et al., 2008 |
Programas de
tamizaje basados en la prueba de HPV como tamizaje primario: el
contexto latinoamericano
Tomando en cuenta
esta evidencia sobre la aplicación de nuevas tecnologías en los
programas de tamizaje de cáncer cérvico-uterino, la OPS elaboró en 2008
una Estrategia Regional y Plan de Acción para la Prevención y Control
del cáncer cérvico-uterino, que fue aprobada por los Ministros de Salud
de América Latina durante el Consejo Directivo de la OPS de ese año.
Como parte de esta estrategia, en junio de 2010 se llevó a cabo en
Panamá el encuentro “Nuevas Tecnologías para la prevención del cáncer
cérvico-uterino: de la evidencia científica a la planificación de
programas”. Las principales conclusiones del encuentro apuntan a que la
implementación de estas nuevas tecnologías, respaldadas por evidencia
científica clara y bien establecida, resulta factible. La Región se
encuentra en un punto de inflexión en el que se reúnen las condiciones
oportunas para lograr la incorporación de cambios en los programas que
permitan lograr un impacto mayor en la reducción de las tasas de
incidencia y mortalidad por esta enfermedad.
LA RECOMENDACION
CIENTIFICA Y DE SALUD PUBLICA INTERNACIONAL ES LA IMPLEMENTACION DE
PROYECTOS DE DEMOSTRACION PARA CAMBIAR LOS PROGRAMAS AL NUEVO PARADIGMA
DE LA PREVENCION DEL CANCER CERVICO-UTERINO BASADO EN LA PRUEBA DE
HPV-HC2 COMO TAMIZAJE PRIMARIO.
En algunos países
latinoamericanos ya se han desarrollado experiencias de incorporación
de la prueba de HPV-HC2 como método de tamizaje, buscando superar las
limitaciones propias de la citología y contribuir a alcanzar la meta de
reducción de la mortalidad. Es el caso de México, que desde el año 2007
ha establecido un esquema de tamizaje basado en la prueba de HPV-HC2
como tamizaje primario, seguido del Pap para las mujeres HPV positivas.
PROPUESTA DE
INCORPORACION DE LA PRUEBA DE HPV-CH2 COMO TAMIZAJE PRIMARIO EN LA
PROVINCIA DE JUJUY.
Se propone la
implementación de un proyecto en la Provincia de Jujuy para incorporar
la prueba de HPV-HC2 como tamizaje primario en mujeres entre 30 y 65
años, seguido de citología para aquellas mujeres con prueba de HPV
positiva.
Se ha seleccionado
la Provincia de Jujuy porque es una de las provincias con mayores tasas
de mortalidad por cáncer cérvico-uterino, y tiene una capacidad
organizativa del sistema de salud adecuada para la implementación del
proyecto.
POBLACION OBJETIVO
Mujeres entre 30 y
65 años sin cobertura de salud de la provincia de Jujuy.
OBJETIVO
GENERAL
Desarrollar
una estrategia de
prevención basada en la prueba de HPV-HC2 como método de tamizaje
primario con
el objetivo de reducir la incidencia y mortalidad por cáncer de cuello
uterino en el país.
OBJETIVOS ESPECIFICOS
a)
Implementar un proyecto de
introducción de la prueba de HPV-HC2 en una provincia seleccionada.
b)
Desarrollar, monitorear y
evaluar los distintos componentes que deben articularse en un programa
de
prevención de cáncer cérvico-uterino basado en la prueba de HPV-HC2:
-
b1) la estrategia de
comunicación dirigida a la población y a los profesionales de la salud.
-
b2) la estrategia de
capacitación de los equipos de salud.
-
b3) las estrategias de búsqueda
activa de mujeres en edad objetivo.
-
b4) la capacidad operativa del
laboratorio de citología en el marco de una estrategia de doble toma
(Prueba de
HPV / citología): dispositivo de almacenamiento (espacio, tiempos),
recursos
humanos, identificación de muestras, carga de trabajo, etc.
-
b5) un sistema de controles
negativos de la prueba de HPV, que incluya la realización del Pap y
colposcopía
a una muestra de mujeres con prueba de HPV negativa.
-
b6) un sistema de calidad para
el seguimiento y tratamiento de las mujeres.
c)
Evaluar en una muestra de
mujeres la eficacia de la prueba de HPV-HC2 para detectar HSIL y cáncer
en una
población con alta mortalidad por cáncer cérvico-uterino.
d)
Evaluar la aceptabilidad y la
eficacia de la autotoma de la prueba de HPV-HC2 como estrategia para
asegurar
la cobertura del tamizaje.
e)
Evaluar un algoritmo
alternativo de seguimiento para las mujeres con prueba de HPV positiva
y
citología negativa.
METAS
Alcanzar
un 80% de cobertura del
tamizaje por medio de la prueba de HPV-HC2, en mujeres entre 30 y 65
años sin
cobertura de salud.
Asegurar
la calidad de la toma de
la prueba de HPV-HC2 y su procesamiento en el laboratorio de HPV.
Lograr
que el 100% de las mujeres
con diagnóstico de HSIL+ accedan al tratamiento efectivo dentro de los
6 meses
después del diagnóstico.
ACTIVIDADES
A.
FIRMA DE CONTRATO CON EMPRESA
PRODUCTORA (Qiagen)
1.
CONSTITUCION DE CONSEJO ASESOR
Integrado
por: Programa Nacional
de Salud Sexual y Procreación Responsable, Sociedad Argentina de
Citología,
Sociedad de Ginecología de Buenos Aires, Sociedad Argentina del Tracto
Genital Inferior
y Colposcopía, Instituto Malbrán, Hospital de Clínicas San Martín,
Organización
Panamericana de la Salud,
Fondo de Población de las Naciones Unidas, Centro de Estudios de Estado
y Sociedad,
Instituto Gino Germani, Consejo Nacional de la Mujer, Secretaría
de Derechos Humanos, y expertos
nacionales e internacionales invitados (Dr. Eduardo Lazcano-Ponce, Dr.
Rolando
Herrero, Dra. Lucrecia Illescas).
-
Elaboración de Resolución de
creación del Consejo Asesor.
2.
FIRMA DE ACTA ACUERDO CON EL
MINISTERIO DE SALUD DE LA PROVINCIA
SELECCIONADA
-
Reunión de presentación del
proyecto con el Ministro de Salud de la Provincia
seleccionada.
-
Reunión de presentación del
proyecto con directores provinciales y jefes de servicio involucrados
en la
implementación del proyecto.
-
Elaboración de Acta Acuerdo:
definición de compromisos del Ministerio de Salud de la Nación y del
Ministerio de
Salud de la
Provincia.
-
Firma de Acta Acuerdo.
3.
REORGANIZACION DE LA
RED DE LABORATORIOS DE
CITOLOGIA DE LA
PROVINCIA
-
Reacondicionamiento del
laboratorio de citología del Hospital Soria para el almacenamiento de
las
muestras citológicas de las mujeres entre 30 y 65 años (en el marco de
la
estrategia de doble toma —Prueba de HPV/citología—).
4.
INSTALACION DEL LABORATORIO DE
HPV EN EL HOSPITAL DE MAYOR COMPLEJIDAD DE LA PROVINCIA
-
Creación de un espacio físico
para su funcionamiento (requerimientos de espacio, teléfono,
refrigeración y
equipamiento).
-
Montaje del laboratorio de HPV
(instalación de equipos).
-
Elaboración de guías y normas
de procedimiento para el laboratorio y su articulación con el
laboratorio de
citología del Hospital.
-
Designación y contratación del
personal a cargo del laboratorio: Jefe de laboratorio, técnico de
laboratorio,
administrativo (a cargo del Ministerio de Salud Provincial).
-
Capacitación del personal que
estará a cargo del laboratorio: provista por Qiagen en Brasil (incluye
vuelo,
hotel, comida y transporte).
5.
ARMADO DE LA RED DE
REFERENCIA,
DEFINICION DE SISTEMAS DE TRANSPORTE DE LAS MUESTRAS.
-
Diseño de la red de referencia.
-
Definición e implementación de
sistemas de transporte de muestras.
6.
DISEÑO DEL PROTOCOLO DE TOMA,
LECTURA, SEGUIMIENTO Y TRATAMIENTO DE MUJERES TAMIZADAS
-
Armado de protocolo de toma,
seguimiento y tratamiento.
-
Elaboración de manuales y guías
para los equipos de salud.
7.
TOMA DE MUESTRAS
-
Definición de efectores y
personal a cargo de la toma.
-
Capacitación de los efectores a
cargo de la toma sobre la toma de la muestra en un contexto de tamizaje
basado
en la prueba de HPV-HC2.
8.
SISTEMA DE INFORMACION PARA EL
MONITOREO Y EVALUACION
-
Contratación del informático a
cargo del SITAM para el diseño del nodo Laboratorio de HPV.
-
Capacitación a usuarios del
SITAM.
9.
INVESTIGACION FORMATIVA PARA
INDAGAR CONOCIMIENTOS Y PERCEPCIONES DE LA POBLACION SOBRE
EL
HPV (Grupos focales; Entrevistas cualitativas a equipos de salud)
-
Contratación de investigadores.
-
Realización de investigación
cualitativa
-
Análisis de resultados y
preparación de informe.
10.
ELABORACION DE MATERIALES
EDUCATIVOS PARA LA POBLACION SOBRE EL TAMIZAJE BASADO EN LA PRUEBA DE HPV
(folletos,
afiches, spots radiales y televisivos)
-
Diseño de materiales.
-
Impresión/grabación.
-
Difusión en los medios.
11.
ELABORACION DE UNA ESTRATEGIA
DE COMUNICACION EN MEDIOS
12.
FORMACION DE RECURSOS HUMANOS
-
Seminario sobre Epidemiología
del HPV y cáncer de cuello de útero, y evidencia científica sobre
estrategias
de tamizaje basadas en la prueba de HPV-HC2:
Destinatarios:
profesionales de
la salud de la provincia: APS, servicios de ginecología, servicios de
patología
cervical, servicios de anatomía patológica, oncología.
Duración:
3-4 días.
Fecha:
Semana del 16 de mayo
2011.
Financiamiento:
Ministerio de
Salud de la Nación/organismos
internacionales.
Se
ha solicitado apoyo a la
UICC para el financiamiento
de los invitados internacionales (Dr.Eduardo Lazcano-Ponce - México;
Dr.
Rolando Herrero - Costa Rica; Dr. R Rengaswamy Sankaranarayanan-
Francia).
-
Taller de capacitación a los
equipos de APS.
-
Taller de actualización en la
técnica de la
Colposcopía
para servicios de ginecología.
-
Capacitaciones específicas
13.
LANZAMIENTO DE PROMOCION,
TAMIZAJE, SEGUIMIENTO Y TRATAMIENTO
-
Búsqueda activa de mujeres en
edad objetivo para la realización de la prueba de HPV
-
Tamizaje de las mujeres en edad
objetivo
-
Implementación del protocolo de
seguimiento y tratamiento establecido
14.
VISITAS DE MONITOREO A LA PROVINCIA
15.
IMPLEMENTACION DE UN SISTEMA
DE CONTROLES NEGATIVOS DE LA PRUEBA DE HPV
-
Diseño e implementación del
sistema de controles negativos.
16.
EVALUACION DE LA
EFICACIA DE LA PRUEBA DE HPV-CH2 PARA
DETECTAR hsIL Y CANCER
-
Diseño e implementación del
estudio.
17.
EVALUAR LA
ACEPTABILIDAD Y LA EFICACIA DE LA AUTOTOMA DE LA PRUEBA DE
HPVHC2 COMO
ESTRATEGIA PARA ASEGURAR LA COBERTURA DEL TAMIZAJE
-
Diseño e implementación de la
evaluación.
18.
IMPLEMENTACION DE UN
ALGORITMO ALTERNATIVO DE SEGUIMIENTO PARA LAS MUJERES CON PRUEBA DE HPV
POSITIVA Y CITOLOGIA NEGATIVA
-
Diseño e implementación del
estudio
*Cálculo
de población estimada a
tamizar en la
Provincia
de Jujuy
Total
mujeres entre 30 y 64 años
sin obra social: 70.000
Cobertura
estimada: 80%
Total
mujeres a tamizar para
alcanzar meta de cobertura en 3 años: 56,000
Total
mujeres a tamizar por año:
20.000
Cantidad
esperada de mujeres con
HPV positivo: 1800 (9%)
Cantidad
esperada de mujeres con
HPV positivo y Pap negativo: 1400
Cantidad
esperada de mujeres con
HPV positivo y Pap positivo: 400 (2% del total mujeres) mujeres
Cantidad
esperada de mujeres con
HPV positivo y HSIL +: 171 (43% de mujeres con HPV positivo y Pap
positivo).
Estas son las mujeres que luego de la confirmación histológica deberán
ser tratadas.
Cantidad
esperada de mujeres a
seguir el año siguiente con repetición de la prueba de HPVHC2 y Pap:
1629.
Proporción
esperada de mujeres
con persistencia de HPV+: 40%, 650 mujeres a las que deberá hacerse una
colposcopía y biopsia. De estas mujeres, se espera que un 15% tengan
hsIL+, es
decir, aproximadamente 100 mujeres que deberán tratarse en el año 2 y
3. En
total, en el año 2, deberán tratarse 271 mujeres con hsIL+. Fuente:
Lazcano-Ponce et al, 2010.
CRONOGRAMA DE ACTIVIDADES PARA EL PRIMER AÑO
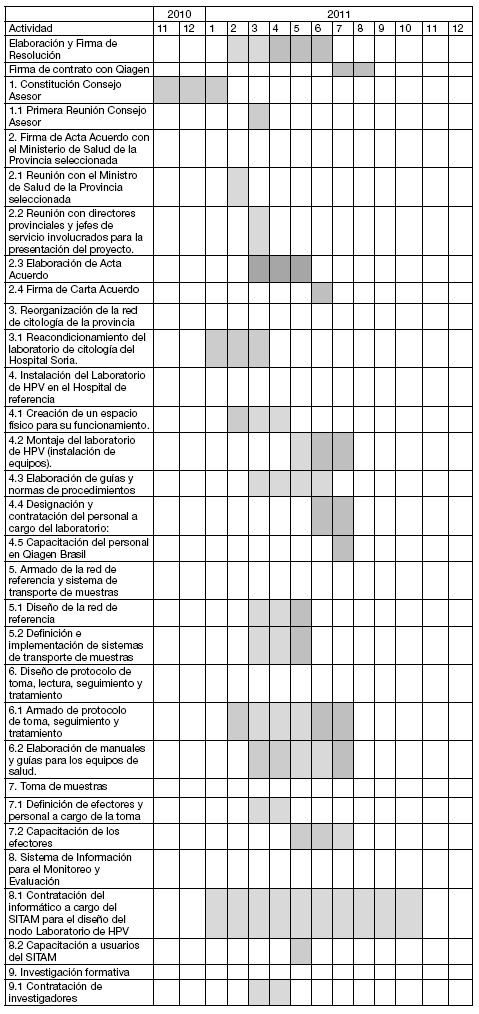
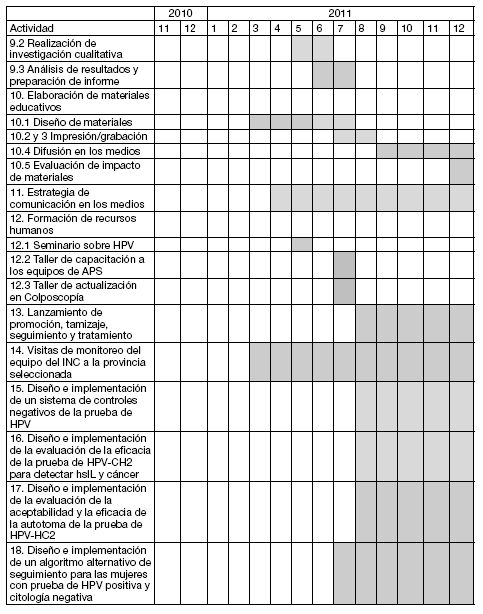
PRESUPUESTO
ESTIMADO
| Actividad |
Costo
unitario |
Total |
| 1.
Constitución Consejo Asesor |
|
|
| 1.1
Viajes 2 miembros internacionales |
9000 |
18000 |
| 2.
Firma de Acta Acuerdo con el Ministerio de Salud de la Provincia |
|
|
| 2.1
Reunión con el Ministro de Salud de la Provincia de Jujuy (viaje a la
provincia, pasajes y viáticos) |
2000 |
4000 |
| 2.2
Reunión con directores provinciales y jefes de servicio involucrados
para la presentación del proyecto (viaje a la provincia, pasajes y
viáticos) |
2000 |
4000 |
| 2.3
Elaboración de Acta Acuerdo |
|
|
| 2.4
Firma de Acta Acuerdo |
|
|
| 3.
Reorganización de la red de citología de la provincia |
|
|
| 4.
Instalación del Laboratorio de HPV en el Hospital Soria |
|
|
| 4.1
Creación de un espacio físico para su funcionamiento |
|
|
| 4.2
Montaje del laboratorio de HPV (instalación de equipos) |
|
|
| 4.3
Elaboración y publicación de guías y normas de procedimientos |
40 |
800 |
| 4.4
Designación y contratación del personal a cargo del laboratorio |
|
|
| 4.5
Capacitación del personal en Qiagen Brasil |
|
|
| 5.
Armado de la red de referencia y sistema de transporte de muestras |
|
|
| 5.1
Diseño de la red de referencia |
|
|
| 5.2
Definición e implementación de sistemas de transporte de muestras |
|
|
| 6.
Diseño de protocolo de toma, lectura, seguimiento y tratamiento |
|
|
| 6.1
Armado de protocolo de toma, seguimiento y tratamiento |
|
|
| 6.2
Elaboración y publicación de manuales y guías para los equipos de salud |
40 |
4000 |
| 7.
Toma de muestras |
|
|
| 7.1
Definición de efectores y personal a cargo de la toma |
|
|
| 7.2
Capacitación de tomadores de muestra |
10000 |
30000 |
| 8.
Sistema de Información para el Monitoreo y Evaluación |
|
|
| 8.1
Contratación del informático a cargo del SITAM para el diseño del nodo
Laboratorio de HPV |
3000 |
36000 |
| 8.2
Capacitación a usuarios del SITAM (2) |
5000 |
10000 |
| 9.
Investigación formativa |
|
|
| 9.1
Realización de investigación cualitativa |
|
60000 |
| 9.2
Análisis de resultados y preparación de informe |
|
|
| 10.
Elaboración de materiales educativos |
|
|
| 10.1
Diseño de materiales |
|
|
| 10.2
Impresión de folletos/afiches |
8 |
160000 |
| 10.3
Grabación de spots |
3000 |
3000 |
| 10.4
Difusión en los medios |
|
|
| 10.5
Evaluación de impacto de materiales |
|
80000 |
| 11.
Estrategia de comunicación en los medios |
|
|
| 12.
Formación de recursos humanos |
|
|
| 12.1
Seminario sobre HPV |
|
300000 |
| 12.2
Talleres de capacitación a los equipos de APS |
|
50000 |
| 12.3
Talleres de actualización en colposcopía |
|
50000 |
| 13.
Lanzamiento de promoción, tamizaje, seguimiento y tratamiento |
|
60000 |
| 14.
Visitas de Monitoreo a la Provincia (2 viajes x mes, pasaje y viáticos) |
5000 |
60000 |
| 15.
Diseño e implementación de un sistema de controles negativos de la
prueba de HPV |
|
|
| 16.
Diseño e implementación de la evaluación de la eficacia de la prueba de
HPV-CH2 para detectar hsIL y cáncer |
|
65000 |
| 17.
Diseño e implementación de la evaluación de la aceptabilidad y la
eficacia de la autotoma de la prueba de HPV-HC2 |
|
160000 |
| 18.
Diseño e implementación de un algoritmo alternativo de seguimiento para
las mujeres con prueba de HPV positiva y citología negativa |
|
25000 |
| 19.
Prueba de HPV (30000 por año) |
68 |
2040000 |
| TOTAL |
|
3219800 |
ANEXO
II. Equipamiento a transferir a la provincia de Jujuy

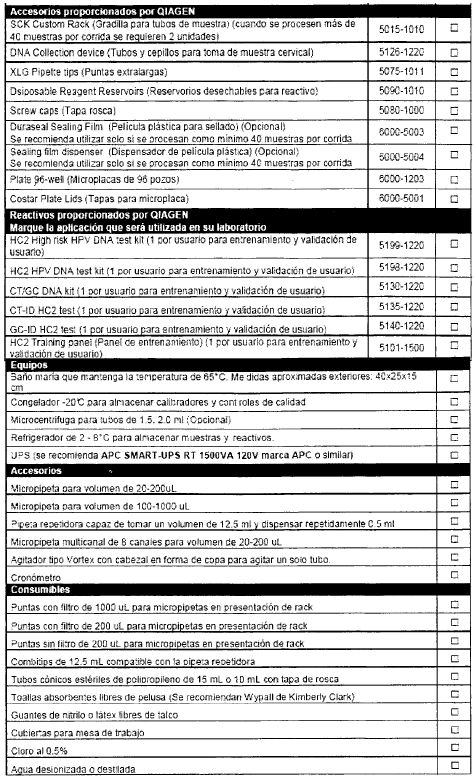
(1) Prueba de detección de ADN del virus de Papiloma Humano (HPV) por
captura de Hóbridos (HC2).







