MINISTERIO
DE SALUD
INSTITUTO NACIONAL CENTRAL UNICO
COORDINADOR DE ABLACION E IMPLANTE
Resolución Nº 119/2012
Bs. As., 23/5/2012
VISTO el expediente Nº 1-2002-4638000068/12-9 y las funciones asignadas
a este INSTITUTO NACIONAL CENTRAL UNICO COORDINADOR DE ABLACION E
IMPLANTE (INCUCAI) por la Ley Nº 24.193 (t.o. Ley Nº 26.066), el
Decreto Nº 512/95 (t.o. Decreto Nº 1949/06) y las Resoluciones del
Ministerio de Salud Nº 610/07 y Nº 1480/11, y
CONSIDERANDO:
Que en el marco de las normas señaladas en el visto, este Organismo
Nacional resulta competente para regular los procesos vinculados a la
utilización de células de origen humano para su implante en seres
humanos, garantizando que los mismos sean operados bajo programas de
garantía de calidad, como así también determinar las condiciones
edilicias, ambientales y de seguridad física y biológica que deben
reunir los establecimientos involucrados.
Que el avance científico de los últimos años ha conducido al desarrollo
de terapias avanzadas, como la celular y la medicina regenerativa,
áreas imbuidas de reconocido espíritu innovador, aunque aún muchas de
ellas todavía en etapa experimental.
Que en concordancia con lo expresado por las Directivas Europeas
2004/23/EC, Reglamento (CE) 1394/2007, y la Resolución WHA 63.22 de la
Organización Mundial de la Salud, el uso clínico de tejidos y células
de origen humano debe ser definido en forma transparente, en base a una
evaluación objetiva de las necesidades médicas.
Que debe tenerse en cuenta que el uso de tejidos y células para
aplicación en el cuerpo humano puede provocar enfermedades y/o efectos
indeseados, que deben ser advertidos al receptor mediante un informe
escrito seguido del respectivo consentimiento informado.
Que asimismo, es menester garantizar la trazabilidad de las células y
tejidos, entendiendo por ello la capacidad de localizar e identificar
los mismos durante cualquier etapa, desde su obtención, pasando por el
procesamiento, evaluación y almacenamiento, hasta su distribución al
receptor o su desestimación o eliminación.
Que dichos procesos deben incluir la capacidad de identificar al
donante, al banco de tejidos y de células, las instalaciones que los
reciben, procesan o almacenan; a los receptores y cualquier producto y
material que entre en contacto con esos tejidos y células que puedan
afectar la calidad y seguridad de los mismos.
Que según se refiere en la Guía para Investigaciones en Salud Humana,
aprobada por Resolución Nº 1480/11 del Ministerio de Salud, los
productos utilizados en forma experimental deben ser elaborados,
manejados y almacenados conforme a normas específicas, tanto en la
investigación clínica como en la elaboración de preparaciones celulares
aprobadas para su aplicación terapéutica.
Que al igual que en el trasplante de órganos, en las prácticas
relacionadas con la utilización de células y tejidos se debe respetar
el anonimato del receptor y del donante, y preservar el altruismo y
solidaridad de éste último.
Que la fiscalización a los establecimientos Elaboradores de
Preparaciones Celulares (EPC), a través de inspecciones técnicas
efectuadas por las autoridades sanitarias, es un mecanismo idóneo que
contribuye a garantizar la calidad de tales preparaciones.
Que dicha fiscalización, debe cubrir aspectos relativos a condiciones
de funcionamiento y sistemas de control de calidad utilizados por los
establecimientos alcanzados por esta normativa, contando con un modelo
que asegure uniformidad de criterio; neutralidad, simetría y
reciprocidad en el tratamiento y aplicación de las normas de regulación.
Que en este sentido, resulta necesario contar con una reglamentación
clara y precisa que establezca normas o guías tendientes a garantizar
la calidad y la seguridad de estas prácticas, con el fin de
salvaguardar la salud pública.
Que la Dirección Científico Técnica ha elaborado una propuesta de
normas de buenas prácticas de elaboración y laboratorio para
preparaciones celulares, juntamente con la Comisión Asesora de expertos
en la materia, convocados a tal efecto.
Que el Registro Nacional de Donantes de Células Progenitoras
Hematopoyéticas (CPH) ha considerado adecuada la propuesta establecida
para asegurar la calidad de los procedimientos, en los cuales se
trabaja con células para su posterior infusión en seres humanos.
Que el Registro Nacional de Donantes de Células Progenitoras
Hematopoyéticas, la Dirección Científico Técnica y el Departamento de
Asuntos Jurídicos han tomado la intervención de su competencia.
Que la Comisión Federal de Trasplante ha tomado la intervención de su
competencia.
Que se actúa en uso de las facultades conferidas por el artículo 44,
inciso b), de la Ley Nº 24.193 (t.o. Ley Nº 26.066) y las Resoluciones
M.S. Nº 610/07 y Nº 1480/11.
Que la medida que se adopta ha sido considerada y aprobada por el
Directorio en su sesión ordinaria del día 23 mayo de 2012, según consta
en Acta Nº 15.
Por ello,
EL DIRECTORIO DEL INSTITUTO NACIONAL CENTRAL UNICO COORDINADOR DE
ABLACION E IMPLANTE
RESUELVE:
ARTICULO 1º — Apruébanse las “NORMAS PARA LAS BUENAS PRACTICAS DE
ELABORACION Y LABORATORIO PARA PREPARACIONES CELULARES” que, como ANEXO
I, forma parte integrante de la presente resolución.
ARTICULO 2º — Apruébanse los “CRITERIOS DE MANIPULACION CELULAR QUE NO
IMPLIQUEN MODIFICACION SUSTANCIAL DE LA PREPARACION CELULAR” que, como
ANEXO II, integra la presente resolución.
ARTICULO 3º — Apruébanse los “CRITERIOS DE ELEGIBILIDAD DE DONANTES DE
CELULAS Y TEJIDOS PARA LA ELABORACION DE PREPARACIONES CELULARES” que,
como ANEXO III, forma parte integrante de la presente resolución.
ARTICULO 4º — Dispónese que los establecimientos clasificados en el
ANEXO I como Elaboradores de Preparaciones Celulares (EPC) 1, que con
anterioridad al dictado de esta norma realicen las actividades
reguladas por la misma, contarán con un plazo de veinticuatro (24)
meses desde su entrada en vigencia, para adecuarse a los requisitos
establecidos en la presente.
(Nota Infoleg: por art. 1° de la Resolución N° 223/2014
del Instituto Nacional Central Único Coordinador de Ablación e Implante
B.O. 8/7/2014 se prorroga hasta el 8 de junio de 2015 el plazo
establecido en el presente artículo, para
que los establecimientos clasificados como Elaboradores de
Preparaciones Celulares (EPC) tipo 1 puedan adecuarse a los requisitos
establecidos en ésta norma)
ARTICULO 5º — Dispónese que los establecimientos definidos en el ANEXO
I como Elaboradores de Preparaciones Celulares (EPC) 2, que con
anterioridad al dictado de la presente norma realicen las actividades
reguladas por la misma, dispondrán de un plazo de doce (12) meses desde
su entrada en vigencia, para adecuarse a los requisitos establecidos en
la presente.
ARTICULO 6º — Dispónese que quedan excluidos de la aplicación de la
presente norma, los bancos de tejidos de origen humano con fines
terapéuticos, cuyo funcionamiento se encuentra regulado por la
Resolución INCUCAI Nº 118/09 o las que eventualmente la deroguen o
modifiquen.
ARTICULO 7º — Regístrese. Notifíquese a la Secretaría de Políticas,
Regulación e Institutos del Ministerio de Salud de la Nación, a la
Sociedad Argentina de Trasplantes, a las Sociedades Científicas
pertinentes, a las Autoridades Sanitarias y Organismos Jurisdiccionales
de Ablación e Implante, al Consejo Asesor de Pacientes y a todos los
equipos de trasplante de Células Progenitoras Hematopoyéticas (CPH)
autorizados. Comuníquese a las áreas competentes del Instituto. Dése a
la Dirección Nacional del Registro Oficial para su publicación.
Cumplido, archívese. — Dr. CARLOS A. SORATTI, Presidente, INCUCAI. —
Dr. MARTIN TORRES, Vicepresidente, INCUCAI.
ANEXO I
“NORMAS PARA LAS
BUENAS PRACTICAS DE ELABORACION Y LABORATORIO PARA PREPARACIONES
CELULARES”
INTRODUCCION
1- DISPOSICIONES GENERALES
1.1- GENERALIDADES
1.2- REQUERIMIENTOS
1.3- APLICABILIDAD
1.4- PROGRAMA DE ASEGURAMIENTO DE
CALIDAD
2- REQUISITOS DEL SISTEMA DE CALIDAD
2.1- OBJETIVO DE CALIDAD
2.1.1- Responsabilidad
2.1.2- Garantía de Calidad
2.2- RESPONSABILIDAD DE LA DIRECCION
DEL EPC
2.2.1- Política de Calidad
2.2.2- Organización
2.2.3- Responsable de Calidad del EPC
2.2.4- Revisión de la Dirección del
EPC
2.3- AUDITORIA DE CALIDAD
2.4- PERSONAL
2.4.1- Instrucciones Generales
2.4.2- Entrenamiento
2.4.3- Consultores
3- ELABORACION DE PREPARACIONES
CELULARES
3.1- LOCALES
3.2- EQUIPAMIENTO
3.2.1- Programación de mantenimiento
3.2.2- Inspección
3.2.3- Ajustes
3.2.4- Calibración
3.2.5- Patrones de calibración
3.2.6- Registros de Calibración
3.2.7- Instalaciones
3.3- PROCESO
3.4- PERSONAL
3.5- VESTIMENTA DEL PERSONAL
3.6- MATERIAS PRIMAS
3.6.1- Identificación y selección
3.6.2- Aptitud
3.6.3- Caracterización
3.6.4- Sueros de origen animal
3.6.5- Garantía de Calidad
3.7- MATERIALES DE ACONDICIONAMIENTO
3.8- MATERIALES DE DESECHO
3.9- CARACTERIZACION DE BANCOS DE
CELULAS
3.9.1- Banco Maestro de Células (BMC)
3.9.2- Banco Celular de Trabajo (BCT)
3.10- ESPECIFICACIONES
3.11- CONSIDERACIONES PARA LA
VALIDACION
3.12- FUENTE DE CELULAS
3.12.1- Células de Origen Autólogo
3.12.2- Células de origen alogénico
4- DOCUMENTOS Y REGISTROS
4.1- OBJETIVOS
4.2- GENERALIDADES
4.2.1- Aprobación y emisión de
documentos
4.2.2- Distribución de documentos
4.2.3- Modificación de documentos
4.2.4- Registros de modificaciones de
documentos. Control de cambios
4.2.5- Registro de reclamos y no
conformidad
4.2.6- Contenidos
4.2.7- Conservación
4.3- DOCUMENTOS REQUERIDOS
4.3.1- Solicitud del médico tratante
4.3.2- Rotulado – Etiquetado
4.3.3- Especificaciones y
procedimientos de análisis
4.3.4- Especificaciones para materias
primas y material de acondicionamiento
4.3.5- Especificaciones para
Preparaciones terminadas
4.3.6- Procedimientos operativos
estandarizados (POE) y otros registros
4.3.7- Reclamos
4.3.8- Documentación del donante
4.3.8.1- Certificado de elegibilidad
4.3.8.2- Consentimiento informado
4.3.8.2.1- Donación con fines
terapéuticos
4.3.8.2.2- Donación con fines de
investigación clínica
5- ESTRUCTURA EDILICIA
5.1- GENERALIDADES
5.2- CIRCUITO LOGISTICO/LOCALES Y AREAS
5.2.1- Areas Auxiliares
5.2.2- Areas de Depósito
5.2.3- Area de pesada
5.2.4- Area de Control de Calidad
5.2.5- Area administrativa y de
archivo
5.2.6- Area de decontaminación,
lavado y esterilizado de materiales y equipos utilizados en el
procesamiento
5.2.7- Areas de elaboración de
Preparaciones celulares
5.2.7.1- Generalidades
5.2.7.2- Areas limpias
6- IDENTIFICACION Y TRAZABILIDAD
7- CONTROLES Y ENSAYOS
7.1- GENERALIDADES
7.2- CONTROL DE CALIDAD
7.2.1- Control de materias primas
7.2.2- Controles de recepción de
fuentes de células
7.2.3- Controles y ensayos durante el
procesamiento
7.2.4- Controles de Preparación
terminada
7.2.4.1- Consideraciones generales
7.2.4.2- Seguridad
7.2.4.2.1- Controles de esterilidad
7.2.4.2.2- Micoplasma
7.2.4.2.3- Virus adventicios
7.2.4.3- Ensayos para determinación
de dosis
7.2.4.4- Potencia
7.2.4.5- Pureza
7.2.4.6- Identidad
7.2.4.7- Estabilidad
7.2.4.7.1- Consideraciones generales
7.2.4.7.2- Desarrollo del protocolo
de estabilidad
7.3- REVISION DE REGISTRO DE LA
PREPARACION CELULAR
7.4- REGISTROS DE CONTROLES Y ENSAYOS
7.5- LIBERACION Y ADMINISTRACION DE
PREPARACIONES CELULARES
7.5.1- Consideraciones generales
7.5.2- Liberación de la Preparación
Celular final
7.5.3- Administración a pacientes
7.6- RESULTADOS DE MEDICIONES Y ENSAYOS
7.7- CONTROL AMBIENTAL
7.8- PROCESOS AUTOMATIZADOS
8- CALIFICACION Y VALIDACION
9- MATERIALES Y PREPARACIONES NO
CONFORMES
10- ACCION CORRECTIVA
11- EMBALAJE, ROTULADO Y TRANSPORTE
11.1- EMBALAJE DE FUENTES DE CELULAS Y
PREPARACIONES CELULARES
11.2- ROTULADO
11.2.1- Integridad de los rótulos
11.2.2- Inspección de los rótulos e
instructivos
11.2.3- Almacenamiento de los rótulos
11.2.4- Control de los rótulos
11.3- DOCUMENTACION
11.4- TRANSPORTE
11.4.1- Condiciones del Transporte
11.4.2- Organización del circuito
11.4.3- Modo de Transporte
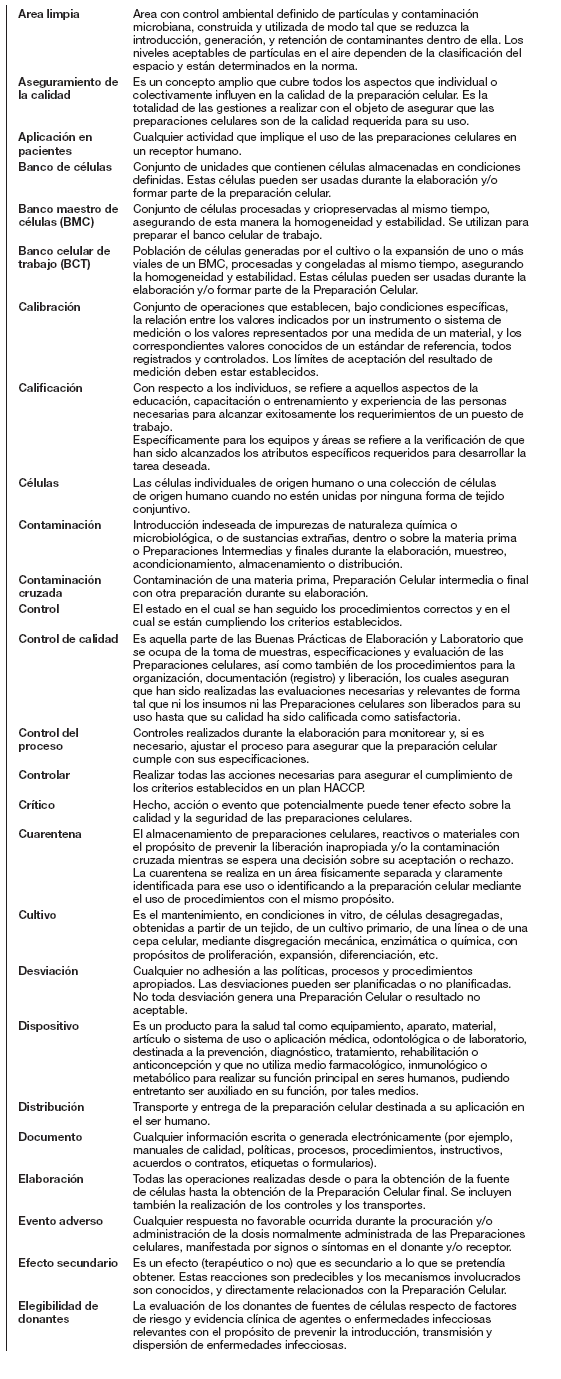
12- GLOSARIO
INTRODUCCION
Este documento proporciona normas y procedimientos para ser utilizados
por los responsables de realizar terapias con células humanas, con o
sin manipulación de las mismas, como así también, preparaciones
biológicas que las contengan. Asimismo, aporta la información vinculada
a la obtención, elaboración, regulación, análisis y control de calidad
que deberá ser incluida en un protocolo de investigación y en el
desarrollo de prácticas de técnica corriente, a fin de proporcionar un
producto de pureza validada, seguro y eficaz.
Esta norma también se aplica a las preparaciones con células
modificadas por terapia génica y a las preparaciones de combinación que
contienen células humanas y un medicamento o dispositivo como parte de
la preparación celular final. Además, instruye a los revisores y
fiscalizadores de INCUCAI sobre la información que deben evaluar y
registrar como parte del material requerido, y establece los
procedimientos a seguir por los centros, laboratorios o industrias que
elaboran las preparaciones celulares, desde ahora denominados:
Elaboradores de Preparaciones Celulares (EPC).
Las terapias con células humanas deben enfrentar determinadas
condiciones en el proceso de aislamiento, producción y elaboración.
Algunos de estos desafíos incluyen la variabilidad y complejidad
inherentes a los componentes utilizados para generar la preparación
celular final, como el origen de las células, la contaminación
potencial por agentes adventicios, la necesidad de procesamiento
aséptico, y las peculiares condiciones de obtención de la preparación
celular final, ya que la misma contiene células vivas.
La distribución de estas preparaciones también puede constituir un
desafío debido a los problemas de estabilidad y al breve período de
vida útil que tienen, requiriendo, en algunos casos, liberar la
preparación celular para su administración antes de contar con los
resultados finales de determinadas pruebas.
Esta norma permite el control de los centros Elaboradores de
Preparaciones celulares (EPC), con uniformidad de criterio,
neutralidad, equidad y transparencia en los procedimientos, en
salvaguarda de la salud de la población.
1-
DISPOSICIONES GENERALES
1.1-
Generalidades
Dentro del concepto de Garantía de Calidad, las NORMAS PARA LAS BUENAS
PRACTICAS DE ELABORACION y LABORATORIO PARA PREPARACIONES CELULARES
(BPEyL) constituyen el factor que asegura que las preparaciones se
fabriquen en forma uniforme y controlada, de acuerdo con las normas de
calidad adecuadas al uso que se pretende dar a las mismas y en
conformidad con los requerimientos del INCUCAI. El objetivo principal
de las reglamentaciones que rigen las BPEyL es disminuir los riesgos
inherentes a toda preparación celular destinada para su uso clínico.
Dichos riesgos son esencialmente de tres tipos: contaminación (por
contaminantes inesperados), mezclas (confusión causada, por ejemplo,
por rótulos falsos colocados en los envases) y desarrollo de tumores u
otro tipo de síndromes proliferativos. Dada su relativamente reciente
aplicación en la clínica no pueden descartarse en algunos casos,
efectos de índole inmunológica y genética.
1.2-
Requerimientos
El texto de las BPEyL exige:
a) que todos los procesos de elaboración se definan claramente, se
revisen sistemáticamente a la luz de la experiencia y se compruebe que
son los procedimientos adecuados para elaborar preparaciones celulares,
a fin de cumplir con las especificaciones para el uso que se le
pretende dar;
b) que se lleven a cabo calificaciones y validaciones;
c) la provisión de todos los recursos necesarios, incluyendo:
1) personal entrenado y apropiadamente calificado,
2) instalaciones y espacios adecuados,
3) servicios y equipamientos adecuados,
4) rótulos, envases y materiales apropiados,
5) instrucciones y procedimientos aprobados,
6) transporte y depósito apropiados,
7) personal, laboratorios y equipamiento adecuado para controles de
proceso y finales;
d) que las instrucciones y procedimientos se redacten en un lenguaje
claro e inequívoco, que sean específicamente aplicables a los medios de
elaboración disponibles;
e) que se mantengan registros (en forma manual y/o electrónica) durante
la elaboración, para demostrar que todas las operaciones exigidas por
los procedimientos e instrucciones definidos se han efectuado y que la
cantidad y calidad de la preparación celular sean las previstas.
Cualquier desviación deberá registrarse e investigarse exhaustivamente;
f) que todos los registros que permiten conocer la historia completa de
un lote se mantengan completos y accesibles;
g) que el almacenamiento y la distribución de las preparaciones sean
adecuados para minimizar cualquier riesgo de disminución de la calidad;
h) que se establezca un sistema que haga posible el retiro de cualquier
Preparación, en cualquier etapa entre su liberación y su utilización,
i) que se estudie todo reclamo contra una Preparación ya liberada, como
así también que se investiguen las causas de los defectos de calidad y
se adopten medidas apropiadas para prevenir que los defectos se repitan.
1.3-
Aplicabilidad
Las NORMAS PARA LAS BUENAS PRACTICAS DE ELABORACION y LABORATORIO PARA
PREPARACIONES CELULARES (BPEyL) establecen los requisitos aplicables a
aquellas preparaciones conformadas por células destinadas a su
utilización clínica en seres humanos. Estos requisitos regulan todas
las actividades relacionadas con la obtención, el procesamiento, el
almacenamiento, la distribución y el transporte de las preparaciones
celulares destinadas a su utilización clínica en seres humanos, a fin
de garantizar que cada preparación sea de pureza validada, segura y
eficaz, tanto para ensayos clínicos como para terapéuticas establecidas:
I) Se aplica a tejidos y células, destinados a la elaboración de
preparaciones celulares, incluidas células progenitoras hematopoyéticas
(CPH) de sangre periférica, médula ósea (MO) y cordón umbilical
(sangre), y otras células troncales.
II) También se aplica a las preparaciones de combinación que contienen
células humanas y un medicamento o dispositivo como parte de la
preparación final.
III) Se aplica a las preparaciones celulares o de combinación que
utilizan células que han sido modificadas genéticamente.
IV) Se aplica a los procesos de elaboración de cualquier preparación
celular, incluyendo aquellas destinadas a estudios de investigación
clínica.
V) Determina que el EPC es un establecimiento público o privado que
realiza actividades relacionadas con la elaboración de células humanas
en la investigación clínica y/o aplicación terapéutica. El EPC es
responsable de todos los procedimientos relacionados con la elaboración
de preparaciones celulares, desde la obtención de la fuente de células
hasta la obtención de la preparación celular, incluyendo el empaque, el
almacenamiento, las pruebas de control de calidad, y la liberación para
su transporte y uso.
VI) Determina que en el caso que el EPC realice investigación básica o
preclínica, la misma debe ser efectuada en ambientes separados de donde
se realiza la elaboración y/o manipulación de células para uso humano.
VII) Clasifica a las preparaciones celulares en dos grupos:
Preparaciones Celulares con Manipulación Mínima (PCMM) y Preparaciones
Celulares con Manipulación Avanzada (PCMA). Las PCMM son aquellas
preparaciones que son sometidas a una o varias de las manipulaciones
descriptas en el ANEXO II. Toda preparación celular que implique alguna
manipulación adicional a las descriptas en el ANEXO II, será definida
como PCMA.
VIII) Los EPC se clasificarán de acuerdo con el tipo de manipulación
que realicen. Así, los EPC que realicen PCMM, se clasifican como EPC
tipo 1 y los que realicen PCMA, se clasifican como EPC tipo 2. En los
EPC tipo 1, sólo se podrán realizar las prácticas celulares descriptas
en el ANEXO II (PCMM). En los EPC tipo 2 se podrán elaborar PCMM y PCMA.
IX) En el caso de existir dudas sobre la clasificación de una
preparación celular, todo EPC podrá solicitar asesoramiento del INCUCAI
para determinar si existen bases científicas para que su preparación
quede encuadrada en la definición de PCMM o PCMA.
X) Para preparaciones que clasifiquen como PCMA y cuya elaboración
incluya tecnología no contemplada en este documento, deberá
confeccionarse una guía complementaria por parte del EPC que deberá ser
aprobada por la autoridad regulatoria.
XI) Consecuencias del no cumplimiento de los requisitos:
- El no cumplimiento de cualquiera de los requisitos aplicables de esta
norma, convierte a la preparación en no apta para uso clínico, por lo
que deberá ser dispuesta (según el punto 3.8), quedando el
correspondiente registro. Toda situación de excepción deberá contar con
la correspondiente justificación, registro, indicación médica y
consentimiento informado, notificando de ello al INCUCAI.
XII) Las BPEyL no cubren los aspectos relacionados con la seguridad del
personal comprometido ni la protección del medio ambiente. El
elaborador deberá garantizar la seguridad de los trabajadores y tomar
las medidas necesarias para prevenir la contaminación del medio
ambiente según legislación vigente. Deberán estar en concordancia con
las normativas de bioseguridad de la Organización Mundial de la Salud
(Manual de Bioseguridad en el Laboratorio).
1.4-
Programa de Aseguramiento de Calidad
Cada EPC deberá establecer y mantener un sistema de calidad para
asegurar que los requisitos de esta norma sean alcanzados y que las
preparaciones celulares sean seguras y eficaces, adecuadas al uso
pretendido.
Como parte de las actividades de su sistema de calidad, cada EPC deberá
establecer y mantener políticas, instrucciones y procedimientos
eficaces del sistema de calidad de acuerdo con las exigencias de esta
norma.
2-
REQUISITOS DEL SISTEMA DE CALIDAD
2.1-
Objetivo de calidad
2.1.1- Responsabilidad
El EPC es responsable por la calidad de la preparación, asegurando que
la misma sea apta para el uso previsto, cumpliendo con los
requerimientos establecidos en la presente norma. Asimismo, asume la
responsabilidad de no poner en riesgo a los pacientes debido a razones
de seguridad, calidad o eficacia inadecuadas. Para que sea posible
alcanzar el mencionado objetivo de calidad se debe contar con un
sistema de Garantía de Calidad de amplio alcance y correctamente
aplicado, que incorpore las BPEyL.
2.1.2- Garantía de Calidad
Es preciso que el sistema de Garantía de Calidad sea plenamente
documentado y que su eficacia sea controlada. Todas las partes del
mismo deben ser atendidas por personal competente y es necesario que se
disponga de áreas, equipos e instalaciones adecuadas. El sistema de
garantía de calidad deberá asegurar que:
a) La elaboración de las preparaciones sean diseñadas y desarrolladas
de forma tal que condigan con los requerimientos de BPEyL,
b) las operaciones de elaboración y control estén claramente
especificadas en forma escrita y se adapten a los requerimientos de las
BPEyL,
c) las responsabilidades de gestión de la actividad estén claramente
especificadas en las descripciones de trabajo,
d) las gestiones para la elaboración, provisión y uso de las materias
primas y materiales de acondicionamiento deben estar aprobadas para el
uso que se propone,
e) se lleven a cabo todos los controles necesarios en materias primas,
preparaciones intermedias y finales, controles de proceso,
calibraciones y validaciones,
f) la preparación final sea correctamente elaborada y controlada de
acuerdo con procedimientos definidos,
g) las preparaciones no sean provistas o utilizadas antes de que las
personas autorizadas hayan certificado que las mismas cumplen con los
requerimientos de elaboración y control establecidos por esta norma,
h) las preparaciones sean almacenadas, distribuidas y manipuladas de
manera tal que se conserve la calidad durante su vida útil,
i) regularmente se efectúen auditorías internas de calidad para evaluar
la efectividad y aplicabilidad del sistema de calidad,
j) los desvíos de calidad sean reportados, investigados y exista
registro de los mismos,
k) exista un sistema que permita aprobar aquellos cambios que puedan
tener un impacto sobre la calidad de la preparación,
l) se lleven a cabo evaluaciones regulares de la calidad de las
preparaciones, con el objeto de verificar la consistencia de los
procesos y asegurar su mejora continua mediante indicadores u otra
herramienta apropiada.
2.2-
Responsabilidad de la Dirección del EPC
2.2.1- Política de Calidad
Cada EPC deberá establecer su política y sus objetivos de cumplimiento
con respecto a la calidad. También deberá mantener la política en todos
los niveles de la organización y asegurar que sea comprendida por todo
el personal que pudiera afectar o influenciar la calidad de la
preparación.
2.2.2- Organización
Cada EPC deberá establecer y mantener una estructura organizacional
adecuada con personal suficiente para asegurar que las preparaciones
sean elaboradas de acuerdo con los requisitos de esta norma.
2.2.3- Responsable de Calidad del EPC
La Dirección de cada EPC deberá designar un responsable que,
independientemente de otras funciones, tendrá autoridad establecida
para:
a) asegurar que los requisitos del sistema de calidad sean establecidos
y mantenidos en conformidad con esta norma;
b) informar el desempeño del sistema de calidad a la Dirección del EPC
para revisar y proveer información sobre la mejoría del mismo. La
designación del responsable deberá estar documentada;
c) iniciar o implementar acciones para prevenir la ocurrencia de
errores;
d) identificar o documentar problemas de calidad;
e) iniciar, recomendar, proveer o implementar soluciones o acciones
correctivas para los problemas de calidad;
f) administrar o controlar la distribución o la disposición de
materiales de procesamiento, envasado y embalaje de la preparación.
2.2.4- Revisión de la Dirección del
EPC
La Dirección del EPC deberá revisar la adecuación y la efectividad del
sistema de calidad en intervalos definidos y con frecuencia
suficientes, para asegurar que satisfaga las exigencias de esta norma y
que atienda los objetivos de la política de calidad establecida. La
revisión de la Dirección deberá ser conducida de acuerdo con los pasos
establecidos en sus procedimientos operativos estándares (POEs) y los
resultados deberán ser documentados.
2.3-
Auditoría de Calidad
Cada EPC deberá realizar auditorías internas para verificar si el
sistema de calidad está en conformidad con los requisitos establecidos.
Las auditorías de calidad deberán ser conducidas por personal
adecuadamente entrenado, de acuerdo con los procedimientos
establecidos, y que no tenga responsabilidades directas en las materias
que están siendo objeto de la auditoría. Deberá hacerse un informe de
cada auditoría de calidad y éste deberá ser revisado por la Dirección
con responsabilidades sobre las materias auditadas. Cuando sea
necesario, se deberán efectuar acciones correctivas, de seguimiento, y
deberán ser documentadas.
2.4-
Personal
2.4.1- Instrucciones Generales
Cada EPC deberá contar con personal en número suficiente con
instrucción, experiencia, entrenamiento y práctica para asegurar que
todas las actividades previstas en esta norma sean correctamente
desempeñadas.
2.4.2- Entrenamiento
Cada EPC deberá asegurar que todo el personal sea entrenado para
ejecutar adecuadamente las tareas a él asignadas. El entrenamiento
deberá ser conducido de acuerdo con los procedimientos establecidos por
personas calificadas, a fin de garantizar que los integrantes del EPC
tengan una comprensión perfecta de sus funciones regulares y de los
equipos de esta norma aplicables a sus funciones. El entrenamiento del
personal deberá estar documentado.
2.4.3- Consultores
Cada EPC deberá asegurar que cualquier consultor que asesore sobre
métodos empleados o en los controles utilizados en los procedimientos
comprendidos desde la selección del paciente o del donante, obtención
de las células u obtención de la fuente de células o línea celular,
procesamiento, almacenamiento, distribución y transporte de las
preparaciones celulares, tenga calificaciones suficientes (instrucción,
entrenamiento, experiencia) para aconsejar sobre los asuntos para los
cuales fue consultado.
Cada EPC deberá mantener registros relativos a cada consultor. Estos
registros deben incluir nombre, dirección, calificaciones, incluyendo
copia de “curriculum vitae” y una lista de empleos o cargos
desempeñados con anterioridad, así como una descripción específica de
los asuntos en que presta su consultoría.
3-
ELABORACION DE PREPARACIONES CELULARES
3.1-
Locales
El procesamiento aséptico de células o tejidos, la apertura de
embalajes y/o la ruptura de sistemas cerrados, deben ser realizados
solamente en una cabina de bioseguridad tipo II, grado A o clase 100.
Para el caso de procesamientos de PCMA dicha cabina deberá estar
ubicada dentro de una sala grado C o clase 10.000 como mínimo (ver
Tabla 1 de la sección 5.2.7.2- “Areas limpias”). Estas zonas deben
estar equipadas con un indicador de gradiente de presión que debe ser
controlado y registrado a diario durante los períodos de funcionamiento.
La manipulación de componentes y materiales de partida estériles, salvo
que se sometan a esterilización a través de un filtro que retenga los
microorganismos en una fase posterior del proceso, debe realizarse en
grado A.
3.2-
Equipamiento
Cada EPC deberá asegurar que todos los equipamientos utilizados en las
distintas etapas de procesamiento y controles sean adecuados al uso
pretendido y correctamente diseñados, construidos, colocados e
instalados para facilitar el mantenimiento, ajuste, limpieza y uso.
Cada EPC deberá establecer y mantener procedimientos para asegurar que
el equipamiento sea rutinariamente calibrado, inspeccionado y
controlado. Deberán ser mantenidos registros documentados de estas
actividades.
3.2.1- Programación de mantenimiento
Cada EPC deberá establecer y mantener una programación para el
mantenimiento, ajustes y, cuando fuera el caso, limpieza del
equipamiento, para asegurar que todas las especificaciones de
procesamiento estén siendo alcanzadas. El programa de mantenimiento
deberá ser fijado en un lugar de gran visibilidad cerca de cada
equipamiento, o al alcance del personal encargado del mantenimiento. Se
deberá confeccionar un registro por escrito documentando, la fecha en
que la programación fue ejecutada y los responsables encargados de las
actividades de mantenimiento.
3.2.2- Inspección
Cada EPC deberá conducir controles periódicos de acuerdo con
procedimientos establecidos para asegurar el cumplimiento de los
programas de mantenimiento de equipamientos. Los controles, incluyendo
fecha y firma del responsable, deben ser documentados.
3.2.3- Ajustes
Cada EPC deberá asegurar que cualquier tolerancia aceptable o límite
inherente sea colocado en lugar visible cerca del equipamiento que
necesite de ajustes periódicos, o estén fácilmente disponibles al
personal encargado de esos ajustes.
3.2.4- Calibración
Cada EPC deberá establecer y mantener procedimientos de calibración
adecuados que incluyan orientaciones específicas y límites de precisión
y exactitud, así como prescripciones para acciones correctivas cuando
los límites de precisión y exactitud no fueran alcanzados. La
calibración deberá ser ejecutada por personal idóneo para tal fin.
3.2.5- Patrones de calibración
Cada EPC deberá establecer y mantener patrones de calibración para los
equipamientos de medición, que sean trazables a los nacionales. Si
éstos no fueran prácticos o no estuvieran disponibles, deberá usarse un
patrón independiente reproducible. Si no hubiera ningún otro aplicable,
se deberá establecer y mantener uno propio, con la aprobación del
INCUCAI.
3.2.6- Registros de Calibración
Cada EPC deberá asegurar que sean mantenidos registros de las fechas de
calibración, del personal encargado de esta tarea y de la fecha
siguiente para esta operación. Los registros deben ser colocados en el
equipamiento o cerca del mismo, debiendo estar disponibles para el
personal que usa este equipamiento y para los responsables de la
calibración del mismo.
3.2.7- Instalaciones
Cada EPC deberá proteger las instalaciones y los equipamientos,
incluyendo hardware y software, contra modificaciones que puedan
invalidar la calibración.
3.3-
Proceso
Durante todas las etapas del proceso deben adoptarse precauciones para
minimizar la contaminación, incluso cuando se realice esterilización,
durante las etapas anteriores a la misma.
Cada EPC deberá establecer y mantener un programa de limpieza adecuado
para evitar la contaminación de equipamientos, materiales de
procesamiento y preparaciones en las distintas etapas de elaboración,
con el uso de materiales de limpieza, desinfección y desinsectización.
No deben elaborarse preparaciones que contengan microorganismos vivos
en áreas usadas para el procesamiento de preparaciones celulares.
Las actividades efectuadas en áreas limpias clasificadas deben
reducirse al mínimo, especialmente cuando se están efectuando
operaciones asépticas y el movimiento de personal debe ser metódico y
controlado, con el fin de evitar el excesivo desprendimiento de
partículas y dispersión de microorganismos.
La presencia de recipientes y materiales que pueden desprender fibras
debe reducirse al mínimo en las áreas limpias y evitarse completamente
cuando se está efectuando un trabajo aséptico.
El intervalo entre el lavado y secado y la esterilización de los
componentes, recipientes y otros equipos, como también el existente
entre la esterilización y el uso, deben ser lo más breves posibles y
estar sometidos a un límite de tiempo acorde con las condiciones
validadas de almacenamiento.
El tiempo transcurrido entre el inicio de la preparación de una
solución y su esterilización o filtración a través de filtros de
retención de miocroorganismos debe ser lo más breve posible y debe ser
validado.
Todo gas utilizado para purgar una solución o un envase debe pasarse a
través de un filtro esterilizante de comprobada eficiencia.
La carga biológica de los insumos debe ser mínima antes de la
esterilización.
Todos los componentes, recipientes de preparaciones, y cualquier otro
artículo que sea necesario en las áreas limpias clasificadas donde se
efectúan trabajos asépticos se deben esterilizar y, de ser posible,
introducir a dichas áreas a través de equipos de esterilización de
doble puerta embutidos en la pared y que descarguen directamente al
área limpia clasificada. En algunas circunstancias podrían ser
aceptables otros procedimientos que dan los mismos resultados en lo que
respecta a impedir la contaminación.
Cada EPC deberá asegurar que el personal que esté en contacto con una
preparación celular o con su ambiente esté saludable, mantenga elevados
niveles de higiene y limpieza personal y se vista adecuadamente.
Cualquier persona que, a través de un examen médico o por observación
de supervisores, aparente estar en una condición que pueda afectar la
preparación celular, deberá ser excluida de las operaciones hasta que
las condiciones sean corregidas. Cada EPC deberá instruir a su personal
para que reporte cualquier situación que pueda causar la liberación de
cantidades o tipos anormales de contaminantes; es conveniente que se
efectúen exámenes periódicos para determinar si existen dichas
condiciones. Una persona competente designada a tal efecto, debe
responsabilizarse por las medidas que deban adoptarse con respecto al
personal que podría estar causando situaciones de peligro
microbiológico.
3.4-
Personal
Sólo el número mínimo necesario de personal debe estar presente en las
áreas limpias; esto es especialmente importante durante los procesos
asépticos. De ser posible, las inspecciones y los controles deben
efectuarse desde afuera de las áreas respectivas.
Todos los empleados (incluyendo el personal de limpieza y
mantenimiento) que trabajan en dichas áreas deben someterse
regularmente a programas de capacitación en disciplinas relacionadas
con la correcta elaboración de preparaciones estériles, incluyendo la
higiene y conocimientos básicos de microbiología. En caso de que sea
necesario el ingreso a las áreas de personas que no hayan recibido
dicha capacitación (por ejemplo, personal de mantenimiento contratado),
deben ser informados y supervisados cuidadosamente.
3.5-
Vestimenta del personal
Cuando fueran necesarias ropas especiales para asegurar que una
preparación sea elaborada correctamente, cada EPC deberá proveer ropas
limpias para su personal. La calidad y tipo de vestimenta del personal
debe ser acorde al lugar de trabajo y al tipo de proceso de elaboración.
Las personas que ingresan a las áreas con cabinas de seguridad
biológica clase A deben usar camisolín o mameluco, cobertor de cabeza
cubriendo totalmente el cabello, barbijo, y guantes de goma o material
plástico que no estén recubiertos con talco. Los guantes deben
desinfectarse regularmente durante las operaciones y las máscaras y los
guantes deben cambiarse para cada sesión de trabajo, como mínimo. Los
extremos de las mangas deben meterse dentro de los guantes. Es posible
que sea necesario utilizar ropas descartables. Estas medidas deben
seguirse según procedimientos operativos estándares.
Las personas que ingresan en las áreas con entorno grado C deben
cumplir todo lo mencionado en el párrafo anterior, con el agregado de
cubrebotas, no deben usar reloj de pulsera ni joyas, ni tampoco
cosméticos de los cuales puedan desprenderse partículas. Las botamangas
de los pantalones deben ser introducidas dentro de los cubrebotas. De
la vestimenta empleada prácticamente no deben desprenderse partículas o
fibras y la misma debe retener toda partícula que se desprenda del
cuerpo humano.
El cabello y, cuando corresponda, la barba deben cubrirse. Se deben
usar trajes de una o dos piezas, cerrados en las muñecas y con cuello
alto, calzados y cubre calzados apropiados. Debe ser mínimo el
desprendimiento de fibra o partícula alguna.
La vestimenta de calle no debe introducirse en los vestuarios que
llevan a las áreas de grado B y C.
La limpieza y el lavado de las ropas utilizadas en las áreas limpias
deben efectuarse de tal forma que no se les adhieran partículas
contaminantes que posteriormente puedan desprenderse de las mismas. Es
conveniente contar con instalaciones separadas para dichas ropas. Si
las ropas se deterioran debido a la limpieza o lavado inadecuados,
puede aumentar el riesgo de que de ellas se desprendan partículas. Las
operaciones de lavado y esterilización deben efectuarse de conformidad
con procedimientos operativos estándares.
3.6-
Materias primas
Se puede utilizar una amplia gama de materias primas en la elaboración
de las preparaciones celulares, a saber: células, enzimas, líquidos
biológicos, matrices poliméricas, soportes mecánicos, hidrogeles,
medios de cultivo, buffers, factores de crecimiento, citoquinas,
anticuerpos, dispositivos de separación de células, entre otros. Estas
materias primas pueden permanecer en la preparación celular final como
excipientes, o bien usarse sólo durante la elaboración como agentes
auxiliares; en este último caso, su objetivo se limitaría a interactuar
con las células pero sin que su presencia sea requerida en la
preparación celular final.
Cada EPC debe establecer y mantener criterios para la evaluación y
selección de potenciales proveedores de materias primas, conforme su
capacidad en atender los requisitos para la elaboración de las
diferentes Preparaciones celulares. Debe, además, establecer y mantener
una lista de proveedores que satisfagan los criterios documentados.
Deben ser mantenidos registros de evaluación, así como sus resultados.
En cada envío se debe controlar, como mínimo, la integridad del
embalaje, el sellado y la correspondencia entre la orden, el remito y
los rótulos del proveedor. Todos los materiales deben ser verificados
para asegurar que el envío corresponde al requerimiento.
Cuando se adosen rótulos adicionales al contenedor, la información
original no debe perderse.
Los daños a los contenedores y cualquier otro problema que pueda
afectar a la calidad de los materiales deben ser registrados,
reportados e investigados.
Todas las materias primas deben ser puestas en cuarentena,
inmediatamente después de ser recibidas hasta que sean liberadas para
su uso.
Todas las materias primas deben ser almacenadas bajo condiciones
apropiadas establecidas por el elaborador y en forma ordenada, para
permitir separar partidas y rotación de stock por la regla “primero
vence, primero sale”.
El agua usada en la elaboración de Preparaciones celulares debe ser la
adecuada para el uso destinado. Deben controlarse regularmente las
fuentes de provisión de agua, los equipos de tratamiento de agua y el
agua tratada, para verificar si existen sustancias químicas,
contaminación biológica, o contaminación con endotoxinas, con el fin de
asegurar, antes de usarla, que el agua cumple con las especificaciones
correspondientes al uso que se le quiere dar. Deben mantenerse
registros de los resultados obtenidos y de las medidas adoptadas.
Dado que la calidad de las materias primas puede influir sobre la
seguridad, la potencia y la pureza de la preparación celular, es
responsabilidad de los EPC garantizar la caracterización de las mismas
utilizadas en la elaboración.
Se deben crear programas científicamente sólidos para la calificación
de materias primas, ajustándose a la naturaleza de cada preparación
celular y de cada materia prima.
La contaminación microbiológica de las materias primas debe ser mínima.
Las especificaciones deben incluir requisitos de calidad microbiológica.
Cuando las materias primas no formen parte de la preparación celular
final, los EPC deben diseñar procedimientos analíticos de control para
garantizar la ausencia de niveles residuales de cada una de ellas.
Cuando la complejidad de la composición de las materias primas o la
naturaleza de la Preparación Celular final imposibilite el desarrollo
de metodologías de análisis apropiadas para la detección de trazas, el
EPC debe garantizar que los residuos de las mismas, presentes en la
Preparación Celular final, no afectan su eficacia y seguridad. Cuando
dichas materias primas puedan desatar reacciones de hipersensibilidad
y/o transmisión de enfermedades infecciosas (como ser, por ejemplo,
antibióticos, material de origen bovino o porcino), se debe justificar
científicamente su utilización en la elaboración y describir las
precauciones necesarias en la etiqueta de la Preparación celular final
para conocimiento del receptor de la misma.
3.6.1- Identificación y selección
Los EPC deben registrar cada material utilizado en el proceso de
elaboración, indicándose la fuente, el lote, el uso previsto, la
cantidad y la concentración.
Los EPC deben solicitar a los proveedores información sobre la
trazabilidad de las materias primas, en especial aquellas derivadas de
seres humanos o animales.
3.6.2- Aptitud
El EPC debe estimar el riesgo que la utilización de cada materia prima
puede representar para la seguridad, potencia y pureza de la
Preparación final, desarrollando metodologías de control apropiadas.
3.6.3- Caracterización
El EPC debe implementar pruebas de caracterización específicas para
cada materia prima, evaluando aspectos de la calidad, como la
identidad, potencia, funcionalidad, ausencia de contaminantes y aptitud
para el uso previsto.
Los reactivos e intermediarios preparados en el EPC, como medios de
cultivo y soluciones salinas, deben prepararse según procedimientos
escritos y ser rotulados adecuadamente. El rótulo debe indicar la
concentración, la vida útil y las condiciones de almacenamiento.
Deben desarrollarse especificaciones para cada materia prima en función
de su perfil de evaluación de riesgos y de los conocimientos adquiridos
durante el desarrollo de la Preparación Celular, como así también
durante los estudios preclínicos y clínicos correspondientes.
Cuando la naturaleza compleja de una materia prima dificulte su
completa caracterización, deben efectuarse, de ser posible, controles
de esterilidad, pirogenicidad, micoplasma y agentes adventicios o
virales infecciosos (dependiendo del origen del componente y su modo de
preparación).
3.6.4- Sueros de origen animal
El suero de origen animal es un aditivo comúnmente utilizado en los
medios de cultivo para favorecer la proliferación celular de una amplia
variedad de tipos celulares. Los factores de crecimiento, hormonas y
demás componentes nutritivos del suero, muchos de los cuales están
indefinidos o presentes en muy pequeñas cantidades, aportan los
componentes requeridos por muchas células para sobrevivir y dividirse
in vitro.
Los EPC que utilicen sueros en el cultivo de las células que formarán
parte de una preparación celular, deberán justificar su utilización,
mediante ensayos comparativos con medios de cultivo sin suero.
Los EPC deben garantizar que el suero que se utiliza en la elaboración
de sus preparaciones celulares proviene de establecimientos
controlados, con ausencia de enfermedades específicas de entornos
agrícolas (como brucelosis o tuberculosis), y que provengan de regiones
libres de encefalopatía espongiforme bovina.
El programa de calificación del suero de origen animal debe incluir,
como mínimo, controles de esterilidad, contenido de endotoxinas y
ausencia de virus específicos.
3.6.5- Garantía de Calidad
En relación con las materias primas utilizadas en la elaboración de
preparaciones celulares, los EPC deben contar con procedimientos
operativos estándares escritos para: recepción, segregación,
inspección, liberación de materias primas previo a su utilización en la
elaboración, programas de auditorías y certificación de distribuidores
o fabricantes, procedimientos y políticas formales para materiales
fuera de especificación, y almacenamiento de muestras.
3.7-
Materiales de acondicionamiento
La adquisición de material de acondicionamiento debe ser realizada a
través de proveedores calificados. La manipulación y control de los
materiales de acondicionamiento se debe realizar con igual
procedimiento al utilizado con las materias primas.
Se debe prestar particular atención a los materiales de
acondicionamiento impresos. Deben ser almacenados en condiciones
seguras para evitar la posibilidad de acceso a personal no autorizado.
Los materiales de acondicionamiento se deben dispensar para su uso,
exclusivamente por el personal designado, siguiendo un procedimiento
aprobado y documentado.
3.8-
Materiales de desecho
Debe existir un local para el almacenamiento apropiado y seguro de los
materiales de desecho hasta su destino final.
No se debe permitir acumular los materiales de desecho. Deben ser
recolectados en recipientes adecuados para su traslado a los puntos de
retiro fuera de los edificios. Deben ser eliminados de manera segura y
sanitaria a intervalos regulares y frecuentes de acuerdo con las normas
que regulan ese aspecto de la generación, manipulación, transporte,
tratamiento y disposición final de residuos peligrosos.
3.9-
Caracterización de Bancos de Células
Un banco de células es un conjunto de viales que contienen células
almacenadas en condiciones definidas.
El banco de células debe obtenerse a partir de una fuente calificada
(exenta de agentes adventicios bacteriales, fúngicos o virales), de
antecedentes conocidos y documentados, que incluyan los métodos,
reactivos y materias primas utilizadas para la creación del banco y las
condiciones de almacenamiento.
Las células del banco deben someterse a ensayos de identidad definidos
por el EPC, para verificar la ausencia de contaminación cruzada con
otras líneas celulares y estabilidad de sus propiedades luego del
almacenamiento. Las pruebas de potencia se diseñarán en función de cada
tipo celular en particular.
Deben conservarse registros de todas las materias primas utilizadas en
el procesamiento y cultivo de las células que formarán parte del banco
de células, a saber: medios de cultivo, enzimas, soluciones salinas,
criopreservantes, etc.
Los bancos de células pueden ser de dos tipos: Bancos Maestro de
Células (BMC) o Bancos Celulares de Trabajo (BCT). Se consideran BMC a
aquellos bancos que almacenan líneas celulares para múltiples ciclos de
elaboración, mientras que los BCT almacenan células utilizadas en la
elaboración puntual de una preparación celular.
3.9.1- Banco Maestro de Células (BMC)
Cada EPC deberá caracterizar su BMC. Para ello deberá establecer y
mantener procedimientos para:
• Realizar el análisis microbiológico de las células del banco,
incluyendo pruebas de esterilidad, micoplasma, pruebas in vitro y/o in
vivo para determinar la presencia de agentes virales adventicios, o
priones según corresponda.
• Determinar la ausencia de patógenos específicos, incluyendo —en el
caso de células humanas— pruebas para CMV, VIH-1 y 2, HTLV-1 y 2, VEB,
B19, VHB y VHC, Chagas, Toxoplasmosis, según corresponda. Para líneas
celulares expuestas a componentes de la especie bovina o porcina (por
ejemplo, suero, componentes del suero, tripsina), se realizarán las
pruebas adecuadas que incluyen las de agentes adventicios de la especie
bovina y/o porcina.
• Determinar la Identidad de las células, incluyendo pruebas para
distinguir las células específicas a través de características físicas
o químicas de la línea celular (es decir, fenotipo, genotipo, u otros
marcadores).
• Determinar la pureza de las células del banco, incluyendo la
identificación y cuantificación de cualquier contaminación.
• Determinar la potencia de las células (por ejemplo, linfocitos
activados, secreción de dopamina, secreción de insulina), estado de
diferenciación, y/o maduración (por ejemplo, células dendríticas).
• Determinar la Estabilidad fenotípica y genética del BMC después de
múltiples subcultivos y criopreservaciones.
3.9.2- Banco Celular de Trabajo (BCT)
La caracterización del BCT es menos extensa ya que la mayoría de las
pruebas fueron realizadas en el BMC. Cada EPC deberá:
• Realizar pruebas in vitro para agentes adventicios virales.
• Realizar el análisis microbiológico de las células incluyendo pruebas
de esterilidad (hongos y bacterias) y detección de micoplasma.
• Determinar la identidad (por ejemplo por Southern blot, citometría de
flujo).
3.10-
Especificaciones
Cada EPC debe establecer las especificaciones de cada una de las
Preparaciones celulares que elabore, con el objeto de confirmar la
calidad de la preparación, mediante ensayos que permitan asegurar,
dentro del conocimiento que se tenga del mismo, su seguridad y eficacia.
Las especificaciones deben establecerse a partir de la caracterización
minuciosa de la preparación durante las distintas fases de su
elaboración. La caracterización incluye, según corresponda, mediciones
de propiedades físico-químicas, ausencia de patógenos conocidos,
pureza, impurezas derivadas del proceso, potencia, viabilidad,
esterilidad, identidad y cantidad.
Los EPC deben disponer de los datos surgidos de los estudios
preclínicos y clínicos correspondientes (en caso de estar disponibles),
a fin de ajustar las especificaciones para cada tipo de preparación
celular.
Los EPC deben actualizar las especificaciones de sus preparaciones en
virtud de nuevos datos aportados por lotes fabricados, experiencia
internacional o solicitud del INCUCAI.
3.11-
Consideraciones para la validación
El potencial para producir una amplia variación biológica en
preparaciones celulares afecta el proceso de validación. Por dicha
razón, el proceso debe estar diseñado de modo que admita una amplia
gama de calidades y cantidades de material inicial.
Los EPC deben diseñar y cumplir con programas de validación que
contemplen dicha variabilidad, y garantizar que los puntos finales
críticos del proceso de elaboración y de las pruebas cumplan
uniformemente con las especificaciones.
Debe procurarse que las validaciones no pongan en peligro el proceso de
elaboración.
Los programas de validación para los procesos de elaboración y control
aplicables a cada preparación celular deben estar siempre disponibles a
requerimiento del INCUCAI.
3.12-
Fuente de células
Como fuente de células para la elaboración de preparaciones celulares,
se puede usar una amplia variedad de células y tejidos. Para su
obtención los EPC deben:
a) desarrollar sistemas que permitan la trazabilidad del material desde
la selección del donante y la procuración;
b) tomar medidas para prevenir la transmisión de enfermedades
infecciosas del donante al receptor;
c) asegurar el cumplimiento de procedimientos asépticos durante la
obtención y el procesamiento, para garantizar la seguridad de la
preparación final.
Los EPC deben contar con procedimientos escritos para la procuración de
células y tejidos, que se ajusten a lo establecido en el Anexo III de
la presente norma.
Las células o tejidos deben obtenerse bajo controles y condiciones
ambientales que permitan la recuperación aséptica de células con un
alto grado de seguridad.
El EPC debe garantizar la capacitación del personal en todos los
aspectos relacionados con la obtención de las células o tejidos, a
saber, diferentes procedimientos de obtención de células, lavado
quirúrgico, vestimenta, comportamiento dentro de la sala de
operaciones, preparación del sitio de intervención, antisepsia, entre
otros.
El material debe ser envasado en recipientes estériles, con cierre
hermético, y cantidad suficiente de medio de transporte para mantener
la viabilidad de las células o tejidos hasta su lugar de procesamiento
en las instalaciones del EPC.
El procesamiento del material celular debe llevarse a cabo en
instalaciones específicamente destinadas para tal fin y físicamente
separadas del sitio de extracción.
El EPC debe demostrar, mediante la documentación que exige el programa
de garantía de calidad referido a ello, que el medio de transporte
utilizado resulta óptimo para mantener la viabilidad de las células.
El EPC debe validar los envases para el transporte, en términos de
hermeticidad, cadena de frío y mantenimiento de las condiciones
adecuadas de almacenaje durante el tiempo de transporte.
3.12.1- Células de Origen Autólogo
El EPC debe determinar si los procedimientos usados en la obtención, o
elaboración implican riesgo de aumentar la propagación de agentes
patógenos que puedan estar presentes en el donante y su transmisión.
Para ello debe requerir a los responsables de esos pacientes un informe
exhaustivo de la situación clínica y biológica de los sujetos. Se debe
documentar si el donante presenta una reacción positiva ante agentes
patógenos específicos. También, debe describir las precauciones
necesarias para evitar la propagación de virus u otros agentes extraños
a personas distintas del receptor.
3.12.2- Células de origen alogénico
El EPC debe cumplir con lo establecido para la selección de donantes
establecido en el ANEXO III.
El EPC debe describir el tipo de pruebas que efectúa, los datos de las
historias clínicas y diagnósticos obtenidos de los donantes y
considerar otras cuestiones, tales como la tipificación de los
polimorfismos y la compatibilidad de los antígenos del complejo
molecular de histocompatibilidad (MHC clase I-II) también denominado
sistema HLA (antígenos leucocitarios humanos), según sea necesario en
cada caso.
4-
DOCUMENTOS Y REGISTROS
4.1- Objetivos
La documentación es un requisito esencial del sistema de aseguramiento
de la calidad y, como tal, debe existir para todos los aspectos de las
BPEyL. Asegura la disponibilidad de la información necesaria para la
validación, revisión y análisis estadístico.
Son sus objetivos:
a) definir las especificaciones y procedimientos para todos los
materiales y métodos de elaboración y control;
b) asegurar que todo el personal involucrado en la elaboración sepa qué
hacer y cuándo hacerlo;
c) asegurar que las personas autorizadas tengan toda la información
necesaria para decidir la liberación o no de una preparación celular;
d) asegurar la existencia de evidencia documentada y la trazabilidad;
e) proveer registros y un informe de auditoría que permita la
investigación.
El diseño y uso de los documentos depende del EPC. Cada EPC deberá
establecer y mantener procedimientos de control para asegurar que todos
los documentos indicados en esta norma y establecidos por ella,
satisfagan los requisitos de la misma y estén correctos y adecuados
para el uso pretendido.
4.2-
Generalidades
4.2.1- Aprobación y emisión de
documentos
La Dirección del EPC deberá designar personas para examinar y aprobar
todos los documentos establecidos en esta norma para su adecuación
antes de su emisión. La aprobación, incluyendo fecha y firma del
responsable, deberá ser documentada.
4.2.2- Distribución de documentos
El EPC deberá asegurar que todos los documentos estén actualizados y
disponibles y que aquellos innecesarios u obsoletos sean removidos a
tiempo. Los documentos reemplazados deben retenerse por un período
especificado. Asimismo, debe existir un sistema para prevenir el uso
inadvertido de la versión reemplazada.
4.2.3- Modificación de documentos
Ningún documento deberá modificarse sin autorización y aprobación.
Cuando se producen modificaciones de especificaciones, métodos o
procedimientos de obtención, procesamiento, almacenamiento,
distribución o transporte, o relativos al sistema de calidad, las
mismas deberán ser documentadas, revisadas y aprobadas por las personas
que están en las mismas funciones o en la misma organización que las
que ejecutaron la revisión y la aprobación original, a menos que otras
personas hubieran sido designadas para tal misión. Además, cualquier
modificación de especificaciones, métodos o procedimientos que puedan
afectar la calidad deberán ser validados como adecuados para el uso
pretendido antes de su aprobación y distribución. Los resultados de las
validaciones deberán ser registrados. Las modificaciones aprobadas
deberán ser comunicadas al personal encargado en tiempo y forma y éste
debe ser capacitado para implementar los cambios.
4.2.4- Registros de modificaciones de
documentos. Control de cambios
Cada EPC deberá mantener registros de las modificaciones de documentos.
Estos registros deberán incluir una descripción de la modificación,
identificación de los documentos que han sufrido algún cambio, la firma
de la persona responsable, la fecha de aprobación y la fecha en que las
modificaciones entrarán en vigor.
4.2.5- Registro de reclamos y no
conformidad
Cada EPC deberá mantener archivos de reclamos. Los documentos en los
que se registran las quejas y no conformidades deben ser revisados
regularmente para la identificación de problemas específicos o
recurrentes que requieran atención, modificación de procesos, nueva
capacitación del personal.
Los EPC deben informar al INCUCAI la implementación de cualquier cambio
que afecte la calidad de una preparación celular.
4.2.6- Contenidos
Todos los registros deberán ser legibles. Los contenidos no deben ser
ambiguos: el título, naturaleza y propósito deben estar claramente
estipulados. Deben redactarse en un estilo ordenado y ser fáciles de
verificar.
4.2.7- Conservación
Todos los registros exigidos en esta norma deberán ser mantenidos en
las instalaciones del EPC o en otro lugar razonablemente accesible para
el personal del EPC o para la autoridad sanitaria competente.
Los registros deberán ser guardados de forma de minimizar su deterioro,
prevenir pérdidas y permitir la búsqueda rápida. La documentación y
registros que deban conservarse podrán ser mantenidos mediante sistemas
electrónicos de procesamiento de datos o por medios fotográficos u otro
medio confiable. Si la documentación se maneja mediante métodos
electrónicos de procesamiento de datos, sólo las personas autorizadas
deben poder ingresar o modificarlos en la computadora, y debe haber un
registro de los cambios y deleciones; el acceso debe restringirse
mediante claves u otros medios y el ingreso de información crítica debe
verificarse en forma independiente. Los registros almacenados
electrónicamente deberán tener un respaldo mediante una copia de
seguridad o cintas magnéticas, microfilms, impresiones en papel u otros
medios.
Todos los registros necesarios relativos a un lote de la preparación
celular deberán ser guardados por un período no menor a diez (10) años
posteriores a la fecha de su liberación.
4.3-
Documentos
4.3.1- Solicitud del médico tratante
Orden escrita y firmada por el médico tratante para la obtención y/o
procesamiento y/o administración de la preparación celular. Debe
identificar inequívocamente al donante y al receptor (o ambos cuando
corresponda), y al tipo de preparación celular solicitado.
4.3.2- Rotulado - Etiquetado
Los rótulos aplicados a envases, equipos e instalaciones deben ser
claros, sin ambigüedades y con el formato acordado por el EPC. Además
del texto, es útil en los rótulos usar colores para indicar el estado
(ejemplos: en cuarentena, aceptado, rechazado, limpio).
El etiquetado de la preparación celular deberá asegurar, a lo largo de
las etapas, la identificación del mismo en los diferentes niveles de
procesamiento.
4.3.3- Especificaciones y
procedimientos de análisis
Aquellos procedimientos de análisis descriptos en los documentos y no
codificados en farmacopeas o compendios internacionalmente reconocidos
deben estar validados en el contexto de las instalaciones y
equipamiento disponibles antes de que sean adoptados como análisis de
rutina.
Debe haber especificaciones fechadas y apropiadamente autorizadas, que
incluyan ensayos de identificación, pureza y calidad para la
preparación celular terminada. Cuando corresponda, también deben estar
disponibles para materias primas, material de acondicionamiento y
preparaciones intermedias.
Cada especificación debe aprobarse, firmarse, fecharse y ser mantenida
por control de calidad, garantía de calidad o centro de documentación.
Serán necesarias revisiones periódicas de las especificaciones para
cumplimentar las nuevas ediciones de los compendios utilizados como
referencia.
Los documentos que describen procedimientos de análisis deben
establecer la frecuencia requerida para el reanálisis de cadamateria
prima, tal como lo determine su estabilidad.
4.3.4- Especificaciones para materias
primas y material de acondicionamiento
Las especificaciones para las materias primas y material de
acondicionamiento impreso deben proveer, si es aplicable, una
descripción de los materiales, que incluya:
a) la referencia, si existe, a un compendio de referencia;
b) requisitos cualitativos y cuantitativos con los límites de
aceptación, de ser aplicable.
Puede adicionarse otra información a las especificaciones, tal como:
c) el proveedor y el productor original de los materiales;
d) una muestra de los materiales impresos;
e) directivas para muestreo y análisis, o una referencia a los
procedimientos;
f) condiciones de almacenamiento y precauciones;
g) el máximo período de almacenamiento antes de reanálisis.
El material de acondicionamiento debe cumplir las especificaciones y
ser compatible con el material y/o con la preparación celular que
contiene. El material debe examinarse para el cumplimiento de las
especificaciones, la presencia de defectos críticos o mayores, como así
también para la correcta identificación de dicho material.
4.3.5- Especificaciones para
Preparaciones terminadas
Las especificaciones para Preparaciones terminadas deben incluir:
a) el nombre designado de la Preparación y el código de referencia,
donde sea aplicable;
b) el/los nombre/s designado/s del/los componente/s celular/es.
c) la dosis o una referencia a la misma;
d) detalles del acondicionamiento, condiciones de almacenamiento y
precauciones, cuando corresponda;
e) directivas para el muestreo y análisis o una referencia a los
procedimientos;
f) los requerimientos cualitativos y cuantitativos, con los límites de
aceptación;
g) el período de vida útil;
4.3.6- Procedimientos operativos
estandarizados (POE) y otros registros
Los procedimientos operativos estandarizados y otros registros, como
por ejemplo acciones tomadas o conclusiones, deben, entre otros, estar
disponibles para:
a) armado de equipos y validación;
b) aparatos analíticos y calibración;
c) mantenimiento, limpieza y sanitización;
d) temas relacionados con el personal, incluyendo calificación,
entrenamiento, vestimenta e higiene;
e) monitoreo ambiental;
f) quejas;
g) devoluciones;
h) actividades relacionadas con: depósitos, producción, control y
garantía de calidad, recursos humanos, etc.;
Debe haber procedimientos operativos estandarizados y registros para la
recepción de cada entrega de materia prima y material de
acondicionamiento.
Debe haber procedimientos operativos estandarizados para el rotulado
interno, cuarentena y almacenamiento de materias primas, materiales de
envasado y otros materiales, en forma apropiada.
Deben estar disponibles y dispuestos en las proximidades de los equipos
los procedimientos operativos estandarizados para cada instrumento (p.
ej.: uso, calibración, limpieza, mantenimiento).
Debe haber procedimientos operativos estandarizados para el muestreo,
que especifiquen a la/s persona/s autorizada/s para tomar las muestras.
Las instrucciones de muestreo deben incluir:
a) el método de muestreo y el plan de muestreo;
b) los equipos a utilizarse;
c) cualquier precaución a observarse para evitar la contaminación del
material o cualquier deterioro de su calidad;
d) la/s cantidad/es de muestra/s a tomarse;
e) instrucciones para cualquier subdivisión requerida de la muestra;
f) el tipo de envase para la muestra a utilizarse y rotulado de la
misma. Debe indicarse si son para muestreo aséptico o no;
g) cualquier precaución específica a observarse, especialmente en
consideración del muestreo de material estéril o nocivo.
Debe haber procedimientos operativos estandarizados que describan los
detalles del sistema de identificación de la Preparación, con el
objetivo de asegurar que cada Preparación intermedia, o final se
identifique de forma específica.
El procedimiento operativo estandarizado para la identificación de la
Preparación debe asegurar que no se utilice la misma identificación
para Preparaciones diferentes. La asignación de la identificación de la
Preparación debe registrarse inmediatamente. El registro debe incluir
al menos la fecha de asignación e identidad de la Preparación Celular.
Debe haber procedimientos operativos estandarizados para el análisis de
materiales y Preparaciones en diferentes etapas de la elaboración,
describiendo los métodos y equipamiento a utilizarse. Los ensayos
llevados a cabo deben registrarse.
Los registros de análisis deben incluir, al menos, la siguiente
información:
a) el nombre del material o preparación y, cuando corresponda, la dosis;
b) el número de lote y, donde sea apropiado, el fabricante y/o
proveedor;
c) referencias a especificaciones relevantes y procedimientos de
análisis;
d) resultados de ensayos, incluyendo observaciones y cálculos, y
referencia a las especificaciones (límites);
e) la aprobación de las distintas etapas del procesamiento de cada
preparación y del equipamiento utilizado en el mismo;
f) fechas/s y número/s de referencia de análisis;
g) las iniciales de las personas que llevaron a cabo el análisis;
h) una declaración clara de la liberación o rechazo (u otra decisión de
estado) y la firma fechada de la persona responsable designada.
Deben estar disponibles los procedimientos operativos estandarizados de
liberación y rechazo de materiales y preparaciones terminadas por una
persona autorizada.
Cada EPC deberá establecer y mantener procedimientos para controlar la
distribución de preparaciones aprobadas a fin de asegurar que sólo
aquellas aptas para su uso en seres humanos sean distribuidas.
Cada EPC deberá mantener registros de distribución de cada lote de
preparaciones, que incluyan o que hagan referencia a:
a) Nombre y dirección del profesional autorizado a cargo de la
aplicación.
b) Identificación y cantidad de preparaciones enviadas, con fecha de
envío.
c) El código o número necesario para la trazabilidad.
d) Todos los datos consignados en el etiquetado de acuerdo con lo
establecido en la normativa vigente.
Deben mantenerse registros de todas las validaciones, calibraciones,
mantenimiento, limpieza u operaciones de reparación de los equipos
principales y críticos, incluyendo fechas y la identidad de las
personas que llevaron a cabo estas operaciones.
El uso de equipos principales y críticos y las áreas donde las
preparaciones han sido procesadas debe registrarse apropiadamente en
orden cronológico.
Debe haber procedimientos operativos estandarizados, asignando la
responsabilidad de la limpieza y sanitización y describiendo con
suficiente detalle los programas de limpieza, métodos, equipos y
materiales a utilizarse e instalaciones y equipos a limpiar. Dichos
procedimientos escritos deben seguirse y registrarse.
4.3.7- Reclamos
Cada EPC deberá establecer y mantener procedimientos para recibir,
examinar, evaluar, registrar, y archivar en tiempo y forma y de manera
uniforme los reclamos que impliquen una posible no conformidad de la
preparación celular, su rotulado o embalado. Tales procedimientos
deberán asegurar que:
a) Los reclamos serán recibidos, examinados, evaluados, investigados y
archivados por personal designado por el EPC. La persona designada será
la responsable de atender todos los reclamos y de decidir qué medidas
deben adoptarse, juntamente con personal suficiente para asistirle en
esa tarea.
b) Los reclamos orales sean documentados luego de su recepción.
c) Se verifique si una investigación es necesaria y se tomen las
acciones correctivas correspondientes. Cuando no fuera hecha una
investigación, el EPC deberá mantener un registro que incluye el motivo
por el cual la investigación no fue realizada y el nombre de los
responsables de la decisión de no investigar.
d) Se deberán incluir prescripciones en los procedimientos para decidir
si el reclamo representa un evento a ser informado al INCUCAI.
e) Se debe contar con procedimientos operativos estandarizados que
describan las medidas que deban adoptarse en caso de reclamo referente
a posibles defectos de la preparación celular.
f) Todas las decisiones y medidas tomadas como resultado de un reclamo
deben ser registradas y referenciadas a los registros de producción
correspondientes.
g) Cualquier queja concerniente a una preparación celular defectuosa
debe ser registrada con todos los detalles originales, e investigada
minuciosamente. La persona responsable de control de calidad debe estar
involucrada normalmente en la revisión de dichas investigaciones.
h) Si se descubre o existe sospecha sobre una preparación celular
defectuosa, debe considerarse la necesidad de constatar otras
preparaciones, para determinar si éstas también han sido afectadas.
i) Cualquier reclamo relativo a eventos adversos (serios o no) o
cualquier riesgo en la seguridad deberá ser inmediatamente examinado,
evaluado e investigado por el personal responsable, debiendo ser
mantenido en una sección especial del archivo de reclamos. Las
investigaciones deberán incluir la verificación de falla en el
desempeño o especificaciones de la preparación; si hubo óbito, lesión o
dolencia grave involucrada, y la relación, si la hubiera, de la
preparación con el incidente o evento adverso comunicado.
j) Cuando fuera hecha una investigación, deberá ser mantenido un
registro por el personal designado por el EPC. El registro de la
investigación deberá incluir:
1) Descripción de la preparación
2) Fecha de recepción del reclamo
3) Código de identificación utilizado (número de lote)
4) Nombre, dirección y teléfono del denunciante
5) Naturaleza del reclamo
6) Resultados de la investigación. Los mismos deberán incluir:
- Fechas de la investigación
- Detalles del reclamo
- Respuesta al denunciante (Cuando no fuera dada una respuesta al
denunciante, el motivo deberá ser registrado)
- Acción correctiva tomada.
4.3.8- Documentación del donante
Todo EPC deberá contar con el certificado de elegibilidad del donante y
el consentimiento informado.
4.3.8.1- Certificado de elegibilidad
Corresponde a la certificación de elegibilidad del donante, rubricada
por el profesional responsable de la misma (Ver ANEXO III).
4.3.8.2- Consentimiento informado
La hoja de información al paciente y el consentimiento informado
deberán ser utilizadas en toda donación de células, sea para su uso
terapéutico en prácticas corrientes como en investigación, debiendo
respetarse todas las exigencias legales y éticas vigentes.
4.3.8.2.1- Donación con fines
terapéuticos
En el caso de que la donación de células humanas se realice con fines
terapéuticos para prácticas consideradas corrientes, se deberá
garantizar la confidencialidad del donante, en los casos de uso
alogénico no relacionado.
El equipo autorizado debe proveer al donante toda la información
pertinente al proceso de donación, riesgos involucrados, ensayos de
laboratorio y toda la información necesaria para la correcta
comprensión del consentimiento informado.
4.3.8.2.2- Donación con fines de
investigación clínica
En el caso de que la donación de células humanas se realice con fines
de investigación clínica, los requisitos de la hoja de información al
donante y consentimiento informado deberán sumar todas las exigencias
previstas en las leyes y normativas nacionales e internacionales que
apliquen en la materia. Tanto aquellas referidas a investigación
clínica e investigación con células, como las referidas a protección de
datos personales y protección de datos genéticos.
En todos los casos la hoja de información al paciente y el
consentimiento informado deberán ser incluidos en el protocolo, para la
correspondiente aprobación por el Comité de Etica de Investigación
(CEI) del INCUCAI.
5- ESTRUCTURA
EDILICIA
Todo EPC deberá contar con una estructura apta para realizar la
elaboración de una preparación celular que contiene células viables de
origen humano. Los locales deben ser adecuados a las operaciones que se
efectuarán.
5.1-
Generalidades
El plano de los locales, su construcción, su concepción y su
utilización deben minimizar los riesgos de confusión o de error
estableciendo un flujo lógico de materiales y de personal,
contribuyendo a la protección del personal y permitiendo una limpieza y
mantenimiento efectivos para evitar la contaminación, contaminación
cruzada, acumulación de polvo o suciedad y, en general, cualquier
efecto adverso sobre la calidad de las preparaciones celulares.
Los locales deben estar claramente identificados y señalizados. Donde
se genere polvo (por ejemplo durante pesadas, muestreos, etc.), se
deben tomar medidas para evitar la contaminación cruzada y facilitar la
limpieza.
Los locales deben ser cuidadosamente limpiados y, donde sea aplicable,
desinfectados de acuerdo con procedimientos operativos estandarizados.
Los locales usados para la elaboración de preparaciones terminadas
deben ser convenientemente diseñados y construidos para facilitar la
correcta limpieza y desinfección de acuerdo con procedimientos
operativos estandarizados.
El suministro eléctrico, iluminación, temperatura, humedad y
ventilación deben ser apropiados de modo tal que no influyan
negativamente, directa o indirectamente, ni sobre las preparaciones
durante su elaboración y almacenamiento, ni sobre el correcto
funcionamiento del equipamiento.
Se debe asegurar que las operaciones de reparación y mantenimiento de
los locales no presenten ningún peligro a la calidad de las
preparaciones.
Los locales deben ser diseñados y equipados para proporcionar la máxima
protección contra la entrada de insectos, pájaros y otros animales.
Las áreas clasificadas, locales y cabinas destinadas al procesamiento
de preparaciones celulares deben haber sido objeto de una calificación.
Para ello, cada área contará con una ficha descriptiva que deberá
actualizarse en caso de modificación y según el ritmo de revisión
previsto por los procedimientos. Estas zonas no deben ser utilizadas
como lugares de paso para el personal ni para el almacenamiento de
insumos, salvo insumos propios del procesamiento.
El acceso a las diferentes zonas de trabajo estará estrictamente
restringido a las personas autorizadas, quedando terminantemente
prohibido fumar, comer o beber, excepto en áreas anexas destinadas a
estos fines.
5.2- Circuito
logístico/Locales y áreas
Se denomina área a la zona de trabajo de un determinado procedimiento.
Varias áreas podrán compartir un mismo espacio físico o estar en
edificios o locaciones diferentes, en tanto el traslado de material o
personas no involucre infringir ninguna normativa de este documento.
5.2.1- Areas Auxiliares
Las zonas de descanso del personal y las destinadas a realizar ingestas
deben estar separadas de las áreas de elaboración y control.
Los vestuarios generales y los sanitarios deben ser de fácil acceso,
apropiados para el número de usuarios y no deben comunicarse
directamente con las áreas productivas y de almacenamiento.
Los talleres de mantenimiento, si los hubiera, deben estar separados de
las áreas de producción.
Los alojamientos de animales (bioterios), si los hubiera, deben estar
bien aislados de otras áreas, con un ingreso independiente y exclusivo
para animales. Las instalaciones de manejo de aire deben ser
independientes.
5.2.2- Areas de Depósito
Las condiciones de almacenamiento de la preparación celular e insumos
dependerán del procesamiento utilizado y del método de conservación
requerido. Cualquiera sea la técnica de conservación utilizada, los
materiales no aprobados o no conformes deberán ser guardados en forma
separada, de los materiales aprobados o conformes. Las preparaciones
deben ser identificadas de manera adecuada a los efectos de evitar
cualquier utilización que no haya sido avalada por personal calificado
y designado a ese efecto.
Cada EPC deberá establecer y mantener procedimientos para el control de
las áreas de almacenamiento de preparaciones e insumos utilizados en el
EPC, para evitar mezclas, daños, deterioros u otros efectos adversos
durante cualquier período anterior a su distribución o uso.
Cada EPC deberá establecer y mantener procedimientos para autorizar la
recepción o retiro de insumos de las áreas de almacenamiento. Cualquier
control numérico u otra forma de identificación deberán ser legibles y
claramente visibles. Cuando la calidad de los insumos utilizados en el
EPC se deteriore con el tiempo, los mismos deberán ser almacenados de
manera de facilitar la rotación de los stocks (vence primero, sale
primero). Las condiciones de los insumos deberán ser evaluadas en
intervalos adecuados.
Las áreas de depósito deben ser de capacidad suficiente para permitir
un almacenamiento ordenado de varias categorías de insumos y
preparaciones con correcta separación y segregación (materias primas,
materiales de acondicionamiento, reactivos, etc.). Se deben mantener
segregados los insumos o preparaciones rechazados, retirados del
mercado o devoluciones con el fin de asegurar que los mismos no sean
inadvertidamente distribuidos o usados.
Cualquier sistema reemplazante de la cuarentena física debe brindar una
seguridad equivalente.
Las áreas de depósito deben ser diseñadas o adaptadas para asegurar
buenas condiciones de almacenamiento. En particular, deben estar
limpias, secas y suficientemente iluminadas y mantenidas a temperaturas
compatibles con los elementos almacenados. Donde sean requeridas
condiciones especiales de almacenamiento (ej.: temperatura y humedad)
éstas deben ser provistas, monitoreadas y registradas.
Las zonas de recepción y expedición deben estar separadas, y además
deben proteger a los insumos y preparaciones de las condiciones
ambientales externas. Las áreas de recepción deben estar diseñadas y
equipadas para, cuando sea necesario, permitir la limpieza de los
contenedores de los materiales entrantes antes de su almacenamiento.
Los materiales peligrosos y sustancias que presenten especial riesgo de
abuso, fuego o explosión, deben ser almacenados en áreas seguras.
Normalmente debe haber un área de muestreo separada para las materias
primas.
5.2.3- Area de pesada
La pesada de materias primas debe ser realizada en áreas de pesada
separadas, destinadas para tal fin, por ejemplo, provistas para el
control de polvo. No se deberán pesar insumos que generen polvo en
áreas clasificadas.
5.2.4- Area de Control de Calidad
Los procedimientos de control de calidad deben estar separados física o
temporalmente de los procesos de producción, pudiendo ser tercerizados
o realizarse en otro edificio. Las áreas donde se realicen ensayos
microbiológicos o con radioisótopos deben estar separadas entre sí.
El almacenamiento de muestras, sustancias y materiales de referencia
(si fuese necesario con refrigeración), solventes, reactivos y
registros debe realizarse en lugares específicos para control de
calidad, evitando mezclas y contaminación cruzada.
5.2.5- Area administrativa y de
archivo
En esta zona se cumple el conjunto de formalidades administrativas
ligadas a todas las actividades del centro elaborador. Deberá contar
con un registro en libro foliado, entregado por el INCUCAI, para el
ingreso de muestras y el egreso de preparaciones. Contará con el
archivo de toda la documentación vinculada a todas las actividades del
centro elaborador.
5.2.6- Area de descontaminación,
lavado y esterilizado de materiales y equipos utilizados en el
procesamiento
El área deberá cumplimentar lo establecido en la normativa vigente
referente a residuos patogénicos.
Cada EPC deberá eliminar los efluentes líquidos, sólidos y semisólidos
de materiales utilizados en el procesamiento y desechos, de manera
segura, oportuna e higiénica, en conformidad con la normativa vigente
para la eliminación de residuos patogénicos. Todo insumo o elemento que
ha tenido contacto con un tejido debe ser tratado como residuo
patogénico. El tratamiento del aire se deberá realizar según los
procedimientos recomendados por la OMS.
5.2.7- Areas de elaboración de
preparaciones celulares
5.2.7.1- Generalidades
La elaboración de preparaciones que contienen células destinadas a ser
aplicadas en seres humanos está sujeta a requisitos especiales, para
minimizar los riesgos de contaminación microbiana, de partículas y de
sustancias pirogénicas.
Para minimizar riesgos debido a la contaminación cruzada se acepta el
principio de “trabajo en campaña” (separación en el tiempo) en las
mismas instalaciones, siempre que se tomen las precauciones específicas
y sean hechas las validaciones necesarias (incluyendo validación de
limpieza).
La adecuación del trabajo, del lugar de incubación y de almacenamiento
de materiales usados durante el proceso, debe permitir la ubicación
lógica y ordenada de los mismos para minimizar el riesgo de la
confusión entre diferentes preparaciones o insumos, evitando la
contaminación cruzada, y minimizando el riesgo de la omisión o mala
aplicación de cualquier etapa de elaboración o control.
Los locales deben ser distribuidos de forma tal que permitan que la
elaboración se lleve a cabo en áreas conectadas en un orden lógico, que
corresponda a la secuencia de las operaciones y a los niveles
requeridos de limpieza.
Donde las materias primas estériles, los materiales de
acondicionamiento primario y las preparaciones intermedias o finales
sean expuestas al ambiente, las superficies interiores (paredes, pisos
y techos) deben ser lisas, sin grietas, ni empalmes abiertos, no deben
liberar partículas de material y deben facilitar la limpieza y, en caso
de ser necesario, la fácil y eficaz desinfección.
Las cañerías, los montajes de luz, los puntos de ventilación y otros
servicios deben estar diseñados para evitar la creación de hendiduras
que sean dificultosas para limpiar. Para el propósito de su
mantenimiento deben también, si es posible, ser accesibles por fuera de
las áreas de elaboración.
Los desagües deben ser de las medidas adecuadas, diseñados y equipados
para prevenir el reflujo. Los canales abiertos deben ser evitados
cuando sea posible, pero si éstos son necesarios deben ser poco
profundos para facilitar la limpieza y desinfección.
Siempre que sea posible, se debe evitar la instalación de sumideros y
drenajes o bien excluirlos de las áreas donde se efectúan operaciones
asépticas. Donde haya necesidad de instalarlos, deben diseñarse,
ubicarse y mantenerse de tal manera que se reduzca al mínimo el riesgo
de contaminación microbiana; deben contar con sifones efectivos y
cierres de aire que sean eficientes y fáciles de limpiar, con el fin de
prevenir el reflujo de los líquidos.
Las áreas de elaboración deben ser monitoreadas regularmente durante
los períodos de elaboración y no elaboración, para asegurar el
cumplimiento con sus especificaciones de diseño.
Las áreas de producción deben estar bien iluminadas.
5.2.7.2- Areas limpias
Las diversas operaciones que comprenden el proceso de elaboración de
preparaciones estériles deben llevarse a cabo en áreas limpias; las
mismas se clasifican en cuatro grados o clases (ver tabla 1), de
acuerdo con las características requeridas del ambiente.
Tabla 1. Sistema de clasificación del aire en la elaboración de
preparaciones estériles
Cada operación de elaboración
requiere de un determinado grado de limpieza para minimizar el riesgo
de contaminación por partículas o microorganismos de las Preparaciones
o insumos que están siendo manipulados. Estas áreas deben mantenerse de
conformidad con normas apropiadas de limpieza y se debe suministrar a
las mismas solamente aire que ha pasado a través de filtros de
eficiencia comprobada correspondiente al nivel de limpieza requerido.
El ingreso a las áreas limpias debe efectuarse a través de esclusas,
tanto para el personal como para los materiales y equipos.
Para reunir las condiciones de “en operación”, estas áreas deben estar
diseñadas para alcanzar ciertos niveles especificados de aire limpio en
el estado de “en reposo”. Este último estado es la condición donde la
instalación está completa, y el equipamiento de producción ha sido
instalado y está operando, pero no está presente el personal. El estado
de “en operación” es la condición donde la instalación está funcionando
en el modo operativo definido y el número de personal especificado está
presente.
• Grado A: Es el área para operaciones de alto riesgo, ejemplos:
procesamiento de tejidos, cultivo de células, preparaciones asépticas.
Normalmente tales condiciones son provistas por una cabina de seguridad
biológica. Los sistemas de corriente de aire laminar deben suministrar
una velocidad de aire homogénea de aproximadamente 0,45 m/s +/- 20%
(valor orientativo).
• Grado B: Es el área que rodea a la de grado A. Se realizan
operaciones que no involucran a la Preparación Celular, ejemplos:
filtración de soluciones de limpieza.
• Grados C y D: Son las áreas limpias para llevar a cabo los pasos
menos críticos de la elaboración de Preparaciones estériles.
Para alcanzar los grados de aire C y D, el número de cambios de aire
debe ser apropiado para el tamaño del área, del equipo y personal
presente en ella. Se requieren al menos 20 cambios de aire por hora
para áreas con un buen patrón de corriente de aire y filtros de aire de
alta eficacia (HEPA).
Se deben establecer límites de alerta y de acción apropiados para los
resultados del monitoreo de partículas y microorganismos. Si éstos se
exceden, se deben tomar las acciones correctivas apropiadas según
procedimientos operativos estandarizados.
Las condiciones de partículas indicadas en la tabla 1 para la situación
“en reposo” deben recuperarse en ausencia de personal tras un breve
período de “limpieza” de 15-20 minutos (valor orientativo), una vez
finalizadas las operaciones.
Durante las operaciones, las áreas limpias deben controlarse a
intervalos preestablecidos, mediante el recuento microbiano del aire y
de las superficies como para asegurar que el ambiente esté dentro de
las especificaciones. Se deben usar métodos tales como placas de
exposición, aire forzado, muestreo de superficies (por ejemplo hisopos
y placas de contacto). Las zonas no deben contaminarse por los métodos
de muestreo utilizados en la operación. Deben tenerse en cuenta los
resultados del control ambiental en la evaluación de los lotes para su
posterior liberación. Tanto las superficies como el personal deben ser
monitoreados después de operaciones críticas.
Se debe controlar también regularmente la calidad del aire con respecto
al contenido de partículas. Es conveniente efectuar controles
adicionales, aun cuando no se efectúen operaciones de elaboración, como
por ejemplo después de la validación de los sistemas, de la limpieza y
de la fumigación.
Los grados de las áreas, como se han especificado, deben ser elegidos
por el EPC sobre la base de la naturaleza de las operaciones del
proceso y a las validaciones.
En la tabla 2 se muestran los límites para el monitoreo microbiológico
de áreas limpias en operación expresados en unidades formadoras de
colonia (UFC). Los métodos de muestreo y los valores que incluye la
tabla no representan especificaciones, sino recomendaciones.
Tabla 2. Límites para el monitoreo de contaminación microbiología.
De ser posible, todos los locales
deben diseñarse de tal forma que se evite el ingreso innecesario de
personal de supervisión o control.
Deben existir vestuarios para permitir el cambio de ropa antes de
ingresar al sector.
Para un EPC tipo 1 toda manipulación que implique ruptura de una
barrera de esterilidad (como por ejemplo tomas de muestra), debe ser
realizada en un ambiente Clase A.
Para un EPC tipo 2 se deben cumplir las siguientes condiciones:
a) El ambiente clase A deberá estar rodeado como mínimo de un área
clase C.
b) Para reducir la acumulación de polvo y facilitar la limpieza, no
debe haber lugares que no puedan limpiarse y los locales deben tener un
mínimo número de repisas, estantes, anaqueles y equipos. Las puertas
deben estar construidas de tal forma que no tengan superficies que no
puedan limpiarse; por esta razón son inconvenientes las puertas
corredizas.
c) En caso de existir cielos rrasos falsos, éstos deben cerrarse
herméticamente para prevenir la contaminación proveniente del espacio
libre.
d) Los vestuarios deben estar diseñados como esclusas de aire, para
separar las diferentes etapas del cambio de ropa, para minimizar así la
contaminación de las ropas de protección con microorganismos y
partículas. Dichas habitaciones deben limpiarse eficientemente con aire
filtrado. A veces es conveniente contar con vestuarios independientes
para la entrada y para la salida de las áreas limpias. Las
instalaciones para el lavado de las manos deben estar ubicadas
preferentemente en los vestuarios, y no en los lugares donde se
efectúan trabajos asépticos.
e) Las esclusas de aire no deben abrirse simultáneamente. Se debe
contar con un sistema de cierre interbloqueado y/o con un sistema de
alarma visual y/o auditivo para prevenir la apertura de más de una
puerta a la vez.
f) La alimentación de aire filtrado mantiene, bajo cualquier
circunstancia, una presión positiva con relación a las zonas vecinas,
imponiendo una circulación de aire desde las de mayor seguridad hacia
las de menor seguridad. Debe quedar demostrado que el diseño de aire
filtrado no presenta contaminación ni circulación de aire hacia una
zona de mayor seguridad, es decir, al ambiente inmediato al cual están
expuestos y con el cual toman contacto las Preparaciones.
g) Las áreas adyacentes de grados diferentes deben tener un gradiente
de presión de 10-15 pascales (valor orientativo). Debe demostrarse que
los patrones de corriente de aire no presenten riesgo de contaminación;
así, por ejemplo, se debe tener especial cuidado para asegurar que las
corrientes de aire no distribuyan partículas provenientes de personas,
máquinas u operaciones, hacia un área de mayor riesgo para las
preparaciones.
h) La alimentación del aire debe estar provista de un sistema de alarma
que detecte cualquier deficiencia. Entre una y otra área, donde la
diferencia de presión de aire es importante, debe instalarse un
indicador de presión y las diferencias deben registrarse regularmente.
i) Debe restringirse el acceso innecesario a las áreas limpias, donde
podrían colocarse barreras para tal efecto.
6-
IDENTIFICACION Y TRAZABILIDAD
Cada EPC deberá establecer y mantener procedimientos para la
identificación de las preparaciones celulares en todas sus etapas
(desde la obtención de la fuente de células hasta la liberación para su
administración).
Para poder realizar el seguimiento de una preparación celular a lo
largo del procesamiento y distribución, es necesaria la identificación
de cada preparación intermedia o terminada mediante la identificación
inequívoca de cada envase.
La identificación del receptor es responsabilidad del EPC. Cada EPC
deberá establecer y mantener procedimientos para asegurarse que una
determinada preparación sea aplicada inequívocamente al receptor
correspondiente.
Para la identificación existen diferentes métodos que permiten
describir la ruta que ha realizado la preparación y el estado en que se
encuentra. Las dos tecnologías más usadas en este ámbito son: los
códigos de barras y el RFID (Identificador de Radio Frecuencia).
La trazabilidad es la propiedad de poder conocer, a partir de la
preparación final, todos los elementos críticos que intervinieron en el
proceso de obtención del mismo incluyendo fechas y horas, identidades y
cantidades de insumos utilizados, condiciones ambientales, operadores,
instrumentos, equipamiento, etc.
Respetando totalmente la confidencialidad, debe haber un sistema que
permita rastrear el trayecto de cada donación de células o tejidos,
tanto a partir del donante, como a partir de la preparación celular
final.
Cuando corresponda, debe establecerse un procedimiento que describa el
sistema de información entre el centro de recolección/banco de tejidos
y el EPC para poder trazar inequívocamente los datos.
El EPC para garantizar la trazabilidad deberá identificar por lo menos:
- El origen de sus componentes
- La historia de los procesos aplicados a la preparación celular
- Las condiciones de almacenamiento y distribución
- El receptor de la preparación final
7-
CONTROLES Y ENSAYOS
7.1-
Generalidades
Los EPC deben desarrollar un sistema de control periódico sobre todas
las etapas involucradas en la elaboración de una preparación celular,
desde la obtención de la fuente de células hasta la preparación final,
con el fin de garantizar la calidad de la misma en todas las instancias
de su elaboración y asegurar que esté en conformidad con sus
especificaciones. Se deberán establecer y mantener procedimientos
escritos de control de los procesos, en donde se incluyan claramente
los puntos críticos en la elaboración de cada preparación celular
(tiempo de cultivo, número de divisiones celulares esperadas,
condiciones de cultivo como temperatura, concentración de gases, medios
de cultivo/soluciones y concentración de los mismos, etc.). En caso de
poseer más de una condición de cultivo celular, se deberán realizar
controles de la eficiencia de cada paso del protocolo de cultivo. En
dichos puntos críticos, se evaluarán los criterios que determinarán la
continuación o no del proceso de elaboración.
Los procedimientos deberán describir los métodos y equipamiento a
utilizarse para el análisis de materiales y preparaciones en diferentes
etapas de la elaboración; deberán contemplar, como mínimo, aspectos
relacionados con la seguridad (esterilidad, micoplasmas, ausencia de
capacidad teratogénica), pureza e identidad (endotoxinas, morfología,
marcadores de membrana —de existir— marcadores bioquímicos —de
existir—).
En el caso de preparaciones que contienen células modificadas
genéticamente, se deberán establecer y mantener procedimientos escritos
en donde se realice una descripción detallada del método de
transferencia génica (vector viral o método no viral utilizado),
eficiencia mínima requerida de la transferencia, nivel y duración de la
expresión del/los transgenes, etc.
Los EPC deben conservar los registros de validaciones de cada uno de
los métodos de control aplicados en los puntos de control del proceso.
Las preparaciones intermedias del proceso que no cumplan con los
criterios de control no podrán continuar con el proceso de elaboración.
Se deberán registrar los controles de procesamiento (Ver “Documentos y
Registros”).
7.2-
Control de calidad
En control de calidad se encuentran involucrados el muestreo,
especificaciones y ensayos, como así también los procedimientos de la
organización, documentación y autorización que aseguren que los ensayos
necesarios y relevantes son llevados a cabo y que no se autorice el uso
de materiales ni la liberación de preparaciones celulares sin que se
haya establecido que su calidad es satisfactoria.
Donde sea aplicable, cada EPC deberá establecer y mantener
procedimientos para identificar técnicas de muestreo válidas,
necesarias para controlar la elaboración de la preparación celular en
todas sus etapas.
Los planes de muestreo deberán ser formalizados por escrito y basados
en una lógica estadística válida. Cada EPC deberá establecer y mantener
procedimientos para asegurar que los métodos de muestreo sean adecuados
al uso pretendido y que sean revisados regularmente, especialmente en
el incremento de eventos tales como el aumento de Preparaciones
celulares y materiales utilizados no conformes, informes de auditoría
de calidad adversos o reclamos continuos.
Cada EPC deberá establecer y mantener las actividades de controles y
ensayos necesarios para asegurar que todos los requisitos especificados
sean alcanzados. Los resultados de todos los controles y ensayos
deberán ser documentados.
Siempre que sea posible, el EPC se esforzará por respetar la
independencia entre las áreas de elaboración y control de calidad.
Los requerimientos básicos para control de calidad son los que siguen:
a) Instalaciones adecuadas, personal entrenado y procedimientos
aprobados deben estar disponibles para muestreo, inspecciones y control
de materias primas, material de acondicionamiento, intermediarios y
preparación final, así como para el monitoreo de las condiciones
ambientales para el cumplimiento de las BPEyL.
b) Las muestras deben ser tomadas por métodos y personal calificado y
entrenado.
c) Se debe realizar calificación de equipos e instrumentos y validación
de metodologías.
d) Se deben realizar registros, demostrando que todos los
procedimientos de muestreo, inspección y control se han llevado a cabo
y que cualquier desvío ha sido completamente registrado e investigado.
e) Las preparaciones terminadas deben respetar la fórmula o
acondicionamiento final especificado. De no poder cumplirse este
requisito, deberá registrarse la desviación y el motivo por el cual fue
utilizada la preparación de todas maneras.
f) Se deben registrar los resultados de las inspecciones y controles de
materiales, intermediarios (de existir) y Preparaciones finales según
especificaciones; la evaluación de las mismas debe incluir la revisión
y evaluación de la documentación de elaboración, como así también de
los desvíos de los procedimientos especificados.
7.2.1- Control de materias primas:
Antes de la liberación de una materia prima o material de
acondicionamiento para su uso, el encargado de control de calidad debe
asegurar que los materiales han sido controlados conforme con las
especificaciones establecidas en los documentos pertinentes.
7.2.2- Controles de recepción de
fuentes de células
Cada EPC deberá asegurar la capacitación del personal encargado de la
toma de fuente de células del tejido a procesar, a fin de que se
ajusten a las especificaciones establecidas para su posterior
procesamiento.
Cada EPC deberá establecer y mantener procedimientos para la evaluación
y aceptación de fuentes de células que serán procesadas en la
elaboración de una preparación celular. Las fuentes de células no
deberán ser procesadas hasta que sea verificada su conformidad a los
requisitos establecidos. La aceptación o rechazo deberá ser documentado.
7.2.3- Controles y ensayos durante el
procesamiento
Los EPC deben desarrollar un sistema de control periódico sobre todas
las etapas involucradas en la elaboración de una preparación celular,
desde la obtención de la fuente de células hasta la preparación final,
con el fin de garantizar la calidad de la misma en todas las instancias
de su elaboración.
En caso de poder reprocesar una preparación intermedia rechazada
(siempre y cuando existan procedimientos para ello), el nuevo material
reprocesado debe cumplir con las especificaciones de proceso originales.
Los EPC deben conservar los registros de validaciones de cada uno de
los métodos de control aplicados en los puntos de control del proceso.
7.2.4- Controles de Preparación
terminada
7.2.4.1-
Consideraciones generales
Las preparaciones celulares deben someterse a métodos analíticos que
permitan garantizar su identidad, pureza y seguridad. La dosis y la
potencia serán analizadas en caso de conocerse la tecnología y disponer
suficiente material para ello. Dada la complejidad y el alcance de las
preparaciones celulares, se dispone de una amplia variedad de
metodologías que pueden emplearse para evaluar su calidad.
En función de las características particulares de cada preparación
celular, cada EPC debe establecer los métodos de control adecuados.
La siguiente tabla brinda una serie de ejemplos de métodos o enfoques
generales para satisfacer los requisitos de las pruebas en
preparaciones celulares. Estos requisitos deben estar subordinados a la
posibilidad tecnológica de realizar los análisis sobre la población
celular de estudio, a la cantidad de células que se pretende utilizar
en la investigación o terapia y que haya conocimiento suficiente para
tal fin.
7.2.4.2-
Seguridad
Las pruebas de seguridad tienen por objetivo prevenir el uso inadecuado
de preparaciones contaminadas, mal manejadas o procesadas, y con riesgo
de transmitir enfermedades infecciosas.
El manejo inadecuado puede alterar la integridad y la función de las
preparaciones al introducir microorganismos o contaminar las mismas con
células de otro donante o paciente durante la recolección, el
procesamiento o el almacenamiento.
Se debe efectuar la detección sistemática y las pruebas de enfermedades
transmisibles a los donantes de todas las fuentes de células que se
pretenden emplear en la elaboración de preparaciones celulares.
Se deben llevar a cabo sobre las preparaciones celulares, ensayos de
esterilidad (aerobios, anaerobios estrictos/facultativos y hongos), y
cuando corresponda ensayos de detección de micoplasmas, como requisitos
mínimos de seguridad.
La vida útil de las preparaciones celulares puede ser más breve que el
tiempo necesario para examinar la esterilidad y detectar agentes
adventicios con métodos tradicionales. El desarrollo de métodos
alternativos rápidos y validados permite la evaluación y la liberación
oportuna. En forma alternativa, se deberá controlar la esterilidad y
los agentes adventicios durante la elaboración con validaciones de
limpieza y controles de calidad de área y protocolos de trabajo
estrictos.
7.2.4.2.1- Controles de esterilidad
Debido a que no existen métodos aprobados para la evaluación de
esterilidad en preparaciones celulares, cada EPC debe elegir y validar
el método que usará.
7.2.4.2.2- Micoplasma
Existen diversas fuentes potenciales de contaminación por micoplasma.
Las preparaciones cuyas materias primas son de origen animal, tal como
el suero utilizado en el cultivo, y el mismo ambiente de cultivo, en
particular en los sistemas de cultivo abierto, son los principales
causantes de contaminación.
Los EPC, cuando corresponda, deben realizar la detección de
contaminación por micoplasma durante el proceso de elaboración, en los
puntos más críticos para detectarla. Por ejemplo, durante un proceso de
expansión celular, tomar la muestra de todos los recipientes de los
cultivos en marcha, antes del lavado de las células.
Debido a la limitada vida útil de muchas preparaciones celulares, no
siempre es posible realizar el ensayo recomendado, basado en el
cultivo, previo a la liberación de la preparación celular. En esos
casos, se deberán utilizar otros métodos más rápidos como el de la
reacción en cadena de la polimerasa (PCR). El EPC deberá documentar los
datos apropiados para demostrar que el análisis de PCR (u otro análisis
alternativo) posee la sensibilidad y especificidad adecuadas.
7.2.4.2.3.- Virus adventicios
Los EPC, en el caso de trabajar con BMC o BCT, deberán realizar la
detección de virus adventicios en las células del banco.
-
Análisis viral in vitro
Los EPC deberán realizar y documentar el análisis de detección viral in
vitro. Para realizar dicho análisis se deberá sembrar la muestra de
células del banco en varias líneas celulares indicadoras susceptibles,
tales como la línea de células humana MRC-5 o Vero de primates. La
elección de las células utilizadas dependerá de la especie de origen de
la preparación celular a analizar.
Un análisis adecuado debe incluir cultivos en monocapa de la misma
especie y tejido utilizado para la elaboración de la Preparación
Celular, así como una línea de células de primates no humanos y humanas
susceptibles a los virus humanos. Además, el análisis debe incluir una
medida de ambos virus citopático y hemadsorbente.
-
Análisis viral in vivo
Los EPC deberán realizar y documentar el análisis de detección viral in
vivo. Para realizar dicho análisis deberán inocular la muestra de
células en animales, tales como ratones adultos y lactantes y huevos
embrionados de gallina.
Se debe considerar la conveniencia de incluir el análisis adicional de
hámsters, conejos y monos. Estos estudios evalúan en los animales de
experimentación cualquier indicio de enfermedad. Si los análisis
adicionales son adecuados, se deben describir y explicar la aptitud de
los animales utilizados.
-
Análisis específicos de especie para
la detección de virus adventicios.
Los EPC deberán realizar y documentar el análisis de detección viral
específico de especie. Cada EPC deberá describir y registrar los
análisis que se llevan a cabo y en la etapa de elaboración en la que se
efectuó el análisis. En el caso de utilizarse una línea celular humana
realizar el análisis para detectar patógenos humanos (CMV, VIH-1 y 2,
HTLV-1 y 2, VEB, VHB, VHC, B19), y otros agentes virales humanos, según
corresponda. Este análisis es importante ya que las células son
manipuladas durante períodos de tiempo prolongados y los patógenos
humanos pueden ser introducidos o propagados durante los períodos de
cultivo extendidos.
7.2.4.3- Ensayos para
determinación de dosis
Las preparaciones celulares se pueden dosificar sobre la base de la
enumeración de una o más poblaciones de células. Cuando la preparación
está en una suspensión homogénea única de células, el ensayo más
utilizado es el número de células viables.
En el caso de preparaciones celulares no homogéneas, con células que
forman una estructura bi o tridimensional, pueden utilizarse mediciones
alternativas para enumeración, como el área total de una capa de
células, el peso húmedo, las proteínas totales o el ADN total, entre
otros.
Todas las metodologías para la determinación de la dosis deberán estar
contempladas en procedimientos escritos, y adecuadamente validados.
La dosis de una determinada preparación celular y los criterios y
metodologías para su determinación deben sustentarse en los
conocimientos adquiridos durante las fases de investigación previas, o
de la bibliografía científica al respecto.
7.2.4.4- Potencia
La potencia se define como la actividad terapéutica de la preparación
celular. Junto con la dosis, la potencia define la actividad biológica
de la preparación.
Los EPC deben definir los ensayos de potencia para cada preparación
celular, en función de la naturaleza de cada uno.
Las especificaciones de potencia deber ser verificadas con datos
surgidos de los estudios preclínicos y clínicos correspondientes, en
donde el estudio de potencia se correlacione con la funcionalidad de la
preparación celular.
Se debe incluir información sobre la valoración de la variabilidad
entre distintos lotes de la preparación, cuando corresponda, y, de ser
posible, contar con un material de referencia para utilizar como
control positivo.
Las determinaciones de potencia deben incluir, de ser posible, ensayos
cuantitativos y cualitativos, que deben ser documentados. Se debe
justificar sólidamente cuando, por la naturaleza de la preparación
celular, se dificulte la determinación cualitativa de la potencia.
7.2.4.5-
Pureza
Se debe optimizar el proceso de elaboración y purificación a fin de
eliminar impurezas constantemente y, al mismo tiempo, conservar la
actividad de la preparación.
Las pruebas de impurezas como parte de las pruebas específicas de
liberación de preparaciones celulares deben reflejar los riesgos de
seguridad asociados con la impureza, sobre todo cuando se trata de
impurezas bioactivas (citoquinas, hormonas), inmunogénicas (agregados
de productos, productos de degradación, proteínas no humanas) o que
ejerzan otros efectos perjudiciales.
Cada EPC debe validar la determinación de impurezas durante la
caracterización de la preparación celular.
Como parte de las pruebas de pureza los EPC deben llevar a cabo el
ensayo de determinación de endotoxinas, cuando corresponda.
7.2.4.6-
Identidad
Las pruebas de identidad deben ser apropiadas para el tipo de células
presentes en la preparación.
Si la preparación final contiene más de un tipo celular, se deberá
establecer la identidad de cada uno de ellos. Dichos controles deberán
registrarse.
Los ensayos de identidad deben validarse durante la etapa de desarrollo
de la preparación celular.
7.2.4.7- Estabilidad
7.2.4.7.1-
Consideraciones generales
El estudio de estabilidad siempre debe diseñarse sobre la base de
principios y enfoques científicamente sólidos, y un conocimiento cabal
de la Preparación final y su uso terapéutico previsto.
Un programa de estabilidad bien diseñado y ejecutado asegurará, en gran
medida, que la Preparación sea estable dentro de la vida útil
especificada.
7.2.4.7.2-
Desarrollo del protocolo de estabilidad
Los estudios de estabilidad deben estar detallados en un plan escrito
que determine cómo se obtendrán y analizarán los datos de estabilidad a
fin de avalar el período de caducidad de la preparación celular.
Los estudios deben incluir el análisis de las condiciones de
almacenamiento, transporte y otras variables que puedan surgir desde la
obtención de la preparación final hasta su aplicación.
Todos los ensayos empleados en el estudio de estabilidad deben ser
validados y estar contemplados en procedimientos escritos.
Los estudios de estabilidad deben verificar que las condiciones de
almacenamiento y transporte conserven la pureza y la potencia, de
manera que cuando la preparación se administre al paciente, siga
cumpliendo con las especificaciones de estabilidad.
Las especificaciones de estabilidad deber ser verificadas con datos
surgidos de los estudios preclínicos y clínicos correspondientes, en
donde el estudio de estabilidad se correlacione con la funcionalidad de
la Preparación Celular.
7.3-
Revisión de registro de la Preparación Celular
Antes de la liberación de una preparación celular, la misma debe contar
con una autorización escrita, extendida por el responsable designado
para ello.
La evaluación de las preparaciones terminadas debe abarcar todos los
factores relevantes, incluyendo las condiciones de elaboración, los
resultados de los controles en proceso, la documentación de la
elaboración (incluyendo el acondicionamiento), cumpliendo con las
especificaciones para la preparación terminada.
Los registros de producción y control de calidad deben ser revisados
como parte del proceso de aprobación de la liberación de la preparación
celular. Cualquier divergencia con las especificaciones deber ser
profundamente investigada. Se debe llevar un registro escrito de la
investigación e incluir la conclusión y la acción a seguir.
7.4-
Registros de controles y ensayos
Cada EPC deberá mantener un registro de los resultados de los controles
y ensayos exigidos por esta norma. Estos registros deben incluir los
criterios de aceptación, las comparaciones de controles realizados, los
resultados, el equipamiento usado y, la fecha y firma del responsable
del control y del ensayo.
7.5-
Liberación y administración de preparaciones celulares
7.5.1-
Consideraciones generales
Antes de administrar una preparación celular a un paciente, puede ser
necesario efectuar operaciones para la obtención de la dosis de la
preparación final, que dependerán de la naturaleza de la misma. Estas
operaciones pueden incluir descongelación, lavado, filtrado para
eliminar sustancias no deseadas acumuladas durante el procesamiento,
transferencia a una solución infusible, preparación con un soporte,
entre otras.
Todas estas modificaciones y sus controles deben ser definidos y
determinarse con precisión las especificaciones a las cuales la
Preparación debe ajustarse.
7.5.2-
Liberación de la preparación celular final
Los EPC deben llevar a cabo controles o pruebas adecuadas sobre las
preparaciones celulares finales para asegurarse que cumplan con las
especificaciones de calidad antes de ser liberadas para su
administración a pacientes.
Los requisitos mínimos deben incluir:
• Inspección física de la preparación celular, que incluyen por lo
general, medidas para garantizar que tenga el aspecto adecuado en
cuanto a color, turbidez, presencia de materia o partículas extrañas,
integridad del envase, temperatura y etiquetado apropiado y exacto.
• Revisión de los registros de los procesos.
• Inspección administrativa de los registros relativos a la identidad
del receptor previsto.
• Revisión de los resultados existentes hasta ese momento, de los
ensayos de calidad que contemplen la identidad, esterilidad, potencia y
pureza de la preparación celular.
• Revisión de los registros de elegibilidad del donante cuando
corresponda.
7.5.3-
Administración a pacientes
El paciente receptor de la preparación celular deberá ser acondicionado
por personal idóneo a fin de reducir aspectos negativos que lleven a
que dicha preparación no brinde el resultado biológico previsto,
minimizando el riesgo de efectos adversos.
Se debe efectuar una evaluación completa del estado general del
paciente y su aptitud para el tratamiento en las cercanías del momento
de la administración de la preparación, independientemente de cualquier
evaluación efectuada con anterioridad.
Se deben evaluar los tratamientos concomitantes que puedan interactuar
con las preparaciones celulares.
El EPC debe contar con políticas y procedimientos escritos para
notificarse de la evolución de los pacientes. El examen de evolución
del paciente debe incluir indicadores capaces de detectar errores o
problemas relacionados con todo el proceso de elaboración, con especial
atención a las manipulaciones, el almacenamiento o el transporte
después de la elaboración de la preparación.
Los efectos adversos serios deben ser debidamente notificados al
INCUCAI.
7.6-
Resultados de mediciones y ensayos
Cada EPC deberá consignar en forma visible los resultados de las
mediciones y de los ensayos de todas las preparaciones celulares en
procesamiento, materias primas utilizadas en la misma, incluyendo
materiales de envasado y embalaje. Se deberá indicar la conformidad o
no conformidad de estos ítems para asegurar que sólo sean distribuidos
y utilizados aquellos que hayan pasado por las inspecciones y ensayos
exigidos.
Cada EPC deberá asegurar que los registros identifiquen la persona
responsable de la liberación de la Preparación Celular.
7.7-
Control ambiental
Cada EPC deberá establecer y mantener un sistema de control para
prevenir la contaminación u otros efectos adversos sobre la preparación
celular apta para su aplicación, y proveer condiciones de trabajo
adecuadas para todas las operaciones. Las condiciones a ser
consideradas para este control incluyen: iluminación, ventilación,
espacio, temperatura, humedad, presión barométrica, contaminación
aérea, electricidad estática y otras condiciones ambientales.
Cada EPC deberá inspeccionar periódicamente sus instalaciones y revisar
su sistema de control para verificar si éste es adecuado y está
funcionando correctamente. Deberá efectuarse un registro y una revisión
de los resultados de esas inspecciones.
7.8-
Procesos automatizados
Cuando fueran usadas computadoras en el procesamiento, en el sistema de
calidad o en los sistemas de procesamiento de datos, personas
designadas por el EPC deberán validar el software de acuerdo con un
protocolo establecido. Los resultados deberán ser documentados. Todas
las modificaciones del software deberán ser hechas a través de una
validación establecida y procedimientos aprobados, de acuerdo con la
modificación de documentos en el Capítulo Documentos y Registros de
este Anexo.
8-
CALIFICACION Y VALIDACION
Cada EPC debe identificar los trabajos de calificación y validación
requeridos para probar que los aspectos críticos de sus operaciones
particulares son controlados. Debe emplearse un enfoque de análisis de
riesgo para determinar el ámbito y la amplitud de la validación.
Los elementos clave de un programa de calificación y validación de un
EPC deben estar claramente definidos y documentados en un plan maestro
de validación.
La calificación y validación debe establecer y proveer evidencia
documentada de que:
a) los locales, sistemas de soporte, equipamiento y procesos han sido
diseñados de acuerdo con los requerimientos para las BPEyL;
b) los locales, sistemas de soporte y equipamiento han sido construidos
e instalados en cumplimiento con las especificaciones de su diseño;
c) los locales, sistemas de soporte y equipamiento operan de acuerdo
con las especificaciones de su diseño;
d) un proceso específico producirá consistentemente una preparación con
sus especificaciones predeterminadas y atributos de calidad.
Cualquier aspecto de operación, incluyendo cambios significativos en
los locales, instalaciones, equipamiento o procesos, los cuales puedan
afectar la calidad de la preparación, directa o indirectamente, debe
estar calificado y validado.
La calificación y validación no deben considerarse excluyentes. Deben
basarse en una revisión anual y se debe seguir un programa continuo
para su implementación.
El compromiso de mantener un estado de validación debe estar
especificado en la documentación relevante del EPC, como el manual de
calidad o un plan maestro de validación.
La responsabilidad de llevar a cabo la validación debe estar claramente
definida.
Se debe preparar y guardar un reporte escrito, resumiendo los
resultados registrados y las conclusiones alcanzadas.
Los procesos y procedimientos deben estar establecidos en base a los
resultados de la validación realizada.
Es de importancia crítica prestar particular atención a la validación
de métodos analíticos de ensayo, sistemas automatizados y
procedimientos de limpieza.
9-
MATERIALES Y PREPARACIONES NO CONFORMES
Cada EPC deberá establecer y mantener procedimientos para asegurar que
materiales y preparaciones que no estén en conformidad con los
requisitos exigidos sean eliminados.
10- ACCION
CORRECTIVA
Cada EPC deberá establecer y mantener procedimientos para:
Analizar todos los procesos, operaciones de procesamiento, informes de
auditoría de calidad, registros de calidad, reclamos y otras fuentes de
datos de calidad para identificar las causas existentes y potenciales
de preparaciones y materiales de procesamiento no conformes y otros
problemas de calidad (el estudio deberá incluir análisis de tendencias
para detectar problemas de calidad recurrentes).
Investigar la no conformidad a las especificaciones.
Identificar la acción necesaria para prevenir la causa y prevenir la
recurrencia de preparaciones celulares, materiales de procesamiento y/o
fuentes de células no conformes o con cualquier otro problema de
calidad.
Verificar o validar la adecuación de la acción correctiva para asegurar
que la misma no afecte adversamente la preparación celular apta para
implante.
Implementar y registrar modificaciones en métodos y procedimientos
necesarios como consecuencia de la identificación de problemas de
calidad y de acciones correctivas.
Asegurar que toda información sobre problemas de calidad sea divulgada
entre todos los responsables de asegurar la calidad.
Todas las actividades exigidas en esta sección, así como sus
resultados, deben ser documentados.
11-
EMBALAJE, ROTULADO Y TRANSPORTE
11.1-
Embalaje de fuentes de células y Preparaciones celulares
Cada EPC deberá proyectar y elaborar el embalaje y contenedores para
proteger a las fuentes de células a procesar y a las preparaciones
celulares de cualquier alteración o daño durante las condiciones
establecidas de obtención, procesamiento, almacenamiento, manipulación
y distribución.
Se deben seleccionar y validar los materiales de refuerzo y aislamiento
para armar un sistema de embalaje que contemple las condiciones
extremas de transporte.
El embalaje que se diseñe debe contemplar, por lo menos, los siguientes
elementos:
1. Embalaje interior. Debe estar compuesto por:
1.1. Envase primario. Debe ser hermético, estanco y estar identificado.
1.2. Envase secundario. Debe cumplir, siempre que sea posible, con las
siguientes condiciones:
a) ser hermético, estanco y estar identificado;
b) en caso de que se coloquen varios envases primarios en un solo
envase secundario, se los debe separar convenientemente para evitar
todo contacto entre ellos, con la finalidad de prevenir roturas y
desplazamientos;
c) llevar adherida a la superficie exterior del envase secundario una
lista pormenorizada de su contenido.
1.3. Material absorbente adecuado. Se debe colocar entre el o los
envases primarios y el envase secundario, en cantidad suficiente para
poder absorber la totalidad del contenido del envase en caso de pérdida
o rotura.
2. Embalaje exterior. Puede contener uno o más envases secundarios y
debe cumplir con las siguientes condiciones:
2.1. poseer una adecuada resistencia con relación a la capacidad, masa
y uso al que esté destinado;
2.2. la dimensión exterior más pequeña no debe ser menor a 100 mm;
2.3. solamente debe contener las fuentes de células para procesamiento
o las preparaciones celulares para aplicación;
2.4. se deben colocar las identificaciones correspondientes, definidas
por la legislación vigente, las cuales se deben aplicar de manera de no
ser fácilmente desprendidas y/o retiradas del embalaje exterior.
11.2-
Rotulado
Cada EPC deberá establecer y mantener procedimientos para asegurar la
integridad del rotulado y para evitar el cambio de los mismos y/o de
etiquetas identificadoras.
11.2.1-
Integridad de los rótulos
Cada EPC deberá asegurar que los rótulos sean diseñados, impresos y,
cuando corresponda, aplicados para permanecer legibles y adheridos al
envase durante las condiciones establecidas de obtención de la fuente
de células, procesamiento, almacenamiento y distribución previa al uso.
11.2.2-
Inspección de los rótulos e instructivos
Los rótulos no deberán ser liberados para depósito o para uso hasta que
una persona autorizada haya examinado su exactitud.
11.2.3-
Almacenamiento de los rótulos
Cada EPC deberá almacenar y mantener los rótulos de manera de
proporcionar su pronta identificación y evitar confusiones.
11.2.4-
Control de los rótulos
Cada EPC deberá controlar los rótulos y las operaciones de embalado
para evitar la confusión de rótulos.
Los rótulos de los envases contenedores de la fuente de células o
Preparación Celular incluirán los siguientes datos:
a) nombre o código de identificación
b) nominación del contenido y uso a los que está destinado;
c) nombre, domicilio y número de teléfono del receptor del envío y del
remitente;
d) fecha y hora de liberación y/o vencimiento del medio de transporte o
de la Preparación Celular, cuando corresponda;
e) las siguientes leyendas “Material para usar por única vez” y “No
utilizar si el envase no está íntegro”;
f) informar la presencia de trazas de antibióticos, preparaciones con
materias primas de origen porcino, bovino u otra fuente animal, si
correspondiese;
g) una etiqueta de “Sustancia infecciosa – División 6.2” y las otras
etiquetas exigidas por la naturaleza del contenido;
h) indicador de posición, informando sobre la orientación del embalaje,
cuando corresponda;
i) indicador de cadena de frío y temperatura de conservación.
Las etiquetas se deben ubicar en cada una de las dos caras opuestas del
embalaje. Si el envase es cilíndrico, se deben ubicar tres etiquetas
equidistantes sobre la superficie lateral del cuerpo, y nunca en la
tapa.
11.3-
Documentación
Al embalaje exterior se debe adjuntar una serie de documentos que deben
incluir, como mínimo:
a) instrucciones para el correcto manejo de la preparación celular a
fin de garantizar el uso aséptico y prevenir contaminaciones en el
momento de su utilización;
b) lista de envío de material biológico, en donde se detallen:
- nombre del receptor del envío, del remitente y del transportista;
- dirección y teléfonos de contacto del receptor del envío, del
remitente y del transportista;
- características y detalles del envío;
- toda otra indicación que se considere pertinente.
La lista de envío se debe hacer por triplicado y debe incluir:
a) una copia que queda en poder del remitente firmada por el
transportista, en la cual se debe registrar hora de salida;
b) otra copia que queda en poder del transportista firmada por el
receptor del envío, en la cual se debe registrar la hora de recepción
del envío;
c) una tercera copia que queda en poder del receptor del envío y debe
estar firmada por el remitente y por el transportista.
11.4-
Transporte
El transporte de fuentes de células y preparaciones celulares deberá
ajustarse a las reglamentaciones vigentes sobre transporte y se
efectuará conforme a los circuitos claramente establecidos y definidos
para cada tipo de preparación. Cada EPC deberá contar con
procedimientos de transporte.
11.4.1-
Condiciones del Transporte
La elección del modo de transporte se hará según criterios de seguridad
y de respeto de las condiciones de conservación correspondiente a las
características de la fuente de células o preparación celular a
transportar. El seguimiento y la transmisión de la información
concerniente al material transportado deben estar asegurados. El
transporte se establece según circuitos validados, asegurando la
información entre las diferentes personas y/o instituciones
intervinientes involucradas con relación a la naturaleza del material y
las condiciones del transporte. La seguridad de las personas que
intervengan debe estar resguardada.
La hora de llegada y las condiciones de recepción, principalmente la
temperatura cuando ésta deba ser mantenida a valores específicos,
deberán ser registradas e informadas.
11.4.2-
Organización del circuito
El circuito deberá estar aprobado por las partes intervinientes. Esta
aprobación debe contener la elección de la empresa de transporte, como
así también información del personal interviniente, del rótulo del
material transportado y de su embalaje.
11.4.3-
Modo de Transporte
Las condiciones de transporte están definidas por un acuerdo de
servicios que le es exigido al transportador que está bajo contrato, o
por reglamentación si el transportador forma parte de un
establecimiento de salud. El acuerdo de servicios debe estar incluido
en el manual de procedimientos de transporte.
El EPC será responsable de validar que el método de transporte asegure
el mantenimiento de la temperatura en los valores especificados.
El material refrigerado debe ser transportado en un recipiente adecuado
que permita una autonomía suficiente, a los efectos de garantizar el
mantenimiento de la temperatura del mismo en caso en que el transporte
hubiese durado dos veces más de lo previsto a la hora de la salida.
Se deben realizar estudios para determinar si las condiciones de
transporte son aceptables para mantener las especificaciones de calidad
y estabilidad de la preparación celular.
Durante el desarrollo del sistema de embalaje, se deben diseñar
estudios de transporte de carga para identificar las condiciones
adversas que podrían afectar a las preparaciones celulares.
El transporte de las preparaciones celulares debe ser efectuado por
transportistas habilitados para transporte de sustancias biológicas.
El transportista debe tener y conocer un plan de contingencia escrito y
contar con el material necesario para poder ejecutarlo.
12-
GLOSARIO
ANEXO
II
“CRITERIOS
DE MANIPULACION CELULAR QUE NO IMPLIQUEN MODIFICACION SUSTANCIAL DE LA
PREPARACION CELULAR”
INTRODUCCION
Ha sido mencionado en el ANEXO I punto 1.3 – VIII, la clasificación de
las preparaciones celulares en dos grupos: preparaciones celulares con
manipulación mínima (PCMM) y preparaciones celulares con manipulación
avanzada (PCMA).
Los PCMM son aquellas células que son sometidas a una o varias de las
manipulaciones que serán descriptas en el ítem siguiente.
Las manipulaciones celulares que se realizan durante el trasplante de
médula ósea para tratar enfermedades sanguíneas ejemplifican a un PCMM.
Toda preparación celular que implique alguna manipulación adicional a
las descriptas en este anexo será definido como PCMA.
LISTADO DE MANIPULACIONES
1- CORTE
2- TRITURACION
3- MOLDEO
4- CENTRIFUGACION
5- IMBIBICION EN DISOLUCIONES
ANTIBIOTICAS O ANTIMICROBIANAS
6- ESTERILIZACION
7- IRRADIACION
8- SEPARACION, CONCENTRACION O
PURIFICACION CELULAR
9- FILTRADO
10- LIOFILIZACION
11- CONGELACION
12- CRIOPRESERVACION
13- VITRIFICACION
ANEXO III
“CRITERIOS DE
ELEGIBILIDAD DE DONANTES DE CELULAS Y TEJIDOS PARA LA ELABORACION DE
PREPARACIONES CELULARES”
1- De
todos los donantes
a) Los EPC deberán definir los criterios de elegibilidad para proteger
la seguridad de los receptores y, cuando sea aplicable, identificar las
condiciones que pueden afectar adversamente el valor potencial
terapéutico de las preparaciones celulares. Para donantes de sangre de
cordón, además de la evaluación de la historia clínica y riesgos de
enfermedades infecciosas de la madre, los EPC deberán definir los
criterios usados para detectar infecciones u otras anormalidades en los
recién nacidos que potencialmente podrían afectar la seguridad de los
receptores, o el valor terapéutico de las preparaciones celulares.
b) Los EPC deberán evaluar la elegibilidad del donante de acuerdo con
estos criterios definidos, basados en el riesgo clínico y ensayos de
laboratorio.
c) La determinación de la elegibilidad deberá ser llevada a cabo y
aprobada de manera tal y en un lapso de tiempo que provea la
información relevante y proteja la seguridad de los receptores.
d) Los registros de elegibilidad de donantes deberán ser revisados
antes de la administración de un régimen de condicionamiento del
receptor.
e) La procuración y uso de preparaciones celulares provenientes de
donantes alogénicos que no alcancen los criterios de elegibilidad,
deberán requerir aprobación por escrito del director médico de la
institución y del profesional médico del paciente.
f) Para donantes que no alcanzan los criterios de elegibilidad, la
institución deberá guardar registros de:
i- Las razones por las que el donante no alcanza los criterios de
elegibilidad.
ii- La notificación del donante.
iii- Identificación y disposición final de fuente de células
previamente colectadas, si se hubiera descubierto posteriormente a la
procuración, que el donante no cumple los criterios de elegibilidad.
2-
Requerimientos específicos de donante
2.1- Donantes alogeneicos
a) La evaluación y aprobación de la elegibilidad deberán ser realizadas
antes de que el receptor reciba la terapia de acondicionamiento de
médula.
b) Los registros de elegibilidad del donante deberán ser revisados
antes de las intervenciones asociadas a la procuración (Por ejemplo,
administración de drogas, factores de crecimiento).
c) Si el donante es considerado absolutamente inelegible antes de la
procuración, el director médico de la institución deberá proveer una
aprobación escrita.
2.2- Donantes autólogos
El profesional médico del donante autólogo deberá realizar una
valoración de la salud del mismo antes de los procedimientos de
procuración planificados.
2.3- Madres de donantes de sangre de
cordón
a) La historia clínica personal y familiar y la historia genética de la
familia del probable donante de sangre de cordón deberán ser obtenidas
antes de la procuración, pero como máximo 7 días antes.
b) Si la historia clínica es obtenida antes de los 7 días previos a la
procuración, deberá ser revisada contemplando probables cambios como
consecuencia de exposición de la madre a enfermedades infecciosas.
En el caso de una madre subrogante, su historia clínica deberá ser
obtenida y documentada, además de los padres biológicos. No será
necesario contar con la historia genética de la madre subrogante.
2.4- Donantes cadavéricos
a) La evaluación de la elegibilidad del donante deberá ser obtenida a
través de la información de un miembro de la familia u otra fuente
relevante.
b) Cuando los tejidos son procurados de donantes cadavéricos, la
institución deberá especificar el tipo de donante (donante a corazón
batiente o corazón parado), según los protocolos en uso.
El EPC debe describir el tipo de pruebas que efectúa, los datos de las
historias clínicas y diagnósticos obtenidos de los donantes y
considerar otras cuestiones, tales como la tipificación de los
polimorfismos y la compatibilidad de los antígenos del complejo
molecular de histocompatibilidad (MHC clase I-II) también denominado
sistema HLA (antígenos leucocitarios humanos), según sea necesario en
cada caso.
2.5- Tabla de elegibilidad
e. 06/06/2012 Nº 61243/12 v. 06/06/2012