MINISTERIO DE SALUD
SECRETARIA DE POLITICAS, REGULACION E INSTITUTOS
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
Disposición Nº 872/2014
Bs. As., 31/1/2014
VISTO las Disposiciones ANMAT N° 241/2013 y 6052/2013 y el Expediente
N° 1-47-0000-014375-13-1 del Registro de esta Administración Nacional
de Medicamentos, Alimentos y Tecnología Médica; y
CONSIDERANDO:
Que por Decreto N° 1490/92 se creó esta Administración Nacional de
Medicamentos, Alimentos y Tecnología Médica (ANMAT) como organismo
descentralizado de la Administración Pública Nacional con un régimen de
autarquía económica y financiera, con jurisdicción en todo el
territorio de la Nación.
Que el aludido decreto declaró de interés nacional las acciones
dirigidas a la prevención, resguardo y atención de la salud de la
población que se desarrollen a través del control y fiscalización de la
calidad y sanidad, entre otros, de los productos, sustancias, elementos
y materiales que se consumen o utilizan en la medicina humana, y del
contralor de las actividades, procesos y tecnologías que mediaren o
estuvieren comprendidos en dichas materias.
Que asimismo el artículo 3º del referido decreto establece que esta
Administración Nacional tendrá competencia en todo lo referido al
control y la fiscalización sobre la sanidad y calidad, entre otros
productos, de los reactivos, elementos de diagnóstico, materiales y
tecnología biomédicos y todo otro producto de uso y aplicación en la
medicina humana.
Que por otra el artículo 8º, inc. m) del Decreto N° 1490/92 otorga a
esta Administración Nacional la atribución de determinar y percibir los
aranceles y tasas retributivas correspondientes a los trámites y
registros que se efectúen, como así también por los servicios que se
presten.
Que, por su parte, de conformidad a lo establecido en el artículo 11
del referido cuerpo normativo, esta Administración Nacional dispone
para el desarrollo de sus acciones de los recursos allí enumerados,
entre los que se encuentran incluidos los provenientes de las tasas y
aranceles que aplique conforme a las disposiciones adoptadas, los
recargos establecidos por la mora en el pago de las tasas, multas y
aranceles que perciba y todo otro tipo de recurso que se determine a
través de las leyes y disposiciones que se establezcan con tal
finalidad.
Que los montos actuales que esta Administración Nacional percibe por
los servicios que presta relación con tales tramitaciones han devenido
insuficientes para llevar a cabo de manera eficiente las tareas
correspondientes, cuya complejidad y especificidad se incrementan con
el permanente avance científico y tecnológico producido en el sector.
Que sobre la base de las sugerencias efectuadas por la Dirección
Nacional de Productos Médicos resulta necesario modificar la
denominación de los Apartados B) Trámites correspondientes a la
Disposición N° 194/99, C) Trámites correspondientes a la Disposición N°
2318/02 (t.o. 2004), D) Trámites correspondientes a la Disposición N°
2319/02 (t.o. 2004), E) Trámites correspondientes a la Disposición N°
806/07 y del ítem Autorización de funcionamiento de empresa fabricante
y/o Importadora de Productos Médicos clase III del Apartado D) punto 1
del Anexo de la Disposición ANMAT N° 241/13.
Que asimismo corresponde la eliminación del punto 2.- Habilitaciones y
el punto 3.- Certificaciones correspondientes al Apartado A) Productos
para Diagnóstico de Uso “In Vitro” del Anexo de la citada Disposición
ANMAT N° 241/13.
Que por otra parte resulta conveniente incorporar los aranceles
correspondientes a 1) “Certificación de Cumplimiento de BPF para
Empresas Radicadas en Países Integrantes de Mercosur” con los
siguientes ítems “Verificación de cumplimiento de BPF por planta
Mercosur, para productos médicos clase I”, “Verificación de
cumplimiento de BPF por planta Mercosur, para productos médicos clase
II”, “Verificación de cumplimiento de BPF por planta Mercosur, para
productos médicos clase III”, “Verificación de cumplimiento de BPF por
planta Mercosur, para productos médicos clase IV”, “Ampliación de rubro
de certificado de cumplimiento de las BPF por planta Mercosur para
productos médicos clase I, II, III y/o IV” y “Modificación de
Estructura por planta Mercosur para productos médicos clase I, II, III
y IV” en el rubro correspondiente a Cumplimiento de Buenas Prácticas de
Fabricación, 2) Cambio de Domicilio Legal en los rubros Autorización de
funcionamiento de empresa (A.F.E), Productos Higiénicos, Absorbentes y
Descartables y Distribuidoras de Productos Médicos y/o Productos para
Diagnósticos de Uso in Vitro 3) Renovación de Certificado de Buenas
Prácticas de reacondicionamiento, Incorporación de Anexo de Certificado
por familia de productos clase I, Incorporación de Anexo de Certificado
por familia de productos clase II, e Incorporación de Anexo de
Certificado por familia de productos clase III en el rubro
correspondiente a Productos Médicos Usados y 4) Certificados de Libre
Venta en el rubro Productos Registrados en el País.
Que finalmente resulta conveniente proceder a la unificación de los
Items Ampliación de Rubro de certificado de Cumplimiento de las BPF
(para producto médico clase I), Ampliación de Rubro de certificado de
Cumplimiento de las BPF (para producto médico clase II), Ampliación de
Rubro de certificado de Cumplimiento de las BPF (para producto médico
clase III y/o IV a partir de certificados clase I), Ampliación de Rubro
de certificado de Cumplimiento de las BPF (para producto médico clase
III y/o IV a partir de certificados clase II), Ampliación de Rubro de
certificado de Cumplimiento de las BPF (para producto médico clase III
y/o IV a partir de certificados clase III/IV) previstos en el Apartado
B) punto 1 del Anexo de Disposición ANMAT N° 241/13 y de los ítems
Ampliación de Rubro de certificado de Cumplimiento de las BPF para
producto médico clase I, Ampliación de Rubro de certificado de
Cumplimiento de las BPF para producto médico clase II, Ampliación de
Rubro de certificado de Cumplimiento de las BPF para producto médico
clase III, Ampliación de Rubro de certificado de Cumplimiento de las
BPF para producto médico clase VI y los ítems Modificación de
Estructura para Productos Médicos Clase I, Modificación de Estructura
para Productos Médicos Clase II, Modificación de Estructura para
Productos Médicos Clase III y Modificación de Estructura para Productos
Médicos Clase IV previstos en el Apartado B) punto 2 del Anexo de la
Disposición ANMAT N° 241/13.
Que en virtud de todo lo expuesto deviene necesario modificar los
montos de los aranceles vigentes respecto de los servicios prestados
por esta Administración Nacional, fijándolos en un valor acorde con la
excelencia en la calidad que requiere la fiscalización de las
industrias involucradas.
Que la Dirección Nacional de Productos Médicos y la Dirección General
de Administración han tomado la intervención de su competencia.
Que la Dirección General de Asuntos Jurídicos ha tomado la intervención de su competencia.
Que se actúa en virtud de las facultades conferidas por los Decretos N° 1490/92 y por el Decreto N° 1271/13.
Por ello,
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
DISPONE:
ARTICULO 1° — Modifícanse los montos de los aranceles que devengarán
las tramitaciones que se realicen ante la Administración Nacional de
Medicamentos, Alimentos y Tecnología Médica (ANMAT) correspondientes a
los productos para diagnóstico de uso “in vitro”, trámites
correspondientes a Cumplimiento de Buenas Prácticas de Fabricación
(BPF), trámites correspondientes para la Inscripción de Productos
Médicos, trámites correspondientes a Autorización de Funcionamiento de
Empresa (A.F.E), trámites correspondientes a Productos Médicos Usados,
Productos higiénicos, absorbentes y descartables, Estudios de
investigación en Tecnología Médica, Certificado de Libre Venta para
Productos Registrados en el País, Distribuidoras de Productos Médicos
y/o Productos para Diagnóstico de Uso in Vitro y certificados de libre
sanción, conforme el detalle que, como Anexo, forma parte integrante de
la presente disposición.
ARTICULO 2° — Establécense los montos de los aranceles que devengarán
las tramitaciones que se realicen ante la Administración Nacional de
Medicamentos, Alimentos y Tecnología Médica correspondientes a: 1)
Verificación de cumplimiento de BPF por planta Mercosur, para productos
médicos clase I, 2) Verificación de cumplimiento de BPF por planta
Mercosur, para productos médicos clase II, 3) Verificación de
cumplimiento de BPF por planta Mercosur, para productos médicos clase
III, 4) Verificación de cumplimiento de BPF por planta Mercosur, para
productos médicos clase IV, 5) Ampliación de rubro de certificado de
cumplimiento de las BPF por planta Mercosur para productos médicos
clase I, II, III y/o IV, 6) Modificación de Estructura para productos
médicos clase I, II, III y IV, 7) Cambio de Domicilio Legal, 8)
Renovación de Certificado de buenas prácticas de reacondicionamiento,
9) Incorporación de Anexo de Certificado por familia de productos clase
I, 10) Incorporación de Anexo de Certificado por familia de productos
clase II, 11) Incorporación de Anexo de Certificado por familia de
productos clase III y 12) Certificados de Libre Venta, conforme el
detalle que, como Anexo, forma parte integrante de la presente
disposición.
ARTICULO 3° — Establécese que los Apartados B) Trámites
correspondientes a la Disposición N° 194/99, C) Trámites
correspondientes a la Disposición N° 2318/02 (t.o. 2004), D) Trámites
correspondientes a la Disposición N° 2319/02 (t.o. 2004), E) Trámites
correspondientes a la Disposición N° 806/07 y el ítem “Autorización de
funcionamiento de empresa fabricante y/o Importadora de Productos
Médicos clase III (Incluye el otorgamiento del primer certificado de
BPF)” del Apartado D punto 1 del Anexo de la Disposición ANMAT N°
241/13 se denominarán, respectivamente: B) Trámites correspondientes a
cumplimiento de Buenas Prácticas de Fabricación (BPF), C) Trámites
correspondientes para la Inscripción de Productos Médicos, D) Trámites
correspondientes a Autorización de funcionamiento de empresa (A.F.E),
E) Trámites correspondientes a Productos Médicos Usados y “Autorización
de funcionamiento de empresa fabricante y/o Importadora de Productos
Médicos clase III y Productos para Diagnóstico de Uso in Vitro (Incluye
el otorgamiento del primer certificado de BPF)”.
ARTICULO 4° — Establécese que los ítems Ampliación de Rubro de
certificado de Cumplimiento de las BPF (para producto médico clase I),
Ampliación de Rubro de certificado de Cumplimiento de las BPF (para
producto médico clase II), Ampliación de Rubro de certificado de
Cumplimiento de las BPF (para producto médico clase III y/o IV a partir
de certificados clase I), Ampliación de Rubro de certificado de
Cumplimiento de las BPF (para producto médico clase III y/o IV a partir
de certificados clase II), Ampliación de Rubro de certificado de
Cumplimiento de las BPF (para producto médico clase III y/o IV a partir
de certificados clase III/IV) previstos en el Apartado B) punto 1 del
Anexo de Disposición ANMAT N° 241/13 quedan incluidos en el ítem
Ampliación de Rubro de Certificado de cumplimiento de las BPF (para
producto médico clase I, II, III y IV) del apartado B punto 1 del Anexo
de la presente disposición.
ARTICULO 5° — Establécese que los ítems Ampliación de Rubro de
certificado de Cumplimiento de las BPF para producto médico clase I,
Ampliación de Rubro de certificado de Cumplimiento de las BPF para
producto médico clase II, Ampliación de Rubro de certificado de
Cumplimiento de las BPF para producto médico clase III, Ampliación de
Rubro de certificado de Cumplimiento de las BPF para producto médico
clase VI y los ítems Modificación de Estructura para Productos Médicos
Clase I, Modificación de Estructura para Productos Médicos Clase II,
Modificación de Estructura para Productos Médicos Clase III y
Modificación de Estructura para Productos Médicos Clase IV previstos en
el Apartado B) punto 2 del Anexo de la Disposición ANMAT N° 241/13
quedan incluidos, respectivamente, en ítem Ampliación de Rubro de
certificado de Cumplimiento de las BPF para producto médico clase I,
II, III y IV y en el ítem Modificación de Estructura para Productos
Médicos Clase I, II, III y IV del Apartado B) punto 2 del Anexo de la
presente disposición.
ARTICULO 6° — Derógase el Anexo de la Disposición ANMAT Nº 241/13.
ARTICULO 7° — La presente disposición entrará en vigencia a partir del día siguiente al de su publicación en el Boletín Oficial.
ARTICULO 8° — Regístrese. Dése a la Dirección Nacional del Registro
Oficial para su publicación. Comuníquese a las Cámaras y Entidades
Profesionales; a la Dirección de Relaciones Institucionales y
Regulación Publicitaria y a la Dirección General de Administración.
Cumplido, archívese. — Dr. CARLOS CHIALE, Administrador Nacional,
A.N.M.A.T.
ANEXO I
PRODUCTOS MEDICOS (TECNOLOGIA MEDICA)
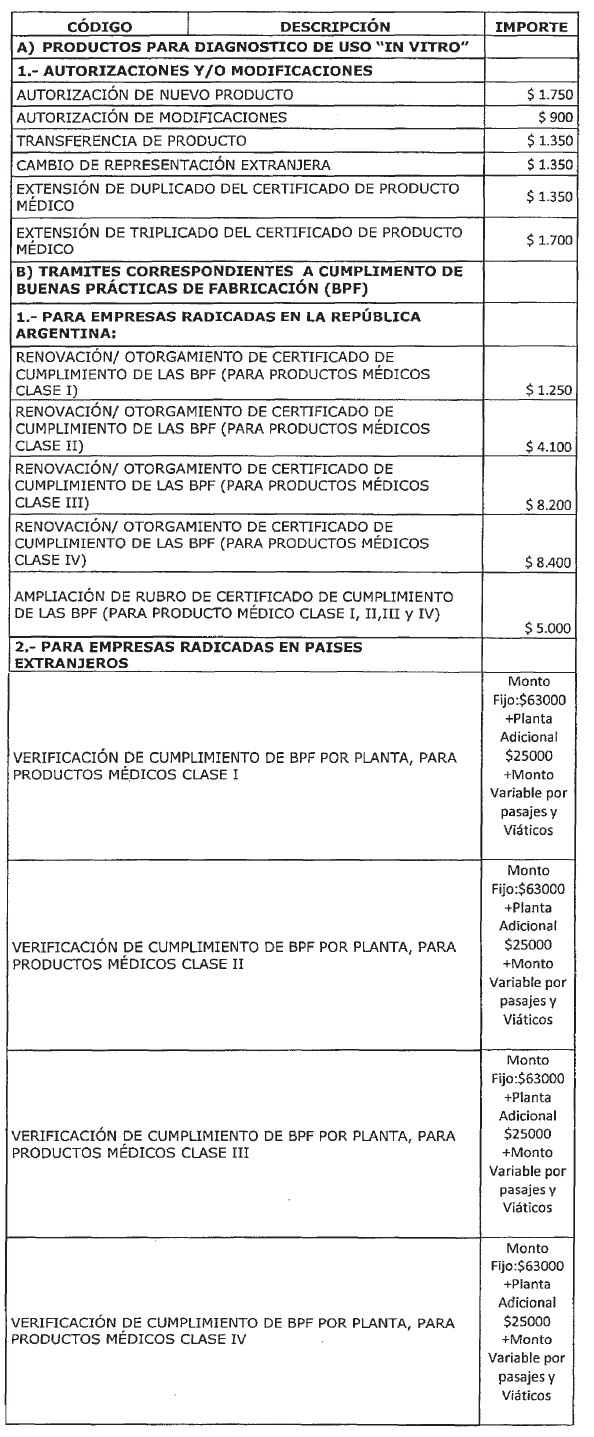

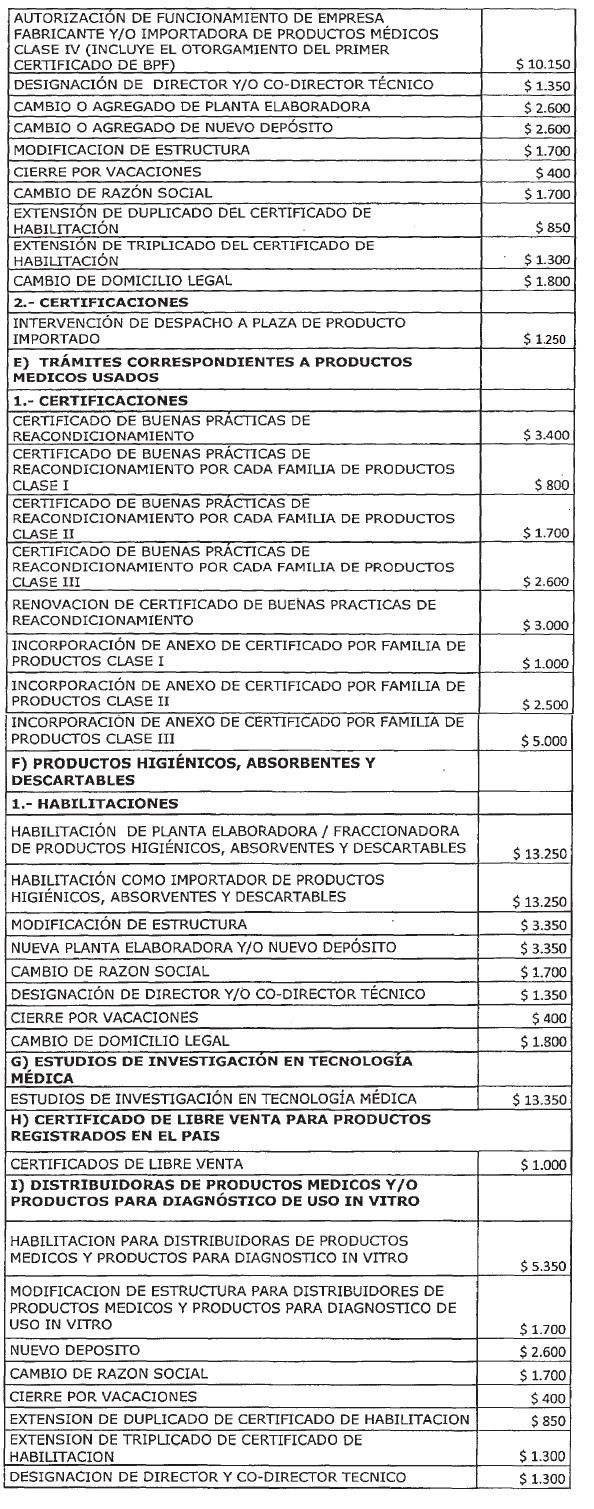
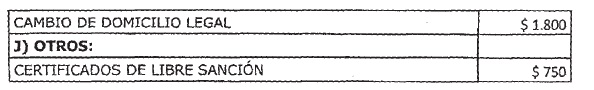
(Anexo,
Apartado D) TRAMITES CORRESPONDIENTES A AUTORIZACION DE FUNCIONAMIENTO
DE EMPRESAS (A.F.E.), ITEM 2.- CERTIFICACIONES: INTERVENCION DE
DESPACHO A PLAZA DE PRODUCTO IMPORTADO, monto del arancel rectificado
por art. 1° de la Disposición N° 1015/2014
de la Administración Nacional de Medicamentos, Alimentos y Tecnología
Médica B.O. 12/02/2014. Vigencia: a partir del día hábil siguiente al
de su publicación en el Boletín Oficial)





