MINISTERIO DE SALUD
SECRETARIA DE POLITICAS, REGULACION E INSTITUTOS
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
Disposición Nº 4548/2014
Bs. As., 1/7/2014
VISTO el Expediente Nº 1-0047-0000-008152-14-6 del registro de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
- ANMAT, organismo que funciona en la órbita de la SECRETARIA DE
POLlTICAS, REGULACION E INSTITUTOS del MINISTERIO DE SALUD, el Decreto
Nº 1271 de fecha 29 de agosto de 2013, y
CONSIDERANDO:
Que por Decreto Nº 1271/13 se aprobó la estructura organizativa de
primer nivel operativo de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA - ANMAT, organismo que funciona en la
órbita de la SECRETARIA DE POLlTICAS, REGULACION E INSTITUTOS del
MINISTERIO DE SALUD, conforme el Organigrama, Objetivos y
Responsabilidad Primaria y Acciones que como Anexos I y II forman parte
integrante del aludido decreto.
Que el artículo 7º del mencionado Decreto establece que esta ANMAT
deberá aprobar la estructura organizativa de nivel inferior a la
aprobada por el citado decreto.
Que por tal motivo corresponde establecer las segundas aperturas a las
aprobadas por la norma mencionada precedentemente del INSTITUTO
NACIONAL DE MEDICAMENTOS, del INSTITUTO NACIONAL DE ALIMENTOS, de la
DIRECCION NACIONAL DE PRODUCTOS MEDICOS, de la DIRECCION GENERAL DE
ASUNTOS JURIDICOS y de la DIRECCION GENERAL DE ADMINISTRACION.
Que la DIRECCION DE RECURSOS HUMANOS Y ORGANIZACION y la DIRECCION
GENERAL DE ASUNTOS JURIDICOS del organismo han tomado la intervención
que resulta de su competencia.
Que la SUBSECRETARIA DE GESTION y EMPLEO PUBLICO de la SECRETARIA DE
GABINETE Y COORDINACION ADMINISTRATIVA de la JEFATURA DE GABINETE DE
MINISTROS ha tomado la intervención de su competencia.
Que la presente disposición se dicta en ejercicio de las atribuciones
conferidas por el artículo 7° del Decreto Nº 1271/13 y el artículo 17
del Decreto Nº 1545 de fecha 31 de agosto de 1994.
Por ello,
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
DISPONE:
ARTICULO 1º — Apruébanse las aperturas inferiores de la estructura
organizativa de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA, organismo descentralizado que funciona en la órbita
de la SECRETARIA DE POLlTICAS, REGULACION E INSTITUTOS del MINISTERIO
DE SALUD, aprobada por Decreto Nº 1271 de fecha 29 de agosto de 2013,
de conformidad con los Organigramas y Acciones que, como Anexos la, lb,
lc, Id, le y II, forman parte integrante de la presente medida.
ARTICULO 2º — Apruébase, en el ámbito de la DIRECCION DE RECURSOS
HUMANOS Y ORGANIZACION dependiente de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA - ANMAT, organismo
descentralizado que funciona en la órbita de la SECRETARIA DE
POLlTICAS, REGULACION E INSTITUTOS del MINISTERIO DE SALUD, la
Coordinación de Capacitación e Investigación Científica Sanitaria,
cuyas Acciones se detallan en Planilla Anexa al presente artículo.
ARTICULO 3º — El gasto que demande el cumplimiento de la presente
medida será atendido con cargo a los créditos presupuestarios de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
ARTICULO 4° — Comuníquese, publíquese, dése a la DIRECCION NACIONAL DEL
REGISTRO OFICIAL y archívese. — Dr. CARLOS CHIALE, Administrador
Nacional, A.N.M.A.T.
ANEXO la
ANEXO lb
ANEXO Ic
ANEXO Id
ANEXO Ie
ANEXO II
MINISTERIO DE SALUD
SECRETARIA DE POLlTICAS, REGULACION E INSTITUTOS
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
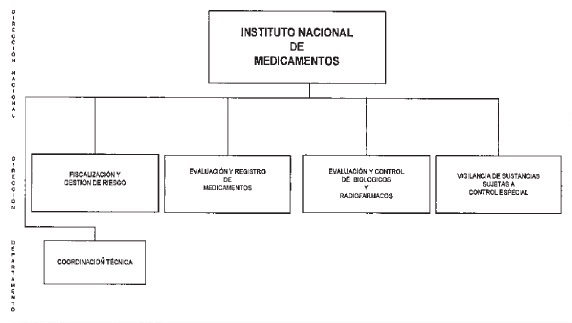
INSTITUTO NACIONAL DE MEDICAMENTOS
COORDINACION TECNICA
ACCIONES:
1.- Brindar apoyo permanente a las actividades técnicas de la Dirección Nacional.
2.- Instrumentar el seguimiento de los planes, programas y proyectos en la órbita de la Dirección Nacional.
3.- Coordinar la evaluación técnica de descargos interpuestos por el
sector regulado, originados como consecuencia de medidas preventivas
y/o sumarios por faltas sanitarias dispuestos por la Administración
Nacional, de productos de competencia de la Dirección Nacional.
4.- Efectuar informe técnico sobre la imputabilidad de riesgo sobre las medidas preventivas adoptadas.
5.- Organizar y coordinar las actividades del Instituto en materia de calidad.
6.- Organizar y coordinar la elaboración de información estadística y
la formulación y seguimiento de indicadores por parte de la Dirección
Nacional.
7.- Ejercer el punto de vinculación entre el Instituto y el servicio de
información a la comunidad, en coordinación con la Dirección de
Relaciones Institucionales y Regulación Publicitaria.
8.- Coordinar la distribución y seguimiento de las muestras recibidas.
9.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
10.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
11.- Contribuir con la Dirección de Recursos Humanos y Organización en el relevamiento de necesidades de capacitación.
12.- Asistir en el cumplimiento de medidas correctivas, a fin de
regularizar las observaciones que pudieran surgir de auditorías
realizadas.
13.- Elaborar el programa anual de actividades y trabajo, el plan anual
de compras, el anteproyecto de presupuesto y el seguimiento de sus
cumplimientos en coordinación con la Dirección General de
Administración.
INSTITUTO NACIONAL DE MEDICAMENTOS
DIRECCION DE FISCALlZACION Y GESTION DE RIESGOS
ACCIONES:
1.- Controlar las actividades, procesos y tecnologías que se realicen
en función de la producción, elaboración, fraccionamiento, importación,
exportación, depósito y comercialización de medicamentos e ingredientes
farmacéuticos activos.
2.- Supervisar los procedimientos de verificación de Buenas Prácticas en los establecimientos bajo su competencia.
3.- Diseñar líneas de acción estratégicas que permitan atender los
desafíos del control de nuevos productos incluyendo la utilización de
nuevas tecnologías de control.
4.- Intervenir en el control, certificación y realización de las
determinaciones analíticas de calidad de los productos de incumbencia.
5.- Dirigir la investigación sobre los reportes de desvíos de calidad
de los productos de su incumbencia así como de aquellos que sean
solicitados por otras Direcciones.
6.- Generar los proyectos de alertas rápidos y comunicados a la
población por problemas de calidad de productos y/o incumplimiento de
las Buenas Prácticas de Fabricación por parte de establecimientos, en
coordinación con la Dirección de Relaciones Institucionales y
Regulación Publicitaria.
7.- Intervenir en las acciones conducentes para otorgar la
certificación, habilitación, licenciamiento y/o autorización de
funcionamiento de establecimientos y plantas dedicadas a la producción,
elaboración, fraccionamiento, importación, exportación y depósito de
medicamentos e ingredientes farmacéuticos activos y las modificaciones
posteriores a las licencias ya otorgadas.
8.- Proponer normas complementarias, modificatorias y/o aclaratorias de
las acciones propias que promuevan los departamentos y/o servicios.
9.- Proponer proyectos de documentos y guías relacionados con las
funciones de fiscalización y control de productos y establecimientos de
su competencia.
10.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
11.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
INSTITUTO NACIONAL DE MEDICAMENTOS
DIRECCION DE EVALUACION Y REGISTRO DE MEDICAMENTOS
ACCIONES:
1.- Entender en la evaluación de los trámites de solicitud de registro de especialidades medicinales y medicamentos.
2.- Entender en la evaluación de los trámites de solicitud de nuevas
formas farmacéuticas, de nuevas concentraciones y otras modificaciones
de especialidades medicinales y medicamentos inscriptos en el Registro.
3.- Brindar asistencia técnica en el proceso de reinscripción de medicamentos.
4.- Intervenir en los procesos de autorización y/o registros especiales
de uso y/o comercialización de productos de competencia de la Dirección.
5.- Supervisar la revisión y evaluación de los rótulos, prospectos e
información para el paciente de acuerdo a la información nacional e
internacional disponible y pertinente para los productos de competencia
de la Dirección.
6.- Intervenir en la asignación de la condición de expendio de
medicamentos de acuerdo a la normativa vigente para los productos de su
competencia.
7.- Intervenir en la aprobación de la ampliación o restricción de las
indicaciones terapéuticas de los productos de su competencia.
8.- Proponer y elevar a la Dirección Nacional normas complementarias,
modificatorias y/o aclaratorias de las acciones propias que promuevan
los departamentos y/o servicios.
9.- Producir y emitir informes respecto a faltas a las normas y reglamentaciones vigentes en el ámbito de su competencia.
10.- Organizar y promover las actividades de farmacovigilancia de los medicamentos inscriptos en el Registro.
11.- Supervisar los procedimientos tendientes a fiscalizar las Buenas Prácticas de Farmacovigilancia.
12.- Supervisar el tratamiento y seguimiento de las notificaciones de eventos adversos relacionadas con los medicamentos.
13.- Supervisar el tratamiento y seguimiento de los planes de gestión
de riesgo y planes de eficacia, efectividad y seguridad de los
medicamentos registrados.
14.- Sugerir a la Dirección Nacional las acciones que considere
corresponder frente a notificaciones, señales o alertas ocurridos con
medicamentos.
15.- Promover la creación de Efectores periféricos del Sistema Nacional
de Farmacovigilancia, su asistencia y estimulación constante.
16.- Entender en los trámites de solicitud de autorización de estudios de investigación en farmacología clínica.
17.- Entender en los trámites de modificación de estudios de investigación en farmacología clínica.
18.- Supervisar la evaluación de estudios preclínicos.
19.- Supervisar los procedimientos de fiscalización de las actividades
correspondientes al desarrollo de estudios en farmacología clínica.
20.- Intervenir en los permisos de importación de medicamentos de uso compasivo y para estudios en farmacología clínica.
21.- Coordinar la comisión interdisciplinaria que evalúa la pertinencia
de otorgar el registro de un medicamento bajo condiciones especiales.
22.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
23.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
INSTITUTO NACIONAL DE MEDICAMENTOS
DIRECCION DE EVALUACION Y CONTROL DE BIOLOGICOS Y RADIOFARMACOS
ACCIONES:
1.- Entender en los procesos de autorización y registro, modificaciones
post-registro y/o reinscripción de medicamentos de origen biológico,
obtenidos de fuentes naturales, por biotecnologías y/o tecnologías
innovadoras, incluyendo entre otros a las vacunas, los hemoderivados,
las enzimas, los productos alergénicos, los medicamentos de terapias
avanzadas, los radiofármacos, y otros medicamentos en cuyos procesos
productivos o de control utilicen insumos de origen biológico y/o
bioensayos.
2.- Intervenir en los procesos de autorización y/o registro especiales
y/o temporales de uso y/o comercialización de productos y/o procesos de
competencia de la Dirección.
3.- Entender en los procesos de autorización de comercialización de
primeros lotes de producción y control, así también como en los
procesos de verificación técnica de productos importados.
4.- Entender en los procesos conducentes al otorgamiento de
habilitaciones y/o autorizaciones de funcionamiento de establecimientos
y plantas dedicadas a la producción, importación de medicamentos,
ingredientes farmacéuticos activos y materiales de partida del área de
su competencia, incluyendo los bancos de sangre y establecimientos de
control relacionados, y las modificaciones posteriores a las licencias
otorgadas.
5.- Entender en los procesos de fiscalización, control y emisión de
certificaciones de establecimientos por medio de verificaciones e
inspecciones de las actividades, procesos y tecnologías, y del
cumplimiento de buenas prácticas que se realicen en función de la
producción, elaboración, fraccionamiento, importación, exportación,
depósito y comercialización de los medicamentos, ingredientes
farmacéuticos activos, materiales de partida y otros productos del área
de su competencia, incluyendo las buenas prácticas de fabricación, de
laboratorio y de bioterios.
6.- Entender en la planificación, ejecución y evaluación de estrategias
y programas de fiscalización y control para el monitoreo de la calidad
y seguridad de los productos.
7.- Entender en los procesos de vigilancia y monitoreo de productos de
su competencia, incluyendo la hemovigilancia y biovigilancia.
8.- Entender en los controles de laboratorio de ingredientes
farmacéuticos activos y medicamentos de origen biológico,
biotecnológico, preparaciones radiofarmacéuticas, medicamentos de
terapias avanzadas y/u obtenidos de nuevas tecnologías y/o fuentes no
convencionales, productos biológicos “in vitro”, y otros productos.
9.- Entender en los controles sobre medicamentos y/o productos de
origen diferente al biológico que requieran de metodologías analíticas
o procesos de evaluación implementados por la Dirección de Evaluación y
Control de Biológicos y Radiofármacos.
10.- Entender en el proceso de liberación de lotes de los productos que
así lo requieran, en especial el de liberación de vacunas preventivas.
11.- Intervenir en el establecimiento de normas y especificaciones
técnicas como también de materiales de referencia de los productos
sujetos a su estudio, proporcionando bases para las reglamentaciones
correspondientes.
12.- Coordinar actividades de investigación, desarrollo y aplicación de
tecnologías, herramientas y métodos de alta complejidad que permitan
atender los desafíos del control de nuevos productos y nuevas
tecnologías.
13.- Proponer y elevar a la Dirección Nacional normas complementarias,
modificatorias y/o aclaratorias de las acciones propias que promuevan
los departamentos y/o servicios.
14.- Elaborar y proponer documentos y guías que permitan decisiones
regulatorias relacionadas con las funciones de evaluación, vigilancia y
control de productos y establecimientos.
15.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
16.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
INSTITUTO NACIONAL DE MEDICAMENTOS
DIRECCION DE VIGILANCIA DE SUSTANCIAS SUJETAS A CONTROL ESPECIAL
ACCIONES:
1.- Supervisar las acciones de fiscalización y control relacionadas con
la elaboración, fraccionamiento, importación, exportación, depósito y
comercialización de sustancias sujetas a control especial.
2.- Supervisar y emitir certificados oficiales de importación,
exportación, licencia de elaboración de sustancias sujetas a control
especial identificadas como psicotrópicos y estupefacientes y
autorización previa de importación y exportación de precursores
químicos.
3.- Intervenir en las acciones conducentes a fin de otorgar la
autorización e inscripción de establecimientos y profesionales para el
manejo de psicotrópicos y estupefacientes.
4.- Supervisar y autorizar la entrega de libros contralor de
competencia, como así también de formularios oficiales para la
comercialización y prescripción de sustancias sujetas a control
especial.
5.- Establecer las necesidades de cuotas o estimaciones anuales para el
país conforme las Convenciones adoptadas de Naciones Unidas sobre
sustancias sujetas a control especial.
6.- Entender en el cumplimiento de requerimientos técnicos-sanitarios
establecidos en: Tratados, Convenciones y todo acuerdo internacional en
relación con los productos de su competencia.
7.- Ejercer el monitoreo de la distribución, consumo, de las sustancias
sujetas a control especial tendientes a evitar el uso indebido de estos
productos.
8.- Elaborar y proponer proyectos de normas técnicas específicas,
modificatorias y/o aclaratorias de las mismas a fin de prevenir el uso
indebido de sustancias de su competencia.
9.- Articular con autoridades sanitarias provinciales la fiscalización
de sustancias sujetas a control especial en toda la cadena de
comercialización.
10.- Establecer estrategias para el control de comercialización y uso de medicamentos sujetos a control especial.
11.- Establecer estrategias para el control de comercialización y uso
de contenidos de ingredientes farmacéuticos activos sujetos a control
especial.
12.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
13.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
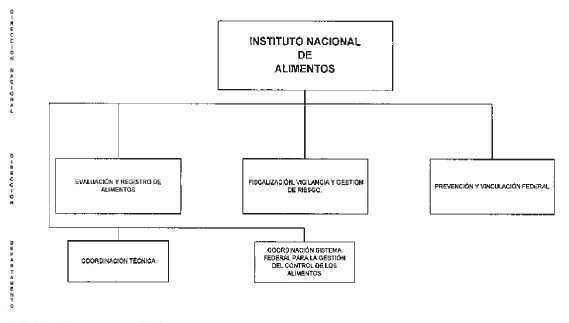
INSTITUTO NACIONAL DE ALIMENTOS
COORDINACION TECNICA
ACCIONES:
1.- Brindar apoyo permanente a las actividades técnicas de la Dirección Nacional.
2.- Instrumentar el seguimiento de los planes, programas y proyectos en la órbita de la Dirección Nacional.
3.- Coordinar la evaluación técnica de descargos interpuestos por el
sector regulado, originados como consecuencia de medidas preventivas
y/o sumarios por faltas sanitarias dispuestos por la Administración
Nacional, de productos de competencia de la Dirección.
4.- Efectuar informe técnico sobre la imputabilidad de riesgo sobre las medidas preventivas adoptadas.
5.- Organizar y coordinar las actividades del Instituto en materia de calidad.
6.- Organizar y coordinar la elaboración de información estadística y
la formulación y seguimiento de indicadores por parte de la Dirección
Nacional.
7.- Ejercer el punto de vinculación entre el Instituto y el servicio de
información a la comunidad, en coordinación con la Dirección de
Relaciones Institucionales y Regulación Publicitaria.
8.- Coordinar la distribución y seguimiento de las muestras recibidas.
9.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
10.- Asistir, en coordinación con la Dirección General de Asuntos
Juridicos, a prestar declaración testimonial, toda vez que le sea
requerido.
11.- Contribuir con la Dirección de Recursos Humanos y Organización en el relevamiento de necesidades de capacitación.
12.- Asistir en el cumplimiento de medidas correctivas, a fin de
regularizar las observaciones que pudieran surgir de auditorías
realizadas.
13.- Elaborar el programa anual de actividades y trabajo, el plan anual
de compras, el anteproyecto de presupuesto y el seguimiento de sus
cumplimientos en coordinación con la Dirección General de
Administración.
INSTITUTO NACIONAL DE ALIMENTOS
COORDINACION DEL SISTEMA FEDERAL PARA LA GESTION DEL CONTROL DE LOS ALIMENTOS
ACCIONES:
1.- Gestionar, desarrollar, implementar e implantar el Sistema de
Información Federal de Gestión para el Control de los Alimentos
(SIFeGA) en coordinación con los organismos sanitarios jurisdiccionales.
2.- Coordinar e instrumentar las acciones para la mejora continua del
sistema de gestión en coordinación con los organismos sanitarios
jurisdiccionales.
3.- Desarrollar y proponer estrategias de mejora sanitarias mediante
acuerdos con los integrantes del Sistema Nacional de Control de
Alimentos y su incorporación al Sistema de Información Federal de
Gestión para el Control de los Alimentos (SIFeGA).
4.- Fomentar y proponer acuerdos de articulación con otros actores
vinculados a salud para mejorar la gestión de la información sanitaria.
5.- Fomentar un sistema de comunicación ágil y permanente con
organismos sanitarios jurisdiccionales y por su intermedio con los
municipios, para el desarrollo y actualización del Sistema de
Información Federal de Gestión para el Control de los Alimentos
(SIFeGA), en coordinación con la Dirección de Prevención y Vinculación
Federal.
6.- Promover canales ágiles de vinculación y comunicación con las áreas
de apoyo técnico informático de los organismos sanitarios
jurisdiccionales, en coordinación con la Dirección General de
Administración y por su intermedio, con la Dirección de Informática.
INSTITUTO NACIONAL DE ALIMENTOS
DIRECCION DE EVALUACION Y REGISTRO DE ALIMENTOS
ACCIONES:
1.- Entender en la evaluación de los trámites de solicitud de
autorización y registro de productos incluidos en el Código Alimentario
Argentino y normas complementarias.
2.- Entender en la evaluación de los trámites de solicitud de
autorización y registro de los establecimientos importadores y
exportadores de alimentos.
3.- Promover y desarrollar la actualización de normas regulatorias
basadas en fundamentos científico-técnicos y en las recomendaciones
regionales e internacionales en la materia.
4.- Coordinar y dirigir la elaboración y propuesta de normas para su
estudio, armonización y adecuación a efectos de ser incorporadas a la
regulación alimentaria.
5.- Asistir en temas referentes a regulación alimentaria a los
organismos sanitarios de orden nacional, jurisdiccional, y por su
intermedio, municipal.
6.- Promover y dirigir el diseño de estrategias desde la perspectiva
regulatoria que contribuyan a la mejora en la composición nutricional
de los alimentos.
7.- Promover el establecimiento de referentes en aspectos regulatorios
en materia de alimentos, en organismos sanitarios de orden nacional,
provincial, y por su intermedio, municipal.
8.- Promover y organizar la participación del Instituto en foros y
grupos técnicos nacionales, regionales e internacionales en temas de su
incumbencia.
9.- Organizar y coordinar la participación del Instituto en la Comisión
Nacional de Alimentos y en los grupos de trabajo de MERCOSUR y comités
del CODEX.
10.- Organizar y dirigir el relevamiento y estudio del desarrollo e
incorporación de nuevas tecnologías en la regulación nacional, regional
e internacional.
11.- Establecer y dirigir la tipificación técnica de las actuaciones
administrativas que deriven del incumplimiento de las normas y
reglamentaciones vigentes.
12.- Organizar y dirigir el relevamiento y estudio de la relación entre
las nuevas tecnologías y la salud en el ámbito de competencia del
Instituto.
13.- Promover la vinculación técnica con las entidades científicas,
académicas, profesionales, de los trabajadores y los organismos no
gubernamentales en acciones propias, en coordinación con la Dirección
de Relaciones Institucionales y Regulación Publicitaria.
14.- Planificar y promover la evaluación de los efectos de las
regulaciones comprendidas en el ámbito de las acciones propias del
Instituto.
15.- Asistir a los responsables técnicos solicitantes para cumplimentar
la autorización de registro de los establecimientos y actividades,
alimentos, insumos y los materiales en contacto en casos que por su
naturaleza técnica requieran una evaluación específica.
16.- Asegurar y proponer la actualización de la información del Sistema
de Información Federal para la Gestión del Control de los Alimentos
(SIFeGA) en vinculación con la Coordinación del Sistema Federal para la
Gestión del Control de los Alimentos.
17.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
18.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
INSTITUTO NACIONAL DE ALIMENTOS
DIRECCION DE FISCALIZACION, VIGILANCIA Y GESTION DE RIESGO
ACCIONES:
1.- Supervisar el tratamiento y seguimiento de los planes de gestión de riesgo de las acciones que le son propias.
2.- Planificar y establecer las actividades de vigilancia de los
alimentos y de las enfermedades relacionadas con los mismos, en el
ámbito de competencia del Instituto.
3.- Promover y planificar el Plan Federal de Vigilancia de Contaminantes y Composición Alimentaria.
4.- Intervenir y coordinar en la gestión de las denuncias realizadas
por consumidores u otros organismos y/o instituciones relacionadas con
los productos de su competencia en coordinación con otros organismos
competentes.
5.- Planificar y establecer en el ámbito nacional las acciones frente a
incidentes asociados a los productos de competencia del Instituto y
coordinar una red de alerta constituida por los organismos sanitarios
de orden nacional y jurisdiccional competentes.
6.- Diseñar, planificar y establecer sistemas de monitoreo, de control
y de auditoría preventivo de establecimientos basado en el análisis de
riesgo.
7.- Diseñar y establecer sistemas de análisis de peligros y estimación
del riesgo para la categorización y seguimiento sanitario de
establecimientos, en el ámbito de su competencia.
8.- Planificar y diseñar la auditoria sanitaria de las actividades,
procesos y tecnologías comprendidas en el ámbito de competencia del
Instituto.
9.- Planificar y definir el control de los alimentos, insumos y los materiales comprendidos en el marco regulatorio alimentario.
10.- Autorizar la solicitud de verificación técnica de productos importados y a exportar.
11.- Planificar y diseñar las actividades de monitoreo y control de productos importados y exportados.
12.- Promover y establecer el estudio de nuevas metodologías técnicas
de análisis para su incorporación a la metodología analítica oficial.
13.- Asegurar y proponer la actualización de la información del Sistema
de Información Federal para la Gestión del Control de los Alimentos
(SIFeGA) en vinculación con la Coordinación del Sistema Federal para la
Gestión del Control de los Alimentos.
14.- Planificar y proponer actuaciones con organismos sanitarios de
orden nacional, jurisdiccional, y por su intermedio municipal,
promoviendo actuaciones integradas e interdisciplinarias en el marco
del Programa Federal de Control de Alimentos.
15.- Planificar los programas de la Red Nacional de Laboratorios
Oficiales de Análisis de Alimentos (RENALOA) en coordinación con la
Dirección de Prevención y Vinculación Federal.
16.- Asegurar y promover la vinculación con las redes de
internacionales de alertas en materia de incidentes sanitarios en
alimentos, en coordinación con la Dirección de Prevención y Vinculación
Federal.
17.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
18.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
INSTITUTO NACIONAL DE ALIMENTOS
DIRECCION DE PREVENCION Y VINCULACION FEDERAL
ACCIONES:
1.- Definir y diseñar el análisis de los comportamientos y tendencias
alimentarias, basado en la mejor evidencia científica disponible, a fin
de evaluar la relación entre la exposición dietética y las condiciones
de salud de la población.
2.- Promover el diseño de estrategias desde la perspectiva de los
procesos tecnológicos que contribuyan a la mejora en la composición
nutricional de los alimentos.
3.- Promover y proyectar la evaluación científica de los alimentos,
ingredientes alimentarios o parte de ellos y las declaraciones de
propiedades en materia de alimentos que confieran beneficios para la
salud.
4.- Programar las estrategias técnicas de información, sensibilización
y educación a los organismos sanitarios de orden nacional y
jurisdiccional y a la población en general, con la finalidad de
promover conductas alimentarias seguras y saludables en coordinación
con la Dirección de Recursos Humanos y Organización para la definición
de las estrategias pedagógicas a aplicar y con la Dirección de
Relaciones Institucionales y Regulación Publicitaria para la definición
de las estrategias comunicacionales a implementar.
5.- Programar y establecer las estrategias técnicas de cooperación y
los vínculos de trabajo integrado con los organismos sanitarios de
orden nacional, provincial, y por su intermedio municipal en
coordinación con la Dirección de Relaciones Institucionales y
Regulación Publicitaria.
6.- Desarrollar la coordinación operativa del Programa Federal de Control de Alimentos.
7.- Diseñar, promover y coordinar la conformación de redes de trabajo,
intercambio y formación entre los diferentes actores públicos y
privados en el ámbito de competencia del Instituto, en coordinación con
la Dirección de Relaciones Institucionales y Regulación Publicitaria, y
cuando corresponda, con la Dirección de Recursos Humanos y Organización.
8.- Promover, potenciar y fortalecer el trabajo de la Red Nacional de Protección de Alimentos (RENAPRA).
9.- Promover, potenciar y fortalecer la Red Nacional de Laboratorios Oficiales de Análisis de Alimentos (RENALOA).
10.- Promover y programar el intercambio y la cooperación con
organismos regionales e internacionales con el fin de alcanzar acuerdos
de trabajo en lo referente a las competencias del Instituto en
coordinación y de acuerdo a los lineamientos de la Dirección de
Relaciones Institucionales y Regulación Publicitaria.
11.- Desarrollar y diseñar las actividades de formación y actualización
técnica de los agentes de los organismos sanitarios de orden nacional,
jurisdiccional, y por su intermedio municipal, en el ámbito de
competencia del Instituto en coordinación con la Dirección de
Relaciones Institucionales y Regulación Publicitaria y cuando
corresponda, con la Dirección de Recursos Humanos y Organización.
12.- Asegurar y proponer la actualización de la información del Sistema
de Información Federal para la Gestión del Control de los Alimentos
(SIFeGA) en vinculación con la Coordinación del Sistema Federal para la
Gestión del Control de los Alimentos.
13.- Planificar los programas de la Red Nacional de Laboratorios
Oficiales de Análisis de Alimentos (RENALOA) en coordinación con la
Dirección de Fiscalización, Vigilancia y Gestión de Riesgo.
14.- Programar y establecer la vinculación con las redes
internacionales de alertas en materia de incidentes sanitarios en
alimentos.
15.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
16.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
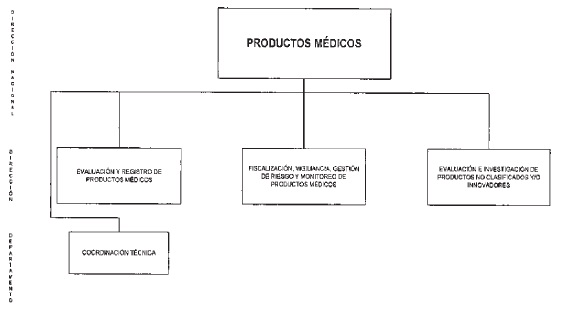
DIRECCION NACIONAL DE PRODUCTOS MEDICOS
COORDINACION TECNICA
ACCIONES:
1.- Brindar apoyo permanente a las actividades técnicas de la Dirección Nacional.
2.- Instrumentar el seguimiento de los planes, programas y proyectos en la órbita de la Dirección Nacional.
3.- Realizar la evaluación técnica de descargos interpuestos por el
sector regulado, originados como consecuencia de medidas preventivas
y/o sumarios por faltas sanitarias dispuestos por la Administración
Nacional, de productos de competencia de la Dirección Nacional.
4.- Efectuar informe técnico sobre la imputabilidad de riesgo sobre las medidas preventivas adoptadas.
5.- Organizar y coordinar las actividades de la Dirección Nacional en materia de calidad.
6.- Organizar y coordinar la elaboración de información estadística y
la formulación y seguimiento de indicadores por parte de la Dirección
Nacional.
7.- Ejercer el punto de vinculación entre la Dirección Nacional y el
servicio de información a la comunidad, en coordinación con la
Dirección de Relaciones Institucionales y Regulación Publicitaria.
8.- Coordinar la distribución y seguimiento de las muestras recibidas.
9.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
10.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
12.- Contribuir con la Dirección de Recursos Humanos y Organización en
el relevamiento de necesidades de capacitación e ingresos.
13.- Asistir en el cumplimiento de medidas correctivas, a fin de
regularizar las observaciones que pudieran surgir de auditorías
realizadas.
14.- Elaborar el programa anual de actividades y trabajo, el plan anual
de compras, el anteproyecto de presupuesto y el seguimiento de sus
cumplimientos en coordinación con la Dirección General de
Administración.
DIRECCION NACIONAL DE PRODUCTOS MEDICOS
DIRECCION DE EVALUACION Y REGISTRO DE PRODUCTOS MEDICOS
ACCIONES:
1.- Entender en la evaluación de los trámites de solicitud de registro de nuevos productos médicos.
2.- Entender en la evaluación de los trámites de solicitud de
modificación de registro de los productos de su competencia ya
inscriptos.
3.- Brindar asistencia técnica en el proceso de revalidación del registro de productos inscriptos.
4.- Intervenir en los procesos de autorización y/o registros especiales de productos de competencia de la Dirección Nacional.
5.- Supervisar la revisión y evaluación de los manuales de uso o
instrucción de uso, rótulos y tarjetas de implante de acuerdo a la
información nacional e internacional disponible para los productos
médicos.
6.- Intervenir en la asignación de la condición de uso de productos médicos de acuerdo a la normativa vigente.
7.- Intervenir en la aprobación de la ampliación o restricción de las
indicaciones, finalidad o uso declarada para los productos de su
competencia.
8.- Proponer y elevar a la Dirección Nacional normas complementarias,
modificatorias y/o aclaratorias de las acciones propias que promuevan
los departamentos y/o servicios.
9.- Producir y emitir informes respecto a faltas a las normas y reglamentaciones vigentes en el ámbito de su competencia.
10.- Coordinar la comisión interdisciplinaria que evalúa la pertinencia de otorgar un registro especial a un producto médico.
11.- Definir los criterios, instrumentos y metodologías tendientes a
facilitar la identificación, control de calidad y evaluación técnica de
los productos médicos.
12.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
13.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
DIRECCION NACIONAL DE PRODUCTOS MEDICOS
DIRECCION DE FISCALlZACION, VIGILANCIA, GESTION DE RIESGO Y MONITOREO DE PRODUCTOS MEDICOS
ACCIONES:
1.- Controlar las actividades, procesos y tecnologías que se realicen
en función de la producción, elaboración, fraccionamiento, importación,
exportación, depósito, comercialización y distribución de productos
médicos.
2.- Intervenir en las acciones conducentes para otorgar la
certificación, habilitación, licenciamiento y/o autorización de
funcionamiento de establecimientos y plantas dedicadas a la producción,
elaboración, fraccionamiento, importación, exportación y depósito de
productos médicos.
3.- Supervisar los procedimientos de verificación de Buenas Prácticas de Fabricación en los establecimientos de su competencia.
4.- Diseñar líneas de acción estratégicas que permitan atender los
desafíos del control de nuevos productos y la utilización de nuevas
tecnologías de control.
5.- Diseñar y dirigir líneas de acción estratégicas para los
Laboratorios de Control y ensayos que permitan atender los desafíos del
control de nuevos productos, la utilización de nuevas tecnologías de
control y la evolución de desempeño y pre comercialización.
6.- Organizar y conducir las actividades de vigilancia sanitaria de los productos médicos.
7.- Promover la creación de Efectores Periféricos del Sistema Nacional
de Vigilancia Sanitaria de productos médicos, su asistencia y
estimulación constante.
8.- Supervisar y conducir la investigación y seguimiento de los eventos
adversos o fallas de calidad de los productos de su incumbencia así
como de aquellos que sean solicitados por otras Direcciones.
9.- Evaluar los informes y conclusiones recibidos de los distintos
servicios, con relación a la calidad de las muestras analizadas,
sugiriendo las medidas que considere corresponder según las no
conformidades y desvíos de calidad de productos.
10.- Sugerir a la Dirección Nacional las acciones que considere
corresponder frente a notificaciones, señales o alertas ocurridos con
productos médicos.
11.- Generar los proyectos de alertas rápidos y comunicados a la
población por problemas de calidad de productos y/o incumplimiento de
las Buenas Prácticas de Fabricación por parte de establecimientos en
coordinación con la Dirección de Relaciones Institucionales y
Regulación Publicitaria.
12.- Supervisar el tratamiento y seguimiento de los planes de gestión de riesgo de los productos médicos comercializados.
13.- Intervenir en los permisos de importación de productos médicos,
productos médicos de uso compasivo y para estudios en investigación
clínica.
14.- Intervenir en la trazabilidad metrológica y verificación de aptitud técnica de los productos médicos activos.
15.- Proponer normas complementarias, modificatorias y/o aclaratorias que promuevan los departamentos y/o servicios.
16.- Proponer proyectos de documentos y guías relacionados con las
funciones de fiscalización y control de productos y establecimientos de
su competencia.
17.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
18.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
DIRECCION NACIONAL DE PRODUCTOS MEDICOS
DIRECCION DE EVALUACION E INVESTIGACION DE PRODUCTOS NO CLASIFICADOS Y/O INNOVADORES
ACCIONES:
1.- Evaluar la factibilidad de pertinencia de categorizar nuevos
productos que puedan afectar la salud humana y no se encuentran
regulados por esta Administración Nacional.
2.- Proponer criterios, instrumentos y metodología tendientes a
facilitar la identificación, control de calidad y evaluación técnica de
los productos no clasificados y/o innovadores que resulten de
incumbencia de la Administración Nacional.
3.- Promover convenios y acuerdos entre instituciones públicas y
privadas, tendientes a conformar las redes de información y
capacitación requeridas para la función específica de la Dirección.
4.- Proponer y elevar a la Dirección Nacional normas y elaborar
informes en referencia a los productos no clasificados a fin de que se
incorporen al plexo normativo vigente.
5.- Entender en los trámites de solicitud de autorización de estudios clínicos de productos médicos.
6.- Supervisar la evaluación de estudios pre-clínicos.
7.- Supervisar los procedimientos de fiscalización de las actividades correspondientes al desarrollo de estudios clínicos.
8.- Intervenir técnicamente en la respuesta de oficios judiciales y
pericias judiciales, en coordinación con la Dirección General de
Asuntos Jurídicos.
9.- Asistir, en coordinación con la Dirección General de Asuntos
Jurídicos, a prestar declaración testimonial, toda vez que le sea
requerido.
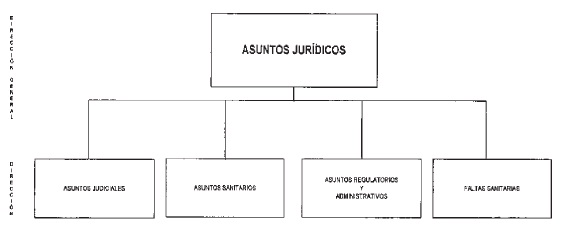
DIRECCION GENERAL DE ASUNTOS JURIDICOS
DIRECCION DE ASUNTOS JUDICIALES
ACCIONES:
1.- Intervenir en las diferentes etapas de los procesos judiciales en
los que la Administración Nacional actúe como parte (actor o demandado)
o como tercero interesado.
2.- Coordinar la elaboración y contestación de demandas, recursos,
denuncias, así como de cualquier otro tipo de presentación judicial.
3.- Coordinar las acciones judiciales en las que se requiera la intervención y/o colaboración de la Administración Nacional.
4.- Mantener relación con la PROCURACION DEL TESORO DE LA NACION en función de las prescripciones de la normativa vigente.
5.- Coordinar, tramitar y dar respuesta a los oficios judiciales y/o
pedidos de informes que se estimen propios de la competencia de esta
Administración Nacional.
6.- Mantener informadas a las áreas que conforman la Dirección General
de Asuntos Jurídicos, sobre fallos judiciales que revisten interés
institucional.
7.- Emitir providencias de mero trámite y dictámenes reiterativos de criterios ya adoptados.
DIRECCION GENERAL DE ASUNTOS JURIDICOS
DIRECCION DE ASUNTOS SANITARIOS
ACCIONES:
1.- Coordinar el estudio y elaboración de dictámenes, providencias y
toda otra documentación administrativa, en todas las cuestiones
jurídicas generadas por la relación entre la Administración Nacional y
el sector regulado.
2.- Coordinar la intervención en las solicitudes de registro de
medicamentos y especialidades medicinales, tanto en soporte de papel
como en los sistemas de gestión electrónica, presentados por el sector
regulado.
3.- Coordinar la evaluación y elaboración de dictámenes relacionados
con las cuestiones jurídicas que se planteen en las inscripciones y
modificaciones a los registros de productos alimenticios, productos
médicos, productos de uso doméstico, productos de higiene, tocador y
cosmética humana, y otros productos vinculados a la salud humana, como
así también en las cuestiones jurídicas que se planteen en las
modificaciones a los registros de medicamentos y especialidades
medicinales.
4.- Coordinar el asesoramiento y elaboración de dictámenes con relación
a las cuestiones legales que se planteen en materia de vigilancia
sanitaria, publicidad y promoción de medicamentos y especialidades
medicinales, productos alimenticios, productos médicos, productos de
uso doméstico, productos de higiene, tocador y cosmética humana, y
otros productos vinculados a la salud humana.
5.- Coordinar la elaboración de dictámenes en los trámites de recursos,
reclamos y denuncias sometidas a su consideración, en los temas de su
competencia, como así también en los trámites en los que se propongan
medidas preventivas que no sean competencia de la Dirección de Faltas
Sanitarias.
6.- Colaborar, a solicitud de la Dirección de Asuntos Regulatorios y
Administrativos, en los proyectos de leyes, decretos, resoluciones,
disposiciones y demás normas de carácter sanitario de competencia de la
Dirección.
7.- Emitir providencias de mero trámite y dictámenes reiterativos de criterios ya adoptados.
DIRECCION GENERAL DE ASUNTOS JURIDICOS
DIRECCION DE ASUNTOS REGULATORIOS Y ADMINISTRATIVOS
ACCIONES:
1.- Coordinar el estudio y elaboración de dictámenes sobre proyectos de
leyes, decretos, resoluciones, disposiciones y demás normas
relacionadas con las competencias de la Administración Nacional.
2.- Coordinar el análisis de los proyectos de normas vinculados con el
MERCOSUR y con los procesos de integración regional e internacional que
se sometan a su consideración.
3.- Intervenir en los aspectos legales relacionados con los convenios y
acuerdos que celebre la Administración Nacional con otros organismos
públicos o entidades privadas así como también en los acuerdos que se
encaren en el orden internacional en materia sanitaria.
4.- Intervenir en los aspectos vinculados con el empleo público y las relaciones laborales en general.
5.- Intervenir en los procesos licitatorios y demás trámites vinculados
a la Ley de Administración Financiera y de los Sistemas de Control del
Sector Público Nacional Nº 24.156 o la que en el futuro la sustituya.
6.- Coordinar la realización del control de la legalidad y legitimidad
de los sumarios por faltas sanitarias y sumarios disciplinarios.
7.- Intervenir en los trámites de recursos, reclamos y denuncias sometidos a su consideración en el ámbito de su competencia.
8.- Coordinar la recopilación de normas, doctrina y jurisprudencia y su
actualización en materias de competencia de la Administración Nacional.
9.- Emitir providencias de mero trámite y dictámenes reiterativos de criterios ya adoptados.
DIRECCION GENERAL DE ASUNTOS JURIDICOS
DIRECCION DE FALTAS SANITARIAS
ACCIONES:
1.- Elaborar dictámenes, informes y notas relacionados con la
iniciación y conclusión de los sumarios por infracciones a la normativa
sanitaria en ejercicio del poder de policía que las normas vigentes en
la materia asigna a la Administración Nacional.
2.- Elaborar los proyectos de actos administrativos sobre medidas de
protección a la salud de la población, propuestas por las áreas
técnicas.
3.- Elaborar los proyectos de actos administrativos conclusivos de los sumarios por faltas sanitarias.
4.- Requerir informes técnicos necesarios para la sustanciación de los sumarios sanitarios.
5.- Instrumentar las notificaciones a los sumariados.
6.- Examinar el estado de los sumarios para verificar el cumplimiento de los procedimientos y plazos legales.
7.- Colaborar, a solicitud de la Dirección de Asuntos Regulatorios y
Administrativos, en los proyectos de leyes, decretos, resoluciones,
disposiciones y demás normas de carácter sanitario en las que se regule
el poder de policía de competencia de la Administración Nacional.
8.- Emitir providencias de mero trámite y dictámenes reiterativos de criterios ya adoptados.
9.- Coordinar el registro de los sumarios ordenados.
DIRECCION GENERAL DE ADMINISTRACION
DIRECCION DE PRESUPUESTO Y CONTABILIDAD
ACCIONES:
1.- Planificar y ejecutar la Administración financiera del organismo,
observando el cumplimiento de la normativa establecida por la Ley
24.156.
2.- Elaborar el presupuesto anual de la Administración Nacional de
acuerdo con los planes y políticas presupuestarias previstas y en
función a los lineamientos que en materia de economía fije la
Secretaría de Hacienda del Ministerio de Economía y de Finanzas
Públicas.
3.- Efectuar el cálculo de recursos, determinando la previsión anual,
realizar el control y proceder al registro de la recaudación de la
Administración Nacional, en concepto de aranceles y tasas retributivas,
correspondientes a los trámites y registros que se efectúen, como así
también de las multas que se apliquen.
4.- Elaborar la programación física (Metas) y financiera trimestral
(Cuotas) del presupuesto de la Administración Nacional y coordinar el
control de su ejecución.
5.- Coordinar el análisis físico y financiero de las metas y objetivos
programados, al momento de la formulación y su grado de cumplimiento al
cierre del ejercicio fiscal, a fin de conocer el grado de eficiencia,
eficacia y economía.
6.- Controlar la ejecución financiera del presupuesto y efectuar las
modificaciones y/o ampliaciones que resulten necesarias para el
cumplimiento de las políticas fijadas por la Administración Nacional.
7.- Coordinar los diferentes Programas y Proyectos financiados con
préstamos, créditos o subsidios externos y/o en el marco de acuerdos de
cooperación técnica con organismos internacionales, interviniendo en la
formulación, gestión, supervisión, monitoreo y evaluación de los mismos.
8.- Informar sobre la disponibilidad de créditos, cuotas y recursos
9.- Entender en la liquidación y órdenes de pagos de las facturas de
proveedores, contratistas, servicios profesionales, indemnizaciones,
gastos de personal y cualquier otra erogación.
10.- Controlar todo lo relativo a las rendiciones de cuentas de “cajas chicas” y “fondos permanentes”.
11.- Controlar y registrar los ingresos y egresos derivados de la gestión financiera de la Administración Nacional.
12.- Controlar el atesoramiento de los fondos líquidos del organismo y administrar sus cuentas bancarias.
13.- Supervisar la contabilidad y la imputación presupuestaria de todos
los hechos económicos y financieros de la Administración Nacional.
14.- Registrar sistemáticamente todas las transacciones que produzcan y
afecten la situación económico-financiera de la Administración,
exponiendo la misma en los balances, cuadros y planillas exigidos por
la normativa vigente.
15.- Confeccionar los Estados Contables que conforman la Cuenta de
Ahorro e Inversión - Financiamiento de la Administración Nacional.
16.- Presentar la información contable y la respectiva documentación de
apoyo ordenadas de tal forma que faciliten las tareas de control y
auditoría, sean éstas internas o externas.
17.- Producir informes económicos-financieros para la adopción de
decisiones por parte de los responsables de la gestión administrativa
del Organismo y para las tareas de control.
18.- Proponer medidas de contención y economía del gasto, de acuerdo a
los lineamientos que en dicha materia establezca la Secretaría de
Hacienda del Ministerio de Economía y Finanzas Públicas.
19.- Constituir el enlace técnico del Organismo con los órganos
rectores del MINISTERIO DE ECONOMIA y FINANZAS PUBLICAS - Oficina
Nacional de Presupuesto, Contaduría General de la Nación y Tesorería
General de la Nación.
DIRECCION GENERAL DE ADMINISTRACION
DIRECCION DE COMPRAS, SUMINISTROS, LOGISTICA Y ARQUITECTURA
ACCIONES:
1.- Planificar y supervisar las gestiones pertinentes destinadas a la
adquisición, contratación y locación de bienes y servicios asegurando
el normal funcionamiento de la Administración Nacional.
2.- Planificar y supervisar la ejecución de los servicios generales
destinados a la conservación de los bienes muebles, inmuebles e
instalaciones afectadas al uso, de acuerdo al plan de mantenimiento
integral del organismo.
3.- Planificar y supervisar la implementación de servicios internos
destinados a lograr el desarrollo óptimo de la Administración Nacional.
4.- Coordinar los métodos y medios de sus acciones propias que resultan
indispensables para el desarrollo y funcionamiento efectivo de la
Administración Nacional.
5.- Planificar y supervisar los procesos de adquisición de bienes de
origen extranjero cuando los requerimientos técnicos de los mismos así
lo exijan.
6.- Mantener relación con la OFICINA NACIONAL DE CONTRATACIONES en función de las prescripciones de la normativa vigente.
7.- Supervisar la elaboración y ejecución del Plan Anual de Compras.
8.- Asesorar sobre la modalidad e interpretación de las normas que rigen en la materia de su propia acción.
9.- Conducir los procesos de Licitación Pública, Privada y/o
Contratación Directa para la adquisición de bienes y/o servicios, de
acuerdo a la normativa vigente, controlando e interviniendo en la
elaboración de los pliegos de licitación de compra y/o contratación de
bienes y servicios.
10.- Gestionar ante la Oficina Nacional de Tecnologías de la
Información de la SUBSECRETARIA DE TECNOLOGIAS DE GESTION de la
SECRETARIA DE LA GESTION PUBLICA de la JEFATURA DE GABINETE DE
MINISTROS la aprobación de las especificaciones técnicas incluidas en
las compras y/o licitaciones encaradas por el Organismo.
11.- Gestionar ante la SINDICATURA GENERAL DE LA NACION el precio
testigo en las contrataciones que, según la normativa vigente, así lo
requiere.
12.- Supervisar la ejecución y seguimiento de las órdenes de compra
originadas en los procesos licitatorios y/o contrataciones directas.
13.- Proponer y registrar las sanciones a los proveedores por incumplimiento de las obligaciones contractuales.
14.- Supervisar la ejecución de las actas emitidas por la Comisión de Condiciones de Medio Ambiente del Trabajo (CyMAT).
15.- Conducir la administración, distribución y control de los bienes de consumo.
16.- Administrar y mantener el parque automotor de la Administración Nacional.
17.- Programar la adquisición de bienes y servicios, analizar las
solicitudes de necesidades de urgencia y definir las modalidades de
compra.
DIRECCION GENERAL DE ADMINISTRACION
DIRECCION DE INFORMATICA
ACCIONES:
1.- Aplicar las políticas relativas a las Tecnologías de la Información
y las Comunicaciones, incluyendo la informática, las
telecomunicaciones, la telefonía, las redes, los sistemas de
información y las tecnologías asociadas, fijadas por la Administración
Nacional.
2.- Elaborar anualmente el plan estratégico de Tecnologías de la Información y las Comunicaciones del Organismo.
3. Entender y supervisar en todo lo atinente a los recursos
informáticos del organismo, y la comunicación en función de las nuevas
tecnologías, asegurando el cumplimiento de las normas legales en la
materia y establecer normas y estándares siguiendo los lineamientos de
la Subsecretaría de Tecnologías de Gestión de la SECRETARIA DE GABINETE
Y COORDINACION ADMINISTRATIVA de la JEFATURA DE GABINETE DE MINISTROS.
4.- Asesorar a las autoridades del organismo en todos aquellos aspectos
referentes a la utilización de las tecnologías de información.
5. Entender en la aprobación de las medidas técnicas reglamentarias y
particulares que propendan a la incorporación de nuevas tecnologías que
incluyan contenidos que permitan el acceso a las personas con
discapacidad.
6.- Entender e instrumentar la seguridad de los sistemas informáticos y
de comunicaciones del organismo, incluyendo el establecimiento de
planes de contingencia para los sistemas críticos, controlando
periódicamente su funcionamiento.
7.- Evaluar el impacto producido por la implementación de los proyectos informáticos.
8.- Intervenir en los convenios institucionales de las acciones que le son propias.
9.- Conducir las actividades vinculadas al uso de las tecnologías de la información y las comunicaciones en el organismo.
10.- Asegurar el mantenimiento y soporte de los sistemas informáticos y
su equipamiento, de los servicios de telecomunicaciones y de telefonía.
11.- Coordinar el análisis, diseño, desarrollo, implementación y mantenimiento de las aplicaciones y/o sistemas de información.
12.- Intervenir en la adquisición y adecuación de equipamiento
informático, software de base, bases de datos, herramientas para
desarrollo e instalación de redes locales y de comunicaciones.
13.- Diseñar, crear y administrar las bases de datos en coordinación
con la Dirección de Gestión de Información Técnica, relacionadas con el
funcionamiento de la Administración Nacional, y con sus necesidades de
información.
14.- Establecer la sistematización de las tareas rutinarias y soporte a la gestión mediante software específico.
PLANILLA ANEXA AL ARTICULO 2º
MINISTERIO DE SALUD
SECRETARIA DE POLlTICAS, REGULACION E INSTITUTOS
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
DIRECCION DE RECURSOS HUMANOS Y ORGANIZACION
COORDINACION DE CAPACITACION E INVESTIGACION CIENTIFICA SANITARIA
ACCIONES:
1.- Coordinar el diseño, implementación, seguimiento y evaluación de
los programas y las actividades vinculadas con la capacitación interna
y externa de la Administración.
2.- Coordinar la elaboración y aprobación de los planes estratégicos y
anuales de capacitación del Organismo, en colaboración con el INSTITUTO
NACIONAL DE LA ADMINISTRACION PUBLICA, a partir del diagnóstico
institucional y la detección de necesidades de capacitación de los
recursos humanos de la Administración.
3.- Coordinar el diseño y el desarrollo del Programa de Formación Permanente de los agentes de la Administración Nacional.
4.- Ejercer la Coordinación Técnica de Capacitación del organismo.
5.- Asistir técnicamente a la delegación jurisdiccional de la Comisión
Permanente de Interpretación de la Carrera Profesional Sanitaria y de
la Comisión Permanente de Interpretación y Carrera vinculadas a la
capacitación.
6.- Promover la implementación de actividades de capacitación para la
calidad ocupacional y la prevención de riesgos del trabajo en
coordinación con el área de seguridad e higiene en el trabajo.
7.- Coordinar el desarrollo del Sistema de Residencias en la Administración Nacional.
8.- Organizar y administrar las Delegaciones de Capacitación Administración Nacional.
9.- Gestionar los convenios académicos de asistencia técnica para la formación de jóvenes profesionales.
10.- Gestionar acuerdos interinstitucionales para la formación técnica y profesional de los recursos humanos.
11.- Intervenir en los convenios institucionales en el marco de
formación permanente de agentes en vigilancia sanitaria, para todo el
país mediante acuerdos con las provincias, municipios y organizaciones
intermedias de la sociedad civil.
12.- Contribuir con el desarrollo de la política de investigación
básica y aplicada en productos para la salud, establecida en los
objetivos estratégicos y vinculada con el impacto en la salud de la
población.
13.- Contribuir con las publicaciones, presentaciones y toda producción
científica desarrollada a partir del ejercicio de la función
institucional para actuar como representante de la Administración
Nacional.
e. 04/07/2014 Nº 46716/14 v. 04/07/2014