MINISTERIO DE SALUD
SECRETARÍA DE POLÍTICAS, REGULACIÓN E INSTITUTOS
ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
Disposición 11247/2016
Buenos Aires, 12/10/2016
VISTO la Ley 16.463 y los Decretos Reglamentarios Nros. 9763/64 y
150/92 (T.O. 1993), 1490/92 y sus modificatorios, las Disposiciones
ANMAT Nos. 3185/99, 5040/06, 1746/07, 556/09, 758/09, 4132/12, 4133/12,
4326/12, 4788/12 y 6766/16 y el Expediente N° 1-0047-0000-011838-16-8
del Registro de esta ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS
Y TECNOLOGÍA MÉDICA; y
CONSIDERANDO:
Que de conformidad con el Artículo 1° de la Ley N° 16.463, quedan
sometidos a su régimen y a los reglamentos que en su consecuencia se
dicten, entre otras, las actividades de comercialización y depósito en
jurisdicción nacional o con destino al comercio interprovincial, de las
drogas, productos químicos, reactivos, formas farmacéuticas,
medicamentos, elementos de diagnóstico y todo otro producto de uso y
aplicación en la medicina humana y las personas de existencia visible o
ideal que intervengan en dichas actividades.
Que por Decreto N° 1490/92, se creó en el ámbito de la ex SECRETARÍA DE
SALUD del MINISTERIO DE SALUD y ACCIÓN SOCIAL, esta ADMINISTRACIÓN
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA (ANMAT), como
organismo descentralizado de la Administración Pública Nacional, con
jurisdicción en todo el territorio de la Nación, asumiendo las
funciones referidas al contralor de actividades, procesos y tecnologías
que se realicen en función del aprovisionamiento, producción,
elaboración, fraccionamiento, importación y/o exportación, depósito y
comercialización de medicamentos, y especialidades medicinales de uso
humano (Artículos 2° y 3°, inciso e).
Que las normas aludidas tienen como finalidad última la protección de
la salud de la población, mediante la adopción de un modelo
fiscalizador de gestión que destina los mayores esfuerzos a garantizar
la eficacia, seguridad y calidad de los productos que consume la
población.
Que mediante las Disposiciones ANMAT Nros. 3185/99, 5040/06 y
modificatorias se establecieron los requerimientos técnicos y
metodológicos para la adecuada realización de estudios de equivalencia
in vivo.
Que mediante la Disposición ANMAT N° 758/09 y 6766/16 se adoptaron los
criterios del Sistema de Clasificación Biofarmacéutica (SCB) y los
requisitos necesarios para solicitar una Bioexención, respectivamente.
Que esta Administración Nacional promueve la adopción de lineamientos
técnicos internacionales y adopta un modelo de fiscalización y gestión
acorde a dichos parámetros.
Que atento a los cambios técnicos, estructurales, societarios, entre
otros, que se han suscitado en las empresas elaboradoras de
especialidades medicinales y procurando una permanente mejora de la
gestión sanitaria, esta Administración considera necesario actualizar
la lista de Productos de Referencia que figuran en el ANEXO III de la
Disposición N° 4788/12 a efectos de llevar a cabo los estudios de
Bioequivalencia.
Que finalmente, desde el punto de vista técnico y administrativo se
hace necesario disponer de un registro ordenado y actualizado de las
empresas titulares de Productos de Referencia para estudios de
Bioequivalencia.
Que el Instituto Nacional de Medicamentos y la Dirección General de
Asuntos Jurídicos han tomado la intervención de su competencia.
Que se actúa en virtud de las facultades conferidas por el Decreto N°
1490 de fecha 20 de agosto de 1992 y el Decreto N° 101 del 16 de
diciembre de 2015.
Por ello,
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
DISPONE:
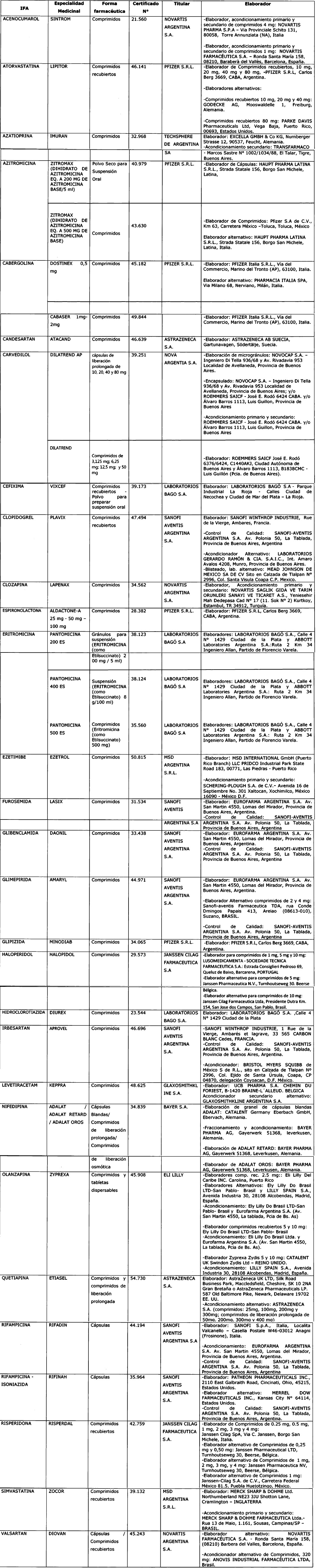
ARTÍCULO 1° — Establécense los productos de referencia para las
especialidades medicinales que contengan ingredientes farmacéuticos
activos sujetos a estudios de Bioequivalencia que figuran como ANEXO y
forma parte de la presente disposición. El referido listado podrá ser
actualizado toda vez que razones de índole sanitaria lo justifiquen.
ARTÍCULO 2° — Para el caso de combinaciones a dosis fijas, el producto
de referencia elegido por el laboratorio quedará sujeto a consideración
y autorización de esta Administración.
ARTÍCULO 3° — Sustitúyese el listado del ANEXO III de la Disposición ANMAT N° 4788/12 por el ANEXO de la presente norma.
ARTÍCULO 4° — La presente disposición entrará en vigencia el día siguiente al de su publicación en el Boletín Oficial.
ARTÍCULO 5° — Regístrese; Dése a la Dirección Nacional del Registro
Oficial para su publicación. Comuníquese a CILFA, CAEME, COOPERALA,
CAPGEN y demás cámaras representativas del sector como así también a la
Confederación Farmacéutica de la República Argentina (COFA), Federación
Argentina de Cámaras de Farmacia (FACAF) y a la Cámara de Farmacias.
Cumplido, archívese. — Dr. CARLOS CHIALE, Administrador Nacional,
A.N.M.A.T.
ANEXO
(Artículo sustituido por art. 1° de la Resolución
N° 8255/2017 del Ministerio de Salud B.O. 31/07/2017, Vigencia: a partir del día siguiente al de su publicación en el Boletín Oficial)
e. 17/10/2016 N° 76507/16 v. 17/10/2016