MINISTERIO
DE AGROINDUSTRIA
Resolución 37/2018
Ciudad de Buenos Aires, 16/03/2018
VISTO el Expediente N° EX-2017-35394053--APN-DDYME#MA del Registro del
MINISTERIO DE AGROINDUSTRIA, el Tratado para la Constitución de un
Mercado Común entre la REPÚBLICA ARGENTINA, la REPÚBLICA FEDERATIVA DEL
BRASIL, la REPÚBLICA DEL PARAGUAY y la REPÚBLICA ORIENTAL DEL URUGUAY,
suscripto en la Ciudad de Asunción (REPÚBLICA DEL PARAGUAY) el 26 de
marzo de 1991, aprobado por la Ley N° 23.981, el Protocolo Adicional al
Tratado de Asunción sobre la Estructura Institucional del MERCOSUR -
Protocolo de Ouro Preto - suscripto por idénticas partes que el
mencionado tratado, en la Ciudad de Ouro Preto (REPÚBLICA FEDERATIVA
DEL BRASIL), el 17 de diciembre de 1994, aprobado por la Ley N° 24.560,
y
CONSIDERANDO:
Que el proceso de integración del MERCADO COMÚN DEL SUR (MERCOSUR) es
de importancia estratégica para la REPÚBLICA ARGENTINA.
Que el 26 de marzo de 1991, la REPÚBLICA ARGENTINA, la REPÚBLICA
FEDERATIVA DEL BRASIL, la REPÚBLICA DEL PARAGUAY y la REPÚBLICA
ORIENTAL DEL URUGUAY suscribieron en la Ciudad de Asunción (REPÚBLICA
DEL PARAGUAY) el Tratado para la Constitución de un Mercado Común,
aprobado por la Ley N° 23.981, creando el MERCADO COMÚN DEL SUR.
Que conforme a los Artículos 2°, 9°, 15, 20, 38 y 42 del Protocolo
Adicional al Tratado de Asunción sobre la Estructura Institucional del
MERCOSUR - Protocolo de Ouro Preto – suscripto el 17 de diciembre de
1994 por idénticas partes que el tratado referido precedentemente en la
Ciudad de Ouro Preto (REPÚBLICA FEDERATIVA DEL BRASIL), aprobado por la
Ley N° 24.560, las normas del MERCADO COMÚN DEL SUR (MERCOSUR)
aprobadas por el CONSEJO DEL MERCADO COMÚN, el GRUPO MERCADO COMÚN y la
COMISIÓN DE COMERCIO DEL MERCOSUR, son obligatorias y deben ser
incorporadas, cuando ello sea necesario, al ordenamiento jurídico
nacional de los Estados Partes mediante los procedimientos previstos en
su legislación.
Que conforme a los Artículos 3°, 14 y 15 de la Decisión N° 20 de fecha
6 de diciembre de 2002 del CONSEJO DEL MERCADO COMÚN, las normas del
MERCADO COMÚN DEL SUR (MERCOSUR) que no requieran ser incorporadas por
vía legislativa podrán ser incorporadas por vía administrativa por
medio de actos del PODER EJECUTIVO de los Estados Partes.
Que el Artículo 7° de la citada Decisión N° 20/02 establece que las
normas del MERCADO COMÚN DEL SUR (MERCOSUR) deberán ser incorporadas a
los ordenamientos jurídicos de los Estados Partes en su texto integral.
Que la Decisión N° 6 de fecha 17 de diciembre de 1996 del CONSEJO DEL
MERCADO COMÚN, incorpora al ordenamiento jurídico del MERCADO COMÚN DEL
SUR (MERCOSUR) el Acuerdo sobre la Aplicación de las Medidas Sanitarias
y Fitosanitarias (MSF) de la ORGANIZACIÓN MUNDIAL DEL COMERCIO (OMC).
Que resulta necesario derogar el Anexo XI de la Resolución Nº 133 de
fecha 16 de marzo de 2011 del ex-MINISTERIO DE AGRICULTURA, GANADERÍA Y
PESCA, dado que la Resolución Nº 28 de fecha 15 de junio de 2010 del
GRUPO MERCADO COMÚN, contenida en dicho anexo, ha sido sustituida por
la Resolución Nº 25 de fecha 13 de septiembre de 2017 del GRUPO MERCADO
COMÚN.
Que en tal sentido, resulta necesario incorporar al ordenamiento
jurídico nacional la citada Resolución N° 25/17, la cual se encuentra
contenida en el Anexo I, que registrado con el Nº
IF-2018-07035886-APN-SECMA#MA, forma parte integrante de la presente
medida.
Que en ocasión de la CV Reunión Ordinaria del GRUPO MERCADO COMÚN,
celebrada en la Ciudad de Brasilia (REPÚBLICA FEDERATIVA DE BRASIL) los
días 12 y 13 de septiembre de 2017, los Estados Partes del MERCOSUR,
aprobaron la Resolución N° 27 de fecha 13 de septiembre de 2017 del
GRUPO MERCADO COMÚN, la cual debe ser incorporada al ordenamiento
jurídico nacional, y se encuentra contenida en el Anexo II que,
registrado con el Nº IF-2018-07036007-APN-SECMA#MA, forma parte
integrante de la presente medida.
Que asimismo, resulta necesario derogar el Anexo I de la Resolución N°
798 de fecha 26 de agosto de 2011 del entonces MINISTERIO DE
AGRICULTURA, GANADERÍA Y PESCA, dado que la Resolución N° 25 de fecha
15 de junio de 2010 del GRUPO MERCADO COMÚN contenida en dicho anexo,
ha sido sustituida por la Resolución N° 44 de fecha 19 de diciembre de
2017 del GRUPO MERCADO COMÚN.
Que en tal sentido, resulta necesario incorporar al ordenamiento
jurídico nacional la Resolución N° 44 de fecha 19 de diciembre de 2017
del GRUPO MERCADO COMÚN mencionada precedentemente, la cual se
encuentra contenida en el Anexo III que, registrado con el Nº
IF-2018-07036141-APN-SECMA#MA, forma parte integrante de la presente
medida.
Que la Dirección General de Asuntos Jurídicos del MINISTERIO DE
AGROINDUSTRIA ha tomado la intervención que le compete.
Que la presente resolución se dicta en ejercicio de las atribuciones
conferidas por la Ley de Ministerios (texto ordenado por Decreto N°
438/92) y sus modificaciones.
Por ello,
EL MINISTRO DE AGROINDUSTRIA
RESUELVE:
ARTÍCULO 1°.- Derógase el Anexo XI de la Resolución Nº 133 de fecha 16
de marzo de 2011 del ex-MINISTERIO DE AGRICULTURA, GANADERÍA Y PESCA,
por los motivos expuestos en los considerandos de la presente medida.
ARTÍCULO 2º.- Derógase el Anexo I de la Resolución N° 798 de fecha 26
de agosto de 2011 del entonces MINISTERIO DE AGRICULTURA, GANADERÍA Y
PESCA, por los motivos expuestos en los considerandos de la presente
medida.
ARTÍCULO 3º.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 25 de fecha 13 de septiembre de 2017 del GRUPO MERCADO
COMÚN “Equivalencias de Denominaciones de Clases y/o Categorías de
Semillas Botánicas (Derogación de la Resolución Nº 28 de fecha 15 de
junio de 2010 del GRUPO MERCADO COMÚN)”, que como Anexo I, registrado
con el Nº IF-2018-07035886-APN-SECMA#MA, forma parte integrante de la
presente medida.
ARTÍCULO 4º.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 27 de fecha 13 de septiembre de 2017 del GRUPO MERCADO
COMÚN “Requisitos Zoosanitarios Adicionales de los Estados Partes para
la Importación de Rumiantes con relación a la Enfermedad de
Schmallenberg” que como Anexo II, registrado con el Nº
IF-2018-07036007-APN-SECMA#MA, forma parte integrante de la presente
medida.
ARTÍCULO 5º.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 44 de fecha 19 de diciembre de 2017 del GRUPO MERCADO
COMÚN “Requisitos Zoosanitarios de los Estados Partes para la
Importación de Embriones Bovinos y Bubalinos Colectados In Vivo y/o
Producidos In Vitro (Derogación de la Resolución N° 25 de fecha 15 de
junio de 2010 del GRUPO MERCADO COMÚN)” que como Anexo III, registrado
con el Nº IF-2018-07036141-APN-SECMA#MA, forma parte integrante de la
presente medida.
ARTÍCULO 6°.- La normativa que se incorpora por la presente resolución
entrará en vigor de conformidad con lo dispuesto por el Artículo 40 del
Protocolo Adicional al Tratado de Asunción sobre la Estructura
Institucional del MERCOSUR - Protocolo de Ouro Preto - suscripto por la
REPÚBLICA ARGENTINA, la REPÚBLICA FEDERATIVA DEL BRASIL, la REPÚBLICA
DEL PARAGUAY y la REPÚBLICA ORIENTAL DEL URUGUAY, en la Ciudad de Ouro
Preto (REPÚBLICA FEDERATIVA DEL BRASIL), el día 17 de diciembre de
1994, aprobado por la Ley N° 24.560.
ARTÍCULO 7°.- Comuníquese, publíquese, dése a la DIRECCIÓN NACIONAL DEL
REGISTRO OFICIAL y archívese. — Luis Miguel Etchevehere.
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la
edición web del BORA -www.boletinoficial.gob.ar-.
e. 21/03/2018 N° 18232/18 v. 21/03/2018
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
ANEXO III
MERCOSUR/GMC/RES. N° 44/17
REQUISITOS
ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE EMBRIONES
BOVINOS Y BUBALINOS COLECTADOS IN VIVO Y/O PRODUCIDOS IN VITRO
(DEROGACIÓN DE LA RES. GMC N° 25/10)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común, la Resolución N° 25/10 y 45/14 del Grupo Mercado Común.
CONSIDERANDO:
Que es necesario actualizar los requisitos zoosanitarios, así como el
modelo de certificado establecido para la importación a los Estados
Parte de embriones bovinos y colectados in vivo, así como también
armonizar los requisitos zoosanitarios para la importación a los
Estados Parte de embriones bovinos y bubalinos producidos in vitro.
Que la Resolución GMC N° 45/14 establece los Requisitos Zoosanitarios
adicionales de los Estados Partes para la importación de semen y
embriones de rumiantes con relación a la enfermedad de Schmallenberg.
EL
GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos Zoosanitarios de los Estados Partes
para la Importación de embriones bovinos y bubalinos colectados in vivo
y/o producidos in vitro" y el Modelo de Certificado Veterinario
Internacional (CVI) que constan como Anexos I y II, respectivamente, y
que forman parte de la presente Resolución.
Art. 2 - Derogar la Resolución GMC N° 25/10.
Art. 3 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento
jurídico de los Estados Partes antes del 17/VI/2018.
XLIX
GMC Ext - Brasilia, 19/XII/17
ANEXO I
REQUISITOS
ZOOSANITARIOS DE LOS ESTADOS PARTE PARA LA IMPORTACIÓN DE EMBRIONES
BOVINOS Y BUBALINOS COLECTADOS IN VIVO Y/O PRODUCIDOS IN VITRO
CAPÍTULO I
DE LA CERTIFICACIÓN
Art.1 - Toda importación de embriones bovinos y bubalinos deberá estar
acompañada del Certificado Veterinario Internacional (CVI) emitido por
la Autoridad Veterinaria del país exportador, que certifique el
cumplimiento de los requisitos zoosanitarios que constan en la presente
Resolución.
1.1. El modelo de CVI deberá ser previamente acordado entre el país
exportador y el Estado Parte importador y de acuerdo con lo establecido
en el Anexo II de la presente Resolución.
Art. 2 - El CVI tendrá una validez de sesenta (60) días a partir de la
fecha de su emisión.
Art.3 - Los exámenes de diagnóstico requeridos deberán ser realizados
en laboratorios oficiales, acreditados o reconocidos por la Autoridad
Veterinaria del país exportador.
3.1. Estos exámenes deberán ser realizados de acuerdo con el Manual de
Pruebas Diagnósticas y Vacunas para los Animales Terrestres de la
Organización Mundial de Sanidad Animal (OIE).
Art. 4 - El país exportador o zona o compartimento del país exportador
que cumple con lo establecido en los capítulos correspondientes del
Código Terrestre de la OIE para ser considerado oficialmente libre y
obtener el reconocimiento del Estado Parte importador para alguna de
las enfermedades para las que se requieren pruebas y vacunaciones,
estará exento de la realización de las mismas, así como exento de la
certificación de establecimientos libres.
4.1. En este caso, la certificación de país, zona o compartimento libre
de las enfermedades en cuestión deberá ser incluida en el CVI.
4.2. En el caso de enfermedades para las cuales la OIE no emite
reconocimiento oficial de país o zona libre, el Estado Parte importador
podrá solicitar información adicional para el reconocimiento de dicha
condición sanitaria del país exportador.
Art. 5 - El Estado Parte importador que cumpla con lo establecido en
los capítulos correspondientes del Código Terrestre de la OIE para ser
considerado oficialmente libre, o que posea un programa oficial de
prevención, control o erradicación para cualquier enfermedad, se
reserva el derecho de requerir medidas de mitigación adicionales, con
el objetivo de prevenir el ingreso de esa enfermedad al país.
Art. 6 - Podrán ser acordados entre el Estado Parte importador y el
país exportador otros procedimientos sanitarios que otorguen garantías
equivalentes o superiores para la importación.
CAPÍTULO
II
INFORMACIONES ZOOSANITARIAS
Art. 7 - Con relación a Pleuroneumonía Contagiosa Bovina, durante el
período de colecta y producción de los embriones, el país exportador
deberá ser reconocido como libre de la enfermedad por la OIE o deberá
declararse libre, de acuerdo con lo establecido en el Código Terrestre
de la OIE, y esa condición deberá ser reconocida por el Estado Parte
importador.
Art. 8 - Con relación a Dermatosis Nodular Contagiosa:
8.1. el país o zona del país exportador deberá cumplir con lo
establecido en el Código Terrestre de la OIE para ser considerado libre
de la enfermedad y esa condición deberá ser reconocida por el Estado
Parte importador, o
8.2 las hembras donantes:
8.2.1. no deberán haber manifestado ningún signo clínico de la
enfermedad el día de la colecta o producción de los embriones ni
durante los veintiocho (28) días posteriores, y
8.2.2 deberán permanecer en establecimiento(s) en el(los) que no fue
registrado ningún caso de la enfermedad durante los sesenta (60) días
anteriores a la colecta y producción, y
8.2.3. alguna de las siguientes opciones:
8.2.3.1 deberán ser vacunadas regularmente contra la enfermedad de
acuerdo con las recomendaciones del fabricante de la vacuna, o
8.2.3.2 deberán resultar negativas en pruebas serológicas para la
detección de anticuerpos específicos del virus de la dermatosis nodular
contagiosa realizadas el día de la colecta y veintiún (21) días después
de la misma, o
8.2.3.3 deberán resultar negativas en una prueba reacción en cadena de
la polimerasis (PCR) para identificación del agente en una muestra de
sangre tomada el día de la colecta.
Art. 9 - Con respecto a Fiebre del Valle del Rift:
9.1 El país o zona del país exportador deberá cumplir con lo
establecido en el Código Terrestre de la OIE para ser considerado como
libre de la enfermedad, y esa condición deberá ser reconocida por el
Estado Parte importador, o
9.2 En caso de embriones colectados in vivo, las hembras donantes:
9.2.1. no deberán manifestar ningún signo clínico de Fiebre del valle
del Rift durante los catorce (14) días anteriores y los catorce (14)
días posteriores a la colecta de los embriones, y
9.2.2 deberán ser sometidas a una prueba de ELISA o virus
neutralización (VN), por lo menos catorce (14) días después de la
última colecta, con resultados negativos
Art. 10 - Con respecto a Tuberculosis, las donantes:
10.1 deberán proceder de rebaños libres de esta enfermedad, o
10.2 deberán presentar resultado negativo a una prueba diagnóstica de
tuberculinización intradérmica, con tuberculina PPD bovina o con PPD
bovina y aviar, realizada durante el período de 30 (treinta) días
previos a la primera colecta.
Art. 11 - El equipo de colecta de embriones in vivo (EC), el equipo de
producción de embriones in vitro (EP) y el laboratorio de manipulación
de embriones (LM) fijos o móviles, deberán estar aprobados y
supervisado por la Autoridad Veterinaria del país exportador.
Art. 12 - Para aprobar los EC, así como los EP y los LM de embriones,
la Autoridad Veterinaria del país exportador deberá utilizar las
"Condiciones aplicables al equipo de la colecta de embriones", las
"Condiciones aplicables al equipo de producción de embriones", así como
los "Las Condiciones aplicables a los laboratorios de manipulación de
embriones", descriptas en el Código Terrestre de la OIE.
Art. 13 - El LM no podrá estar localizado o los EC o EP no podrán
actuar en zonas con restricciones sanitarias relativas a las
enfermedades de bovinos y bubalinos, cuya transmisión pueda ocurrir por
medio de los embriones.
Art. 14 - Las donantes deberán permanecer en el rebaño de origen por un
período mínimo de treinta (30) días anteriores a la colecta de los
embriones. En ese período, así como en los treinta (30) días
posteriores a la colecta, en dicho rebaño no deberá haber sido
reportado oficialmente ningún caso de Diarrea viral bovina, y las
referidas donantes no deberán presentar ningún signo clínico de
enfermedades pasibles de ser transmitidas por embriones.
14.1. En caso de embriones producidos in vitro, los animales donantes
no deberán proceder de establecimientos que sean objeto de
restricciones en relación con la fiebre aftosa ni peste de pequeños
rumiantes, y no deberá ser extraído ningún tejido ni ser aspirados
ovocitos en una zona infectada o que sea objeto de restricciones
veterinarias en relación con las citadas enfermedades.
Art. 15. En el caso de donantes importadas, éstas deberán ser
procedentes de países libres de Pleuroneumonía Contagiosa Bovina y
deberán permanecer al menos sesenta (60) días previos a la colecta en
el país exportador de los embriones.
Art. 16 - El semen utilizado para la producción de los embriones deberá
ser obtenido en un Centro de Colecta y Procesamiento de Semen (CCPS)
aprobado por la Autoridad Veterinaria del país de origen del semen,
cumpliendo con las "Condiciones generales de higiene en los centros de
toma y tratamiento de semen", y las descriptas en el Capítulo referente
a "Toma y tratamiento de semen de bovinos, de pequeños rumiantes y de
verracos" del Código Terrestre de la OIE.
Art. 17 - Los embriones deberán ser colectados, procesados y
almacenados de acuerdo con las recomendaciones establecidas en el
Código Terrestre de la OIE y en el Manual de la Sociedad Internacional
de Transferencia de Embriones (IETS). En todos los casos, se utilizará
el protocolo que incluye los lavados suplementarios con tripsina,
contemplado en dicho Manual.
17.1. En el CVI deberá constar que después de los lavados, la zona
pelúcida de cada embrión fue examinada en su superficie, usando
microscopio con aumento no menor que 50 veces, encontrándose intacta y
libre de material adherente.
Art. 18 - Todo equipamiento utilizado para colectar, producir,
manipular, lavar, congelar y almacenar los embriones deberá ser
esterilizado antes del uso, de acuerdo con las recomendaciones del
Manual de la IETS.
Art. 19 - Todos los productos biológicos de origen animal utilizados en
la colecta, producción, procesamiento y almacenamiento de los embriones
deberán estar libres de microorganismos. Solamente podrá ser utilizado
suero fetal bovino, albúmina sérica o cualquier otro producto de origen
de rumiantes cuando procedan de países reconocidos por la OIE como de
riesgo insignificante o de riesgo controlado y sin registro de casos,
en relación a Encefalopatía Espongiforme Bovina.
Art. 20 - Los embriones deberán ser almacenados en contenedores nuevos
o lavados y desinfectados, utilizando nitrógeno líquido de primer uso,
por un período mínimo de treinta (30) días anteriores al embarque.
Durante ese período, ningún signo clínico de enfermedades transmisibles
deberá haber sido registrado, en el establecimiento donde los embriones
fueron colectados y en las hembras donantes.
Art. 21 - En el momento del embarque, el contenedor deberá ser
precintado bajo supervisión de la Autoridad Veterinaria del país
exportador y el número de precinto deberá ser registrado en el CVI.
CAPITULO
III
DISPOSICIONES FINALES
Art. 22 - El no cumplimiento de los términos de la presente Resolución
permitirá a la Autoridad Veterinaria del Estado Parte importador
adoptar las medidas correspondientes, de acuerdo con las normas
vigentes en cada Estado Parte.
Art. 23 - A consideración de cada Estado Parte importador, por razones
de identificación y trazabilidad de los embriones producidos in vitro a
partir de la colecta de ovocitos de hembras en mataderos, tal
importación podrá no ser autorizada.
ANEXO
II
MODELO DE CERTIFICADO VETERINARIO
INTERNACIONAL PARA LA EXPORTACIÓN DE EMBRIONES DE BOVINOS Y BUBALINOS
COLECTADOS IN
VIVO Y/O PRODUCIDOS IN VITRO A LOS ESTADOS PARTES
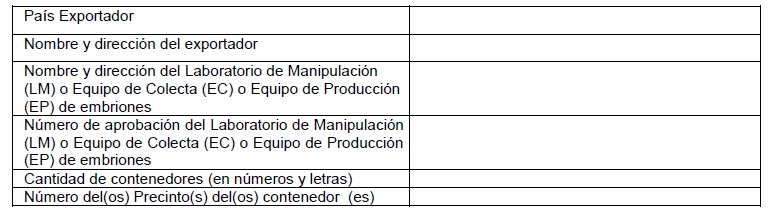
I. PROCEDENCIA:
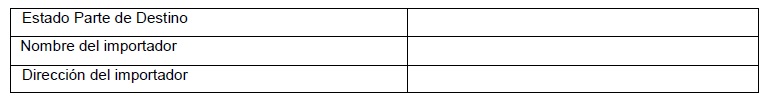
II. DESTINO:
III. TRANSPORTE
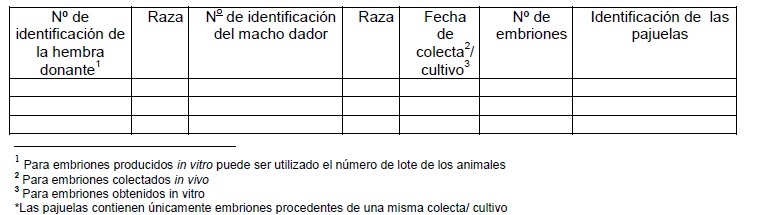
IV. INFORMACIONES REFERENTES A LOS
EMBRIONES DE CADA DONANTE:
V. INFORMACIONES ZOOSANITARIAS
El Veterinario Oficial abajo firmante certifica que:
1. Con relación a Pleuroneumonía Contagiosa Bovina, durante el período
de colecta y producción de los embriones (tachar lo que no corresponda)
1.1 el país exportador es reconocido como libre de la enfermedad por la
OIE o
1.2 el país exportador se declara libre, de acuerdo con lo establecido
en el Código Terrestre de la OIE, y esa condición es reconocida por el
Estado Parte importador;
2. Con relación a Dermatosis Nodular Contagiosa (tachar lo que no
corresponda)
2.1. el país o zona del país exportador cumple con lo establecido en el
Código Terrestre de la OIE para ser considerado como libre de la
enfermedad y esa condición es reconocida por el Estado Parte importador,
o
2.2 las hembras donantes:
2.2.1. no manifestaron ningún signo clínico de la enfermedad el día de
la colecta o producción de
los embriones ni durante los veintiocho (28) días posteriores, y
2.2.2 permanecieron en establecimiento(s) en el(los) que no fue
registrado ningún caso de la
enfermedad durante los sesenta (60) días anteriores a la colecta o
producción de los embriones, y
2.2.3. una de las siguientes opciones:
2.2.3.1 fueron vacunadas regularmente contra la enfermedad de acuerdo
con las recomendaciones del fabricante de la vacuna,
o
2.2.3.2 resultaron negativas a dos (2) pruebas serológicas para la
detección de anticuerpos específicos contra el virus de la dermatosis
nodular contagiosa realizadas el día de la colecta y veintiún (21) días
después de la misma,
o
2.2.3.3 resultaron negativas en una prueba PCR de identificación del
agente en una muestra de sangre tomada el día de la colecta;
3.
Con respecto a Fiebre del Valle del Rift: (tachar lo que no corresponda)
3.1 El país o zona del país exportador cumple con lo establecido en el
CódigoTerrestre de la OIE para ser considerado(a) libre de Fiebre del
Valle del Rift y esa condición es reconocida por el Estado Parte
importador,
o
3.2 En caso de embriones colectados in vivo, las hembras donantes:
3.2.1. no manifestaron ningún signo de fiebre del valle del Rift
durante los 14 (catorce) días anteriores y los 14 (catorce) días
posteriores a la colecta de los embriones,
3.2.2 fueron sometidas a una prueba de ELISA o virus neutralización,
por lo menos 14 (catorce) días después de la última colecta, con
resultados negativos
4. Con respecto a Tuberculosis: (tachar lo que no corresponda) 4.1 las
donantes proceden de rebaños libres de la enfermedad, o
4.2 presentaron resultado negativo a una prueba diagnóstica de
tuberculinización intradérmica con tuberculina PPD bovina o con PPD
bovina y aviar, realizada durante el período de 30 (treinta) días
previos a la primera colecta.
5. El equipo de colecta de embriones in vivo (EC), el equipo de
producción de embriones in vitro (EP) y el laboratorio de manipulación
de embriones (LM) fijos o móviles, están aprobados y supervisados por
la Autoridad Veterinaria del país exportador.
6. El LM no están localizado o los EC y EP no actuaron en zonas con
restricciones sanitarias relativas a las enfermedades de bovinos y
bubalinos, cuya transmisión pueda ocurrir por medio de los embriones.
7. Las donantes permanecieron en el rebaño de origen por un período
mínimo de treinta (30) días anteriores a la colecta de los embriones.
En ese período, así como en los treinta (30) días posteriores a la
colecta, en dicho rebaño no fue reportado oficialmente ningún caso de
Diarrea viral bovina y las referidas donantes no presentaron ningún
signo clínico de enfermedades pasibles de ser transmitidas por
embriones.
7.1. En caso de embriones producidos in vitro: los animales donantes no
proceden de establecimientos que sean objeto de restricciones en
relación con la fiebre aftosa ni peste de pequeños rumiantes, y no fue
extraído ningún tejido ni fueron aspirados ovocitos en una zona
infectada o que fue objeto de restricciones veterinarias en relación
con las citadas enfermedades. (tachar en caso que no corresponda)
8. En el caso de donantes importadas, éstas son procedentes de países
libres de Pleuroneumonía Contagiosa Bovina y permanecieron al menos
sesenta (60) días previos a la colecta en el país exportador de los
embriones.
9. El semen utilizado para la producción de los embriones a ser
exportados fue ^btenidQ..en un Centro de Colecta y Procesamiento de
Semen (CCPS) aprobado por la Autoridad VeteANEax° l ^ís de origen del
semen, cumpliendo con las "Condiciones generales de higiene en los
centros de toma y tratamiento de semen", y las descriptas en el
Capítulo referente a "Toma y tratamiento de semen de bovinos, de
pequeños rumiantes y de verracos" del Código Terrestre de la OIE.
10. Los embriones fueron colectados, procesados y almacenados de
acuerdo con las recomendaciones establecidas en el Código Terrestre de
la OIE y en el Manual de la Sociedad Internacional de Transferencia de
Embriones (IETS). En todos los casos, fue utilizado el protocolo que
incluye los lavados suplementarios con tripsina, contemplado en dicho
Manual.
10.1. Después de los lavados, la zona pelúcida de cada embrión fue
examinada en su superficie, usando microscopio con aumento no menor que
50X, encontrándose intacta y libre de material adherente.
11. Todo equipamiento utilizado para colectar, producir, manipular,
lavar, congelar y almacenar los embriones fue esterilizado antes del
uso, de acuerdo con las recomendaciones del Manual de la IETS.
12. Todos los productos biológicos de origen animal utilizados en la
colecta, producción, procesamiento y almacenamiento de los embriones
están libres de microorganismos. Solamente fue utilizado suero fetal
bovino, albúmina sérica o cualquier otro producto de origen de
rumiantes procedente de países reconocidos por la OIE como de riesgo
insignificante o de riesgo controlado y sin registro de casos, en
relación a Encefalopatía Espongiforme Bovina.
13. Los embriones fueron almacenados en contenedores nuevos o lavados y
desinfectados, utilizando nitrógeno líquido de primer uso, por un
período mínimo de treinta (30) días anteriores al embarque. Durante ese
período, ningún signo clínico de enfermedades transmisibles fue
registrado, en el establecimiento donde los embriones fueron colectados
y en las hembras donantes.
14. En el momento del embarque el contenedor fue precintado bajo
supervisión de la Autoridad Veterinaria del país exportador y el número
de precinto fue registrado en el CVI.
Este CVI tiene una validez de sesenta (60) días a partir de su emisión
para ingresar al Estado Parte importador.
Lugar de Emisión:..................................
Fecha:......................................
Nombre y Firma del Veterinario
Oficial:......................................
Sello del Servicio Veterinario
Oficial:............................................................
IF-2018-07036141 -APN-SECMA#MA
ANEXO II
MERCOSUR/GMC/RES. N° 27/17
REQUISITOS
ZOOSANITARIOS ADICIONALES DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE
RUMIANTES CON RELACIÓN A LA ENFERMEDAD DE SCHMALLENBERG
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto y la Decisión N° 06/96 del Consejo del
Mercado Común.
CONSIDERANDO:
Que la enfermedad de Schmallenberg está ampliamente distribuida por
distintos países de Europa y que no existen registros de la misma en
los Estados Partes.
Que la enfermedad de Schmallenberg provoca significativas pérdidas
económicas a través de la disminución en la productividad así como a
través de abortos y efectos teratogénicos en rumiantes.
Que las evidencias científicas disponibles dan sustento a la adopción
de medidas de mitigación de riesgo para prevenir la introducción de la
enfermedad en el MERCOSUR, en el caso de la importación de rumiantes
procedentes de países que registraron casos.
Que la armonización de los requisitos zoosanitarios del MERCOSUR tiende
a eliminar los obstáculos que se generan por las diferencias de las
regulaciones nacionales vigentes, dando cumplimiento a lo establecido
en el Tratado de Asunción.
EL
GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos zoosanitarios adicionales de los
Estados Partes para la importación de rumiantes con relación a la
Enfermedad de Schmallenberg", que constan como Anexo y forman parte de
la presente Resolución.
Art. 2 - Los Estados Partes indicarán, en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8), los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 3 - Los requisitos a los que hace referencia el Artículo 1 deberán
constar como certificación adicional en los modelos de Certificado
Veterinario Internacional aprobados para exportar rumiantes a los
Estados Partes.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento
jurídico de los Estados Partes antes del 13/III/2018.
CV GMC
- Brasilia, 13/IX/17.
ANEXO
REQUISITOS ZOOSANITARIOS ADICIONALES
DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE RUMIANTES CON RELACIÓN A
LA ENFERMEDAD DE SCHMALLENBERG
Art. 1 - En los casos en los que los Estados Partes importen rumiantes,
el país de origen deberá certificar que los animales:
I) sean originarios de un país donde nunca se hayan registrado casos de
la enfermedad de Schmallenberg;
o,
II) en caso de que sean originarios de países donde se hayan registrado
casos de la enfermedad de Schmallenberg:
i) provengan de un establecimiento donde no haya habido evidencias
clínicas ni serológicas de la enfermedad durante al menos seis (6)
meses previos al inicio de la cuarentena;
ii) hayan sido sometidos a una cuarentena bajo supervisión oficial en
un establecimiento donde no haya habido evidencias clínicas ni
serológicas de la enfermedad así como en un radio de diez (10) Km de
este, durante los treinta (30) días previos al embarque;
iii) hayan sido sometidos a una prueba de ELISA o Inmunofluorescencia
indirecta o Virus Neutralización con resultado negativo realizada al
menos veintiún (21) días posteriores al inicio de la cuarentena;
iv) hayan sido protegidos contra vectores en todo momento desde el
inicio de la cuarentena hasta su embarque en el punto de salida del
país exportador.
IF-2018-07036007-APN-SECMA#MA
ANEXO I
MERCOSUR/GMC/RES. N° 25/17
EQUIVALENCIAS
DE DENOMINACIONES DE CLASES Y/O CATEGORÍAS DE SEMILLAS BOTÁNICAS
(DEROGACIÓN DE LA RES. GMC N° 28/10)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto y las Resoluciones N° 77/00, 43/05, 03/09,
28/10 y 21/17 del Grupo Mercado Común.
CONSIDERANDO:
Que por la Resolución GMC N° 28/10 se aprobaron las "Equivalencias de
denominaciones de clases y/o categorías de semillas botánicas".
Que a los efectos de facilitar el comercio de semillas entre los
Estados Partes, es necesario actualizar la tabla de equivalencias de
denominaciones de Clases y/o Categorías de Semillas Botánicas.
EL
GRUPO MERCADO COMÚN
RESUELVE:
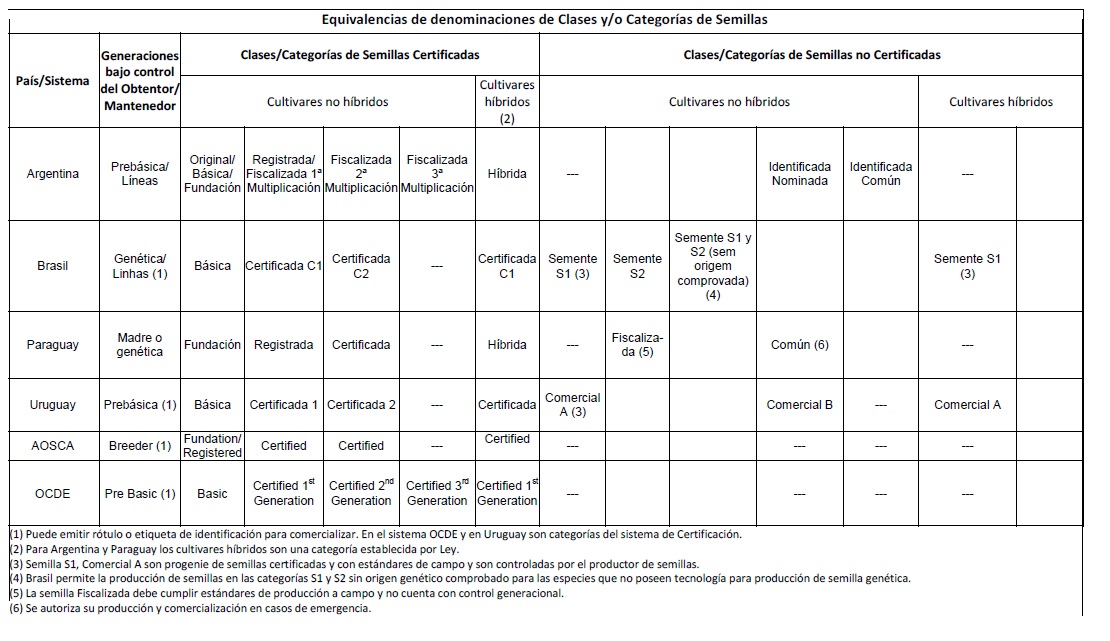
Art. 1 - Aprobar las "Equivalencias de Denominaciones de Clases y/o
Categorías de Semillas Botánicas", que constan como Anexo y forman
parte de la presente Resolución.
Art. 2 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 3 - Derogar la Resolución GMC N° 28/10.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento
jurídico de los Estados Partes antes del 13/III/2018.
CV GMC
- Brasilia, 13/IX/17.
ANEXO
IF-2018-07035 886-APN-SECMA#MA