MERCOSUR/GMC/RES. N° 44/17
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE EMBRIONES BOVINOS Y BUBALINOS COLECTADOS IN VIVO Y/O PRODUCIDOS IN VITRO
(DEROGACIÓN DE LA RES. GMC N° 25/10)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común, la Resolución N° 25/10 y 45/14 del Grupo Mercado Común.
CONSIDERANDO:
Que es necesario actualizar los requisitos zoosanitarios, así como el
modelo de certificado establecido para la importación a los Estados
Parte de embriones bovinos y colectados in vivo, así como también
armonizar los requisitos zoosanitarios para la importación a los
Estados Parte de embriones bovinos y bubalinos producidos in vitro.
Que la Resolución GMC N° 45/14 establece los Requisitos Zoosanitarios
adicionales de los Estados Partes para la importación de semen y
embriones de rumiantes con relación a la enfermedad de Schmallenberg.
EL GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos Zoosanitarios de los Estados Partes
para la Importación de embriones bovinos y bubalinos colectados in vivo
y/o producidos in vitro" y el Modelo de Certificado Veterinario
Internacional (CVI) que constan como Anexos I y II, respectivamente, y
que forman parte de la presente Resolución.
Art. 2 - Derogar la Resolución GMC N° 25/10.
Art. 3 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento jurídico de los Estados Partes antes del 17/VI/2018.
XLIX GMC Ext - Brasilia, 19/XII/17
ANEXO I
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTE PARA LA IMPORTACIÓN DE EMBRIONES BOVINOS Y BUBALINOS COLECTADOS IN VIVO Y/O PRODUCIDOS IN VITRO
CAPÍTULO I
DE LA CERTIFICACIÓN
Art.1 - Toda importación de embriones bovinos y bubalinos deberá estar
acompañada del Certificado Veterinario Internacional (CVI) emitido por
la Autoridad Veterinaria del país exportador, que certifique el
cumplimiento de los requisitos zoosanitarios que constan en la presente
Resolución.
1.1. El modelo de CVI deberá ser previamente acordado entre el país
exportador y el Estado Parte importador y de acuerdo con lo establecido
en el Anexo II de la presente Resolución.
Art. 2 - El CVI tendrá una validez de sesenta (60) días a partir de la fecha de su emisión.
Art.3 - Los exámenes de diagnóstico requeridos deberán ser realizados
en laboratorios oficiales, acreditados o reconocidos por la Autoridad
Veterinaria del país exportador.
3.1. Estos exámenes deberán ser realizados de acuerdo con el Manual de
Pruebas Diagnósticas y Vacunas para los Animales Terrestres de la
Organización Mundial de Sanidad Animal (OIE).
Art. 4 - El país exportador o zona o compartimento del país exportador
que cumple con lo establecido en los capítulos correspondientes del
Código Terrestre de la OIE para ser considerado oficialmente libre y
obtener el reconocimiento del Estado Parte importador para alguna de
las enfermedades para las que se requieren pruebas y vacunaciones,
estará exento de la realización de las mismas, así como exento de la
certificación de establecimientos libres.
4.1. En este caso, la certificación de país, zona o compartimento libre
de las enfermedades en cuestión deberá ser incluida en el CVI.
4.2. En el caso de enfermedades para las cuales la OIE no emite
reconocimiento oficial de país o zona libre, el Estado Parte importador
podrá solicitar información adicional para el reconocimiento de dicha
condición sanitaria del país exportador.
Art. 5 - El Estado Parte importador que cumpla con lo establecido en
los capítulos correspondientes del Código Terrestre de la OIE para ser
considerado oficialmente libre, o que posea un programa oficial de
prevención, control o erradicación para cualquier enfermedad, se
reserva el derecho de requerir medidas de mitigación adicionales, con
el objetivo de prevenir el ingreso de esa enfermedad al país.
Art. 6 - Podrán ser acordados entre el Estado Parte importador y el
país exportador otros procedimientos sanitarios que otorguen garantías
equivalentes o superiores para la importación.
CAPÍTULO II
INFORMACIONES ZOOSANITARIAS
Art. 7 - Con relación a Pleuroneumonía Contagiosa Bovina, durante el
período de colecta y producción de los embriones, el país exportador
deberá ser reconocido como libre de la enfermedad por la OIE o deberá
declararse libre, de acuerdo con lo establecido en el Código Terrestre
de la OIE, y esa condición deberá ser reconocida por el Estado Parte
importador.
Art. 8 - Con relación a Dermatosis Nodular Contagiosa:
8.1. el país o zona del país exportador deberá cumplir con lo
establecido en el Código Terrestre de la OIE para ser considerado libre
de la enfermedad y esa condición deberá ser reconocida por el Estado
Parte importador, o
8.2 las hembras donantes:
8.2.1. no deberán haber manifestado ningún signo clínico de la
enfermedad el día de la colecta o producción de los embriones ni
durante los veintiocho (28) días posteriores, y
8.2.2 deberán permanecer en establecimiento(s) en el(los) que no fue
registrado ningún caso de la enfermedad durante los sesenta (60) días
anteriores a la colecta y producción, y
8.2.3. alguna de las siguientes opciones:
8.2.3.1 deberán ser vacunadas regularmente contra la enfermedad de
acuerdo con las recomendaciones del fabricante de la vacuna, o
8.2.3.2 deberán resultar negativas en pruebas serológicas para la
detección de anticuerpos específicos del virus de la dermatosis nodular
contagiosa realizadas el día de la colecta y veintiún (21) días después
de la misma, o
8.2.3.3 deberán resultar negativas en una prueba reacción en cadena de
la polimerasis (PCR) para identificación del agente en una muestra de
sangre tomada el día de la colecta.
Art. 9 - Con respecto a Fiebre del Valle del Rift:
9.1 El país o zona del país exportador deberá cumplir con lo
establecido en el Código Terrestre de la OIE para ser considerado como
libre de la enfermedad, y esa condición deberá ser reconocida por el
Estado Parte importador, o
9.2 En caso de embriones colectados in vivo, las hembras donantes:
9.2.1. no deberán manifestar ningún signo clínico de Fiebre del valle
del Rift durante los catorce (14) días anteriores y los catorce (14)
días posteriores a la colecta de los embriones, y
9.2.2 deberán ser sometidas a una prueba de ELISA o virus
neutralización (VN), por lo menos catorce (14) días después de la
última colecta, con resultados negativos
Art. 10 - Con respecto a Tuberculosis, las donantes:
10.1 deberán proceder de rebaños libres de esta enfermedad, o
10.2 deberán presentar resultado negativo a una prueba diagnóstica de
tuberculinización intradérmica, con tuberculina PPD bovina o con PPD
bovina y aviar, realizada durante el período de 30 (treinta) días
previos a la primera colecta.
Art. 11 - El equipo de colecta de embriones in vivo (EC), el equipo de
producción de embriones in vitro (EP) y el laboratorio de manipulación
de embriones (LM) fijos o móviles, deberán estar aprobados y
supervisado por la Autoridad Veterinaria del país exportador.
Art. 12 - Para aprobar los EC, así como los EP y los LM de embriones,
la Autoridad Veterinaria del país exportador deberá utilizar las
"Condiciones aplicables al equipo de la colecta de embriones", las
"Condiciones aplicables al equipo de producción de embriones", así como
los "Las Condiciones aplicables a los laboratorios de manipulación de
embriones", descriptas en el Código Terrestre de la OIE.
Art. 13 - El LM no podrá estar localizado o los EC o EP no podrán
actuar en zonas con restricciones sanitarias relativas a las
enfermedades de bovinos y bubalinos, cuya transmisión pueda ocurrir por
medio de los embriones.
Art. 14 - Las donantes deberán permanecer en el rebaño de origen por un
período mínimo de treinta (30) días anteriores a la colecta de los
embriones. En ese período, así como en los treinta (30) días
posteriores a la colecta, en dicho rebaño no deberá haber sido
reportado oficialmente ningún caso de Diarrea viral bovina, y las
referidas donantes no deberán presentar ningún signo clínico de
enfermedades pasibles de ser transmitidas por embriones.
14.1. En caso de embriones producidos in vitro, los animales donantes
no deberán proceder de establecimientos que sean objeto de
restricciones en relación con la fiebre aftosa ni peste de pequeños
rumiantes, y no deberá ser extraído ningún tejido ni ser aspirados
ovocitos en una zona infectada o que sea objeto de restricciones
veterinarias en relación con las citadas enfermedades.
Art. 15. En el caso de donantes importadas, éstas deberán ser
procedentes de países libres de Pleuroneumonía Contagiosa Bovina y
deberán permanecer al menos sesenta (60) días previos a la colecta en
el país exportador de los embriones.
Art. 16 - El semen utilizado para la producción de los embriones deberá
ser obtenido en un Centro de Colecta y Procesamiento de Semen (CCPS)
aprobado por la Autoridad Veterinaria del país de origen del semen,
cumpliendo con las "Condiciones generales de higiene en los centros de
toma y tratamiento de semen", y las descriptas en el Capítulo referente
a "Toma y tratamiento de semen de bovinos, de pequeños rumiantes y de
verracos" del Código Terrestre de la OIE.
Art. 17 - Los embriones deberán ser colectados, procesados y
almacenados de acuerdo con las recomendaciones establecidas en el
Código Terrestre de la OIE y en el Manual de la Sociedad Internacional
de Transferencia de Embriones (IETS). En todos los casos, se utilizará
el protocolo que incluye los lavados suplementarios con tripsina,
contemplado en dicho Manual.
17.1. En el CVI deberá constar que después de los lavados, la zona
pelúcida de cada embrión fue examinada en su superficie, usando
microscopio con aumento no menor que 50 veces, encontrándose intacta y
libre de material adherente.
Art. 18 - Todo equipamiento utilizado para colectar, producir,
manipular, lavar, congelar y almacenar los embriones deberá ser
esterilizado antes del uso, de acuerdo con las recomendaciones del
Manual de la IETS.
Art. 19 - Todos los productos biológicos de origen animal utilizados en
la colecta, producción, procesamiento y almacenamiento de los embriones
deberán estar libres de microorganismos. Solamente podrá ser utilizado
suero fetal bovino, albúmina sérica o cualquier otro producto de origen
de rumiantes cuando procedan de países reconocidos por la OIE como de
riesgo insignificante o de riesgo controlado y sin registro de casos,
en relación a Encefalopatía Espongiforme Bovina.
Art. 20 - Los embriones deberán ser almacenados en contenedores nuevos
o lavados y desinfectados, utilizando nitrógeno líquido de primer uso,
por un período mínimo de treinta (30) días anteriores al embarque.
Durante ese período, ningún signo clínico de enfermedades transmisibles
deberá haber sido registrado, en el establecimiento donde los embriones
fueron colectados y en las hembras donantes.
Art. 21 - En el momento del embarque, el contenedor deberá ser
precintado bajo supervisión de la Autoridad Veterinaria del país
exportador y el número de precinto deberá ser registrado en el CVI.
CAPITULO III
DISPOSICIONES FINALES
Art. 22 - El no cumplimiento de los términos de la presente Resolución
permitirá a la Autoridad Veterinaria del Estado Parte importador
adoptar las medidas correspondientes, de acuerdo con las normas
vigentes en cada Estado Parte.
Art. 23 - A consideración de cada Estado Parte importador, por razones
de identificación y trazabilidad de los embriones producidos in vitro a
partir de la colecta de ovocitos de hembras en mataderos, tal
importación podrá no ser autorizada.
ANEXO II
MODELO DE CERTIFICADO VETERINARIO INTERNACIONAL PARA LA EXPORTACIÓN DE EMBRIONES DE BOVINOS Y BUBALINOS COLECTADOS IN VIVO Y/O PRODUCIDOS IN VITRO A LOS ESTADOS PARTES
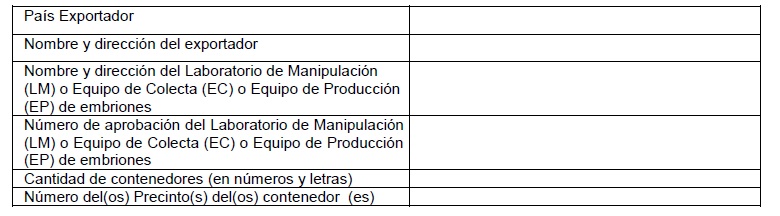
I. PROCEDENCIA:
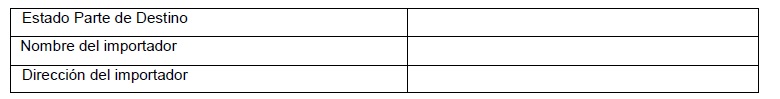
II. DESTINO:
III. TRANSPORTE
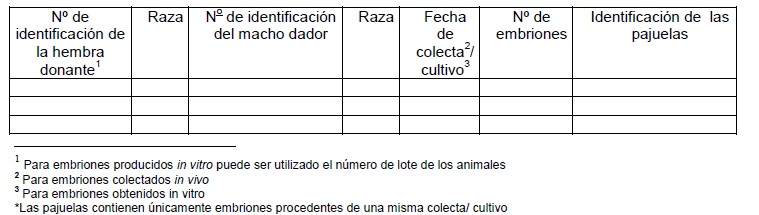
IV. INFORMACIONES REFERENTES A LOS EMBRIONES DE CADA DONANTE:
V. INFORMACIONES ZOOSANITARIAS
El Veterinario Oficial abajo firmante certifica que:
1. Con relación a Pleuroneumonía Contagiosa Bovina, durante el período
de colecta y producción de los embriones (tachar lo que no corresponda)
1.1 el país exportador es reconocido como libre de la enfermedad por la OIE o
1.2 el país exportador se declara libre, de acuerdo con lo establecido
en el Código Terrestre de la OIE, y esa condición es reconocida por el
Estado Parte importador;
2. Con relación a Dermatosis Nodular Contagiosa (tachar lo que no corresponda)
2.1. el país o zona del país exportador cumple con lo establecido en el
Código Terrestre de la OIE para ser considerado como libre de la
enfermedad y esa condición es reconocida por el Estado Parte importador,
o
2.2 las hembras donantes:
2.2.1. no manifestaron ningún signo clínico de la enfermedad el día de la colecta o producción de
los embriones ni durante los veintiocho (28) días posteriores, y
2.2.2 permanecieron en establecimiento(s) en el(los) que no fue registrado ningún caso de la
enfermedad durante los sesenta (60) días anteriores a la colecta o producción de los embriones, y
2.2.3. una de las siguientes opciones:
2.2.3.1 fueron vacunadas regularmente contra la enfermedad de acuerdo con las recomendaciones del fabricante de la vacuna,
o
2.2.3.2 resultaron negativas a dos (2) pruebas serológicas para la
detección de anticuerpos específicos contra el virus de la dermatosis
nodular contagiosa realizadas el día de la colecta y veintiún (21) días
después de la misma,
o
2.2.3.3 resultaron negativas en una prueba PCR de identificación del
agente en una muestra de sangre tomada el día de la colecta;
3.
Con respecto a Fiebre del Valle del Rift: (tachar lo que no corresponda)
3.1 El país o zona del país exportador cumple con lo establecido en el
CódigoTerrestre de la OIE para ser considerado(a) libre de Fiebre del
Valle del Rift y esa condición es reconocida por el Estado Parte
importador,
o
3.2 En caso de embriones colectados in vivo, las hembras donantes:
3.2.1. no manifestaron ningún signo de fiebre del valle del Rift
durante los 14 (catorce) días anteriores y los 14 (catorce) días
posteriores a la colecta de los embriones,
3.2.2 fueron sometidas a una prueba de ELISA o virus neutralización,
por lo menos 14 (catorce) días después de la última colecta, con
resultados negativos
4. Con respecto a Tuberculosis: (tachar lo que no corresponda) 4.1 las donantes proceden de rebaños libres de la enfermedad, o
4.2 presentaron resultado negativo a una prueba diagnóstica de
tuberculinización intradérmica con tuberculina PPD bovina o con PPD
bovina y aviar, realizada durante el período de 30 (treinta) días
previos a la primera colecta.
5. El equipo de colecta de embriones in vivo (EC), el equipo de
producción de embriones in vitro (EP) y el laboratorio de manipulación
de embriones (LM) fijos o móviles, están aprobados y supervisados por
la Autoridad Veterinaria del país exportador.
6. El LM no están localizado o los EC y EP no actuaron en zonas con
restricciones sanitarias relativas a las enfermedades de bovinos y
bubalinos, cuya transmisión pueda ocurrir por medio de los embriones.
7. Las donantes permanecieron en el rebaño de origen por un período
mínimo de treinta (30) días anteriores a la colecta de los embriones.
En ese período, así como en los treinta (30) días posteriores a la
colecta, en dicho rebaño no fue reportado oficialmente ningún caso de
Diarrea viral bovina y las referidas donantes no presentaron ningún
signo clínico de enfermedades pasibles de ser transmitidas por
embriones.
7.1. En caso de embriones producidos in vitro: los animales donantes no
proceden de establecimientos que sean objeto de restricciones en
relación con la fiebre aftosa ni peste de pequeños rumiantes, y no fue
extraído ningún tejido ni fueron aspirados ovocitos en una zona
infectada o que fue objeto de restricciones veterinarias en relación
con las citadas enfermedades. (tachar en caso que no corresponda)
8. En el caso de donantes importadas, éstas son procedentes de países
libres de Pleuroneumonía Contagiosa Bovina y permanecieron al menos
sesenta (60) días previos a la colecta en el país exportador de los
embriones.
9. El semen utilizado para la producción de los embriones a ser
exportados fue ^btenidQ..en un Centro de Colecta y Procesamiento de
Semen (CCPS) aprobado por la Autoridad VeteANEax° l ^ís de origen del
semen, cumpliendo con las "Condiciones generales de higiene en los
centros de toma y tratamiento de semen", y las descriptas en el
Capítulo referente a "Toma y tratamiento de semen de bovinos, de
pequeños rumiantes y de verracos" del Código Terrestre de la OIE.
10. Los embriones fueron colectados, procesados y almacenados de
acuerdo con las recomendaciones establecidas en el Código Terrestre de
la OIE y en el Manual de la Sociedad Internacional de Transferencia de
Embriones (IETS). En todos los casos, fue utilizado el protocolo que
incluye los lavados suplementarios con tripsina, contemplado en dicho
Manual.
10.1. Después de los lavados, la zona pelúcida de cada embrión fue
examinada en su superficie, usando microscopio con aumento no menor que
50X, encontrándose intacta y libre de material adherente.
11. Todo equipamiento utilizado para colectar, producir, manipular,
lavar, congelar y almacenar los embriones fue esterilizado antes del
uso, de acuerdo con las recomendaciones del Manual de la IETS.
12. Todos los productos biológicos de origen animal utilizados en la
colecta, producción, procesamiento y almacenamiento de los embriones
están libres de microorganismos. Solamente fue utilizado suero fetal
bovino, albúmina sérica o cualquier otro producto de origen de
rumiantes procedente de países reconocidos por la OIE como de riesgo
insignificante o de riesgo controlado y sin registro de casos, en
relación a Encefalopatía Espongiforme Bovina.
13. Los embriones fueron almacenados en contenedores nuevos o lavados y
desinfectados, utilizando nitrógeno líquido de primer uso, por un
período mínimo de treinta (30) días anteriores al embarque. Durante ese
período, ningún signo clínico de enfermedades transmisibles fue
registrado, en el establecimiento donde los embriones fueron colectados
y en las hembras donantes.
14. En el momento del embarque el contenedor fue precintado bajo
supervisión de la Autoridad Veterinaria del país exportador y el número
de precinto fue registrado en el CVI.
Este CVI tiene una validez de sesenta (60) días a partir de su emisión para ingresar al Estado Parte importador.
Lugar de Emisión:.................................. Fecha:......................................
Nombre y Firma del Veterinario Oficial:......................................
Sello del Servicio Veterinario Oficial:............................................................
IF-2018-07036141 -APN-SECMA#MA