ANEXO I
REGLAMENTO PARA LA SOLICITUD DE AUTORIZACIÓN PARA LA LIBERACIÓN
EXPERIMENTAL EN CONDICIONES CONTROLADAS DE MICROORGANISMOS
GENÉTICAMENTE MODIFICADOS (MGM) CON FINES AGROINDUSTRIALES O USOS EN EL
CONTEXTO AGROPECUARIO.
CAPÍTULO 1. GENERALIDADES
1.1. AUTORIZACIÓN PREVIA.
Las personas humanas o jurídicas interesadas en realizar liberaciones
experimentales a campo, en invernáculo y/o boxes con Microorganismos
Genéticamente Modificados (MGM) deberán contar con la autorización
previa de la SECRETARÍA DE ALIMENTOS Y BIOECONOMÍA de la SECRETARÍA DE
GOBIERNO DE AGROINDUSTRIA del MINISTERIO DE PRODUCCIÓN Y TRABAJO,
conforme el procedimiento que se detalla en el presente Reglamento.
Ello, sin perjuicio de contar con otras autorizaciones emanadas de los
distintos organismos competentes en la regulación de la materia bajo
estudio.
Consecuentemente, los interesados sólo podrán proceder a la liberación
al agroecosistema de los materiales una vez que se haya notificado en
forma fehaciente al Solicitante de la pertinente autorización otorgada
por la citada Secretaria.
1.2. FORMA DE SOLICITAR LA AUTORIZACIÓN.
1.2.1. De tratarse de MGM para uso en animales, la documentación deberá
ser remitida a las oficinas de la Dirección General de Laboratorios y
Control Técnico, dependiente del SERVICIO NACIONAL DE SANIDAD y CALIDAD
AGROALIMENTARIA, en adelante SENASA, con domicilio en la calle
Talcahuano N° 1.660, localidad de Martínez, Código Postal N° 1.640,
provincia de BUENOS ARES.
1.2.2. De tratarse de MGM para uso en vegetales u otros no incluidos en
el punto anterior, la documentación deberá ser remitida a las oficinas
de la Coordinación de Bioseguridad Agroambiental que depende de la
Dirección Nacional de Protección Vegetal del SENASA, con domicilio en
Avenida Paseo Colón N° 315, 4° Piso, Código Postal C1063ACD, CIUDAD
AUTÓNOMA DE BUENOS AIRES.
1.2.3. En los casos contemplados en los puntos 1.2.1 y 1.2.2, el SENASA
incluirá en el expediente las actuaciones que correspondan a su
competencia. Con ello, remitirá el expediente a la Dirección de
Biotecnología de la SECRETARÍA DE ALIMENTOS Y BIOECONOMÍA de la
mencionada Secretaría de Gobierno, la que arbitrará los medios para que
la COMISIÓN NACIONAL ASESORA DE BIOTECNOLOGÍA AGROPECUARIA (CONABIA)
realice la evaluación pertinente. En los casos en que corresponda, se
dará asimismo intervención al COMITÉ ASESOR EN BIOINSUMOS DE USO
AGROPECUARIO (CABUA).
1.3. Obligaciones Emergentes de la Autorización. La autorización y las
obligaciones emergentes de la misma respecto del Solicitante comprenden
todas las etapas involucradas en la conducción de las actividades
experimentales, esto es, el manejo bioseguro de los materiales de la
solicitud desde el ingreso a la REPÚBLICA ARGENTINA (si corresponde),
durante la actividad que se realice y hasta la disposición final.
Asimismo, comprende el monitoreo posterior del sitio de la liberación
utilizado por el período que se determine en la respectiva
autorización. Estas obligaciones se extienden a los empleados,
dependientes, agentes y/o colaboradores del Solicitante, no pudiendo
éste último eximirse de responsabilidad invocando las acciones de
aquellos.
1.3.1 Inspecciones. El Solicitante y sus dependientes se encuentran
obligados a permitir el acceso de los Inspectores habilitados al lugar
donde se realizará la liberación experimental con el MGM en cualquier
momento y a simple requerimiento de ingreso. 1.3.2. Asimismo el
Solicitante deberá comunicar al SENASA y a la mencionada Dirección con
una anticipación que no podrá ser inferior a SIETE (7) días hábiles la
intención de realizar las actividades incluidas en el cronograma de
operaciones propuesto (introducción, transporte, fecha de experimentos,
entre otros) con el fin de facilitar las inspecciones. Las erogaciones
necesarias para la realización de cada una de las inspecciones estarán
a cargo del Solicitante, quién a su vez deberá cumplir previamente los
requisitos exigidos en las normativas del SENASA, aplicables al caso en
cuestión.
1.4.- Modificaciones a las autorizaciones otorgadas. Podrán solicitarse
modificaciones sobre las actividades a realizarse con el MGM. Dichas
modificaciones serán evaluadas por la mencionada Dirección, la CONABIA
y el CABUA (si corresponde).
1.5.- Finalización de la liberación. El Solicitante deberá enviar una
nota informando la interrupción o la finalización de la actividad con
el MGM para realizar las inspecciones pertinentes.
1.6.- Detección del MGM en el ambiente. El Solicitante deberá contar
con técnicas de detección y los materiales necesarios que permitan
diferenciar el MGM presentado en cada solicitud y las tendrá que
suministrar a simple requerimiento de las autoridades.
CAPÍTULO 2.- PROCEDIMIENTO
2.1.- Instancia de Consulta Previa (ICP): El propósito de la ICP es
poner a disposición de los Solicitantes un mecanismo directo de
intercambo con evaluadores el cual servirá para limitar las dudas
acerca de la información a incluir en el formulario y definir el
criterio general que se utilizará en la presentación. Se trata de una
instancia optativa, diseñada a beneficio del Solicitante, y no un
ámbito de debate, ni de fijación de criterios normativos y
consecuentemente no reemplaza a la intervención de la CONABIA y/o CABUA
en la evaluación científica. El Solicitante que opte por esta instancia
presentará ante el área competente del SENASA una nota que incluirá un
resumen ejecutivo del/los caso/s, el que será respondido por la citada
Dirección la que (luego de la consulta a la CONABIA y/o CABUA) dará
respuesta por escrito. Esta herramienta podrá utilizarse como máximo en
DOS (2) oportunidades para cada MGM. 2.2.- Los interesados presentarán
la "SOLICITUD DE LIBERACIÓN EXPERIMENTAL EN CONDICIONES CONTROLADAS DE
MICROORGANISMOS GENÉTICAMENTE MODIFICADOS (MGM) CON FINES
AGROINDUSTRIALES O USOS EN EL CONTEXTO AGROPECUARIO" contenida en el
Anexo II que, registrado con el N° IF-2018-XXXXXX, forma parte
integrante de la presente medida juntamente con toda la documentación
requerida.
2.2.1- Todas las presentaciones deberán hacerse ante el área competente
del SENASA.
2.2.2.- Junto con la documentación original, el Solicitante presentará
TRES (3) copias en papel de la solicitud y de la documentación anexada,
en idioma castellano, con todas las fojas numeradas y firmadas por el
Representante Legal o Apoderado y por el Responsable Técnico, quien
deberá poseer reconocida idoneidad profesional. En caso de designarse
más de un Responsable Técnico, los mismos actuarán indistintamente.
Asimismo, si durante la conducción de las actividades se pretendiera su
reemplazo, el Solicitante deberá informar fehacientemente dicha
circunstancia y la designación del nuevo, quien asumirá las
obligaciones emergentes del permiso en la misma extensión que el
reemplazado.
2.2.3.- Adicionalmente, el Solicitante deberá efectuar el envío
electrónico de la Solicitud y documentos conexos (bibliografía, notas
de respuesta, planos, cartas acuerdo, entre otros) de conformidad con
los requerimientos que establezca la citada Dirección.
2.2.4.- Declaración Jurada. Todas las manifestaciones efectuadas por el
Solicitante por sí o a través de sus representantes en los expedientes
iniciados peticionando permisos de liberación experimental de MGM
tendrán el carácter de Declaración Jurada, por lo que su falsedad o
inexactitud será considerado un incumplimiento conforme lo establecido
en Artículo 8° de la Resolución N° 763 de fecha 17 de agosto de 2011 de
la SECRETARIA DE AGRICULTRA, GANADERÍA Y PESCA del entonces MINISTERIO
DE AGRICULTURA, GANADERÍA Y PESCA.
2.2.5.- En los casos en que el Solicitante encomiende la ejecución de
alguna de las actividades derivadas de la concesión de la autorización
a terceras personas, o bien requiera utilizar equipamiento o lugares
pertenecientes a terceros (aquí denominado Colaborador) deberá
notificar a la citada Dirección de dicha circunstancia mediante nota
suscripta por ambas partes en la cual constará la individualización del
Colaborador, la actividad a realizar, el material involucrado, el
destino del mismo si correspondiere y las medidas de bioseguridad
garantizadas conforme a la actividad pretendida y deberá contar con
firma certificada de las partes. Esta circunstancia, en ningún caso,
eximirá al Solicitante de las obligaciones derivadas de la autorización
conforme lo previsto en el punto 1.3 del presente Anexo.
2.2.6.- Notificación de contingencias. El Solicitante deberá dar aviso
mediante notificación electrónica y por correo postal de todos aquellos
acontecimientos no previstos en oportunidad de la solicitud y que
puedan haber surgido durante las actividades propuestas, dentro del
plazo de SETENTA Y DOS (72) horas de ocurridas las novedades, tanto al
SENASA como a la citada Dirección.
2.2.7.- Finalización de las actividades e Informe Final. El Solicitante
deberá remitir un informe final de las actividades realizadas que
garanticen la eliminación del MGM del ambiente e incluyan los
monitoreos pos liberación. El informe final será remitido al SENASA en
un plazo no mayor a NOVENTA (90) días corridos posteriores a la
finalización de todas las actividades.
CAPÍTULO 3.- CONFECCIÓN DEL FORMULARIO DE SOLICITUD
3.1.- La solicitud para la liberación experimental de MGM, estará
contemplada en el Formulario que se encuentra en el citado Anexo II de
la presente medida.
Para su confección, se utilizará una tipografía diferente a la del
Formulario y deberán responderse todos los puntos, sin dejar blancos.
Los enunciados del formulario no deberán modificarse. Las páginas
deberán estar correlativamente numeradas.
3.2.- Todas las aseveraciones de tipo técnico y científico que el
Solicitante realice deberán estar acompañadas por las correspondientes
referencias bibliográficas. El material bibliográfico completo deberá
estar disponible en su idioma original. A requerimiento de la citada
Dirección, se podrá solicitar si fuera necesario, a costa del
Solicitante, la correspondiente versión traducida por traductor público
matriculado, si su idioma original fuera distinto del castellano.
3.3.- Individualización del Sitio de la Liberación. A fin de
individualizar correctamente el sitio de la liberación, el Solicitante
deberá acompañar:
3.3.1.- Título de propiedad o contrato de arrendamiento u otro
instrumento jurídico al efecto y/o Carta Compromiso suscripta por quien
declare ostentar la tenencia legal del predio, mediante el cual le
confieran al Solicitante el derecho a la explotación a título oneroso o
gratuito del establecimiento declarado para efectuar las actividades de
experimentación con el MGM, según corresponda.
3.3.1.1.- El plazo de duración del contrato de arrendamiento o
instrumento jurídico y/o Carta Compromiso a que hace alusión el punto
precedente deberá guardar relación con el plazo de las solicitudes de
liberación efectuadas, como así también de corresponder, los controles
y monitoreos posteriores a la finalización de la liberación
experimental. Asimismo, deberá contener:
a) La individualización de las partes. En caso de actuar por
Representante Legal o apoderado deberá acompañar en copia los
instrumentos legales correspondientes para justificar la personería
invocada.
b) La descripción del establecimiento donde se realizaran las
actividades incluyendo nombre del establecimiento, localidad, partido y
provincia.
c) El detalle de las condiciones de bioseguridad garantizadas, la
obligación de facilitar el acceso a los inspectores de la Autoridad de
Aplicación, las pautas de monitoreo y toda otra condición que resulte
menester contemplar en relación al tipo de autorización pretendida.
d) Si los datos mencionados precedentemente no constaren en el contrato
de arrendamiento o instrumento jurídico deberá acompañarse como
documento adicional una Carta Compromiso que los contenga.
e) La firma certificada de las partes y aclaración.
3.3.1.2.- Los datos del título de propiedad, el Contrato de
Arrendamiento o instrumento jurídico y/o la Carta Compromiso (nombre
del establecimiento, localidad, provincia, entre otros) deberán
coincidir exactamente con aquellos volcados en la solicitud
electrónica. La falta de coincidencia entre los datos consignados entre
la presentación en papel y la electrónica impedirá la tramitación de la
solicitud respectiva hasta tanto se regularice la misma mediante una
nueva presentación electrónica en concordancia con los datos de la
presentación original en papel.
3.3.2.- Cuando se tramite más de una solicitud con respecto a un mismo
establecimiento, bastará con presentar en la primera oportunidad el
ejemplar original del instrumento y en las subsiguientes, copia
debidamente certificada.
3.3.3.- Planos detallados, indicando orientación cardinal e
individualizando las vías de acceso.
3.3.4.- Indicación de los puntos de geoposicionamiento satelital (GPS)
de los vértices que contengan la totalidad de la superficie del
establecimiento, relevados utilizando la referencia del Datum WGS84 y
expresados en grados y SEIS (6) decimales de grado. Asimismo deberán
declararse las coordenadas geográficas del acceso al establecimiento.
3.3.5.- Indicación de los puntos de geoposicionamiento satelital (GPS)
de los vértices que contengan la totalidad de la superficie de todos
los posibles sitios de liberación, relevados utilizando la referencia
del Datum WGS84 y expresados en grados y SEIS (6) decimales de grado.
3.4.- Protocolos Especiales.
Para aquellas actividades que impliquen desafío, ya sea por infección o
infestación, con patógenos o plagas, el Solicitante deberá adjuntar un
protocolo especial correspondiente a éstas, consignando todos los datos
(nombre o razón social, domicilio, información de contacto) del
profesional a cargo de las mismas, debiendo incluirse además la
procedencia de los organismos a utilizar y la autorización de los
organismos de control competentes.
3.5.- Información Confidencial. Si el Solicitante desea que algunos de
los datos requeridos en la Solicitud sean gestionados de manera
confidencial, deberá indicarlo mediante la colocación de la sigla ICE
(Información Confidencial Eliminada) en el frente de la solicitud
destinada a iniciar el expediente, y en el cuerpo del texto, en cada
lugar en el cual dichos datos fueron omitidos.
3.5.1.- Cuando la Solicitud contenga ICE, el Solicitante deberá remitir
al área competente del SENASA en sobre lacrado y firmado, una solicitud
completa que incluya en tipografía resaltada la información que desea
mantener confidencial (Información Confidencial, en adelante IC). Este
documento deberá presentar en el margen superior derecho de cada una de
sus páginas la inscripción "Copia con IC". La información bibliográfica
completa, que haya sido considerada como confidencial, deberá ser
remitida en formato digital junto con el resto de la IC y en formato
texto.
3.5.2.- No podrán considerarse como IC las siguientes informaciones:
a) Denominación del MGM.
b) Características fenotípicas introducidas en el MGM.
c) Nombre y dirección del Solicitante, del Representante Legal o
Apoderado y del Responsable Técnico.
d) Propósito de la autorización solicitada.
e) Lugar de la liberación.
f) Métodos y planes para controlar el MGM.
g) Acciones a realizar en caso de emergencia.
h) Disposición final del material biológico.
i) Toda información que sea necesaria para la evaluación de la
bioseguridad a ser considerada por la CONABIA y/o CABUA y la mencionada
Dirección.
3.5.3.- Será responsabilidad del área competente del SENASA resguardar
la IC de acuerdo a las normas vigentes.
3.5.4.- Toda información que fuera revelada en cualquier instancia de
la evaluación ya no podrá ser incluida como parte de la IC. Tampoco
podrá ser IC toda información que ya estuviera en conocimiento
irrestricto (no confidencial) de cualquier otra autoridad regulatoria.
3.5.5.- Ni los miembros de la CONABIA o CABUA, ni los expertos que
pudieren ser consultados podrán revelar a terceros la información y/o
documentación a la que tengan acceso en el marco de sus funciones, ni
utilizarla en beneficio propio.
3.5.6.- La citada Dirección suministrará una nómina de expertos que
estarán habilitados para examinar dicha IC, los que de ser aceptados
por la CONABIA y/o CABUA podrán evaluar dicha información. El
Solicitante dará conformidad mediante nota suscripta por el
representante legal o apoderado, para la vista de la documentación,
teniendo derecho a seleccionar de la nómina presentada UN (1) evaluador
primario y DOS (2) evaluadores adicionales.
3.5.7.- En forma previa a dar conformidad para la vista de la
documentación el Solicitante también podrá proponer un experto "ad
referéndum" de su aprobación por la mencionada Dirección y por la
CONABIA y/o CABUA (si coorespode).
3.5.8.- En forma simultánea a dar conformidad para la vista de la
documentación el Solicitante podrá designar, por escrito, a la persona
que lo representará en el acto de vista de la IC. En ausencia de dicho
representante, el acto de vista se podrá realizar igual, salvo que el
Solicitante exprese su negativa por escrito.
3.5.9.- El/los evaluador/es firmará/n un compromiso de confidencialidad
previo a tomar vistas de la IC. La/s persona/s presente/s en el acto de
vista de la IC firmarán tantos ejemplares como correspondan de un mismo
tenor del acta en la que se volcará la opinión de/l los experto/s. UN
(1) ejemplar será entregado al Solicitante.
CAPÍTULO 4.- MANEJO DE LA LIBERACIÓN EXPERIMENTAL
4.1.- Fecha de inicio de la liberación experimental. Una vez notificado
fehacientemente del permiso otorgado, el Solicitante deberá informar la
fecha de inicio de las actividades en un plazo no menor a DIEZ (10)
días corridos previos a la misma. Dicha notificación deberá presentarse
por nota simultáneamente en original y DOS (2) copias en la mesa de
entrada correspondiente y a las direcciones electrónicas que
correspondan (según puntos 1.2.1 y 1.2.2).
4.2.- Restricción de Acceso. El Solicitante será responsable del
control de acceso al sitio donde se realizan las actividades vinculadas
a la liberación experimental.
4.3.- Personal. El personal a cargo del manejo de la liberación, deberá
estar técnicamente capacitado y en conocimiento del tipo de material
con el cual está trabajando.
4.4.- En todas las actividades en que intervengan MGM se aplicarán los
principios de las buenas prácticas, así como los principios
fundamentales en bioseguridad y de higiene en el lugar de trabajo. Si
procede, se dispondeán señales con riesgo biologico.
4.5.- Inspecciones. Las inspecciones serán realizadas por los agentes
del SENASA y/o los agentes habilitados por la SECRETARÍA DE ALIMENTOS Y
BIOECONOMÍA de la mencionada Secretaría de Gobierno para tal fin; y se
realizarán todas las veces que resulte necesario en forma previa a las
actividades de liberación experimental a fin de verificar la
bioseguridad del sitio, durante el desarrollo del mismo, así como
durante el período de monitoreo posterior a la conclusión del ensayo
y/o posterior a la destrucción de los materiales utilizados en la
liberación hasta la finalización de la liberación (de corresponder).
4.6.- Notificación de Desvíos. Si durante el desarrollo de las
actividades y hasta que se haya completado el período de monitoreo
posterior, el Solicitante observara alguna desviación en las
características esperadas del MGM o en las de materiales o condiciones
asociadas con la liberación, que no fueran los previstos y/o descriptos
en la Solicitud, deberá notificar esta circunstancia a la citada
Dirección, por escrito, dentro de las CUARENTA Y OCHO (48) horas de
producida tal desviación. Dicha notificación deberá presentarse por
nota simultáneamente en original y DOS (2) copias en la mesa de entrada
correspondiente y a las direcciones electrónicas que correspondan
(según puntos 1.2.1 y 1.2.2).
4.7.- Escapes. De producirse un escape del MGM, el Solicitante deberá
ejecutar el plan de contingencia declarado en la solicitud aprobada e
inmediatamente comunicarlo. Dicha notificación deberá presentarse por
nota simultáneamente en original y DOS (2) copias en la mesa de entrada
correspondiente y a las direcciones electrónicas que correspondan
(según puntos 1.2.1 y 1.2.2).
4.8.- Monitoreo durante la liberación experimental. Verificación de las
condiciones de bioseguridad y manejo de las liberaciones determinadas
en la autorización, la que será efectuada por inspectores oficiales.
4.9.- Registro de actividades. El Solicitante deberá arbitrar los
medios para que el personal abocado a las actividades con el MGM lleve
un registro documentado en cuadernos foliados de las mismas, el que
deberá ser puesto a disposición de los inspectores actuantes a simple
requerimiento.
4.10.- Fecha estimada de finalización de las actividades de liberación
experimental. El Solicitante deberá indicar la fecha estimada de
finalización de las actividades incluidas aquellas de eliminación del
MGM y monitoreo posteriores a las mismas.
IF-2018-46274670-APN-DBT#MA
ANEXO II
FORMULARIO DE SOLICITUD DE AUTORIZACIÓN PARA LA LIBERACIÓN EXPERIMENTAL
EN CONDICIONES CONTROLADAS DE MICROORGANISMOS GENÉTICAMENTE MODIFICADOS
(MGM) CON FINES AGROINDUSTRIALES O USOS EN EL CONTEXTO AGROPECUARIO
Completar solamente los puntos o ítems finalizados en DOS (2) puntos
(:)
1. Solicitante Nombre:
Domicilio real/legal:
Domicilio constituido en la CIUDAD AUTÓNOMA DE BUENOS AIRES: Teléfono:
Correo electrónico:
1.1 Responsable Legal/Apoderado
Nombre:
Tipo y número de documento:
Domicilio legal:
Teléfono:
Correo electrónico:
1.2 Responsable Técnico Nombre:
Tipo y número de documento:
Profesión:
Cargo:
Cargo en la entidad:
Domicilio:
Teléfono:
Correo electrónico:
2. Datos de la institución que desarrolló y/o proveyó el Microorganismo
Genéticamente Modificado (MGM).
Nombre:
Dirección:
Teléfono:
Correo electrónico:
3. Datos de la/s persona/s que desarrolla/ron y/o proveyeron los MGM.
Nombre:
Profesión:
Cargo:
Dirección:
Teléfono:
Correo electrónico:
Entidad:
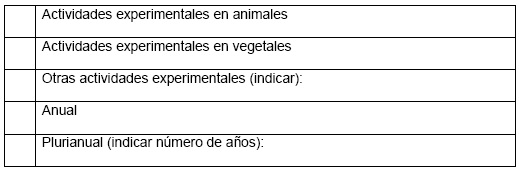
4. Tipo de autorización solicitada (marcar lo que corresponda con una
X):
5. MGM objeto de la presente solicitud
5.1. Nombre científico:
5.2. Cepa (si corresponde):
5.3. Método utilizado para la identificación:
5.4. Denominación asignada por el solicitante:
6. Procedencia del MGM o del material que lo contiene.
6.1 Nacional:
6.2 Importado:
7. Objetivo/s de la liberación experimental del MGM motivo de la
presente solicitud:
8. Características descriptivas generales del microorganismo receptor o
nativo.
8.1. Ciclo de vida y características bioquímicas y/o moleculares
generales:
8.2. Género, especie y denominación de la cepa, en el caso que
corresponda del microorganismo receptor o nativo:
8.3. Procedencia del microorganismo receptor:
8.4. Incluir grado de parentesco (filogenia) entre el/los organismo/s
donante/s y el microorganismo receptor del nuevo material genético en
caso que corresponda:
8.5 Nivel de bioseguridad utilizado en su manipulación:
9. Información sobre el/los organismos donantes, la/s secuencias
modificadas y la/s funciones codificadas.
9.1 Breve descripción de los organismos donantes:
9.2 Descripción detallada de la biología molecular del sistema que ha
sido utilizado en la obtención del MGM sujeto a control:
En este ítem deben identificarse los vectores e incluirse un mapa de
los vectores (en caso de haberse utilizado dicho sistema). También
habrán de describirse las características del/los vectores, tales como
genes marcadores, promotores, secuencias no codificantes y/o
regulatorias, intrones, entre otros:
9.3 Caracterización molecular de la/s secuencia/s modificada/s. Remitir
secuencia nucleotídica completa de la/s secuencia/s modificada/s.
Indicar si la/s secuencia/s declarada/s corresponde/n a información
obtenida de bases de datos públicas o si fueron obtenida por
secuenciación del MGM:
9.4 Descripción de la/s proteína/s expresada/s u otros productos (por
ejemplo, ARNs) que confieren el nuevo fenotipo:
9.5 Descripción acerca del/los mecanismos de acción del/los productos
expresados en el MGM que confieren el nuevo fenotipo:
10. Información disponible de las características del MGM.
10.1. Detalle del fenotipo en relación a la/s modificación/es
introducida/s (estén éstas relacionadas o no con el objetivo de la
liberación):
10.2. Presencia de vectores moleculares (plásmidos, profagos, otros),
especificidad de los mismos, frecuencia de movilización y número de
copias: 10.3 Presencia de secuencias de genomas virales u otros agentes
adventicios. Especificidad de los mismos, frecuencia de movilización:
10.4. Presencia de elementos genéticos móviles (transposones,
retrotransposones, helitrones, otros):
10.5. Estabilidad de la modificación genética introducida (de
corresponder con y sin presión de selección):
10.6 Protocolos usados para la detección, indicando la sensibilidad y
especificidad de éstos para el MGM:
10.7. Metodología y procedimientos utilizados para la producción,
amplificación y/o escalado:
10.8. Mecanismos de transmisión y diseminación del MGM:
10.9. Forma de resistencia y persistencia en el ambiente:
10.10. Forma de resistencia y persistencia en el huésped donde será
utilizado (si corresponde):
10.11. Indicar si posee resistencia a antibióticos y señalar el
espectro de acción:
10.12. Inocuidad del MGM y de sus productos derivados para humanos,
animales y vegetales (incluir referencias y/o estudios realizados
disponibles
en cuanto a la toxicidad, infectividad, patogenicidad y/o
alergenicidad del MGM o de los nuevos productos de expresión
incorporados):
10.13. Capacidad del MGM de producir cambios en los procesos
biogeoquímicos (si corresponde):
10.14. Capacidad de colonización de aire, suelo y agua:
10.15. Interacciones ecológicas del MGM con otras especies (sear
patógenos, predadores, simbiontes, parásitos, competidores y/o
huéspedes): 10:16. Formulación o composición del preparado en la que
estará incluido e MGM:
10.17. Ausencia de agentes adventicios en las formulaciones o
preparaciones a ensayar:
11. Información sobre la liberación experimental.
11.1. Antecedentes sobre otras liberaciones realizadas, tanto en le
REPÚBLICA ARGENTINA como en el extranjero.
11.1.1. Antecedentes de liberación en la REPÚBLICA ARGENTINA. Indicar
números de expedientes de autorizaciones anteriores:
11.1.2. Autorizaciones previas en otros países:
11.2. Detalle de/l los protocolo/s y diseño experimental:
11.3. Cronograma de actividades.
- Fecha estimada y descripción de toda actividad a efectuar durante el
desarrollo de la liberación (descripción de cada una):
- Fecha estimada y descripción de todas las actividades a realizar a
fin de cumplir con las condiciones especificadas en la autorización y
con el objetivo solicitado:
- Fecha estimada de disposición final de todos los materiales
involucrados en la liberación:
11.4. Cantidad de material a liberar, metodología y unidades de
cuantificación:
11.5. Indicación sobre cómo será etiquetado y/o se realizará su
trazabilidad durante la liberación experimental y/o trasporte de ser
este necesario:
11.6. Detalle de las condiciones de aislamiento y bioseguridad
incluidas en el diseño experimental y durante todo el desarrollo de las
actividades de liberación experimental:
11.7. Descripción de las metodologías, protocolos de muestreo y
frecuencia de monitoreo del MGM durante las actividades de liberación.
En el caso de realizarse liberaciones experimentales a campo, indicar
monitoreos de la flora, fauna y/o microorganismos de la filosfera,
rizosfera, rizoplano, raíz y suelo adyacente y aguas superficiales y
subterráneas):
11.8. Los métodos propuestos para el control de potenciales vectores de
transmisión del MGM y/o su material genético recombinante:
11.9. Descripción detallada de los métodos y procedimientos de
eliminación y/o inactivación del MGM, de posibles contaminantes
adventicios asociados al material que lo contiene y demás materiales
usados en las actividades de liberación experimental incluyendo:
tratamiento de las herramientas y equipos, información sobre la gestión
de residuos comunes o patogénicos y el
destino que se dará al material inactivado desechado que contenga el
MGM. De corresponder, incluir contrato con empresa de tratamiento de
residuos:
11.10. Descripción detallada del destino final propuesto de los
animales o vegetales o subproductos derivados y/o cualquier otro
material biológico que forma parte de las actividades propuestas:
11.11. Indicar lugar de guarda del material si corresponde, condiciones
de bioseguridad y destino final en caso que no se lleven a cabo las
actividades propuestas:
11.12. Alcance geográfico del área de monitoreo y/o control de
inactivación o eliminación del MGM, si corresponde:
11.13. Descripción de las metodologías, protocolos de muestreo y
frecuencia de monitoreo y efectividad de los tratamientos de
inactivación y/o eliminación del MGM posterior a las actividades
propuestas tanto en el área de liberación como las áreas circundantes:
11.14. Ante la eventualidad de un escape durante las actividades de
liberación experimental describir los procedimientos y el plan de
contingencia, control y monitoreo a aplicar:
12. Descripción detallada del lugar de liberación experimental y el
área circundante:
12.1. Indicar nombre del establecimiento:
12.2. Describir las características del lugar/área donde se realizará
la liberación experimental del MGM, invernáculo y/o boxes y/o campo que
garanticen las condiciones de bioseguridad. Adjuntar plano de las
instalaciones:
12.3. Remitir plano general con ubicación del establecimiento y escala
del mismo:
12.4. Indicar coordenadas geográficas del sitio donde se realizarán las
actividades y su ubicación exacta en un mapa:
12.5. Remitir croquis del establecimiento y sitio de liberación en
escala UNO EN DOS MIL (1:2000):
12.6. Indicar descripción del área de liberación experimental y
circundante en cuanto a flora y fauna, animales de uso pecuario,
accidentes geográficos, asentamientos poblacionales, vías de
ferrocarril, rutas, cursos de agua, clima, características edafológicas
y topográficas:
12.7. Indicar distancia a caminos más cercanos, a lugares muy
transitados y a los límites del campo de cada sitio de liberación:
12.8. Indicar normas de control de acceso:
13. Detalle de las condiciones de bioseguridad utilizadas en el
transporte del MGM y el material conteniéndolo o asociado al mismo
tanto previo, como durante o posterior a la liberación indicando
motivos de tales traslados e incluyendo contratos con empresas
transportistas; tanto para materiales desarrollados localmente como
materiales introducidos en el país:
14. Citar la bibliografía referenciada en el texto, conforme lo
indicado en el punto 3.2 del Anexo I:
IF-2018-46274834-APN-DBT#MA