SECRETARÍA DE REGULACIÓN Y GESTIÓN SANITARIA
Y
SECRETARÍA DE ALIMENTOS Y BIOECONOMÍA
Resolución Conjunta 4/2018
RESFC-2018-4-APN-SRYGS#MSYDS
Ciudad de Buenos Aires, 23/10/2018
VISTO el Expediente Nº 1-0047-2110-007121-17-0 del Registro de la
ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA;
y
CONSIDERANDO:
Que el Instituto Nacional de Alimentos (INAL) dependiente de la
ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
(ANMAT), detectó la necesidad de realizar una revisión del listado de
aditivos contemplados en el Artículo 1.398 del Código Alimentario
Argentino (CAA), y en consecuencia actualizar sus respectivas
especificaciones, utilizando criterios elaborados y/o adoptados por
organismos especializados de reconocimiento internacional, como el
Comité Mixto FAO/OMS de Expertos en Aditivos Alimentarios (JECFA) y
Food Chemicals Codex (FCC).
Que la Comisión Nacional de Alimentos (CONAL) acordó conformar un Grupo de Trabajo Ad-Hoc para trabajar al respecto.
Que el mencionado Grupo de Trabajo elaboró una propuesta de
actualización del CAA de aquellas sustancias que se encuentran
contempladas actualmente en el Capítulo XVIII del referido Código pero
que no son aditivos.
Que del análisis del listado de sustancias contempladas en el Artículo
1.398 del CAA, el mencionado Grupo de Trabajo sugiere derogar los
siguientes ítems: 1. Aceites Vegetales Bromados; 23.1. Almidones
Modificados; 38. Cafeína; 52.1.1. L-Carnitina; 52.1.2. Carnitina
(Clorhidrato); 58. Clorotetraciclina (Clorhidrato); 61. Difenilo; 63.
Esperma de Ballena; 66.0. Fructosa; 83.1. Hierro Electrolítico; 83.3.1.
Hierro (II) Fumarato; 83.4. Hierro (III) Pirofosfato; 83.5. Hierro (II)
Lactato; 83.5. Glicinato Férrico; 83.5.1. Glicinato Ferroso; 83.6.
Hierro (II) Sulfato; 86.2.1. Monoclorhidrato de l-Lisina; 96.1
Metionina; 103. Oxitetraciclina (Clorhidrato); 112. POTASIO BROMATO:
Bromato de potasio; y 162.0. Taurina.
Que la eliminación de los Aceites Vegetales Bromados del listado de
aditivos contemplados en el precitado Artículo 1.398 surge debido a que
actualmente se encuentran prohibidos en la UNIÓN EUROPEA, en el ESTADO
DE JAPÓN y en la REPÚBLICA DE LA INDIA; y que los ESTADOS UNIDOS DE
AMÉRICA los mantiene en la lista de aditivos bajo estudio.
Que la eliminación de los conservantes Clorotetraciclina y Clorhidrato
de Oxitetraciclina, se debe a que estudios han demostrado que la
utilización de los antibióticos mencionados, puede provocar la
aparición de cepas antibiótico-resistentes con efectos perjudiciales
para la salud.
Que por otra parte, la ORGANIZACIÓN DE LAS NACIONES UNIDAS PARA LA
ALIMENTACIÓN Y LA AGRICULTURA (FAO), LA ORGANIZACIÓN MUNDIAL DE LA
SALUD (OMS) y la ORGANIZACIÓN MUNDIAL DE SANIDAD ANIMAL (OIE) han
planteado la cuestión del uso irresponsable de antibióticos en todos
los sectores de la producción, con especial referencia a los riesgos
potenciales para la salud pública.
Que actualmente el uso de Bromato de Potasio no está permitido debido a
que la Resolución Nº 3 de fecha 11 de enero de 1995 del ex- MINISTERIO
DE SALUD Y ACCIÓN SOCIAL que incorporó al CAA la Resolución Nº 73 de
fecha 7 de julio de 1993del Grupo Mercado Común (GMC) del MERCADO COMÚN
DEL SUR (MERCOSUR), estableció el retiro de Bromato de Potasio de la
Lista General Armonizada de Aditivos del Mercosur.
Que con respecto al fungistático Difenilo, en la actualidad no se reportan datos de uso.
Que la Farmacopea Argentina eliminó de la lista de activos el Esperma
de Ballena y además actualmente sólo se utiliza en cosmética.
Que las especificaciones de los Almidones Modificados se encuentran
detalladas en el Artículo 3° de la Resolución Nº 106 de fecha 15 de
octubre de 1994 del GMC, incorporada al CAA mediante la Resolución N°
184 de fecha 30 de mayo de 1995 del entonces MINISTERIO DE SALUD Y
ACCIÓN SOCIAL, en el Capítulo IX, Alimentos Farináceos - Cereales,
Harinas y Derivados.
Que por otro parte, resulta necesario reubicar ciertos ingredientes que
se encuentran contemplados en el Artículo 1.398 del precitado Código
pero que dada su función no corresponde que sean considerados aditivos.
Que la Cafeína se utiliza como ingrediente en la elaboración de “Bebida
analcohólica con cafeína y taurina”; por lo que sus especificaciones de
identidad y pureza deberían contemplarse dentro del Artículo 1.388 del
CAA.
Que el Monoclorhidrato de l-Lisina y la Metionina solo se utilizan para
la elaboración de “alimentos fortificados con aminoácidos esenciales”
contemplados en el Artículo 1.367 del referido Código, por lo que sus
especificaciones deberían contemplarse dentro de dicho artículo.
Que la Fructosa es un azúcar, por lo que sus especificaciones deberían
contemplarse dentro del Capítulo X - Alimentos Azucarados.
Que la L-Carnitina y la Carnitina (Clorhidrato) se utilizan como
ingredientes para suplementos dietarios, fórmulas infantiles y
alimentos para propósitos médicos; por lo tanto, sus especificaciones
de identidad y pureza deberían incorporarse dentro de Capítulo XXII –
Misceláneos, junto a sus respectivas especificaciones de uso.
Que el Hierro Electrolítico; el Hierro (II) Fumarato; el Hierro (III)
Pirofosfato; el Hierro (II) Lactato; el Glicinato Férrico; el Glicinato
Ferroso; y el Hierro (II) Sulfato, se utilizan como ingrediente en
suplementos dietarios y alimentos fortificados; por lo que, sus
especificaciones de identidad y pureza deberían incorporarse dentro de
Capítulo XXII – Misceláneos junto con sus respectivas usos.
Que el Alcohol Etílico, alcohol, etanol, contemplado en el ítem 21.2
del Artículo 1.398 del CAA corresponde sólo al alcohol etílico de
síntesis química que se utiliza como vehículo para aromatizantes y
aditivos; sus especificaciones de identidad y pureza deberían
mantenerse dentro del Artículo 1.398 del mencionado Código
especificando su forma de obtención.
Que la Taurina se utiliza tanto para la elaboración de bebidas
analcohólicas con cafeína y taurina como para fórmulas y alimentos para
propósitos médicos específicos; sus especificaciones de identidad y
pureza deberían incorporarse dentro de Capítulo XXII – Misceláneos con
sus respectivas restricciones de uso.
Que el CONSEJO ASESOR DE LA COMISIÓN NACIONAL DE ALIMENTOS (CONASE) ha
tomado la intervención de su competencia y se sometió a la Consulta
Pública.
Que la precitada Comisión Nacional ha intervenido expidiéndose favorablemente.
Que los Servicios Jurídicos Permanentes de los organismos involucrados han tomado la intervención de su competencia.
Que se actúa en virtud de las facultades conferidas por los Decretos Nº
815 de fecha 26 de julio de 1999 , Nº 174 de fecha 2 de marzo de 2018,
sus modificatorios y complementarios, y Nº 802 de fecha5 de septiembre
de 2018.
Por ello,
LA SECRETARIA DE REGULACIÓN Y GESTIÓN SANITARIA
Y
EL SECRETARIO DE ALIMENTOS Y BIOECONOMÍA
RESUELVEN:
ARTÍCULO 1°.- Deróguese del Artículo 1.398 del Código Alimentario Argentino (CAA) los siguientes ítems:
“1. Aceites Vegetales Bromados
23.1. Almidones Modificados
38. Cafeína
52.1.1. L-Carnitina
52.1.2. Carnitina (Clorhidrato)
58. Clorotetraciclina (Clorhidrato)
61. Difenilo
63. Esperma de Ballena
66.0. Fructosa
83.1. Hierro Electrolítico
83.3.1. Hierro (II) Fumarato
83.4. Hierro (III) Pirofosfato
83.5. Hierro (II) Lactato
83.5. Glicinato Férrico
83.5.1. Glicinato Ferroso
83.6. Hierro (II) Sulfato
86.2.1. Monoclorhidrato de l-Lisina
96.1. Metionina
103. Oxitetraciclina (Clorhidrato)
112. POTASIO BROMATO: Bromato de potasio
162.0. Taurina”
ARTÍCULO 2°. - Sustitúyese del Artículo 1.398 del Código Alimentario
Argentino, el ítem 21.2. Alcohol Etílico: Alcohol, etanol, el que
quedará redactado de la siguiente manera: “Artículo 1398:
21.2. Alcohol Etílico de síntesis química: Alcohol, etanol
Fórmula empírica: C2H6O
Peso molecular: 46,07
Descripción:
Líquido móvil, límpido e incoloro, olor suave característico y sabor ardiente, inflamable.
Usos: Vehículo para aromatizantes y aditivos.
Especificaciones de identificación y pureza según lo establecido en JECFA, FCC, FA, USP y otras Farmacopeas.”
ARTÍCULO 3°. - Sustitúyese el Artículo 1.367 del CAA, el que quedará
redactado de la siguiente manera: “Artículo 1.367: Los alimentos
fortificados con aminoácidos esenciales deberán responder a las
siguientes exigencias: a) Sólo podrán ser empleados los siguientes
aminoácidos esenciales que deberán responder a las especificaciones de
identificación y pureza según lo establecido en FCC:
DL-metionina FCC
L-cistina FCC
L-creonina FCC
L-fenilalanina FCC
L-histidina FCC
L-isoleucina FCC
L-leucina FCC
L-lisina monoclorhidrato FCC
L-metionina FCC
L-tirosina FCC
L-triptofano FCC
L-valina FCC
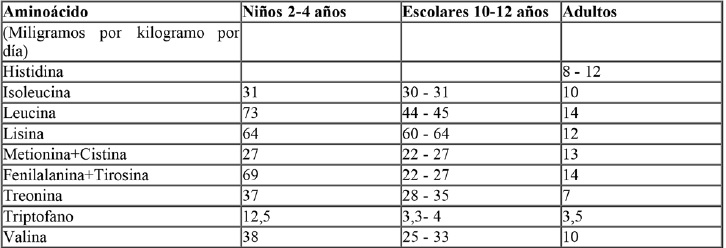
TABLA: REQUERIMIENTOS ESTIMADOS DE AMINOÁCIDOS A DIFERENTES
EDADES FAO/WHO/UNU. Serie de Informes Técnicos Nº 724 (1985) Pág 65.
b) Las cantidades agregadas no deben hacer superior 100, el índice
químico de la fracción proteica de los alimentos fortificados en
proteínas y/o aminoácidos. El índice químico de una proteína es el
resultado obtenido al multiplicar por 100 el cociente más pequeño
obtenido al dividir la cantidad de cada uno de los aminoácidos
esenciales o grupo de aminoácidos esenciales presente en 100 g de esa
proteína, por la correspondiente cantidad presente en 100 g de la
proteína de referencia. La proteína de referencia se caracteriza por
los tenores siguientes, referidos a 100 g (FAO/OMS/UNU. Serie de
Informes Técnicos Nº 724 (1985) Pág. 121):

El valor biológico de las proteínas del alimento fortificado con
aminoácidos no será menor del 60% y su digestibilidad verdadera no será
menor del 80%. Los alimentos se rotularán con la denominación del
producto de que se trata seguido de la indicación “Fortificado con
Aminoácidos Esenciales”. Deberán consignar todos los requisitos de
rotulación insertos en el Artículo 1.345 y listado cuali-cuantitativo
de los aminoácidos agregados”.
ARTÍCULO 4°.- Sustitúyese el Artículo 1.388 del CAA el que quedará
redactado de la siguiente manera: “Artículo 1.388: Se entiende por
“Bebida analcohólica con cafeína y taurina” a aquella bebida no
alcohólica gasificada o no que contenga en su composición cafeína y
taurina, asociadas o no con glucuronolactona y/o inositol, con los
valores máximos que se detallan a continuación:
Taurina: 400 mg/100 ml
Glucuronolactona: 250 mg/100 ml
Cafeína: 32 mg/100 ml
Inositol: 20 mg/100 ml
Los que deberán responder a las especificaciones de identificación y
pureza según lo establecido en FCC, FNA y USP y otras Farmacopeas.
Podrá contener además hidratos de carbono, vitaminas, minerales y/o
aminoácidos, y los otros ingredientes autorizados para bebidas
analcohólicas por el presente Código. Este producto se rotulará con la
denominación de venta
“Bebida analcohólica con cafeína y taurina”. El rótulo deberá cumplir
con las exigencias generales obligatorias establecidas en el presente
Código para alimentos envasados y con la siguiente información
obligatoria específica:
- El contenido en mg/100 ml de: taurina, glucuronolactona, cafeína e inositol en el listado de ingredientes.
- Los componentes cafeína, taurina, glucuronolactona, inositol y
cualquier otro nutriente presente en el producto expresados en g, mg o
µg según corresponda por porción establecida, en la Información
Nutricional Obligatoria.
Deberá consignar además las siguientes leyendas obligatorias:
• “No consumir en caso de embarazo, lactancia, niños y personas de edad avanzada”.
• “Se sugiere no consumir con alcohol”.
• “Alto contenido de cafeína” cuando ésta supere los 20 mg/ 100 ml. La
publicidad de estas bebidas deberá cumplir con las exigencias
establecidas en el presente Código, además de las siguientes
restricciones, cualquiera sea el medio de difusión que se utilice: a)
No deben ser asociadas directa o indirectamente al consumo con bebidas
alcohólicas. b) No deben presentarse como productores de bienestar o
salud. c) Su consumo no debe vincularse con ideas o imágenes de mayor
éxito en la vida afectiva y/o sexual de las personas o hacer exaltación
de prestigio social, virilidad o femineidad. d) En el mensaje no deben
participar en imágenes o sonidos, menores de DIECIOCHO (18) años de
edad.
ARTÍCULO 5°.- Incorpórase al Artículo 778 cuarto del CAA el siguiente texto: FRUCTOSA Levulosa, D-Fructosa o Azúcar de Fruta.
Fórmula empírica C6H12O6
Peso molecular: 180,16
Características: Cristales blancos o polvo cristalino higroscópico con
sabor dulce y sin olor. Soluble en metanol, etanol y agua.
Restricción del uso: Sólo para alimentos de bajo contenido glucídico.
Especificaciones de identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.”
ARTÍCULO 6º.- Incorpórase al Artículo 1.417 del CAA, el inciso 5, el que quedará redactado de la siguiente manera:
“5. L - Carnitina
Identificación y pureza según lo establecido en FCC.
Uso: como ingrediente para utilizar en suplementos dietarios, fórmulas infantiles y alimentos para propósitos médicos.”
ARTÍCULO 7º.- Incorpórase al Artículo 1.417 del CAA el inciso 6, el que quedará redactado de la siguiente manera:
“6. Carnitina (Clorhidrato)
Identificación y pureza según lo establecido en FCC.
Uso: como ingrediente para utilizar en suplementos dietarios, fórmulas infantiles y alimentos para propósitos médicos.”
ARTÍCULO 8º.- Incorpórase al Artículo 1.417 del CAA el inciso 7, el que quedará redactado de la siguiente manera:
“7. Hierro Electrolítico
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.”
ARTÍCULO 9º.- Incorpórase al Artículo 1.417 del CAA el inciso 8, el que quedará redactado de la siguiente manera:
“8. Hierro (II) Fumarato
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.”
ARTÍCULO 10.- Incorpórase al Artículo 1.417 del CAA el inciso 9, el que quedará redactado de la siguiente manera:
“9. Hierro (III) Pirofosfato
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.”
ARTÍCULO 11.- Incorpórase al Artículo 1.417 del CAA el inciso 10, el que quedará redactado de la siguiente manera:
“10. Hierro (II) Lactato
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.”
ARTÍCULO 12.- Incorpórase al Artículo 1.417 del CAA el inciso 11, el que quedará redactado de la siguiente manera:
“11. Hierro (II) Sulfato
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.”
ARTÍCULO 13.- Incorpórase al Artículo 1.417 del CAA el inciso 12, el que quedará redactado de la siguiente manera:
“12. Taurina
Identificación y pureza según lo establecido en FCC, FA Y USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en elaboración de bebidas
analcohólicas con cafeína y taurina, y en la elaboración de fórmulas
infantiles.”
ARTÍCULO 14.- La presente resolución entrará en vigencia a partir del día siguiente al de su publicación en el Boletín Oficial.
ARTÍCULO 15.- Regístrese. Dése a la DIRECCIÓN NACIONAL DEL REGISTRO
OFICIAL para su publicación. Comuníquese a quienes corresponda.
Cumplido, archívese. Josefa Rodriguez Rodriguez - William Andrew
Murchison
e. 21/11/2018 N° 88469/18 v. 21/11/2018