Resolución 39/2019
RESOL-2019-39-APN-MAGYP
Ciudad de Buenos Aires, 12/09/2019
VISTO el Expediente N° EX-2018-60636175- -APN-DGDMA#MPYT del Registro
de la ex–SECRETARÍA DE GOBIERNO DE AGROINDUSTRIA del MINISTERIO DE
PRODUCCIÓN Y TRABAJO, el Tratado para la Constitución de un Mercado
Común entre la REPÚBLICA ARGENTINA, la REPÚBLICA FEDERATIVA DEL BRASIL,
la REPÚBLICA DEL PARAGUAY y la REPÚBLICA ORIENTAL DEL URUGUAY,
suscripto en la Ciudad de Asunción (REPÚBLICA DEL PARAGUAY) el 26 de
marzo de 1991, aprobado por la Ley N° 23.981, el Protocolo Adicional al
Tratado de Asunción sobre la Estructura Institucional del MERCOSUR -
Protocolo de Ouro Preto - suscripto por idénticas partes que el
mencionado tratado, en la Ciudad de Ouro Preto (REPÚBLICA FEDERATIVA
DEL BRASIL) el 17 de diciembre de 1994, aprobado por la Ley N° 24.560, y
CONSIDERANDO:
Que el proceso de integración del MERCADO COMÚN DEL SUR (MERCOSUR) es de importancia estratégica para la REPÚBLICA ARGENTINA.
Que el 26 de marzo de 1991, la REPÚBLICA ARGENTINA, la REPÚBLICA
FEDERATIVA DEL BRASIL, la REPÚBLICA DEL PARAGUAY y la REPÚBLICA
ORIENTAL DEL URUGUAY suscribieron el Tratado de Asunción para la
Constitución de un Mercado Común, creando el MERCADO COMÚN DEL SUR.
Que conforme a los Artículos 2°, 9°, 15, 20, 38 y 42 del Protocolo
Adicional al Tratado de Asunción sobre la Estructura Institucional del
MERCOSUR - Protocolo de Ouro Preto - suscripto por idénticas partes que
el tratado referido precedentemente, en la Ciudad de Ouro Preto
(REPÚBLICA FEDERATIVA DEL BRASIL), el 17 de diciembre de 1994, aprobado
por la Ley N° 24.560, las normas del MERCADO COMÚN DEL SUR (MERCOSUR)
aprobadas por el CONSEJO DEL MERCADO COMÚN, el GRUPO MERCADO COMÚN y la
COMISIÓN DE COMERCIO DEL MERCOSUR, son obligatorias y deben ser
incorporadas, cuando ello sea necesario, al ordenamiento jurídico
nacional de los Estados Partes mediante los procedimientos previstos en
su legislación.
Que conforme a los Artículos 3°, 14 y 15 de la Decisión N° 20 de fecha
6 de diciembre de 2002 del CONSEJO DEL MERCADO COMÚN, las normas del
MERCADO COMÚN DEL SUR (MERCOSUR) que no requieran ser incorporadas por
vía legislativa podrán ser incorporadas por vía administrativa por
medio de actos del PODER EJECUTIVO de los Estados Partes.
Que el Artículo 7° de la citada Decisión N° 20/02 establece que las
normas del MERCADO COMÚN DEL SUR (MERCOSUR) deberán ser incorporadas a
los ordenamientos jurídicos de los Estados Partes en su texto integral.
Que la Decisión N° 6 de fecha 17 de diciembre de 1996 del CONSEJO DEL
MERCADO COMÚN, incorpora al ordenamiento jurídico del MERCADO COMÚN DEL
SUR (MERCOSUR) el Acuerdo sobre la Aplicación de las Medidas Sanitarias
y Fitosanitarias (MSF) de la ORGANIZACIÓN MUNDIAL DEL COMERCIO (OMC).
Que resulta necesario incorporar al ordenamiento jurídico nacional la
Resolución N° 39 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN, la cual se encuentra contenida en el Adjunto, que registrado con
el Nº IF-2019-40744949-APN-DNMAI#MPYT forma parte integrante de la
presente medida.
Que en consecuencia, resulta necesario derogar el Anexo XII de la
Resolución N° 584 de fecha 20 de septiembre de 2006 de la ex-SECRETARÍA
DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS del entonces MINISTERIO DE
ECONOMÍA Y PRODUCCIÓN dado que la Resolución N° 31 de fecha 10 de
diciembre de 2003 del GRUPO MERCADO COMÚN contenida en dicho anexo ha
sido derogada por la precitada Resolución N° 39 de fecha 8 de noviembre
de 2018 del GRUPO MERCADO COMÚN.
Que resulta necesario incorporar al ordenamiento jurídico nacional la
Resolución N° 40 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN, la cual se encuentra contenida en el Adjunto, que registrado con
el Nº IF-2019-40744517-APN-DNMAI#MPYT forma parte integrante de la
presente medida.
Que en consecuencia, resulta necesario derogar el Anexo XIII de la
Resolución N° 584 de fecha 20 de septiembre de 2006 de la ex-SECRETARÍA
DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS del entonces MINISTERIO DE
ECONOMÍA Y PRODUCCIÓN dado que la Resolución N° 32 de fecha 10 de
diciembre de 2003 del GRUPO MERCADO COMÚN contenida en dicho anexo ha
sido derogada por la mencionada Resolución N° 40 de fecha 8 de
noviembre de 2018 del GRUPO MERCADO COMÚN.
Que resulta necesario incorporar al ordenamiento jurídico nacional la
Resolución N° 41 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN, la cual se encuentra contenida en el Adjunto, que registrado con
el Nº IF-2019-40744090-APN-DNMAI#MPYT forma parte integrante de la
presente medida.
Que en consecuencia, resulta necesario derogar el Anexo XIV de la
Resolución N° 574 de fecha 25 de noviembre de 2008 de la ex-SECRETARÍA
DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS del entonces MINISTERIO DE
ECONOMÍA Y PRODUCCIÓN dado que la Resolución N° 43 de fecha 11 de
diciembre de 2007 del GRUPO MERCADO COMÚN contenida en dicho anexo ha
sido derogada por la precitada Resolución N° 41 de fecha 8 de noviembre
de 2018 del GRUPO MERCADO COMÚN.
Que resulta necesario incorporar al ordenamiento jurídico nacional la
Resolución N° 42 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN, la cual se encuentra contenida en el Adjunto, que registrado con
el Nº IF-2019-40743317-APN-DNMAI#MPYT forma parte integrante de la
presente medida.
Que en consecuencia, resulta necesario modificar el Anexo I de la
Resolución N° 173 de fecha 11 de mayo de 2016 del ex–MINISTERIO DE
AGROINDUSTRIA, dado que el Artículo 11 del Capítulo III del Anexo I y
el Artículo 25 del Capítulo VI del Anexo I de la Resolución Nº 49 de
fecha 27 de noviembre de 2014 del GRUPO MERCADO COMÚN, contenida en
dicho Anexo, han sido modificados por la mencionada Resolución N° 42 de
fecha 8 de noviembre de 2018 del GRUPO MERCADO COMÚN.
Que resulta necesario incorporar al ordenamiento jurídico nacional la
Resolución N° 43 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN, la cual se encuentra contenida en el Adjunto, que registrado con
el Nº IF-2019-40742962-APN-DNMAI#MPYT forma parte integrante de la
presente medida.
Que en consecuencia, resulta necesario modificar el Anexo XIII de la
Resolución N° 574 de fecha 25 de noviembre de 2008 de la ex-SECRETARÍA
DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS del entonces MINISTERIO DE
ECONOMÍA Y PRODUCCIÓN, dado que el Artículo 9º del Capítulo II de la
Resolución N° 42 de fecha 11 de diciembre de 2007 del GRUPO MERCADO
COMÚN, contenido en dicho Anexo, ha sido sustituido por la precitada
Resolución N° 43 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN.
Que la Dirección General de Asuntos Jurídicos del MINISTERIO DE
AGRICULTURA, GANADERÍA Y PESCA ha tomado la intervención de su
competencia.
Que la presente resolución se dicta en ejercicio de las atribuciones
conferidas por la Ley de Ministerios (texto ordenado por Decreto N°
438/92) y sus modificaciones.
Por ello,
EL MINISTRO DE AGRICULTURA, GANADERÍA Y PESCA
RESUELVE:
ARTÍCULO 1°.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 39 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN “Requisitos Zoosanitarios de los Estados Partes para la
Importación de Bovinos y Bubalinos para Engorde (Derogación de la
Resolución GMC N° 31/03)” que con DOCE (12) hojas, en copia autenticada
como Adjunto registrado con el Nº IF-2019-40744949-APN-DNMAI#MPYT forma
parte integrante de la presente medida.
ARTÍCULO 2°.- Derógase el Anexo XII de la Resolución N° 584 de fecha 20
de septiembre de 2006 de la ex-SECRETARÍA DE AGRICULTURA, GANADERÍA,
PESCA Y ALIMENTOS del entonces MINISTERIO DE ECONOMÍA Y PRODUCCIÓN, por
los motivos expuestos en los considerandos de la presente medida.
ARTÍCULO 3°.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 40 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN “Requisitos Zoosanitarios de los Estados Partes para la
Importación de Bovinos y Bubalinos para Faena Inmediata (Derogación de
la Resolución GMC Nº 32/03)” que con NUEVE (9) hojas, en copia
autenticada como Adjunto registrado con el Nº
IF-2019-40744517-APN-DNMAI#MPYT forma parte integrante de la presente
medida.
ARTÍCULO 4°.- Derógase el Anexo XIII de la Resolución N° 584 de fecha
20 de septiembre de 2006 de la ex-SECRETARÍA DE AGRICULTURA, GANADERÍA,
PESCA Y ALIMENTOS del entonces MINISTERIO DE ECONOMÍA Y PRODUCCIÓN, por
los motivos expuestos en los considerandos de la presente medida.
ARTÍCULO 5°.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 41 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN “Requisitos Zoosanitarios de los Estados Partes para la
Importación de Équidos para Faena Inmediata (Derogación de la
Resolución GMC Nº 43/07)” que con DIEZ (10) hojas, en copia autenticada
como Adjunto registrado con el Nº IF-2019-40744090-APN-DNMAI#MPYT forma
parte integrante de la presente medida.
ARTÍCULO 6°.- Derógase el Anexo XIV de la Resolución N° 574 de fecha 25
de noviembre de 2008 de la ex-SECRETARÍA DE AGRICULTURA, GANADERÍA,
PESCA Y ALIMENTOS del entonces MINISTERIO DE ECONOMÍA Y PRODUCCIÓN, por
los motivos expuestos en los considerandos de la presente medida.
ARTÍCULO 7°.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 42 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN “Modificación de los Requisitos Zoosanitarios de los Estados
Partes para la Importación de Semen Bovino y Bubalino Congelado
(Modificación de la Resolución GMC N° 49/14)” que con DOS (2) hojas, en
copia autenticada como Adjunto registrado con el Nº
IF-2019-40743317-APN-DNMAI#MPYT forma parte integrante de la presente
medida.
ARTÍCULO 8°.- Modifícase el Anexo I de la Resolución N° 173 de fecha 11
de mayo de 2016 del ex–MINISTERIO DE AGROINDUSTRIA, por los motivos
expuestos en los considerandos de la presente medida.
ARTÍCULO 9°.- Incorpórase al ordenamiento jurídico nacional la
Resolución N° 43 de fecha 8 de noviembre de 2018 del GRUPO MERCADO
COMÚN “Modificación de los Requisitos Zoosanitarios de los Estados
Partes para la Importación de Embriones Equinos (Modificación de la
Resolución GMC Nº 42/07)” que con DOS (2) hojas, en copia autenticada
como Adjunto registrado con el Nº IF-2019-40742962-APN-DNMAI#MPYT forma
parte integrante de la presente medida.
ARTÍCULO 10.- Modifícase el Anexo XIII de la Resolución N° 574 de fecha
25 de noviembre de 2008 de la ex-SECRETARÍA DE AGRICULTURA, GANADERÍA,
PESCA Y ALIMENTOS del entonces MINISTERIO DE ECONOMÍA Y PRODUCCIÓN, por
los motivos expuestos en los considerandos de la presente medida.
ARTÍCULO 11.- La normativa que se incorpora por la presente resolución
entrará en vigor de conformidad con lo dispuesto por el Artículo 40 del
Protocolo Adicional al Tratado de Asunción sobre la Estructura
Institucional del MERCOSUR - Protocolo de Ouro Preto - suscripto por la
REPÚBLICA ARGENTINA, la REPÚBLICA FEDERATIVA DEL BRASIL, la REPÚBLICA
DEL PARAGUAY y la REPÚBLICA ORIENTAL DEL URUGUAY, en la Ciudad de Ouro
Preto (REPÚBLICA FEDERATIVA DEL BRASIL), el 17 de diciembre de 1994,
aprobado por la Ley N° 24.560.
ARTÍCULO 12.- Comuníquese, publíquese, dése a la DIRECCIÓN NACIONAL DEL REGISTRO OFICIAL y archívese. Luis Miguel Etchevehere
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la edición web del BORA -www.boletinoficial.gob.ar-
e. 16/09/2019 N° 69468/19 v. 16/09/2019
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
ANEXO I
MERCOSUR/GMC/RES. N° 39/18
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE BOVINOS Y BUBALINOS PARA ENGORDE
(DEROGACIÓN DE LA RESOLUCIÓN GMC N° 31/03)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común y la Resolución N° 31/03 del Grupo Mercado Común.
CONSIDERANDO:
Que por la Resolución GMC N° 31/03 se aprobaron los requisitos
zoosanitarios para el intercambio de bovinos para recría y engorde
entre los Estados Partes del MERCOSUR.
Que es necesario proceder a la actualización de los requisitos
indicados, de acuerdo a las modificaciones de la normativa
internacional de referencia de la Organización Mundial de Sanidad
Animal (OIE).
Que la armonización de los requisitos zoosanitarios del MERCOSUR
elimina los obstáculos que se generan por las diferencias de las
regulaciones nacionales vigentes, dando cumplimiento a lo establecido
en el Tratado de Asunción.
EL GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos Zoosanitarios de los Estados Partes
para la importación de bovinos y bubalinos para engorde" que constan
como Anexo I, así como el modelo de Certificado Veterinario
Internacional (CVI) que consta como Anexo II, los cuales forman parte
de la presente Resolución.
Art. 2 - En el caso de bubalinos, esta Resolución solamente se aplica a la importación de la especie Bubalus bubalis.
Art. 3 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 4 - Derogar la Resolución GMC N° 31/03.
Art. 5 - Esta Resolución deberá ser incorporada al ordenamiento jurídico de los Estados Partes antes del 08/V/2019.
CX GMC - Montevideo, 08/XI/18.
ANEXO I
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE BOVINOS Y BUBALINOS PARA ENGORDE
CAPÍTULO I
DE LA CERTIFICACIÓN
Art. 1 - Toda importación de bovinos y bubalinos para engorde deberá
estar acompañada del Certificado Veterinario Internacional (CVI),
emitido por la Autoridad Veterinaria del país exportador que certifique
el cumplimiento de los requisitos zoosanitarios que constan en la
presente Resolución.
El CVI deberá ser previamente acordado entre el país exportador y el
Estado Parte importador basado en el modelo que consta en el Anexo II
de la presente Resolución.
Art. 2 - El CVI deberá ser emitido dentro de los diez (10) días previos al embarque.
Art. 3 - Deberá ser realizada una inspección en el momento del
embarque, certificando la condición sanitaria satisfactoria, conforme a
lo establecido en la presente Resolución y dicha condición deberá ser
ratificada por la Autoridad Veterinaria en el punto de salida del país
exportador.
Art. 4 - El país exportador deberá proporcionar las informaciones que
permitan evaluar el cumplimiento de las exigencias de trazabilidad del
Estado Parte importador.
Art. 5 - Las pruebas de diagnóstico y las vacunaciones deberán ser
realizadas de acuerdo con el Manual de las Pruebas de Diagnóstico y de
las Vacunas para los Animales Terrestres de la Organización Mundial de
Sanidad Animal (OIE) (Manual Terrestre de la OIE) y, en el primer caso,
en laboratorios oficiales, acreditados o reconocidos por la Autoridad
Veterinaria del país exportador.
Los exámenes laboratoriales, cuando sean requeridos, tendrán una
validez de 30 (treinta) días a partir de la toma de la muestra,
pudiendo extenderse hasta 60 (sesenta) días en tanto los animales
permanezcan aislados, bajo supervisión oficial y no entren en contacto
con animales de condición sanitaria inferior o desconocida.
Art. 6 - El país exportador, zona o compartimento del país exportador,
que cumpla con lo establecido en los capítulos correspondientes del
Código Sanitario para los Animales Terrestres de la OIE (Código
Terrestre de la OIE) para ser considerado libre de una enfermedad y
obtenga el reconocimiento de dicha condición del Estado Parte
importador, estará exento de la realización de pruebas y/o vacunaciones.
6.1. En este caso, la condición de país, zona o compartimento libre deberá constar en el certificado.
6.2. Cuando no existe reconocimiento oficial por parte de la OIE, el
Estado Parte importador podrá solicitar informaciones adicionales para
evaluar la condición sanitaria del país exportador.
6.3. En caso de Fiebre Aftosa, la realización de pruebas y vacunaciones
será acordada entre el Estado Parte importador y el país exportador.
Art. 7 - El Estado Parte importador que cumpla con lo establecido en
los capítulos correspondientes del Código Terrestre de la OIE para ser
considerado oficialmente libre o posea un programa oficial de
prevención, control o erradicación para cualquier enfermedad que afecta
a la especie, se reserva el derecho de requerir medidas de mitigación
de riesgo adicionales, con el objetivo de prevenir el ingreso de esa
enfermedad al país.
Art. 8 - Podrán ser acordados entre el Estado Parte importador y el
país exportador otros procedimientos sanitarios que otorguen garantías
equivalentes para la importación.
CAPÍTULO II
INFORMACIONES ZOOSANITARIAS
Art. 9 - Los animales a ser exportados deberán haber permanecido en el
país exportador por lo menos noventa (90) días previos al embarque. En
caso de animales importados, deberán cumplir con lo establecido en los
artículos 11,12 y 13 del presente Anexo.
Art. 10 - Los animales a ser exportados deberán haber sido
cuarentenados en el país exportador en un establecimiento aprobado bajo
supervisión de la Autoridad Veterinaria, por un período mínimo de
treinta (30) días.
Art. 11 - Con relación a Pleuroneumonía Contagiosa Bovina, Fiebre del Valle del Rift y Dermatosis Nodular Contagiosa:
Los animales a ser exportados deberán proceder de un país reconocido
como libre por la OIE o que cumpla con lo establecido en los capítulos
correspondientes del Código Terrestre de la OIE para ser considerado
libre y dicha condición ser reconocida por el Estado Parte importador.
Art. 12 - Con relación a Fiebre Aftosa:
12.1. Los animales a ser exportados deberán proceder de un país o zona
libre de Fiebre Aftosa con o sin vacunación reconocido/a por la OIE; o
12.2. Los animales a ser exportados deberán proceder de un
compartimento libre de Fiebre Aftosa de acuerdo con lo establecido en
el capítulo correspondiente del Código Terrestre de la OIE y reconocido
por el Estado Parte importador;
12.3. Si corresponde, las pruebas de diagnóstico serán acordadas por la
Autoridad Veterinaria, considerando la situación sanitaria del país o
zona de origen/procedencia y destino;
12.4. Los animales a ser exportados que proceden de una zona libre de
Fiebre Aftosa con vacunación reconocida por la OIE deberán haber sido
vacunados con vacuna inactivada y con adyuvante oleoso, en un plazo no
menor a quince (15) días y no mayor a ciento ochenta (180) días previos
al embarque.
De acuerdo con su condición sanitaria, el Estado Parte importador podrá
no permitir la importación de bovinos y bubalinos vacunados con tipos
de virus exóticos para su territorio.
12.5. En el caso que los animales a ser exportados estén destinados a
un país, zona o compartimento libre de Fiebre Aftosa sin vacunación,
deberán provenir de países o zonas libres de Fiebre Aftosa sin
vacunación reconocidos por la OIE, o de compartimentos reconocidos por
el Estado Parte importador como libres de Fiebre Aftosa sin vacunación.
Art. 13 - En relación con la Encefalopatía Espongiforme Bovina (EEB):
13.1. Los animales a ser exportados deberán proceder de un país
reconocido por la OIE como de riesgo insignificante o de riesgo
controlado de EEB; y
13.2. Para los países de riesgo insignificante que hayan presentado
casos o para los países de riesgo controlado, los bovinos y bubalinos a
ser exportados deberán:
13.2.1. Haber nacido después de la fecha en que se inició el monitoreo
auditable del sistema de alimentación para garantizar el efectivo
cumplimiento de la prohibición del uso de proteínas animales para
alimentación de rumiantes, a excepción de las proteínas consideradas
exentas de riesgo por el Estado Parte importador; y
13.2.2. Estar identificados de forma individual y permanente mediante un sistema auditable de trazabilidad.
13.3. Los animales a ser exportados deberán haber nacido y haber sido
criados en el país exportador o en otro país con igual o superior
condición sanitaria.
Nota: Es facultad de un Estado Parte importador permitir, considerando
su condición sanitaria y su evaluación de riesgo, la importación de
bovinos y bubalinos originarios o procedentes de países de riesgo
insignificante con casos o riesgo controlado para EEB.
Art. 14 - Con relación a Brucelosis Bovina, los animales a ser exportados
(a excepción de los machos castrados) deberán:
14.1. Proceder de un país, zona o rebaño libre con o sin vacunación de acuerdo con el Código Terrestre de la OIE; o
14.2. Haber presentado resultado negativo a una (1) prueba de
diagnóstico efectuada durante la cuarentena, mediante la técnica de
Antígeno Acidificado Tamponado (AAT) o Enzyme-linked Immunosorbent
Assay (ELISA) indirecto. Los positivos, deberán ser sometidos a prueba
de Fijación de Complemento (FC) o Seroaglutinación (SAT) y
2-mercaptoetanol, o Polarización Fluorescente (FPA) con resultado
negativo.
Nota: En el caso de hembras recién paridas, las pruebas serán efectuadas por lo menos treinta (30) días después de la parición.
Las hembras menores de veinticuatro (24) meses de edad, vacunadas con
cepa B19 entre tres (3) y ocho (8) meses de edad, podrán ser excluidas
de la realización de las pruebas. En este caso, las informaciones de la
vacunación deberán ser incluidas en el certificado.
El Estado Parte importador que no vacune con la cepa B19 podrá permitir
la importación exclusivamente de hembras negativas para Brucelosis.
Art. 15 - Con relación a Tuberculosis Bovina, los animales a ser exportados deberán:
15.1. Proceder de un país, zona o rebaño libre de acuerdo con el Código Terrestre de la OIE; o
15.2. Haber presentado resultado negativo a una (1) prueba de
diagnóstico efectuada durante la cuarentena, mediante la técnica de
tuberculinización intradérmica simple con tuberculina Purified Protein
Derivative (PPD) bovina o comparada con PPD bovina y aviar.
Art. 16 - Con relación a Estomatitis Vesicular, los animales a ser
exportados deberán proceder de establecimientos donde no fueron
reportados oficialmente casos de la enfermedad durante los últimos
veintiún (21) días previos al embarque.
Art. 17 - Con relación a Lengua Azul los animales a ser exportados
deberán proceder de establecimientos donde no fueron reportados
oficialmente casos de la enfermedad durante los últimos sesenta (60)
días previos al embarque.
Art. 18 - Con relación a Carbunco Bacteridiano (Antrax) los animales a
ser exportados deberán proceder de establecimientos donde no fueron
reportados oficialmente casos de la enfermedad durante los últimos
veinte (20) días o deberán haber sido vacunados no menos de veinte (20)
días y no más de doce (12) meses previos al embarque.
Art. 19 - Los animales a ser exportados deberán haber sido sometidos a
tratamiento contra parásitos internos y externos durante la cuarentena
y en el CVI deberá constar el principio activo del producto y la fecha
del tratamiento.
Art. 20 - Los animales a ser exportados deberán haber sido
transportados directamente del lugar de cuarentena hasta el lugar de
embarque en medios de transporte precintados, previamente lavados,
desinfectados y desinsectados, con productos registrados por la
Autoridad Competente del país exportador. Los animales a ser exportados
no podrán mantener contacto con animales de condición sanitaria
inferior o desconocida respecto a las enfermedades que afectan a la
especie.
Art. 21 - Los animales a ser exportados no deberán presentar el día del
embarque ningún signo clínico de enfermedades transmisibles, así como
heridas o presencia de parásitos externos.
ANEXO II
MODELO DE CERTIFICADO VETERINARIO
INTERNACIONAL PARA LA EXPORTACIÓN DE BOVINOS Y BUBALINOS PARA ENGORDE
DESTINADOS A LOS ESTADOS PARTES
IV. Información Sanitaria
El Veterinario Oficial abajo firmante certifica que:
1. Los animales a ser exportados permanecieron en el país exportador
por lo menos noventa (90) días previos al embarque. En caso de animales
importados, cumplieron con lo establecido en los puntos 3, 4, 5, 6 y 7
del presente Certificado.
2. Los animales a ser exportados fueron cuarentenados en un
establecimiento aprobado, bajo supervisión de la Autoridad Veterinaria,
por un periodo mínimo de 30 (treinta) días.
3. Con relación a Pleuroneumonía Contagiosa Bovina:
(tachar lo que no corresponda)
3.1. Los animales a ser exportados provienen de un país reconocido como libre de la enfermedad por la OlE; o
3.2. Los animales a ser exportados provienen de un país que cumple con
lo establecido en los capítulos correspondientes del Código Terrestre
de la OIE para ser considerado como libre de la enfermedad y dicha
condición es reconocida por el Estado Parte importador.
4. Con relación a Fiebre del Valle del Rift, los animales provienen de
un país que cumple con lo establecido en los capítulos correspondientes
del Código Terrestre de la OIE para ser considerado como libre de la
enfermedad y dicha condición es reconocida por el Estado Parte
importador.
5. Con relación a Dermatosis Nodular Contagiosa, los animales provienen
de un país que cumple con lo establecido en los capítulos
correspondientes del Código Terrestre de la OIE para ser considerado
como libre de la enfermedad y dicha condición es reconocida por el
Estado Parte importador.
6. Con relación a Fiebre Aftosa:
(tachar lo que no corresponda)
6.1 Los animales a ser exportados provienen de un país o zona
reconocido por la OIE como libre de Fiebre Aftosa sin vacunación; o
6.2 Los animales a ser exportados provienen de un país o zona
reconocido por la OIE como libre de Fiebre Aftosa con vacunación; y
6.2.1 Fueron inmunizados con vacuna inactivada y con adyuvante oleoso,
administrada en un plazo no menor a quince (15) días y no mayor que
ciento ochenta (180) días previos al embarque.
o
6.3 Los animales a ser exportados proceden de un compartimento libre de
Fiebre Aftosa de acuerdo con lo establecido en el capítulo
correspondiente del Código Terrestre de la OIE y es reconocido por el
Estado Parte importador.
6.4 Los animales a ser exportados, dieron resultado negativo a la
prueba diagnóstica que se realizó a partir de muestras extraídas
durante el período de cuarentena, según lo acordado entre las
Autoridades Veterinarias.
Nota: En el caso que los animales estén destinados a un país, zona o
compartimento libre de Fiebre Aftosa sin vacunación, deberán provenir
de países o zonas libres de Fiebre Aftosa sin vacunación reconocidos
por la OIE, o de compartimentos reconocidos por el Estado Parte
importador.
7. Con relación a Encefalopatia Espongiforme Bovina (EEB):
(tachar lo que no corresponda)
7.1 Los animales a ser exportados provienen de un país reconocido por la OIE como de riesgo insignificante; o
7.2 Los animales a ser exportados provienen de un país reconocido por la OIE como de riesgo controlado; o
7.3 Para los países de riesgo insignificante que hayan presentado casos o para los países de riesgo controlado:
7.3.1 Los animales a ser exportados nacieron después de la fecha en que
se inició el monitoreo auditable del sistema de alimentación para
garantizar el efectivo cumplimiento de la prohibición del uso de
proteínas animales para alimentación de rumiantes, a excepción de
proteínas consideradas exentas de riesgo por el Estado Parte
importador; y
7.3.2 Los animales a ser exportados están identificados de forma
individual y permanente mediante un sistema auditable de trazabilidad.
7.4 Los animales a ser exportados nacieron y fueron criados en el país
exportador o en otro país con igual o superior condición sanitaria.
Nota: Es facultad del Estado Parte importador permitir, considerando su
condición sanitaria y su evaluación de riesgo, la importación de
bovinos y bubalinos originarios o procedentes de países de riesgo
insignificante con casos o de riesgo controlado para EEB.
8. Con relación a Brucelosis Bovina: (tachar lo que no corresponda)
8.1 Los animales a ser exportados provienen de un país, zona o rebaño
libre con o sin vacunación de acuerdo con el Código Terrestre de la
OIE; o
8.2 Los animales a ser exportados, dieron resultado negativo en una
prueba diagnóstica que se realizó a partir de muestras extraídas
durante el periodo de cuarentena previo al embarque (con excepción de
machos castrados);
Nota: En el caso de hembras recién paridas, las pruebas fueron efectuadas por lo menos treinta (30) días después de la parición.
o
8.3 Son hembras menores de veinticuatro (24) meses de edad, vacunadas con cepa B19 entre tres (3) y ocho (8) meses de edad.
Nota: El Estado Parte importador que no vacune con la cepa B19 podrá
permitir la importación exclusivamente de hembras negativas para
Brucelosis.
9. Con relación a Tuberculosis: (tachar lo que no corresponda)
9.1 Los animales proceden de país, zona o rebaños libres de Tuberculosis; o
9.2. Los animales a ser exportados, dieron resultado negativo a una
prueba diagnóstica que se realizó durante el período de cuarentena.
10. Con relación a Estomatitis Vesicular, los animales proceden de
establecimientos donde no fueron reportados oficialmente casos de la
enfermedad durante los veintiún (21) días previos al embarque.
11. Con relación a Lengua Azul, los animales proceden de
establecimientos di no fueron reportados oficialmente casos de la
enfermedad durante los sesenta días previos al embarque.
12. Con relación a Carbunco Bacteridiano (Antrax), los animales: (tachar lo que corresponda)
12.1 proceden de establecimientos donde no fueron reportados
oficialmente casos de la enfermedad durante los últimos veinte (20)
días previos al embarque; o
12.2 fueron vacunados no menos de veinte (20) días y no más de doce (12) meses previos al embarque.
13. Con relación a parásitos internos y externos, los animales fueron
tratados durante el periodo de cuarentena con productos aprobados por
la Autoridad Competente del país exportador.
14. Las pruebas de diagnóstico y las vacunaciones fueron realizadas de
acuerdo con el Manual Terrestre de la OIE. Las pruebas, fueron
realizadas en laboratorios oficiales, acreditados o reconocidos por la
Autoridad Veterinaria del país exportador.
15. Los animales fueron transportados directamente del lugar de
cuarentena hasta el lugar de embarque en medios de transporte
precintados, previamente lavados, desinfectados y desinsectados, con
productos registrados por la Autoridad Competente del país exportador.
Los animales no mantuvieron contacto con animales de condición
sanitaria inferior o desconocida respecto a las enfermedades que
afectan a la especie.
V. Embarque de los animales
El Veterinario Oficial abajo firmante certifica que los animales fueron
examinados en el momento de embarque y no presentaron signos clínicos
de enfermedades transmisibles, y se encontraron libres de heridas y de
parásitos externos.
IF-2019-40744949-APN-DNMAI#MPYT
ANEXO II
MERCOSUR/GMC/RES. N° 40/18
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE BOVINOS Y BUBALINOS PARA FAENA INMEDIATA
(DEROGACIÓN DE LA RESOLUCIÓN GMC N° 32/03)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común y la Resolución N° 32/03 del Grupo Mercado Común.
CONSIDERANDO:
Que por la Resolución GMC N° 32/03 se aprobaron los requisitos
zoosanitarios para el intercambio de bovinos para faena inmediata entre
los Estados Partes del MERCOSUR.
Que es necesario proceder a la actualización de los requisitos
indicados, de acuerdo a las modificaciones de la normativa
internacional de referencia de la Organización Mundial de Sanidad
Animal (OIE).
Que la armonización de los requisitos zoosanitarios del MERCOSUR
elimina los obstáculos que se generan por las diferencias de las
regulaciones nacionales vigentes, dando cumplimiento a lo establecido
en el Tratado de Asunción.
EL GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos Zoosanitarios de los Estados Partes
para la importación de bovinos y bubalinos para faena inmediata" que
constan como Anexo I, así como el modelo de Certificado Veterinario
Internacional (CVI) que consta como Anexo II, los cuales forman parte
de la presente Resolución.
Art. 2 - En el caso de bubalinos, esta Resolución solamente se aplica a la importación de la especie Bubalus bubalis.
Art. 3 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 4 - Derogar la Resolución GMC N° 32/03.
Art. 5 - Esta Resolución deberá ser incorporada al ordenamiento jurídico de los Estados Partes antes del 08/V/2019.
CX GMC - Montevideo, 08/XI/18.
ANEXO I
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE BOVINOS Y BUBALINOS PARA FAENA INMEDIATA
CAPÍTULO I
DE LA CERTIFICACIÓN
Art. 1 - Toda importación de bovinos y bubalinos para faena inmediata
deberá estar acompañada del Certificado Veterinario Internacional
(CVI), emitido por la Autoridad Veterinaria del país exportador que
certifique el cumplimiento de los requisitos zoosanitarios que constan
en la presente Resolución.
El CVI deberá ser previamente acordado entre el país exportador y el
Estado Parte importador basado en el modelo que consta en el Anexo II
de la presente Resolución.
Art. 2 - El CVI deberá ser emitido dentro de los cinco (5) días previos al embarque.
Art. 3 - Deberá ser realizada una inspección en el momento del
embarque, certificando la condición sanitaria satisfactoria, conforme a
lo establecido en la presente Resolución y dicha condición deberá ser
ratificada por la Autoridad Veterinaria en el punto de salida del país
exportador.
Art. 4 - El país exportador deberá proporcionar las informaciones que
permitan evaluar el cumplimiento de las exigencias de trazabilidad del
Estado Parte importador.
Art. 5 - Las pruebas de diagnóstico y las vacunaciones deberán ser
realizadas de acuerdo con el Manual de las Pruebas de Diagnóstico y de
las Vacunas para los Animales Terrestres de la Organización Mundial de
Sanidad Animal (OIE) (Manual Terrestre de la OIE) y, en el primer caso,
en laboratorios oficiales, acreditados o reconocidos por la Autoridad
Veterinaria del país exportador.
Art. 6 - El país exportador, zona o compartimento, que cumpla con lo
establecido en los capítulos correspondientes del Código Sanitario para
los Animales Terrestres de la OIE (Código Terrestre de la OIE) para ser
considerado libre de una enfermedad y obtenga el reconocimiento de
dicha condición del Estado Parte importador, estará exento de la
realización de pruebas y/o vacunaciones.
6.1. En este caso, la condición de país, zona o compartimento libre deberá constar en el certificado;
6.2. Cuando no existe reconocimiento oficial por parte de la OIE, el
Estado Parte importador podrá solicitar informaciones adicionales para
evaluar la condición sanitaria del país exportador;
6.3. En caso de Fiebre Aftosa, la realización de pruebas y vacunaciones
será acordada entre el Estado Parte importador y el país exportador.
Art. 7 - El Estado Parte importador que cumpla con lo establecido en
los capítulos correspondientes del Código Terrestre de la OIE para ser
considerado oficialmente libre o posea un programa oficial de
prevención, control o erradicación para cualquier enfermedad que afecta
a la especie, se reserva el derecho de requerir medidas de mitigación
de riesgo adicionales, con el objetivo de prevenir el ingreso de esa
enfermedad al país.
Art. 8 - Podrán ser acordados entre el Estado Parte importador y el
país exportador otros procedimientos sanitarios que otorguen garantías
equivalentes para la importación.
CAPÍTULO II
INFORMACIONES ZOOSANITARIAS
Art. 9 - Los animales a ser exportados deberán haber permanecido en el
país exportador por lo menos noventa (90) días previos al embarque. En
caso de animales importados, deberán cumplir con lo establecido en los
artículos 10, 11 y 12 del presente Anexo.
Art. 10 - Con relación a Pleuroneumonía Contagiosa Bovina, Fiebre del Valle del Rift y Dermatosis Nodular Contagiosa:
Los animales a ser exportados deberán proceder de un país reconocido
como libre por la OIE o que cumpla con lo establecido en los capítulos
correspondientes del Código Terrestre de la OIE para ser considerado
libre y dicha condición debe ser reconocida por el Estado Parte
importador.
Art. 11 - Con relación a Fiebre Aftosa:
11.1. Los animales a ser exportados deberán proceder de un país o zona
libre de Fiebre Aftosa con o sin vacunación reconocido/a por la OIE; o
11.2. Los animales a ser exportados deberán proceder de un
compartimento libre de Fiebre Aftosa de acuerdo con lo establecido en
el capítulo correspondiente del Código Terrestre de la OIE y reconocido
por el Estado Parte importador;
11.3. Si corresponde, las pruebas de diagnóstico serán acordadas por la
Autoridad Veterinaria, considerando la situación sanitaria del país o
zona de origen/procedencia y destino;
11.4. Los animales a ser exportados que proceden de una zona libre de
Fiebre Aftosa con vacunación reconocida por la OIE deberán haber sido
vacunados con vacuna inactivada y con adyuvante oleoso, en un plazo no
menor a quince (15) días y no mayor a ciento ochenta (180) días previos
al embarque.
De acuerdo con su condición sanitaria, el Estado Parte importador podrá
no permitir la importación de bovinos y bubalinos vacunados con tipos
de virus exóticos para su territorio.
11.5. En el caso que los animales a ser exportados estén destinados a
un país, zona o compartimento libre de Fiebre Aftosa sin vacunación,
deberán provenir de países o zonas libres de Fiebre Aftosa sin
vacunación reconocidos por la OIE, o de compartimentos reconocidos por
el Estado Parte importador como libres de Fiebre Aftosa sin vacunación.
Art. 12 - En relación con la Encefalopatía Espongiforme Bovina (EEB):
12.1. Los animales a ser exportados deberán proceder de un país
reconocido por la OIE como de riesgo insignificante o de riesgo
controlado de EEB;
12.2. Para los países de riesgo insignificante que hayan presentado
casos o para los países de riesgo controlado, los bovinos y bubalinos a
ser exportados deberán ser menores de treinta (30) meses;
12.3. Los animales a ser exportados a ser exportados deberán haber
nacido y haber sido criados en el país exportador o en otro país con
igual o superior condición sanitaria.
Nota: Es facultad de un Estado Parte importador permitir, considerando
su condición sanitaria y su evaluación de riesgo, la importación de
bovinos y bubalinos originarios o procedentes de países de riesgo
insignificante con casos o riesgo controlado para EEB.
Art. 13 - Con relación a Carbunco Bacteridiano (Antrax), previo al embarque, los animales a ser exportados:
13.1 Deberán proceder de establecimientos donde no fueron reportados
oficialmente casos de la enfermedad durante los últimos veinte (20)
días; y
13.2 No deberán haber sido vacunados con vacuna viva durante los
últimos catorce (14) días o un periodo más largo según las indicaciones
del fabricante.
Art. 14 - Los animales a ser exportados no deberán ser objeto de
descarte en razón de un programa de control y/o erradicación de
enfermedades en ejecución en el país exportador.
Art. 15 - Si fueran administradas sustancias farmacológicas a los
animales, deberán ser respetados los periodos de carencia pre faena
indicados por el fabricante.
Art. 16 - Los animales a ser exportados no deberán haber sido tratados
con sustancias anabolizantes de acuerdo a la legislación del Estado
Parte importador.
Art. 17 - Los animales a ser exportados deberán haber sido examinados
dentro de las cuarenta y ocho (48) horas previas al embarque y en el
punto de salida, no
debiendo presentar ningún signo clínico de enfermedades transmisibles, así como heridas o presencia de parásitos externos.
Art. 18 - Los animales a ser exportados deberán haber sido
transportados directamente del establecimiento de origen hasta el punto
de salida en medios de transporte precintados, previamente lavados,
desinfectados y desinsectados, con productos registrados por la
Autoridad Competente del país exportador. Los animales no podrán
mantener contacto con animales de condición sanitaria inferior o
desconocida respecto a las enfermedades que afectan a la especie.
ANEXO II
MODELO DE CERTIFICADO VETERINARIO
INTERNACIONAL PARA LA EXPORTACIÓN DE BOVINOS Y BUBALINOS PARA FAENA
INMEDIATA A LOS ESTADOS PARTES
IV. Información Sanitaria
El Veterinario Oficial abajo firmante certifica que:
1. Los animales a ser exportados permanecieron en el país exportador
por lo menos noventa (90) días previos al embarque. En caso de animales
importados, cumplieron con lo establecido en los puntos 2, 3, 4, 5, y 6
del presente Certificado.
2. Con relación a Pleuroneumonía Contagiosa Bovina: (tachar lo que no corresponda)
2.1 Los animales a ser exportados provienen de un país reconocido como libre de la enfermedad por la OIE; o
2.2 Los animales a ser exportados provienen de un país que cumple con
lo establecido en los capítulos correspondientes del Código Terrestre
de la OIE para ser considerado como libre de la enfermedad y dicha
condición es reconocida por el Estado Parte importador.
3. Con relación a Fiebre del Valle del Rift, los animales provienen de
un país que cumple con lo establecido en los capítulos correspondientes
del Código Terrestre de la OIE para ser considerado como libre de la
enfermedad y dicha condición es reconocida por el Estado Parte
importador.
4. Con relación a Dermatosis Nodular Contagiosa, los animales a ser
exportados provienen de un país que cumple con lo establecido en los
capítulos correspondientes del Código Terrestre de la OIE para ser
considerado como libre de la enfermedad y dicha condición es reconocida
por el Estado Parte importador.
5. Con relación a Fiebre Aftosa:
(tachar lo que no corresponda)
5.1 Los animales a ser exportados provienen de un país o zona
reconocido por la OIE como libre de Fiebre Aftosa sin vacunación; o,
5.2 Los animales a ser exportados provienen de un país o zona
reconocido por la OIE como libre de Fiebre Aftosa con vacunación y
fueron inmunizados con vacuna inactivada y con adyuvante oleoso,
administrada en un plazo no menor a quince (15) días y no mayor que
ciento ochenta (180) días previos al embarque.
o
5.3 Los animales a ser exportados proceden de un compartimento libre de
Fiebre Aftosa de acuerdo con lo establecido en el capítulo
correspondiente del Código Terrestre de la OIE y es reconocido por el
Estado Parte importador.
5.4 Los animales a ser exportados, dieron resultado negativo a la prue
ba diagnóstica, según lo acordado entre las Autoridades Veterinarias.
Nota: En el caso que los animales a ser exportados estén destinados a
un país, zona o compartimento libre de Fiebre Aftosa sin vacunación,
deberán provenir de países o zonas libres de Fiebre Aftosa sin
vacunación reconocidos por la OIE, o de compartimentos reconocidos como
libre de Fiebre Aftosa por el Estado Parte importador.
6. Con relación a Encefalopatía Espongiforme Bovina (EEB):
(tachar lo que no corresponda)
6.1 Los animales a ser exportados provienen de un país reconocido por la OIE como de riesgo insignificante; o
6.2 Para los países de riesgo insignificante que hayan presentado casos
o para los países de riesgo controlado, los animales son menores de
treinta (30) meses;
6.3 Los animales a ser exportados nacieron y fueron criados en el país
exportador o en otro país con igual o superior condición sanitaria.
Nota: Es facultad del Estado Parte importador permitir, considerando su
condición sanitaria y su evaluación de riesgo, la importación de
bovinos y bubalinos originarios o procedentes de países de riesgo
insignificante con casos o de riesgo controlado para EEB.
7. Con relación a Carbunco Bacteridiano (Antrax), los animales a ser exportados:
7.1 Proceden de establecimientos donde no fueron reportados
oficialmente casos de la enfermedad durante los últimos veinte (20)
días previos al embarque; y
7.2 No fueron vacunados con vacuna viva durante los últimos catorce
(14) días previos al embarque o un periodo más largo según las
indicaciones del fabricante.
8. Los animales a ser exportados no son objeto de descarte en razón de
un programa de control y/o erradicación de enfermedades en ejecución en
el país exportador.
9. En caso que hayan sido administradas sustancias farmacológicas a los
animales, fueron respetados los periodos de carencia prefaena indicados
por el fabricante.
10. Los animales a ser exportados no fueron tratados con sustancias
anabolizantes de acuerdo a la legislación del Estado Parte importador.
11. Las pruebas de diagnóstico y las vacunaciones fueron realizadas de
acuerdo con el Manual de las Pruebas de Diagnóstico y de las Vacunas
para los Animales Terrestres de la OIE (Manual Terrestre de la OIE).
Las pruebas, fueron realizadas en laboratorios oficiales, acreditados o
reconocidos por la Autoridad Veterinaria del país exportador.
12. Los animales a ser exportados fueron examinados dentro de las
cuarenta y ocho (48) horas previo al embarque y no presentaron ningún
signo clínico de enfermedades transmisibles, así como heridas o
presencia de parásitos externos
13. Los animales a ser exportados fueron transportados directamente del
establecimiento de origen hasta el punto de salida en medios de
transporte precintados, previamente lavados, desinfectados y
desinsectados, con productos registrados por la Autoridad Competente
del país exportador. Los animales no mantuvieron contacto con animales
de condición sanitaria inferior o desconocida respecto a las
enfermedades que afectan a la especie.
V. Embarque de los animales
El Veterinario Oficial abajo firmante certifica que los animales a ser
exportados fueron examinados en el momento de embarque y no presentaron
signos clínicos de enfermedades transmisibles, y se encontraron libres
de heridas y de parásitos externos.
IF-2019-40744517-APN-DNMAI#MPYT
ANEXO III
MERCOSUR/GMC/RES. N° 41/18
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE ÉQUIDOS PARA FAENA INMEDIATA
(DEROGACIÓN DE LA RESOLUCIÓN GMC N° 43/07)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común y la Resolución N° 43/07 del Grupo Mercado Común.
CONSIDERANDO:
Que por la Resolución GMC N° 43/07 fueron aprobados los requisitos
zoosanitarios para la importación de équidos para faena inmediata
destinados a los Estados Partes.
Que es necesario proceder a la actualización de los requisitos
indicados, de acuerdo con las recientes modificaciones de las normas
internacionales de referencia de la Organización Mundial de Sanidad
Animal (OIE).
Que la armonización de los requisitos zoosanitarios del MERCOSUR
elimina los obstáculos que se generan por las diferencias de las
regulaciones nacionales vigentes, dando cumplimiento a lo establecido
en el Tratado de Asunción.
EL GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos Zoosanitarios de los Estados Partes
para la importación de équidos para faena inmediata" que constan como
Anexo I, así como el modelo de Certificado Veterinario Internacional
(CVI) que consta como Anexo II, los cuales forman parte de la presente
Resolución.
Art. 2 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 3 - Derogar la Resolución GMC N° 43/07.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento jurídico de los Estados Partes antes del 08/V/2019.
CX GMC - Montevideo, 08/XI/18.
ANEXO I
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE ÉQUIDOS PARA FAENA INMEDIATA
CAPÍTULO I
DE LA CERTIFICACIÓN
Art. 1 - Toda importación de équidos deberá estar acompañada del
Certificado Veterinario Internacional (CVI), emitido por la Autoridad
Veterinaria del país exportador que certifique el cumplimiento de los
requisitos zoosanitarios que constan en el presente Anexo.
El CVI deberá ser previamente acordado entre el país exportador y el
Estado Parte importador basado en el modelo que consta en el Anexo II
de la presente Resolución.
Art. 2 - El CVI deberá ser emitido dentro de los cinco (5) días previos a la fecha de ingreso al Estado Parte importador.
Art. 3 - Los exámenes de diagnóstico, cuando sean requeridos, deberán
ser realizados en laboratorios oficiales, acreditados o reconocidos por
la Autoridad Veterinaria del país exportador, de acuerdo con el Manual
de Pruebas Diagnósticas y Vacunas para los Animales Terrestres de la
OIE y tendrán una validez de treinta (30) días a partir de la toma de
muestra.
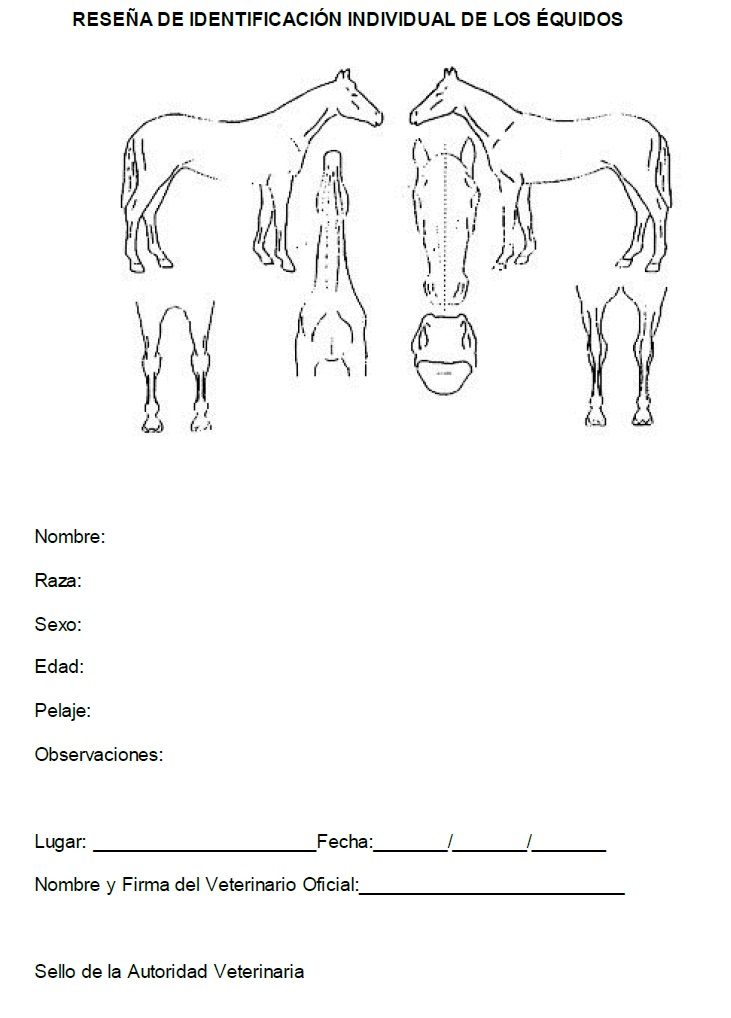
Art. 4 - Los équidos deberán ser identificados por medio de reseñas emitidas por el Veterinario Oficial del país exportador.
4.1. En caso de que sean presentados documentos como el "Pasaporte
Equino" u otra documentación equivalente, emitidos por entidades
reconocidas y debidamente endosados por la Autoridad Veterinaria del
país correspondiente, podrá ser aceptada la reseña que conste en estos
documentos.
4.2. En ese caso, la referencia del documento deberá constar en el CVI que acompañe la exportación.
4.3. Cualquier otra identificación individual, tales como tatuaje o microchip, también deberá constar en el CVI.
Art. 5 - El país exportador o zona o compartimento del país exportador
que cumple con lo establecido en los capítulos correspondientes del
Código Sanitario para los Animales Terrestres (Código Terrestre de la
OIE) para ser considerado libre y obtenga el reconocimiento del Estado
Parte importador para alguna de las enfermedades para las que se
requieren pruebas o vacunaciones, estará exento de la realización de
las mismas, así como exento de la certificación de establecimientos
libres.
5.1. En ese caso, la certificación de país, zona o compartimento libre
de las enfermedades en cuestión deberá ser incluida en el CVI;
5.2. Las enfermedades para las cuales la OIE no emite reconocimiento
oficial de país o zona libre, el Estado Parte importador podrá
solicitar, al país exportador, información adicional para el
reconocimiento de dicha condición sanitaria.
Art. 6 - El Estado Parte importador que cumpla con lo establecido en
los capítulos correspondientes del Código Terrestre de la OIE para ser
considerado libre o que posea un programa oficial de prevención,
control o erradicación para cualquier enfermedad, se reserva el derecho
de requerir medidas de mitigación adicionales, con el objetivo de
prevenir el ingreso de esa enfermedad al país.
Art. 7 - Podrán ser acordados entre el Estado Parte importador y el
país exportador otros procedimientos sanitarios que otorguen garantías
equivalentes o superiores para la importación.
Art. 8 - En caso de condiciones sanitarias particulares, en que sea
necesaria alguna identificación especial de los équidos, cada Estado
Parte podrá establecer, de acuerdo con su reglamentación interna
vigente, condiciones específicas para esa finalidad (tatuaje,
microchip, entre otras). Esa condición deberá ser puesta en
conocimiento previo del país exportador.
CAPÍTULO II
INFORMACIONES ZOOSANITARIAS
Art. 9 - Los équidos a ser exportados deberán haber permanecido en el
país exportador por lo menos cuarenta (40) días inmediatamente previos
al embarque. En caso de animales importados, estos deberán cumplir con
las exigencias sanitarias que constan en los artículos 11 y 12 del
presente Anexo.
Art. 10 - Los équidos a ser exportados deberán ser procedentes de
establecimientos que no fueron sometidos a restricciones sanitarias
durante los últimos noventa (90) días previos al embarque.
Art. 11 - Con relación a Peste Equina:
11.1. Los équidos a ser exportados deberán permanecer por lo menos
cuarenta (40) días previos al embarque en un país reconocido como libre
por la OIE o que se declare libre de la enfermedad de acuerdo con lo
establecido en el Código Terrestre de la OIE, y esta condición deberá
ser reconocida por el Estado Parte importador; y
11.2. Los équidos a ser exportados no deberán haber sido vacunados contra la enfermedad.
Art. 12 - Con relación a Encefalomielitis Equina Venezolana (EEV):
12.1. Los équidos a ser exportados deberán ser procedentes de un país
que se declara libre de la enfermedad de acuerdo con lo establecido en
el Código Terrestre de la OIE, y esta condición deberá ser reconocida
por el Estado Parte importador; o
12.2 En caso de proceder de países no libres de la enfermedad:
12.2.1. Los équidos a ser exportados no podrán estar vacunados contra la enfermedad; y
12.2.2. Los équidos a ser exportados deberán permanecer aislados en el
país exportador, bajo supervisión de la Autoridad Veterinaria, durante
los veintiún (21) días previos al embarque, protegidos contra vectores
y clínicamente sanos durante ese período; y
12.2.3. Los équidos a ser exportados deberán ser sometidos a dos (2)
pruebas de Inhibición de la Hemoaglutinación para la enfermedad, sobre
muestras pareadas, efectuadas con un intervalo mínimo de catorce (14)
días entre ellas, siendo la segunda muestra tomada dentro de los siete
(7) días previos al embarque, con resultados negativos, y
12.2.4. Los équidos a ser exportados deberán estar protegidos contra
vectores durante el transporte del establecimiento de origen hasta el
local de aislamiento y hasta el momento del embarque.
Art. 13 - Con relación a Carbunco Bacteridiano (Antrax), previo al embarque, los équidos a ser exportados:
13.1 Deberán proceder de establecimientos donde no fueron reportados
oficialmente casos de la enfermedad durante los últimos veinte (20)
días; y
13.2 No deberán haber sido vacunados con vacuna viva durante los
últimos catorce (14) días o un periodo más largo según las indicaciones
del fabricante.
Art. 14 - Los équidos a ser exportados, no deberán ser objeto de
descarte como consecuencia de un programa de control y/o erradicación
de enfermedades, en ejecución en el país exportador.
Art. 15 - Si fueran administradas sustancias farmacológicas a los
équidos a ser exportados, deberán ser respetados los periodos de
carencia prefaena indicados por el fabricante.
Art. 16 - Los équidos a ser exportados no deberán haber sido tratados
con sustancias anabolizantes de acuerdo a la legislación del Estado
Parte importador.
Art. 17 - Los équidos a ser exportados deberán ser transportados
directamente desde el lugar de embarque hasta el punto de salida del
país exportador en medios de transporte, precintados, con adecuada
protección contra vectores, previamente limpios, desinfectados y
desinsectados con productos aprobados por la Autoridad Competente del
país exportador y no deberán mantener contacto con animales de
condición sanitaria inferior o desconocida.
Art. 18 - Los équidos a ser exportados deberán ser examinados dentro de
las cuarenta y ocho (48) horas previas al embarque y en el punto de
salida del país exportador, no presentando signos clínicos de
enfermedades trasmisibles, sin heridas abiertas y sin parásitos
externos.
Art. 19 - Los équidos a ser exportados identificados en el certificado
deberán ser transportados directamente al establecimiento de faena
habilitado por el Servicio Veterinario del Estado Parte importador.
De acuerdo a su evaluación de riesgo el Estado Parte importador podrá
destinar los animales a un predio autorizado bajo control oficial
cumpliendo un periodo de permanencia hasta el momento de la faena
acordada.
ANEXO II
MODELO DE CERTIFICADO VETERINARIO INTERNACIONAL PARA LA EXPORTACIÓN DE ÉQUIDOS PARA FAENA INMEDIATA A LOS ESTADOS PARTES
IV. Informaciones Sanitarias
El Veterinario Oficial abajo firmante certifica que:
1. Los équidos exportados permanecieron en el país exportador por lo
menos cuarenta (40) días inmediatamente previos al embarque. En caso de
animales importados, cumplieron con las exigencias sanitarias que
constan en los puntos 3 y 4 del presente certificado.
2. Los équidos proceden de establecimientos que no fueron sometidos a
restricciones sanitarias durante los últimos noventa (90) días previos
al embarque.
3. Con relación a Peste Equina:
(tachar lo que no corresponda)
3.1.Los équidos permanecieron por lo menos cuarenta (40) días previos al embarque en:
3.1.1. Un país reconocido como libre por la OIE; o
3.1.2. Un país que se declara libre de la enfermedad de acuerdo con lo
establecido en el Código Terrestre de la OIE y esa condición es
reconocida por el Estado Parte importador; y
3.2. Los équidos a ser exportados no fueron vacunados contra la enfermedad.
4. Con relación a Encefalomielitis Equina Venezolana (EEV):
(tachar lo que no corresponda)
4.1. Los équidos a ser exportados proceden de un país que se declara
libre de la enfermedad de acuerdo con lo establecido en el Código
Terrestre de la OIE, y esa condición es reconocida por el Estado Parte
importador; o
4.2.Los équidos a ser exportados proceden de un país no libre de la enfermedad; y
4.2.1. No fueron vacunados y permanecieron aislados en el país
exportador, bajo supervisión de la Autoridad Veterinaria, durante los
veintiún (21) días previos al embarque, protegidos contra vectores,
estando clínicamente sanos durante ese período; y
4.2.2. Fueron sometidos a dos (2) pruebas de Inhibición de la
Hemoaglutinación para la enfermedad, sobre muestras pareadas,
efectuadas con un intervalo mínimo de catorce (14) días entre ellas,
siendo la segunda muestra tomada dentro de los siete (7) días previos
al embarque con resultados negativos.
y
4.2.3. Fueron protegidos contra vectores durante el transporte del
establecimiento de origen al lugar de aislamiento y hasta el momento
del embarque.
5. Con relación a Carbunco Bacteridiano (Antrax), los équidos a ser exportados:
5.1 Proceden de establecimientos donde no fueron reportados
oficialmente casos de la enfermedad durante los últimos veinte (20)
días previos al embarque; y
5.2 No fueron vacunados con vacuna viva durante los últimos catorce
(14) días previos al embarque o un periodo más largo según las
indicaciones del fabricante.
6. Los équidos a ser exportados no son objeto de descarte como
consecuencia de un programa de control y/o erradicación de
enfermedades, en ejecución en el país exportador.
7. En caso que hayan sido administradas sustancias farmacológicas a los
équidos a ser exportados, fueron respetados los periodos de carencia
prefaena indicados por el fabricante.
8. Los équidos a ser exportados no fueron tratados con sustancias
anabolizantes de acuerdo a la legislación del Estado Parte importador.
9. Los équidos a ser exportados fueron examinados dentro de las
cuarenta y ocho (48) horas previas al embarque no presentando signos
clínicos de enfermedades trasmisibles, sin heridas abiertas y sin
parásitos externos.
10. Los équidos a ser exportados fueron transportados directamente
desde el lugar de embarque hasta el punto de salida del país exportador
en medios de transporte precintados, con adecuada protección contra
vectores, previamente limpios, desinfectados y desinsectados con
productos aprobados por la Autoridad Competente del país exportador y
no mantuvieron contacto con animales de condición sanitaria inferior o
desconocida.
Sello de la Autoridad Veterinaria:
V. Embarque de los animales
El Veterinario Oficial abajo firmante certifica que los équidos a ser
exportados fueron examinados en el momento de salida del país
exportador y no presentaron signos clínicos de enfermedades
transmisibles y no fueron encontradas heridas abiertas ni parásitos
externos.
IF-2019-40744090-APN-DNMAI#MPYT
ANEXO IV
MERCOSUR/GMC/RES N° 42/18
MODIFICACIÓN DE LOS REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE SEMEN BOVINO Y BUBALINO CONGELADO
(MODIFICACIÓN DE LA RESOLUCIÓN GMC N° 49/14)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común y la Resolución N° 49/14 del Grupo Mercado Común.
CONSIDERANDO:
Que de acuerdo con los avances en el conocimiento científico respecto a
la Dermatitis Nodular Contagiosa (DNC) y las recomendaciones del Código
Sanitario para los Animales Terrestres de la Organización Mundial de
Sanidad Animal (OIE), corresponde actualizar los requisitos
zoosanitarios de los Estados Partes para la importación de semen bovino
y bubalino congelado.
EL GRUPO MERCADO COMUN
RESUELVE:
Art. 1 - Sustituir el artículo 11 del Capítulo III del Anexo I de la Resolución GMC N° 49/14, por el siguiente texto:
"Art. 11 - Durante el período de
colecta de semen y por lo menos hasta treinta (30) días posteriores a
la última colecta de semen, el país exportador deberá cumplir con lo
establecido en los capítulos correspondientes del Código Terrestre de
la OIE para ser considerado oficialmente libre de Pleuroneumonía
Contagiosa Bovina y dicha condición ser reconocida por el Estado Parte
importador."
Art. 2 - Incorporar en el artículo 25 del Capítulo VI del Anexo I de la
Resolución GMC N° 49/14 los siguientes requisitos relacionados a
Dermatosis Nodular Contagiosa (DNC), según esta redacción:
"5. DERMATOSIS NODULAR CONTAGIOSA:
Los dadores:
5.1 O bien
5.1.1 Deberán haber sido vacunados
regularmente, siendo la última vacunación dentro de los sesenta (60)
días antes de la primera colecta del semen y deberá haberse demostrado
la presencia de anticuerpos contra Dermatosis Nodular Contagiosa
treinta (30) días después de la vacunación; o
5.1.2 Deberán haber sido sometidos
con resultado negativo a una prueba de Virusneutralización para la
detección de Dermatosis Nodular Contagiosa cada veintiocho (28) días
durante el período de colecta del semen y veintiún (21) días después de
la última colecta; y
5.1.3 Deberán haber sido sometidos
con resultado negativo a la prueba de Polymerase Chain Reaction (PCR) a
partir de muestras de sangre tomadas al principio y al final del
período de colecta y por lo menos cada veintiocho (28) días durante
este período.
5.2 El semen exportado deberá haber sido sometido a una prueba de detección del agente por PCR."
Art. 3 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento jurídico de los Estados Partes antes del 08/V/2019.
CX GMC - Montevideo, 08/XI/18.
IF-2019-40743 317-APN-DNMAI#MPYT
ANEXO V
MERCOSUR/GMC/RES. N° 43/18
MODIFICACIÓN DE LOS REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA IMPORTACIÓN DE EMBRIONES EQUINOS
(MODIFICACIÓN DE LA RESOLUCIÓN GMC N° 42/07)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común y las Resoluciones N° 42/07, 08/18 y 09/18 del Grupo
Mercado Común.
CONSIDERANDO:
Que conforme a los avances en las recomendaciones internacionales
emanadas de la Organización Mundial de Sanidad Animal (OIE),
específicamente en lo relacionado a la Encefalomielitis Equina
Venezolana (EEV) y Peste Equina, se actualizaron los requisitos
zoosanitarios de los Estados Partes para la importación definitiva y
temporal de équidos.
Que, de acuerdo con lo anterior, se hace necesaria la modificación de
los requisitos zoosanitarios para la importación de embriones equinos.
EL GRUPO MERCADO COMUN
RESUELVE:
Art. 1 - Sustituir el artículo 9 del Capítulo II de la Resolución GMC N° 42/07, por el siguiente texto:
"Art. 9 - Con relación a Peste Equina:
- Las donantes deberán haber
permanecido por lo menos cuarenta (40) días previos a la colecta de los
embriones a exportar y durante la misma, en un país reconocido como
libre de la enfermedad por la OIE o que se declare libre de acuerdo con
lo establecido en el Código Terrestre de la OIE, y esta condición
deberá haber sido reconocida por el Estado Parte importador; y
- Las donantes no deberán haber sido
vacunadas contra la enfermedad con vacunas vivas atenuadas, durante los
cuarenta (40) días previos a la colecta.
Con relación a Encefalomielitis Equina Venezolana (EEV):
- Las donantes deberán haber
permanecido durante el período de colecta de los embriones a exportar,
en un país que se declara libre de la enfermedad de acuerdo con lo
establecido en el Código Terrestre de la OIE, y esta condición deberá
haber sido reconocida por el Estado Parte importador; o
- Las donantes no podrán estar vacunadas contra la enfermedad; y
- Las donantes deberán haber sido
sometidas, previo a la colecta de los embriones a exportar, a dos (2)
pruebas de Inhibición de la
Hemoaglutinación para la enfermedad,
sobre muestras pareadas, efectuadas con un intervalo mínimo de catorce
(14) días entre ellas, siendo la segunda muestra tomada dentro de los
siete (7) días previos a la colecta, con resultados negativos; y
- Las donantes deberán haber sido protegidas contra vectores durante el período de la colecta de los embriones a exportar."
Art. 2 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 3 - Esta Resolución deberá ser incorporada al ordenamiento jurídico de los Estados Partes antes del 08/V/2019.
CX GMC - Montevideo, 08/XI/18.
IF-2019-40742962-APN-DNMAI#MPYT