Resolución 1691/2019
RESOL-2019-1691-APN-SSS#MSYDS
Ciudad de Buenos Aires, 11/10/2019
VISTO el Expediente N° EX-2019-88051683-APN-GGE#SSS del Registro de la
SUPERINTENDENCIA DE SERVICIOS DE SALUD, las Leyes Nº 23.660 y Nº
23.661, los Decretos N° 1615 de fecha 23 de diciembre de 1996 y Nº 2710
de fecha 28 de diciembre de 2012, las Resoluciones Nº 1200 de fecha 21
de septiembre de 2012, Nº 1561 de fecha 30 de noviembre de 2012, Nº 400
de fecha 25 de octubre de 2016, Nº 46 de fecha 13 de enero de 2017 y Nº
1284 de fecha 6 de septiembre de 2019, todas del Registro de la
SUPERINTENDENCIA DE SERVICIOS DE SALUD y,
CONSIDERANDO:
Que por Decreto N° 1615/96 se ordenó la fusión de la ADMINISTRACIÓN
NACIONAL DEL SEGURO DE SALUD (ANSSAL), el INSTITUTO NACIONAL DE OBRAS
SOCIALES (INOS) y la DIRECCIÓN NACIONAL DE OBRAS SOCIALES (DINOS),
constituyendo la SUPERINTENDENCIA DE SERVICIOS DE SALUD como organismo
descentralizado de la Administración Pública Nacional y en jurisdicción
del entonces MINISTERIO DE SALUD Y ACCIÓN SOCIAL
Que mediante el Decreto Nº 2710/12 se aprobó la estructura organizativa
de la SUPERINTENDENCIA DE SERVICIOS DE SALUD, cuyo Anexo II define sus
objetivos, entre ellos, “el de implementar, reglamentar y administrar
los recursos provenientes del Fondo Solidario de Redistribución,
dirigiendo todo su accionar al fortalecimiento cabal de la atención de
la salud de los beneficiarios del Sistema Nacional del Seguro de Salud,
destinando todos los recursos disponibles para la cobertura de
subsidios por reintegros por prestaciones de alto impacto económico y
que demanden una cobertura prolongada en el tiempo, a fin de asegurar
el otorgamiento de prestaciones de salud igualitarias, garantizando a
los beneficiarios la obtención del mismo tipo y nivel de prestaciones”.
Que con ese objetivo se dictó la Resolución Nº 1200/12-SSSALUD, que
implementó el nuevo sistema de reintegros, el que se denominó SISTEMA
ÚNICO DE REINTEGRO (SUR).
Que por la Resolución Nº 1561/12-SSSALUD se instaura el PROCEDIMIENTO
PARA AUTORIZACIÓN DE REINTEGROS DEL SISTEMA DE TUTELAJE DE TECNOLOGÍAS
SANITARIAS EMERGENTES, con el objetivo de velar por la adecuada
utilización de las innovaciones tecnológicas en materia de salud.
Que por las Resoluciones Nº 400/16-SSSALUD y Nº 046/17- SSSALUD se
aprobaron las normas generales y específicas, sobre las cuales los
Agentes del Seguro de Salud deben ajustar sus presentaciones ante el
SISTEMA ÚNICO DE REINTEGRO para el recupero de las erogaciones
efectuadas por determinadas prestaciones médicas a sus beneficiarios.
Que esta SUPERINTENDENCIA DE SERVICIOS en uso de las facultades
legalmente conferidas, tiene la potestad de revisar periódicamente, las
coberturas, valores de recupero y condiciones de acceso a los
reintegros para su eventual actualización.
Que en el marco de ello, la Gerencia de Gestión Estratégica del
Organismo tomó la intervención de su competencia y emitió el Informe
Técnico GDE N° IF-2019-88070899-APN-SGE#SSS, el que da cuenta del
análisis realizado respecto del abordaje de las tecnologías
contempladas para el tratamiento de la patología INFECCIÓN POR VIRUS DE
LA INMUNODEFICIENCIA HUMANA (VIH), cuya evaluación permite obtener
información objetiva sobre la utilidad de las mismas.
Que se han evaluado la totalidad de las opciones de tecnologías
disponibles al momento del análisis, y se han seleccionado aquéllas que
cumplimentan una alternativa válida en términos de efectividad,
costo-efectividad, impacto presupuestario y en la salud pública.
Que en tal sentido, y con fundamento en el avance de la evidencia
científica sobre la materia, se concluyó en la conveniencia y
oportunidad de modificar e incorporar determinadas tecnologías al
SISTEMA ÚNICO DE REINTEGRO, dada su prevalencia de uso y su relación
costo – efectividad, respecto a la patología Infección por VIH.
Que se han tomado en consideración para las modificaciones propuestas,
las guías de orientación de tratamiento, como recomendaciones prácticas
basadas en la evidencia científica, que abordan el tratamiento más
efectivo y el seguimiento de la enfermedad y que se encuentran avaladas
científicamente.
Que en tal sentido, por la Resolución Nº 1284/19-SSSALUD se decidió
implementar el Protocolo de Recupero - Infección por VIH, el cual
entrara en vigencia a partir del 1º de septiembre de 2019.
Que sin perjuicio de ello, previo a la entrada en vigencia de la nueva
normativa, se evidenció la conveniencia de realizar modificaciones en
los Anexos integrantes de la misma, a los fines de determinar
condiciones que permitan un mejor acceso por parte de los beneficiarios
a dichas prestaciones.
Que la presente medida contribuye a una racional y eficiente
distribución de los recursos afectados por el Fondo Solidario de
Redistribución.
Que ha tomado la intervención de su competencia el Servicio Jurídico del Organismo.
Que la presente medida se dicta de conformidad con las facultades
conferidas por los Decretos Nº 1615 de fecha 23 de diciembre de 1996,
Nº 2710 de fecha 28 de diciembre de 2012 y Nº 1132 de fecha 13 de
diciembre de 2018.
Por ello,
EL SUPERINTENDENTE DE SERVICIOS DE SALUD
RESUELVE:
ARTÍCULO 1º - Sustitúyese el Anexo I (IF-2019-79390151-APN-SGE#SSS) de
la Resolución Nº 1284/19-SSSALUD, por el Anexo I -
IF-2019-88077350-APN-SGE#SSS que forma parte integrante de la presente.
ARTÍCULO 2º - Sustitúyese el Anexo II (IF-2019-79391270-APN-SGE#SSS) de
la Resolución Nº 1284/19-SSSALUD, por el Anexo II -
IF-2019-88081758-APN-SGE#SSS que forma parte integrante de la presente.
ARTÍCULO 3º - Sustitúyese el Anexo III (IF-2019-79391709-APN-SGE#SSS)
de la Resolución Nº 1284/19-SSSALUD, por el Anexo III -
IF-2019-88084569-APN-SGE#SSS que forma parte integrante de la presente.
ARTÍCULO 4º - Instrúyase a la Gerencia de Sistemas de información del
Organismo a adecuar los conceptos a reconocer por el SISTEMA ÚNICO DE
REINTEGRO (SUR).
ARTIÍCULO 5º - Regístrese, comuníquese, publíquese, dése a la DIRECCIÓN
NACIONAL DEL REGISTRO OFICIAL y oportunamente, archívese. Sebastián
Nicolás Neuspiller
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la edición web del BORA -www.boletinoficial.gob.ar-
e. 16/10/2019 N° 78405/19 v. 16/10/2019
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
Anexo I
Protocolo de recupero
Se define infección por VIH la que presenta un paciente adulto o niño
mayor a 18 meses en quien se determine al menos una prueba de tamizaje
(por metodología ELISA, aglutinación de partículas o test rápido)
positiva para VIH con un test confirmatorio por carga viral. El uso de
Western Blot u otros estudios de tipo de los inmunoensayos de línea
debe limitarse a situaciones puntuales.
En niños menores de 18 meses se considera el diagnóstico con dos pruebas de PCR positivas para VIH.
Fundamento terapéutico general:
Debe ofrecerse el tratamiento antirretroviral a todas las personas con
infección por VIH, independientemente del recuento de células CD4. El
tratamiento antirretroviral debe iniciarse lo más pronto posible.
Prestaciones incluidas en el módulo:
Una vez se ha tomado la decisión de iniciar el tratamiento
antirretroviral, la elección del esquema a utilizar debe seguir las
recomendaciones vigentes de las guías de práctica clínica, tanto
nacionales, como internacionales, y adecuarse a la situación vital de
cada persona para garantizar la adherencia al mismo. A modo de ejemplo
pueden citarse las siguientes especificaciones:
En el momento de la elección del esquema deben considerarse las
comorbilidades del paciente, edad, estado HLA B5701 (solo cuando se
utilice abacavir), embarazo, test de resistencia cuando esté indicado,
y/o contraindicaciones específicas de los medicamentos.
Para el inicio del Terapia Antiretroviral (TARV) se recomienda una
combinación de uno o dos inhibidores nucleosídicos de la transcriptasa
inversa (INTI), asociados a otro antirretroviral de alguna de las
siguientes clases, preferentemente utilizando combinaciones de dosis
fijas una vez al día:
- Un inhibidor no nucleosídico de la transcriptasa inversa (INNTI)
- Un inhibidor de la proteasa potenciado con ritonavir (IP/r) o cobicistat (IP/c)
- Un inhibidor de la transferencia de cadena mediada por integrasa (INSTI)
Fallo de tratamiento: se define como fallo virológico a la presencia de
carga viral (CV) plasmática por encima del límite de detección después
de al menos 24 semanas de tratamiento. Este dato debe ser confirmado en
2 muestras consecutivas. Si la carga viral plasmática es muy elevada
antes del inicio del TARV puede requerirse más de 24 semanas para
lograr la no detectabilidad. También constituye fallo virológico cuando
la CV aumenta por encima del límite de detección luego de haber
alcanzado la no detectabilidad, dato que requiere también confirmación
con una segunda muestra. Se considera fallo al valor de CV mayor a 200
copias/ml.
El esquema utilizado después del primer fallo y subsiguientes,
dependerá del test de resistencia y de la historia de drogas
antirretrovirales utilizadas. Se considerará como fallo virológico a la
situación clínica donde la carga viral y la historia clínica lo
confirmen, aun sin la disponibilidad del test de resistencia, cuando
dicha situación sea justificada por causales válidas. La condición de
multifallo solo podría ser considerada a partir de un segundo fallo.
Resulta fundamental en todas las situaciones el chequeo de la correcta adherencia.
El cambio de TARV en pacientes con Carga Viral suprimida (no
detectable), puede ser realizado luego de objetivar al menos 6 meses de
carga viral no detectable. Puede responder a diferentes motivos
incluyendo:
- Simplificación: utilización de un esquema de menos comprimidos o menor dosis
- Intolerancia o toxicidad: Se modifica la droga a la que se atribuye la intolerancia o toxicidad y se la reemplaza.
- Interacciones medicamentosas
- Embarazo
En todos estos casos, en los cuales el cambio se realiza con carga viral suprimida, no se requiere test de resistencia.
Anexo II
Fundamento terapéutico
Módulo A
Drogas base del esquema
- Abacavir (ABC)
- Emtricitabina (FTC)
- Lamivudina (3TC)
- Tenofovir alafenamida (TAF)
- Tenofovir fumarato (TDF)
Módulo B.1
Drogas base del esquema
- Atazanavir
- Lopinavir/Ritonavir
- Bictegravir Darunavir
- Dolutegravir
- Doravirina
- Elvitegravir
- Raltegravir
- Rilpivirina
- Cobicisistat *
- Ritonavir *
*Para asociar con Inhibidores de la Proteasa
Módulo B.2
Drogas base del esquema
- Efavirenz
- Nevirapina
Todo esquema de tratamiento debe incluir drogas del módulo A asociadas
a las del módulo B.1 o B.2, por lo cual se reintegrará,
independientemente de si las drogas están co-formuladas o no,
exclusivamente la suma de los módulos (A + B.1) o (A + B.2).
Módulo C: Multifallo
Para el caso de esquemas de multifallo, se reconocerán las siguientes
drogas, que deberán reintegrarse adicionalmente a los módulos
previamente descriptos (A+B.1) o (A + B.2).
- Dolutegravir (doble dosis)
- Etravirina (ETV)
- Maraviroc (MRV)
MÓDULO D: Transmisión Vertical
Se reconocerán las acciones implementadas durante el parto, periparto y
seguimiento del recién nacido para evitar el contagio del mismo.
Prestaciones incluidas:
1) Antiretrovirales de administración en el parto y tratamiento del recién nacido.
Fundamento terapéutico:
- Intraparto: Iniciar AZT endovenoso en el inicio del trabajo de parto
o desde 2 a 3 horas antes de la cesárea. Puede administrarse también
según situación específica 3TC + NVP.
- Neonato:
Bajo riesgo (Madre adherente en TARV, con CV < 50 copias/ml): AZT durante las primeras 4 semanas de vida.
Moderado riesgo (Madre en TARV con CV > 50 copias o desconocida):
AZT por 6 semanas + NPV los días 0, 2 y 6 de vida + 3TC por 7 días
Alto riesgo: (Madres sin TARV, que sólo recibieron profilaxis o con
infección aguda intraembarazo): AZT + 3TC + NVP por 4 semanas
2) PCR de seguimiento del recién nacido.
MODULO E: Enfermedades oportunistas
El tratamiento y profilaxis que será reconocido tendrá una duración mínima de 30 (treinta) días y una máxima de 12 (doce) meses.
Se otorgará reintegro para las siguientes drogas según presentación como unidad de medida:
- Anfotericina liposomal
- Valganciclovir
- Foscarnet
- Rifabutina
Documentación específica a presentar (para todos los módulos)
- Prescripción médica firmada y sellada por médico tratante y médico
auditor, correspondiente al mes de la prestación que se solicita el
reintegro.
- Documentación para trazabilidad de medicamentos según resoluciones
vigente. Comprobante de dispensa donde figura la trazabilidad de los
medicamentos.
- En caso de modificación del esquema de tratamiento, se deberá justificar la causa del mismo.
- En el caso del Módulo D, se deberá adjuntar Resumen de Historia
Clínica del perinatal con datos de seguimiento del recién nacido,
firmado y sellado por médico tratante y auditor.
- En el caso del Módulo E, se deberá adjuntar la documentación que
acredite el compromiso de infección oportunista. Planilla donde se
constate la justificación del uso de la medicación solicitada, con
fecha de inicio, dosis en función de unidad de tiempo (semanal o
mensual) y fecha de suspensión.
Anexo III
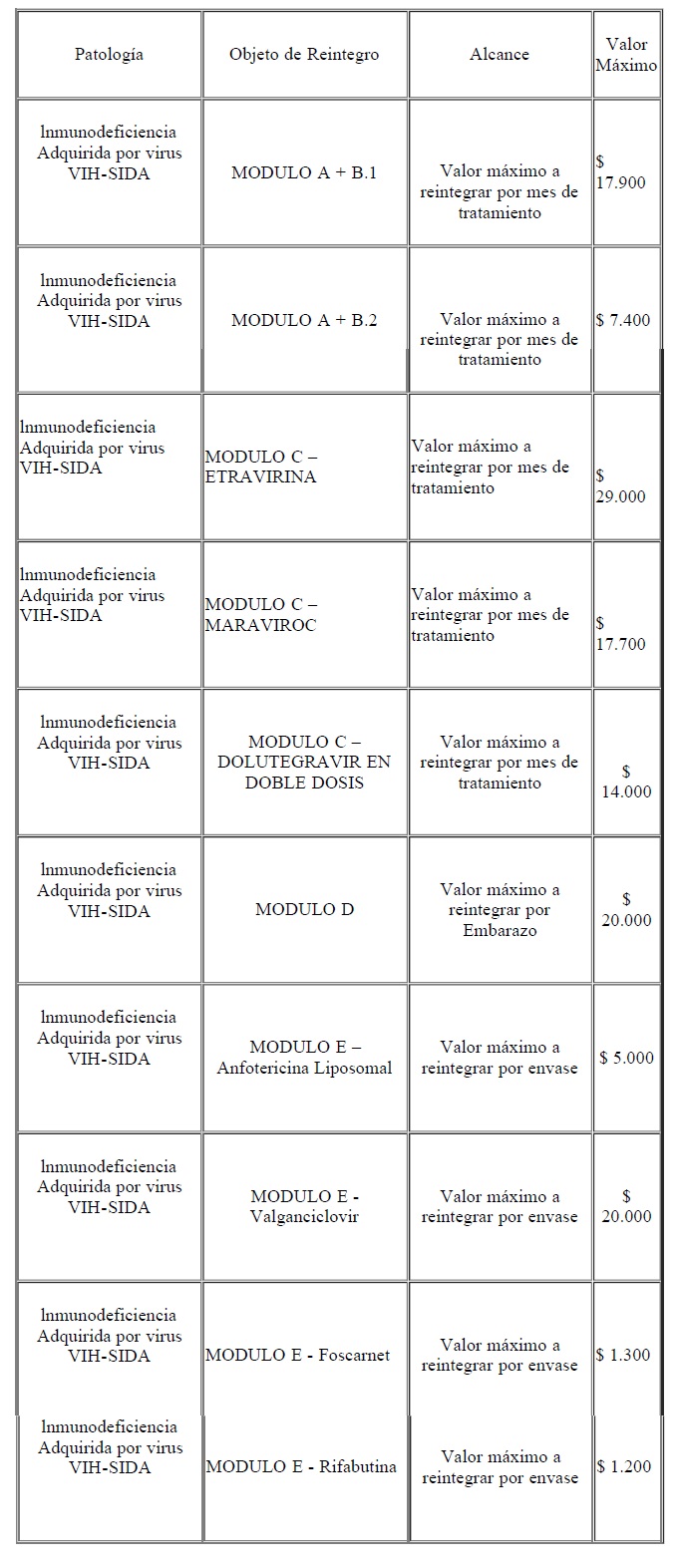
Valores de recupero por tratamiento VIH
El valor máximo a recuperar por módulo incluye a la totalidad de drogas
incluidas en el mismo. Se recuperará el valor de la suma del esquema
comprendido por la suma de los módulos A+B.1 o A+B.2 de acuerdo a las
drogas involucradas.
El valor de los módulos incluye un prorrateo del valor de 2 cargas
virales y recuentos de CD4 anuales para cada afiliado, y eventuales
test de resistencia.
Para el caso del módulo C, multifallo, se adicionará el monto
correspondiente a cada droga utilizada al valor máximo del esquema
A+B.1 o A+B.2.