ADMINISTRACIÓN
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
Disposición 9708/2019
DI-2019-9708-APN-ANMAT#MSYDS
Ciudad de Buenos Aires, 29/11/2019
VISTO la Ley Nº 16.643, sus Decretos Reglamentarios Nros. 9763/64,
150/92 (T.O 1993), las Disposiciones ANMAT Nº 3185/99 con sus
complementarias y modificatorias, 5040/06 y sus modificatorias, 758/09,
4132/12, 8255/17, 5068/19 y el EX-2019-89229904-APN-ANMAT#MSYDS de la
Administración Nacional de Medicamentos, Alimentos y Tecnología Médica;
y
CONSIDERANDO:
Que por Disposición ANMAT Nº 3185/99 se aprobó la Guía “Cronograma para
exigencia de estudios de equivalencia entre medicamentos de riesgo
sanitario significativo” que incluye recomendaciones para la
realización de estudios de bioequivalencia, y estableció un cronograma
de implementación gradual, comenzando por ingredientes farmacéuticos
activos (IFAs) caracterizados como de riesgo sanitario significativo.
Que mediante disposiciones posteriores, la ANMAT ha ido incorporando
ingredientes farmacéuticos activos a la obligatoriedad de demostración
de bioequivalencia.
Que en la Disposición ANMAT Nº 3185/99 se establecen los métodos
idóneos para demostrar equivalencia terapéutica a los estudios de
bioequivalencia y los de disolución comparativa.
Que en la Disposición ANMAT N° 758/09 se establecieron los requisitos
necesarios para reemplazar los estudios de bioequivalencia por estudios
de disolución comparativos basados en el Sistema de Clasificación
Biofarmacéutica.
Que la mencionada Disposición establece que sólo los IFA pertenecientes
a la categoría I y III de la Clasificación Biofarmacéutica son pasibles
de solicitar bioexención.
Que por Disposición ANMAT N° 4132/12 se establecieron las exigencias de
demostración de bioequivalencia para todas las concentraciones de una
especialidad medicinal sólida oral que contenga alguno de los IFA con
requerimiento de bioequivalencia.
Que por Disposición ANMAT N° 5068/19 se aprobó la Guía para la
Solicitud de Bioexención que establece los lineamientos operativos para
la demostración de bioequivalencia por bioexención.
Que en el mercado local existen especialidades medicinales que
contienen IFA que pueden ser tomados como referencia para la
realización de estos estudios.
Que las propiedades biofarmacéuticas de las especialidades medicinales
que contienen los IFAs considerados como candidatos bioexceptuables
pueden ser caracterizados en el marco de la Disposición ANMAT Nº 758/09.
Que la Dirección de Asuntos Jurídicos ha tomado la intervención de su
competencia.
Que se actúa en virtud de las facultades conferidas por los Decretos Nº
1490/92 y sus modificatorios.
Por ello;
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACIÓN NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
DISPONE:
ARTÍCULO 1º.- Incorpóranse a la exigencia de realización de estudios de
Bioequivalencia establecida por la Disposición ANMAT Nº 3185/99, a los
ingredientes farmacéuticos activos Alprazolam, Bisoprolol, Pregabalina,
Memantina y Enalapril.
ARTÍCULO 2º.- De cumplir con los requisitos establecidos en las
Disposiciones ANMAT Nº 758/09 y Nº 5068/19 o las que en un futuro las
complementen o reemplacen, el laboratorio titular podrá optar por
solicitar la bioexención de estudios in vivo para las especialidades
medicinales en sus formas farmacéuticas sólidas orales de liberación
inmediata cuyos IFA se mencionan en el artículo 1° de la presente
disposición.
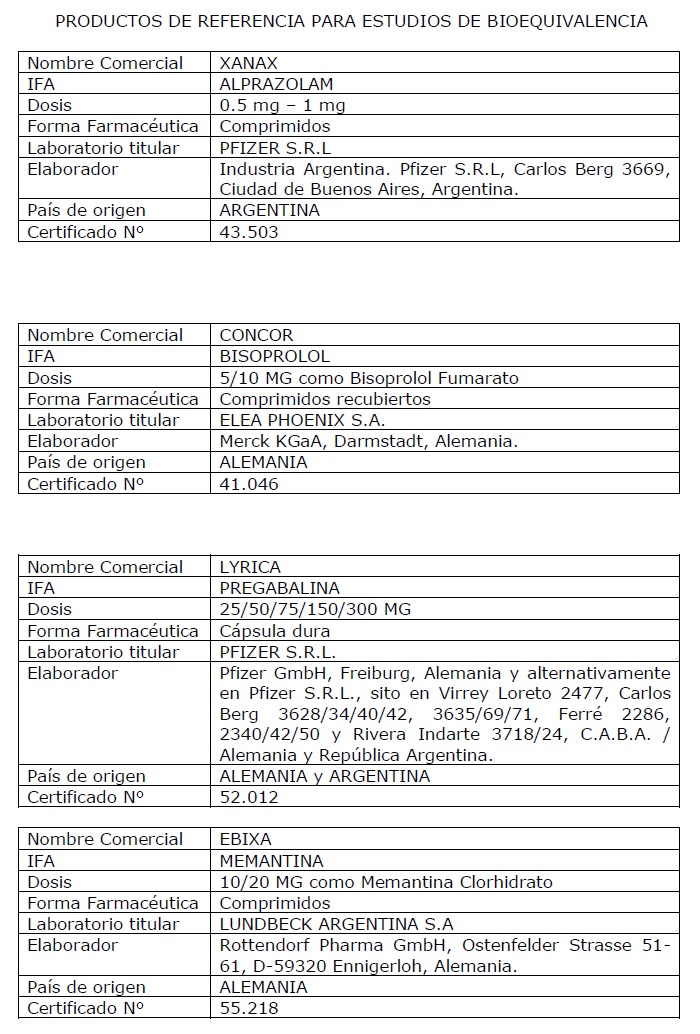
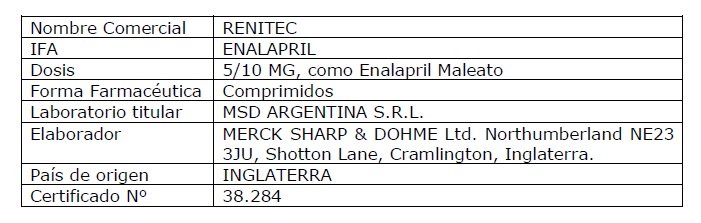
ARTÍCULO 3º.- Establécense como productos de referencia a los
enumerados en el Anexo I (IF-2019-89234562-APN-ANMAT#MSYDS) que forma
parte integrante de la presente disposición.
ARTÍCULO 4º.- Las solicitudes de bioexención de estudios in vivo para
los IFAs indicados en el artículo 1° de la presente disposición,
deberán realizarse de acuerdo a los requisitos de la Disposición ANMAT
Nº 5068/19, o la que en un futuro complemente o reemplace, en los
plazos allí establecidos.
ARTÍCULO 5º.- Para los laboratorios titulares de especialidades
medicinales con bioequivalencia demostrada para una de sus
concentraciones y que posean más de una concentración comercializada,
deberán cumplimentar las Disposiciones ANMAT Nº 758/09 y N° 4132/12, o
las que en un futuro complementen o reemplacen, presentando los
protocolos de solicitud de bioexención para todas las concentraciones,
según Disposición ANMAT Nº 5068/19, o la que en un futuro completamente
o reemplace.
ARTÍCULO 6º.- En caso que los resultados de los estudios in vitro no
hayan demostrado bioequivalencia con el producto de referencia esta
Administración Nacional evaluará la posibilidad de solicitar los
estudios in vivo correspondientes.
ARTÍCULO 7°.- Derógase la Disposición ANMAT N° 4788/12.
ARTÍCULO 8°.- La presente disposición entrará en vigencia a partir del
día siguiente al de su publicación en el Boletín Oficial.
ARTÍCULO 9°.- Regístrese. Dése a la Dirección Nacional del Registro
Oficial para su publicación. Dése a la Coordinación de Gestión de
Optimización y Modernización de Procesos, a la Dirección de Gestión de
Información Técnica, al Instituto Nacional de Medicamentos y a la
Dirección de Relaciones Institucionales. Comuníquese a las Cámaras de
la industria farmacéutica CILFA, CAEME, COOPERALA, CAPGEN y CAPEMVEL,
SAFyBI. Cumplido archívese. Carlos Alberto Chiale
NOTA: El/los Anexo/s que integra/n este(a) Disposición se publican en
la edición web del BORA -www.boletinoficial.gob.ar-
e. 03/12/2019 N° 93094/19 v. 03/12/2019
(Nota
Infoleg: Los anexos referenciados en la presente norma han sido
extraídos de la edición web de Boletín Oficial.)
ANEXO
I
Hoja
Adicional de Firmas
Anexo
Número:
IF-2019-89234562-APN-ANMAT#MSYDS
CIUDAD DE BUENOS AIRES
Martes 1 de Octubre de 2019
Referencia: Productos de
Referencia para Estudios de BE
El documento fue importado por el sistema GEDO con un total de 2
pagina/s.