ANEXO I
MERCOSUR/GMC/RES. N° 15/19
REQUISITOS
ZOOSANITARIOS DE LOS ESTADOS PARTES PARA LA
IMPORTACIÓN DE EMBRIONES CAPRINOS
RECOLECTADOS IN VIVO
(DEROGACIÓN DE LA RESOLUCIÓN GMC N°
47/14)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común y la Resolución N° 47/14 del Grupo Mercado Común.
CONSIDERANDO:
Que por la Resolución GMC N° 47/14 fueron aprobados los Requisitos
Zoosanitarios de los Estados Partes del MERCOSUR para la importación de
embriones caprinos recolectados in vivo.
Que han sido motivo de revisión los requisitos zoosanitarios de los
Estados Partes para la importación de caprinos y ovinos para
reproducción y engorde, lo cual genera la necesidad de la actualización
en paralelo de algunos puntos de los requisitos zoosanitarios para la
importación de embriones caprinos recolectados in vivo establecidos
mediante la Resolución GMC N° 47/14.
Que se considera más oportuno y conveniente reemplazar la citada
Resolución actualizando solo los puntos divergentes entre los
requisitos para importación de animales en pie y aquellos para material
genético, en vistas de una futura actualización integral.
Que la armonización de los requisitos zoosanitarios del MERCOSUR
elimina los obstáculos que se generan por las diferencias de las
regulaciones nacionales vigentes, dando cumplimiento a lo establecido
en el Tratado de Asunción.
Que es necesario proceder a la actualización de los requisitos
indicados, de acuerdo con las recientes modificaciones de las normas
internacionales de referencia de la Organización Mundial de Sanidad
Animal (OIE).
EL
GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos Zoosanitarios de los Estados Partes
para la importación de embriones caprinos recolectados in vivo" que
constan como Anexo I, así como el modelo de Certificado Veterinario
Internacional (CVI) que consta como Anexo II, los cuales forman parte
de la presente Resolución.
Art. 2 - Los Estados Partes indicarán en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8) los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 3 - Derogar la Resolución GMC N° 47/14.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento
jurídico de los Estados Partes antes del 01/1/2020.
CXII GMC - Buenos Aires, 05/VI/19.
IF-2019-97350659-APN-DNMAI#MPYT
ANEXO
I
REQUISITOS ZOOSANITARIOS DE LOS
ESTADOS PARTES PARA LA
IMPORTACIÓN DE EMBRIONES CAPRINOS
RECOLECTADOS IN VIVO
CAPÍTULO I
DISPOSICIONES GENERALES
Art. 1 - Toda importación de embriones caprinos deberá estar acompañada
del Certificado Veterinario Internacional (CVI), emitido por la
Autoridad Veterinaria del país exportador.
El país exportador deberá elaborar el modelo de CVI que será utilizado
para la exportación de embriones caprinos a los Estados Partes del
MERCOSUR, incluyendo las garantías zoosanitarias que constan en la
presente Resolución, para su previa autorización por el Estado Parte
importador.
Art. 2 - El Estado Parte importador considerará para el CVI una validez
de treinta (30) días corridos a partir de la fecha de su emisión.
Art. 3 - Las pruebas diagnósticas deberán ser realizadas en
laboratorios oficiales, habilitados, acreditados o reconocidos por la
Autoridad Veterinaria del país de origen de los embriones. Estas
pruebas deberán ser realizadas de acuerdo con el Manual Terrestre de la
Organización Mundial de Sanidad Animal (OIE).
Art. 4 - La toma de muestras para la realización de las pruebas
diagnósticas establecidas en la presente Resolución deberá ser
supervisada por un veterinario oficial o por el veterinario autorizado
por la Autoridad Veterinaria.
Art. 5 - En el punto de salida del país exportador, la Autoridad
Veterinaria realizará una inspección en el momento del embarque,
certificando la integridad de los contenedores criogénicos y de los
precintos correspondientes, conforme a lo establecido en la presente
Resolución.
Art. 6 - El Estado Parte importador podrá acordar con la Autoridad
Veterinaria del país exportador otros procedimientos o técnicas de
diagnóstico, que otorguen garantías equivalentes para la importación.
Art. 7 - El país o zona de origen de los embriones a exportar que sea
reconocido oficialmente por la OIE como libre, o el país, zona o el
establecimiento de origen de los embriones, que cumpla con las
condiciones del Código Terrestre de la OIE para ser considerado libre
de alguna de las enfermedades para las cuales se requieran pruebas
diagnósticas o vacunaciones, podrá ser exceptuado de la realización de
las mismas. En ambos casos, deberá contar con el reconocimiento de
dicha condición por el Estado Parte importador. de dicha condición por
el Estado Parte importador.
La condición de país, zona o establecimiento libre de las enfermedades
en cuestión deberá ser incluida en el CVI.
Art. 8 - El Estado Parte importador que posea un programa oficial de
control o erradicación para cualquier enfermedad no contemplada en la
presente Resolución, se reserva el derecho de requerir medidas de
protección adicionales, con el objetivo de prevenir el ingreso de esa
enfermedad al país.
Art. 9 - Además de las exigencias establecidas en la presente
Resolución, deberá cumplirse con los "Requisitos zoosanitarios
adicionales de los Estados Partes para la importación de semen y
embriones de rumiantes con relación a la enfermedad de Schmallenberg",
según lo establecido en la Resolución GMC N° 45/14, sus modificatorias
y/o complementarias.
Art. 10 - Los procedimientos requeridos para el cumplimiento de la
presente Resolución deberán ajustarse a las recomendaciones de la OIE
con respecto al bienestar animal.
CAPÍTULO
II
DEL PAÍS EXPORTADOR
Art. 11 - Durante el período de recolección de los embriones a ser
exportados, el país exportador deberá cumplir con lo establecido en los
capítulos correspondientes del Código Terrestre de la OIE para ser
considerado un país libre de Peste de los Pequeños Rumiantes, Viruela
Ovina y Caprina, Pleuroneumonía Contagiosa Caprina y dicha condición
debe ser reconocida por el Estado Parte importador.
Art. 12 - Con respecto a Fiebre Aftosa:
12.1 - Si el país o zona del país exportador es reconocido por la OIE
como libre de Fiebre Aftosa sin vacunación:
Las donantes no deberán haber manifestado ningún signo clínico de
Fiebre Aftosa el día de la recolección de embriones ni durante los
treinta (30) días posteriores a dicha recolección, y
Deberán haber permanecido durante por los menos los tres (3) meses
anteriores a la recolección de los embriones en un país o una zona
libre de Fiebre Aftosa sin vacunación, o
12.2 - Si el país o zona del país exportador es reconocido por la OIE
como libre de Fiebre Aftosa con vacunación:
Las donantes no deberán haber manifestado ningún signo clínico de
Fiebre Aftosa el día de la recolección de los embriones ni durante los
treinta (30) días posteriores a dicha recolección, y
Deberán haber permanecido en un país o zona libre de Fiebre Aftosa,
durante por los menos los tres (3) meses anteriores a la recolección de
los embriones, o
12.3 - Si el país o zona del país exportador no cuenta con el
reconocimiento de libre de Fiebre Aftosa, deberán realizarse las
pruebas diagnósticas relativas a Fiebre Aftosa descriptas en el
Capítulo VI - De las Pruebas de Diagnóstico - del presente Anexo.
Art 13 - Con relación a Prurigo Lumbar (Scrapie):
13.1 - El país exportador deberá declararse libre de Prurigo Lumbar
(Scrapie) ante la OIE de acuerdo con lo establecido en el Código
Terrestre de la OIE y dicha condición deberá ser reconocida por el
Estado Parte importador.
13.2 - Las donantes y su ascendencia directa nacieron y fueron criadas
en el país exportador o en otro país con igual condición sanitaria
respecto a Prurigo Lumbar (Scrapie).
13.3 - Es facultad de un Estado Parte importador permitir, considerando
su
condición sanitaria y su evaluación de riesgo, la importación de
embriones caprinos originarios o procedentes de países que no se
declaren libres de Prurigo Lumbar (Scrapie) o que no sean reconocidos
como libres por dicho Estado Parte, siempre que conste en el CVI que
los embriones son originarios de donantes que:
a) nacieron y fueron criadas en un compartimiento o explotación libre
de Prurigo Lumbar (Scrapie) de acuerdo a lo definido en el Capítulo
correspondiente del Código Terrestre de la OIE, y
b) no son descendientes ni hermanas de caprinos afectados por Prurigo
Lumbar (Scrapie), y
c) son originarias de un país exportador que adopta las medidas
recomendadas por el Código Terrestre de la OIE, para el control y
erradicación del Prurigo Lumbar (Scrapie).
13.4. - El Estado Parte que adopte las condiciones establecidas en el
punto 13.3 deberá informarlo previamente a los demás Estados Partes.
CAPÍTULO
III
DEL EQUIPO DE RECOLECCIÓN Y DEL
LABORATORIO DE MANIPULACIÓN
DE EMBRIONES
Art. 14 - El equipo de recolección y el laboratorio de manipulación de
embriones deberá estar aprobado y supervisado por la Autoridad
Veterinaria del país exportador.
Art. 15 - Para aprobar los equipos de recolección y laboratorios de
manipulación de embriones, la Autoridad Veterinaria del país exportador
deberá considerar las "Condiciones aplicables al equipo de recolección
de embriones", así como las "Condiciones aplicables a los laboratorios
de manipulación", descriptas en el Código Terrestre de la OIE.
Art. 16 - Los embriones deberán ser recolectados y procesados bajo la
supervisión del veterinario autorizado del equipo de recolección de
embriones.
Art. 17 - Al momento de la recolección, el laboratorio de manipulación
de embriones no podrá estar localizado ni el equipo de recolección
podrá actuar en zonas con restricciones sanitarias relativas a las
enfermedades de caprinos, cuya transmisión pueda ocurrir por medio de
los embriones.
CAPÍTULO
IV
DE LAS DONANTES DE LOS EMBRIONES
Art. 18 - Las donantes deberán haber nacido y haber sido criadas en el
país exportador o haber permanecido en dicho país por lo menos noventa
(90) días anteriores a la recolección de los embriones. En caso de
animales importados, el país exportador deberá cumplir con lo
establecido en los Capítulos II - Del País Exportador - y V - De los
Establecimientos de Recolección - del presente Anexo, en lo referente a
la importación de esas donantes.
Art. 19 - Las donantes no deberán haber presentado síntomas ni signos
de enfermedades infectocontagiosas propias de la especie durante al
menos treinta (30) días antes y treinta (30) días posteriores a la
recolección.
CAPÍTULO
V
DE LOS ESTABLECIMIENTOS DE RECOLECCIÓN
Art. 20 - Las donantes deberán haber permanecido al menos treinta (30)
días antes y treinta (30) días posteriores a la recolección, en un
establecimiento que reúna las siguientes condiciones:
20.1 - Que no esté localizado en zonas con restricciones sanitarias
relativas a las enfermedades de los caprinos, cuya transmisión pueda
ocurrir por medio de los embriones.
20.2 - Que no haya habido ingreso de animales susceptibles de
enfermedades de los caprinos, que tuviesen una condición sanitaria
inferior.
20.3 - Que no se hayan reportado oficialmente casos de Artritis
Encefalitis
Caprina (CAE) y Fiebre del Valle del Rift en los tres (3) años previos
a la recolección de embriones.
20.4 - Que no se hayan reportado oficialmente casos de Aborto Enzoótico
de las ovejas (Chlamydophila abortus) y Adenomatosis pulmonar ovina en
los dos (2) años previos a la recolección de embriones.
20.5 - Que no se hayan reportado oficialmente casos de Fiebre Q en los
doce (12) meses previos a la recolección de embriones.
20.6 - Que no se hayan reportado oficialmente casos de Agalactia
contagiosa, Brucelosis (Brucella abortus y B melitensis), Tuberculosis,
y Lengua Azul durante los seis (6) meses previos a la recolección de
embriones.
20.7 - Que no se hayan reportado oficialmente casos de Estomatitis
vesicular en los veintiún (21) días previos a la recolección.
Art. 21- Las donantes deberán haber sido inseminadas con semen que
reúne las condiciones sanitarias establecidas por el MERCOSUR para la
importación de semen caprino.
CAPÍTULO
VI
DE LAS PRUEBAS DE DIAGNÓSTICO
Art. 22 - Con respecto a Fiebre del Valle del Rift:
22.1 - Las donantes deberán ser sometidas a dos (2) pruebas de Virus
Neutralización, siendo la primera realizada dentro de los treinta (30)
días previos a la recolección de embriones a ser exportados y la
segunda entre los veintiún (21) y los sesenta (60) días posteriores a
la última recolección, ambas con resultado negativo, o
22.2 - En el caso de donantes vacunadas, los resultados de las pruebas
deberán demostrar estabilidad o reducción de títulos. Cuando se
utilicen vacunadas atenuadas, esta inmunización no deberá realizarse
durante el período de recolección de embriones ni dentro de los dos (2)
meses previos al inicio de esa recolección, previos al inicio de esa
recolección.
La certificación de la vacunación deberá constar en el CVI.
Art. 23 - Para las donantes que provengan de un país o zona no
reconocida por la OIE como libre de Fiebre Aftosa:
23.1 - En el caso de donantes vacunadas contra Fiebre Aftosa,
presentaron resultado negativo a una prueba contemplada en el Manual
Terrestre de la OIE para la detección de proteínas no estructurales.
23.2 - En el caso de donantes no vacunadas contra Fiebre Aftosa,
presentaron resultado negativo a una prueba de ELISA o Virus
Neutralización para anticuerpos estructurales de los serotipos
presentes en el país exportador.
Art. 24 - Las donantes deberán ser sometidas, entre los veintiún (21) y
sesenta (60) días posteriores a la última recolección de embriones a
ser exportados, salvo otra indicación, y presentar resultados negativos
a las pruebas de diagnóstico para las siguientes enfermedades:
ARTRITIS ENCEFALITIS CAPRINA (CAE):
ELISA o Inmunodifusión en Gel de Agar (AGID).
ABORTO ENZOÓTICO DE LAS OVEJAS:
Fijación de Complemento o ELISA.
BRUCELOSIS (B. abortus y B.
melitensis): Antígeno Acidificado Tamponado (AAT) o Rosa de Bengala o
ELISA.
En caso de resultado positivo, podrán ser sometidas a Fijación de
complemento o 2- mercaptoetanol.
LENGUA AZUL: Inmunodifusión en
Gel de Agar (AGID) o ELISA para la detección de anticuerpos contra el
grupo del virus de la Lengua Azul o Polymerase Chain Reaction (PCR) o
Aislamiento viral.
En caso de PCR o Aislamiento viral, la prueba deberá ser realizada el
día de la recolección de los embriones.
CAPÍTULO
VII
DE LA RECOLECCIÓN, PROCESAMIENTO Y
ALMACENAMIENTO
Art. 25 - Los embriones deberán ser recolectados, procesados y
almacenados en el país exportador de acuerdo con las recomendaciones
establecidas en el Código Terrestre de la OIE y en el Manual de la
Sociedad Internacional de Transferencia de Embriones (IETS). En todos
los casos se utilizará el protocolo, que incluye los lavados con
tripsina, contemplado en dicho Manual.
Art. 26 - En el CVI deberá constar que efectivamente después de los
lavados, la zona pelúcida de cada embrión fue examinada en su
superficie, usando microscopio con aumento no menor de 50X,
encontrándose intacta y libre de material adherente.
Art. 27 - Todos los productos biológicos de origen animal utilizados en
la recolección, procesamiento y almacenamiento de los embriones,
deberán estar libres de microorganismos patógenos. Solamente podrá ser
utilizado suero fetal bovino, albúmina sérica o cualquier otro producto
de origen de rumiantes cuando procedan de países reconocidos por la OIE
como de riesgo insignificante o de riesgo controlado y sin registro de
casos, con relación a Encefalopatía Espongiforme Bovina.
Art. 28 - Los embriones deberán ser almacenados en contenedores
criogénicos nuevos o lavados y desinfectados, conteniendo nitrógeno
líquido de primer uso, por un período mínimo de treinta (30) días
anteriores al embarque. Durante ese período, ninguna evidencia clínica
de enfermedades transmisibles deberá haber sido registrada en el
establecimiento donde los embriones fueron recolectados ni en las
donantes.
CAPÍTULO
VIII
DEL PRECINTO
Art. 29 - En el momento previo a la salida del establecimiento o
depósito, el contenedor criogénico conteniendo los embriones a
exportar, deberá ser precintado bajo supervisión de la Autoridad
Veterinaria del país exportador y el número de precinto deberá constar
en el CVI.
CAPÍTULO
IX
DISPOSICIONES GENERALES
Art. 30 - El no cumplimiento de los términos de la presente Resolución
permitirá a la Autoridad Veterinaria del Estado Parte importador
adoptar las medidas correspondientes, de acuerdo con la normativa
vigente en cada Estado Parte.
ANEXO
II
MODELO
DE CERTIFICADO VETERINARIO INTERNACIONAL PARA LA
IMPORTACIÓN DE EMBRIONES
CAPRINOS RECOLECTADOS IN VIVO
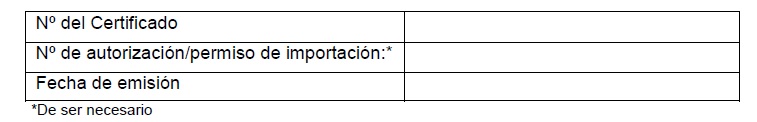
Conforme Resolución GMC N° 15/19
El presente Certificado Veterinario Internacional (CVI) para la
Exportación de Embriones de Caprinos Recolectados In Vivo a los Estados
Partes del MERCOSUR tendrá una validez de treinta (30) días corridos a
partir de la fecha de su emisión.
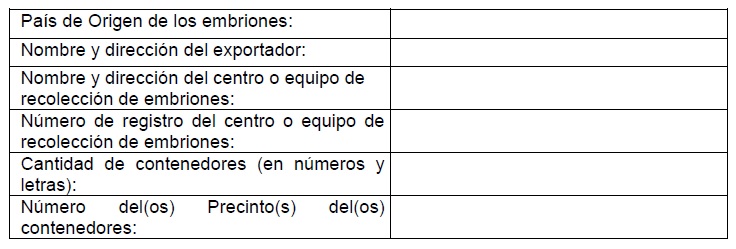
I. PROCEDENCIA:
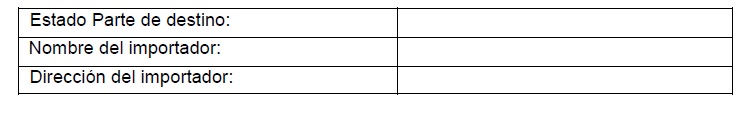
II. DESTINO:
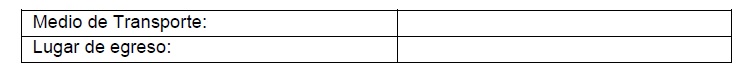
III. TRANSPORTE:
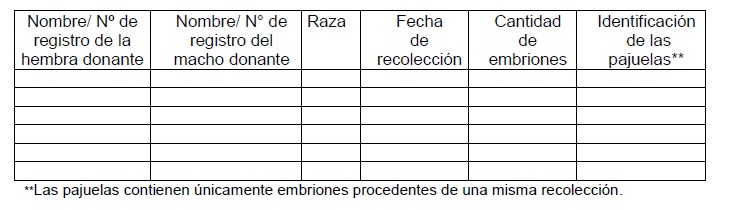
IV. INFORMACIONES REFERENTES A LOS EMBRIONES DE CADA DONANTE:
V. INFORMACIONES ZOOSANITARIAS
Deberán ser detalladas las informaciones que constan en los Capítulos
II, III, IV, V y VII de la referida Resolución sobre "Requisitos
Zoosanitarios de los Estados Partes para la importación de embriones
caprinos recolectados in vivo".
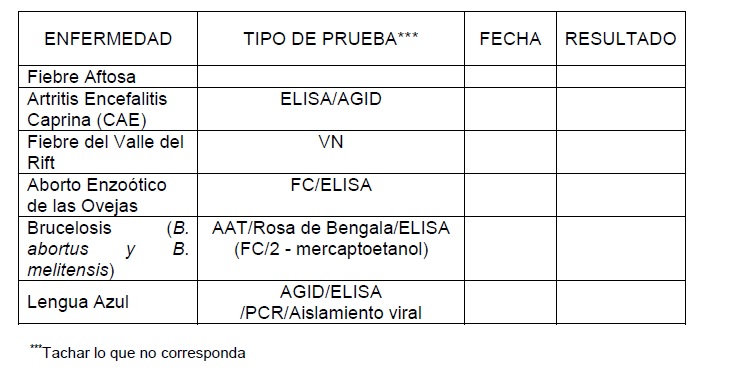
VI. PRUEBAS DIAGNÓSTICAS
Deberán ser detalladas las informaciones que constan en el Capítulo VI
de la referida Resolución sobre "Requisitos Zoosanitarios de los
Estados Partes para la importación de embriones caprinos recolectados
in vivo".
VII. DE LA RECOLECCIÓN, DEL PROCESAMIENTO Y DEL ALMACENAMIENTO:
Deberán ser incluidas las informaciones requeridas en el Capítulo VII
de la referida Resolución sobre "Requisitos Zoosanitarios de los
Estados Partes para la importación de embriones caprinos recolectados
in vivo".
VIII. DEL PRECINTO:
Deberán ser incluidas las informaciones que constan en el Capítulo VIII
de la referida Resolución sobre "Requisitos Zoosanitarios de los
Estados Partes para la importación de embriones caprinos recolectados
in vivo".
IF-2019-97350659-APN-DNMAI#MPYT
Hoja
Adicional de Firmas
Anexo
Número:
IF-2019-97350659-APN-DNMAI#MPYT
CIUDAD DE BUENOS AIRES
Martes 29 de Octubre de 2019
Referencia: EX-2019-56722119-
-APN-DGDMA#MPYT ANEXO I
El documento fue importado por el sistema GEDO con un total de 12
pagina/s.