SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
Resolución 1667/2019
RESOL-2019-1667-APN-PRES#SENASA
Ciudad de Buenos Aires, 09/12/2019
VISTO el Expediente Nº EX-2019-66450429- -APN-DGTYA#SENASA, la Ley N°
18.284 reglamentada a través del Decreto N° 2.126 del 30 de junio de
1971, el Decreto N° 4.238 del 19 de julio de 1968, y
CONSIDERANDO:
Que la melanosis (mancha negra) en crustáceos es consecuencia de la
actuación del sistema de profenoloxidasa presente en su hemolinfa. Esta
es una proenzima, de forma inactiva de la polifenoloxidasa que, tras un
proceso de activación por enzimas proteolíticas y/o sustancias de
origen microbiano origina la polifenoloxidasa activa, responsable de la
melanosis, permaneciendo activa durante la refrigeración, el
almacenamiento en hielo y el descongelamiento.
Que ello constituye un proceso natural producto de reacciones químicas
y, más allá de que los invertebrados que presentan esta característica
no son nocivos y no influyen sobre su sabor ni su aroma, su apariencia
es motivo de rechazo por parte de los consumidores originando
potenciales pérdidas económicas.
Que la melanosis puede prevenirse con el uso de aditivos que mejorarían
la estabilidad o la calidad de conservación de un alimento o mejoraría
sus propiedades organolépticas a condición de que no se altere la
naturaleza, sustancia o calidad del alimento de tal manera que se
induzca a error al consumidor.
Que el 4-Hexilresorcinol (4HR) es un aditivo que, con una concentración
menor que la utilizada para otros aditivos (ejemplo el sulfito) y
siempre que los residuos en la carne no excedan los DOS MILIGRAMOS POR
KILOGRAMO (2 mg/kg), previene la melanosis al actuar como inhibidor
específico de la polifenoloxidasa y que, según estudios de la Generally
Recognized As Safe (GRAS), es seguro para la salud humana y su empleo
en la industria alimenticia.
Que, en igual sentido, la opinión del Comité Científico de Alimentación
(SCF) sobre la seguridad en el uso de 4-Hexilresorcinol del 5 de marzo
de 2003, concluyó que dicho aditivo previene la melanosis en crustáceos.
Que, por su parte, la UNIÓN EUROPEA (UE) a través del Reglamento Nº
1.129 del 11 de noviembre de 2011 de la Comisión Europea, establece en
qué alimentos y de qué manera se debe usar el 4HR, y, mediante el
Reglamento Nº 231 del 9 de marzo de 2012 de la citada Comisión, se
reglamentan las especificaciones técnicas del uso del 4HR, en el marco
de las normas generales sobre el uso y especificaciones de los aditivos
aprobadas por el Reglamento Nº 1.333 del 16 de diciembre de 2008 del
Parlamento Europeo y del Consejo de la UE.
Que, en el ámbito nacional, el Código Alimentario Argentino (CAA),
aprobado por la Ley N° 18.284, reglamentada por el Decreto N° 2.126 del
30 de junio de 1971, en su Capítulo I, define como aditivo alimentario
a cualquier sustancia o mezcla de sustancias que directa o
indirectamente modifiquen las características físicas, químicas o
biológicas de un alimento, a los efectos de su mejoramiento,
preservación o estabilización, siempre que sean inocuos por sí mismos o
a través de su acción como aditivos en las condiciones de uso y su
empleo se justifique por razones tecnológicas, sanitarias,
nutricionales o psicosensoriales necesarias.
Que por el Artículo 1.392 del referido Código, se establecen las
finalidades permitidas para el uso de aditivos alimentarios, a saber:
mantener o mejorar el valor nutritivo del alimento, aumentar su
estabilidad o capacidad de conservación, incrementar la aceptabilidad
de alimentos sanos y genuinos pero faltos de atractivo, permitir la
elaboración económica y en gran escala de alimentos de composición y
calidad constante en función del tiempo.
Que, del mismo modo, en el Artículo 1.393 de dicho cuerpo normativo, se
regulan las finalidades no permitidas, a saber: enmascarar técnicas y
procesos defectuosos de elaboración y/o manipulación, provocar una
reducción considerable del valor nutritivo de los alimentos, perseguir
objetivos que puedan lograrse con prácticas licitas de fabricación,
económicamente factibles, o engañar al consumidor.
Que, en tal sentido, el Artículo 1.394 del aludido Código, indica que
la cantidad de un aditivo autorizado que se agrega a un producto
alimenticio será siempre la mínima para lograr el efecto lícito deseado.
Que, por otra parte, el Capítulo XVIII del Reglamento de Inspección de
Productos, Subproductos y Derivados de Origen Animal aprobado por el
Decreto N° 4.238 del 19 de julio de 1968, entiende por aditivos a
aquellas sustancias que carecen de valor nutritivo o agregadas sin
intención nutricia, se incorporen a los alimentos para mejorar su
presentación, sus caracteres organolépticos, su sabor o sus condiciones
de conservación.
Que, asimismo, dicha norma fija las condiciones en las que pueden
usarse los aditivos, a saber: pudieran demostrar francamente su
inocuidad para la salud humana; no afecten las condiciones higiénicas,
nutricionales y tecnológicas de los alimentos que los contuvieran y no
pudieran dar lugar a posibles fraudes; fueran exigidos como
indispensables bajo el punto de vista tecnológico o no pudieran ser
evitados o sustituidos por un producto natural de inocuidad reconocida;
y hubiera posibilidad práctica de controlarlos; y estatuye que su
composición debe ser definida y de pureza adecuada (calidad
alimentaria), teniéndose en cuenta para la autorización su denominación
científica o tecnológica y en ningún caso su marca registrada.
Que de acuerdo al Numeral 18.2.2 del Capítulo XVIII de ese cuerpo
normativo, se consideran aditivos de uso permitido los consignados en
el citado Reglamento o aquellos que en el futuro autorice el SERVICIO
NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA.
Que, en consecuencia, es posible afirmar que el aditivo 4HR se ajusta a
los requerimientos que la normativa vigente nacional establece, para
permitir su uso en crustáceos, por lo que se recomienda su
incorporación a tal fin al referido Reglamento de Inspección.
Que la Dirección de Asuntos Jurídicos ha tomado la intervención que le compete.
Que el suscripto es competente para resolver en esta instancia de
conformidad con las facultades conferidas por el Artículo 8º, inciso f)
del Decreto Nº 1.585 del 19 de diciembre de 1996, sustituido por su
similar Nº 825 del 10 de junio de 2010.
Por ello,
EL PRESIDENTE DEL SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
RESUELVE:
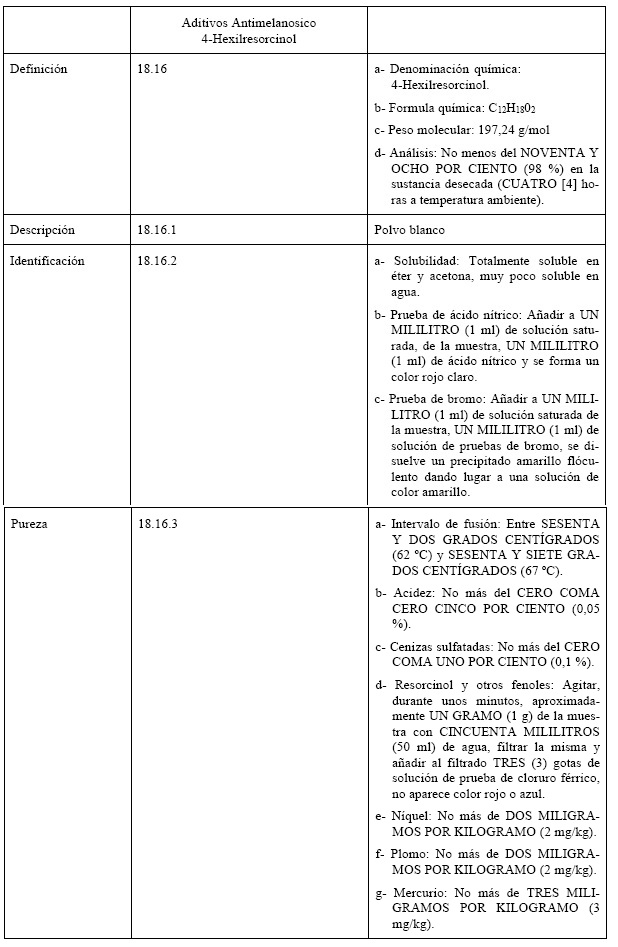
ARTÍCULO 1º.- Incorporación. Capítulo XVIII - Numeral 18.16. Se
incorpora el Numeral 18.16 al Capítulo XVIII del Reglamento de
Inspección de Productos, Subproductos y Derivados de Origen Animal,
aprobado por el Decreto N° 4.238 del 19 de julio de 1968, el que, como
Anexo I (IF-2019-107801069-APN-DNIYCA#SENASA), forma parte integrante
de la presente resolución.
ARTÍCULO 2º.- Incorporación. Capítulo XXIII - Numeral 23.12.10, inciso
9). Se incorpora el inciso 9) al Numeral 23.12.10 al Capítulo XXIII del
citado Reglamento de Inspección, el que, como Anexo II
(IF-2019-107801034-APN-DNIYCA#SENASA), forma parte integrante de la
presente resolución.
ARTÍCULO 3º.- La presente resolución entra en vigencia a partir del día siguiente al de su publicación en el Boletín Oficial.
ARTÍCULO 4º.- Comuníquese, publíquese, dese a la DIRECCIÓN NACIONAL DEL REGISTRO OFICIAL y archívese. Ricardo Luis Negri
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la edición web del BORA -www.boletinoficial.gob.ar-
e. 11/12/2019 N° 95597/19 v. 11/12/2019
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
ANEXO I
IF-2019-107801069-APN-DNIYCA#SENASA
ANEXO II
IF-2019-107801034-APN-DNIYCA#SENASA