ANEXO I
REGLAMENTO PARA EL ANÁLISIS DE RIESGO DE ORGANISMOS GENÉTICAMENTE
MODIFICADOS VEGETALES.
GENERALIDADES.
A. DEFINICIONES.
En la presente norma se entenderá por:
a) Acumulación de eventos: acumulación por cruzamiento sexual de
eventos de transformación que fueran obtenidos separadamente, como así
también la re-transformación o cotransformación que resulte en insertos
separados.
b) Agroecosistema: ecosistema manejado y/o adaptado para la producción
agrícola, pecuaria, ictícola/acuícola, pesquera, forestal y
agroindustrial.
c) Biotecnología moderna: por "biotecnología moderna" se entiende la
aplicación de: (a) Técnicas in vitro de ácido nucleico, incluidos el
ácido desoxirribonucleico (ADN) recombinante y la inyección directa de
ácido nucleico en células u orgánulos, o (b) La fusión de células más
allá de la familia taxonómica, que superan las barreras fisiológicas
naturales de la reproducción o de la recombinación y que no son
técnicas utilizadas en la reproducción y selección tradicional.
d) Construcción genética o “construcción”: segmento de ácido nucleico
constituido por DOS (2) o más secuencias contiguas de nucleótidos que
han sido combinadas por medio de técnicas in vitro de ácido nucleico,
incluidos el ácido desoxirribonucleico (ADN) recombinante.
e) Construcciones esencialmente similares: son construcciones que
comparten las mismas características de interés utilizando los mismos
mecanismos moleculares.
f) Documento de Decisión: documento técnico suscrito por la COMISIÓN
NACIONAL ASESORA DE BIOTECNOLOGÍA AGROPECUARIA (CONABIA) en el cual se
concluye el análisis de riesgo de la posible liberación comercial del
OGM vegetal en el agroecosistema.
g) Evento: evento de transformación individual, consistente en la
inserción en el genoma de una construcción genética definida. Se
considerará un mismo evento a la inserción en tándem de múltiples
copias de una misma construcción o de diferentes construcciones. En el
caso de retransformaciones o cotransformaciones que resulten en
insertos separados se considerará que el OGM vegetal resultante
contiene una acumulación de tantos eventos como insertos diferentes
existan.
h) Especie receptora: especie biológica a la que pertenece el OGM
vegetal.
i) Genoma: dotación completa de ácidos nucleicos con capacidad
replicativa de un organismo viviente y refiriéndose, según el contexto,
a las mismas moléculas de ácidos nucleicos y/o a sus secuencias
nucleotídicas. A los fines de la presente se entenderá que el genoma
vegetal incluye el ADN nuclear, plastídico y mitocondrial. Lo anterior
incluye cualquier elemento transponible o retroelemento integrado al
genoma, como así también episomas tales como los cromosomas
artificiales.
j) Inserto: fragmento de ADN insertado en el genoma vegetal.
k) Organismo donante: cualquier entidad biológica utilizada como fuente
de material genético.
l) Organismo Genéticamente Modificado (OGM): cualquier entidad
biológica capaz de transferir o replicar material genético que posea
una combinación nueva de material genético que se haya obtenido
mediante la aplicación de la biotecnología moderna.
m) Organismo parental: individuo, variedad o ecotipo vegetal que fue
objeto de una modificación genética específica para obtener un OGM
determinado.
n) Plaga: cualquier especie, raza o biotipo vegetal o animal o agente
patógeno dañino para las especies vegetales o productos vegetales.
o) Semilla: toda estructura vegetal que sea utilizada para siembra o
propagación.
p) Solicitante: persona humana o jurídica inscripta en el Registro
Nacional de Operadores con Organismos Vegetales Genéticamente
Modificados (RNOOVGM) que solicita un análisis de riesgo del OGM
vegetal en el marco de la presente medida.
q) Vector/es: agentes biológicos, moléculas de ácidos nucleicos y
medios físicos que actuaron como intermediarios en la generación e
incorporación intracelular de las construcciones presentes en el OGM.
B. CONCEPTOS GENERALES
B.1. OBJETO
El objetivo de la evaluación del riesgo, en el marco del presente
reglamento, es determinar y evaluar los posibles efectos adversos de la
liberación al agroecosistema de los OGM vegetales, incluyendo los
efectos en la conservación y utilización sostenible de la diversidad
biológica, y teniendo también en cuenta los riesgos para la salud
humana por exposición no alimentaria.
Las autoridades competentes utilizarán el análisis del riesgo para
adoptar decisiones fundamentadas en relación con la autorización
comercial de los OGM vegetales.
B.2. PRINCIPIOS
La evaluación del riesgo deberá realizarse de forma transparente y
científicamente competente, y al realizarla deberán tenerse en cuenta
el asesoramiento de los expertos y las directrices elaboradas por las
organizaciones internacionales pertinentes.
La falta de conocimientos científicos o de consenso científico no se
interpretarán necesariamente como indicadores de un determinado nivel
de riesgo, de la ausencia de riesgo, o de la existencia de un riesgo
aceptable.
Los riesgos relacionados con los OGM o sus productos deberán tenerse en
cuenta en el contexto de los riesgos planteados por la especie
receptora, o por los organismos parentales (cuando estos últimos
presenten características diferenciales relevantes respecto de su
especie) en el probable medio receptor.
La evaluación del riesgo deberá realizarse caso por caso, sobre la base
de la formulación de hipótesis de riesgo y tomando en cuenta el peso de
la evidencia. La naturaleza y el nivel de detalle de la información
requerida puede variar de un caso a otro, dependiendo del OGM de que se
trate, su uso previsto y el probable medio receptor.
B.3. METODOLOGÍA
El proceso de evaluación del riesgo puede dar origen, por una parte, a
la necesidad de obtener más información acerca de aspectos concretos,
que podrán determinarse y solicitarse durante el proceso de evaluación,
y por otra parte, a que la información sobre otros aspectos pueda
carecer de interés en algunos casos.
Para cumplir sus objetivos, la evaluación del riesgo entraña, según
proceda, las siguientes etapas:
a) Una identificación de cualquier característica genotípica y
fenotípica nueva relacionada con el organismo vivo modificado que pueda
tener efectos adversos;
b) Una evaluación de la probabilidad de que esos efectos adversos
ocurran realmente, teniendo en cuenta el nivel y el tipo de exposición
del probable medio receptor al organismo vivo modificado;
c) Una evaluación de las consecuencias si esos efectos adversos
ocurriesen realmente;
d) Una estimación del riesgo general planteado por el organismo vivo
modificado basada en la evaluación de la probabilidad de que los
efectos adversos determinados ocurran realmente y las consecuencias en
ese caso;
e) Una recomendación sobre si los riesgos son aceptables o gestionables
o no, incluida, cuando sea necesaria, la determinación de estrategias
para gestionar esos riesgos; y
f) Cuando haya incertidumbre acerca del nivel de riesgo, se podrá
tratar de subsanar esa incertidumbre solicitando información adicional
sobre las cuestiones concretas motivo de preocupación, o poniendo en
práctica estrategias de gestión del riesgo apropiadas y/o vigilando al
organismo vivo modificado en el medio receptor.
B.4. ASPECTOS A TENER EN CUENTA
Según el caso, el análisis de riesgo tiene en cuenta los datos técnicos
y científicos pertinentes sobre las características de los siguientes
elementos:
a) Especie receptora u organismos parentales. Las características
biológicas de la especie receptora o de los organismos parentales
(cuando estos últimos presenten características diferenciales
relevantes respecto de su especie), incluida información sobre la
situación taxonómica, el nombre común, el origen, los centros de origen
y los centros de diversidad genética, si se conocen, y una descripción
del hábitat en que los organismos pueden persistir o proliferar;
b) Organismo u organismos donantes. Situación taxonómica y nombre
común, fuente y características biológicas pertinentes de los
organismos donantes;
c) Vector. Características del vector, y en relación a los vectores
biológicos su identidad, si la tuviera, su fuente de origen y el área
de distribución de sus huéspedes;
d) Inserto o insertos y/o características de la modificación.
Características genéticas del ácido nucleico insertado y de la función
que especifica, y/o características de la modificación introducida;
e) OGM. Identidad del OGM y diferencias entre las características
biológicas del mismo y las del organismo receptor o de los organismos
parentales (cuando estos últimos presenten características
diferenciales relevantes respecto de la especie);
f) Detección e identificación del OGM. Métodos sugeridos de detección e
identificación y su especificidad, límite de detección y selectividad;
g) Información sobre el uso previsto. Información acerca del uso
previsto del organismo vivo modificado, incluido un uso nuevo o
distinto comparado con los de la especie receptora o los organismos
parentales, y
h) Medio receptor. Información sobre la ubicación y las características
geográficas, climáticas y ecológicas, incluida información pertinente
sobre la diversidad biológica y la existencia de centros de origen de
la especie receptora en el probable medio receptor.
C. ANÁLISIS DE RIESGO
C.1. PROPÓSITO.
El propósito principal del análisis de riesgo de los OGM vegetales en
el marco de la presente es evaluar los riesgos nuevos o incrementados
respecto de la especie receptora que pudieran derivarse de su
autorización comercial para fines agroindustriales que incluyen la
liberación al agroecosistema. En función de dicha evaluación, en los
casos que corresponda, proponer medidas de manejo de riesgo y
comunicación de riesgo. Evaluación de riesgos, manejo de riesgos y
comunicación de riesgos son TRES (3) etapas interdependientes que
conforman el análisis de riesgo en su conjunto.
C.2. RESPONSABILIDAD
El análisis de riesgo de OGM vegetales será efectuado por la CONABIA
con la asistencia de la Coordinación de Innovación y Biotecnología de
la Dirección Nacional de Bioeconomía de la SECRETARÍA DE ALIMENTOS,
BIOECONOMÍA Y DESARROLLO REGIONAL del MINISTERIO DE AGRICULTURA,
GANADERÍA Y PESCA, utilizando el criterio de caso por caso.
D. INSTANCIA DE CONSULTA PREVIA (ICP)
D.1. PROPÓSITO.
El propósito de la INSTANCIA DE CONSULTA PREVIA (ICP) es poner a
disposición de los interesados un mecanismo formal a fin de realizar
consultas específicas en cuestiones de criterio, en forma opcional y
previa a la presentación de una solicitud de análisis de riesgo,
incluyendo la solicitud de evaluación de acumulaciones de eventos.
D.2. REQUERIMIENTOS.
La información deberá incluir una justificación e información técnica
acorde al contenido de la consulta y estar escrita en idioma español.
La misma deberá ser presentada ante la citada Coordinación de
Innovación y Biotecnología para ser evaluada por la CONABIA.
En forma previa a solicitar la ICP, los interesados deberán encontrarse
inscriptos en el RNOOVGM creado por la Resolución N° 46 de fecha 7 de
enero de 2004 de la ex-SECRETARÍA DE AGRICULTURA, GANADERÍA, PESCA Y
ALIMENTOS del entonces MINISTERIO DE ECONOMÍA Y PRODUCCIÓN. En caso
contrario, el interesado deberá realizar una acreditación equivalente
ante la mencionada Coordinación de Innovación y Biotecnología sólo a
los fines de estar habilitados a realizar la consulta.
La presentación tendrá carácter de declaración jurada en los mismos
términos y efectos que lo anteriormente descripto para las solicitudes
de autorización comercial de OGM. D.3. EVALUACIÓN.
Tanto la citada Coordinación de Innovación y Biotecnología como la
CONABIA podrán requerir a los Solicitantes información y estudios
complementarios a los fines de completar su análisis.
La CONABIA podrá solicitar la comparecencia del interesado en la
reunión donde se trate la ICP. A su vez podrá convocar, de acuerdo al
caso y a la necesidad, expertos en temas específicos relacionados con
la temática a tratar.
Toda ICP deberá resolverse en el plazo máximo de OCHENTA (80) días
hábiles contados desde la fecha de presentación. Para el caso de ICP
que requieran un análisis complejo, se determina un plazo máximo de
análisis de CIENTO VEINTE (120) días hábiles. El cómputo de dicho plazo
máximo se suspenderá durante los períodos en los cuales se deba esperar
a recibir respuestas a requerimientos de información adicional,
documentación faltante u otras acciones imprescindibles para la
prosecución del trámite y que dependan del interesado o entidades
externas.
E. SOLICITUD DE ANÁLISIS DE RIESGO
E.1. REQUERIMIENTOS FORMALES
E.1.1. INSCRIPCIÓN PREVIA.
El Solicitante deberá poseer inscripción vigente en el RNOOVGM, creado
por la mencionada Resolución Nº 46/04.
E.1.2. PRESENTACIÓN DE LA SOLICITUD.
Los interesados presentarán el formulario “SOLICITUD DE ANÁLISIS DE
RIESGO DE ORGANISMOS GENÉTICAMENTE MODIFICADOS VEGETALES (OGM
VEGETALES)” contemplado en el Anexo II de la presente medida.
Todos los ítems deben ser contestados, en forma concisa, cuidando la
claridad, compaginación de la información y consistencia a lo largo de
toda la presentación. Para identificar a los OGM vegetales deberá
utilizarse un código único establecido de acuerdo a las
especificaciones de la Organización para la Cooperación y el Desarrollo
Económico (OCDE), teniendo en cuenta la definición de evento utilizada
en la presente medida.
La presentación y toda comunicación formal subsecuente deberá estar a
cargo del Representante Legal acreditado ante el RNOOVGM y se realizará
ante el INSTITUTO NACIONAL DE SEMILLAS (INASE), organismo
descentralizado en la órbita del MINISTERIO DE AGRICULTURA, GANADERÍA Y
PESCA – Dirección de Certificación mediante el sistema de Trámite a
Distancia (TAD).
E.1.3. MÉTODO DE DETECCIÓN.
El solicitante incluirá en la solicitud una descripción de los mejores
y más actualizados métodos analíticos de que disponga para detectar en
forma específica los eventos incluidos en la solicitud, y los
materiales que resulten suficientes para ejecutar dichos métodos.
Asimismo, presentará una declaración asumiendo el compromiso permanente
de suministrar los insumos correspondientes en forma inmediata e
incondicional al solo requerimiento de las autoridades competentes y
para los fines que fueron solicitados. Dentro de los insumos se incluye
al material de referencia que deberá ser semilla, pudiendo estar
desvitalizada toda vez que el proceso de desvitalización no invalide la
aplicación del método.
El solicitante será responsable por la especificidad y selectividad del
método y, en particular, de que todo material que resulte positivo
pueda presumirse que corresponde al evento en cuestión. Por otra parte, el laboratorio adoptará las
medidas adecuadas a fin de resguardar los materiales e información
confidencial suministrada por el solicitante.
E.1.4. MÓDULO AGROFENOTOICO
Todos los estudios incluidos en el módulo agrofenotípico de la
solicitud deberán consistir en un análisis comparativo entre el OGM
vegetal y su contraparte convencional. Podrán proponerse otros
comparadores en casos particulares, cuya relevancia quedará a criterio
de la CONABIA. Lo anterior puede incluir, sin limitarse a, otros OGM
vegetales que cuenten con autorización comercial en la REPÚBLICA
ARGENTINA.
E.1.5. INFORMACIÓN EXTENDIDA.
El solicitante, a fin de brindar información más extendida, precisa y
detallada, podrá aportar trabajos y documentos provenientes de la
literatura científico-técnica que figuren como referencias
bibliográficas de la solicitud, en aquellos casos donde la
justificación de las respuestas esté total o parcialmente basada en el
conocimiento científico-técnico general. Cuando no aporte
espontáneamente dichas referencias bibliográficas, las mismas podrán
serle requeridas en caso que la CONABIA lo estime necesario. Deberá
remitir copia de dichas publicaciones en su formato original, sin
modificaciones. Si el idioma original fuera distinto del español, la
CONABIA podrá requerir su traducción. El solicitante es responsable de
la veracidad y fiabilidad de todas las publicaciones que utilice como
referencias bibliográficas en su solicitud, por el simple hecho de
utilizarlas como sustento de la misma, aun cuando sean el resultado del
trabajo de terceros. E.1.6. DECLARACIÓN JURADA.
Todas las manifestaciones efectuadas por el Solicitante por sí mismo o
a través de su representante en los expedientes deberán ser veraces,
exactas y tendrán el carácter de declaración jurada. Su falsedad o
inexactitud podrá dar lugar a la revocación de la autorización
otorgada, a las sanciones que prevé la Resolución N° 763 de fecha 17 de
agosto de 2011 del ex- MINISTERIO DE AGRICULTURA, GANADERÍA Y PESCA,
y/o a la exclusión del RNOOVGM, sin perjuicio de la aplicabilidad de
los regímenes de responsabilidad civil y penal según corresponda en
virtud de las consecuencias que pueda tener la falta.
F. INFORMACIÓN CONFIDENCIAL.
F.1. PRESENTACIÓN
Si el solicitante desea que algunos de los datos o información
requerida en la solicitud sean gestionados de manera confidencial,
deberá proceder indicando esta circunstancia al frente de la solicitud,
y en el cuerpo del texto, donde dichos datos fueron omitidos mediante
la frase “Información Confidencial Eliminada”.
El Solicitante deberá remitir al INASE, en sobre lacrado y firmado, una
solicitud completa que incluya en tipografía resaltada la información
que desea mantener confidencial (Información Confidencial, en adelante
IC). Este documento deberá presentar en el margen superior derecho de
cada una de sus páginas la inscripción “Copia con IC”.
F.2. EXCLUSIONES.
La siguiente información no podrá ser presentada como IC.
• Denominación del OGM vegetal.
• Características fenotípicas introducidas en el OGM vegetal.
• Nombre y dirección del Solicitante, del Representante Legal o
Apoderado y del Responsable Técnico.
• Toda información que hubiera sido publicada o comunicada en forma
irrestricta (no confidencial) a las autoridades regulatorias nacionales
o a terceros (incluyendo, pero sin limitarse a, otras autoridades
regulatorias), en cualquier formato, por cualquier medio, en cualquier
lugar del mundo.
Sin perjuicio de lo anterior, la CONABIA podrá establecer que una
información presentada como IC debe ser presentada en forma no
confidencial para permitir un análisis de riesgo adecuado (por ejemplo,
porque se requiere su tratamiento detallado en los debates o porque
deba ser analizada por múltiples integrantes de la Comisión).
En tales casos, se le dará la opción al Solicitante de remitir dicha
información en carácter no confidencial o desistir de la solicitud.
F.3. EXAMEN.
La referida Coordinación de Innovación y Biotecnología suministrará,
con la anuencia de CONABIA, una propuesta de técnicos y expertos
habilitados para examinar la IC. Dicha propuesta requerirá la
conformidad del Solicitante previo a cualquier toma de vista de la
documentación, teniendo derecho éste último a prestar una conformidad
parcial, en la cual las exclusiones de la lista tengan motivos fundados.
El Solicitante podrá requerir que su Representante Legal o
Representante Técnico estén presentes en el acto de apertura y vista de
la IC.
Los evaluadores firmarán un compromiso de confidencialidad previo a
tomar vista de la IC. Las personas presentes en el acto de vista de la
IC firmarán tantos ejemplares como correspondan de un mismo tenor del
acta en la que se volcará la opinión de los expertos. UN (1) ejemplar
será entregado al Solicitante y otro se incluirá en el expediente
correspondiente.
F.4. PRESERVACIÓN
La IC deberá ser preservada por la misma cantidad de tiempo que exista
el expediente de la evaluación correspondiente.
G. EXAMEN DE LA SOLICITUD.
G.1. ANÁLISIS DE RIESGO.
G.1.1. PROCEDIMIENTO.
La CONABIA, con la asistencia de la citada Coordinación de Innovación y
Biotecnología, procederá a la evaluación de los aspectos
científico-técnicos involucrados. Si surgieran preguntas,
observaciones, o necesidad de aclaraciones, se dará traslado al
solicitante para responder las preguntas y formular las aclaraciones
que se estimen pertinentes. G.1.2. PLAZO.
La evaluación deberá ser finalizada en el plazo máximo de CIENTO
OCHENTA (180) días hábiles contados desde la fecha de presentación de
la solicitud ante el INASE- Dirección de Certificación. El cómputo de
dicho plazo máximo se suspenderá durante los períodos en los cuales se
deba esperar a recibir respuestas a requerimientos de información
adicional, documentación faltante u otras acciones imprescindibles para
la prosecución de la evaluación y que dependan del interesado o
entidades externas. G.1.3. MANEJO Y COMUNICACIÓN DEL RIESGO
Para aquellos hipotéticos casos en que la evaluación de riesgo reporte
que el OGM vegetal presenta riesgos significativos, ya sean nuevos o
incrementados respecto de la especie receptora, deberá generarse una
propuesta de manejo y comunicación del riesgo que formen parte del
Documento de Decisión.
G.1.4. DOCUMENTO DE DECISIÓN.
Una vez finalizada la evaluación la mencionada Coordinación de
Innovación y Biotecnología junto con la CONABIA tendrán a su cargo la
emisión de un Documento de Decisión en el que se describirán los
aspectos relevantes del OGM vegetal, el resultado de la evaluación de
riesgos y, de encontrarse riesgos nuevos o incrementados, sus
recomendaciones sobre el manejo y comunicación de los mismos. El
Documento de Decisión es un dictamen técnico no vinculante para uso de
la Autoridad de Aplicación que, por sí mismo, no confiere permiso o
derecho alguno, ni modifica el estado regulado de los OGM vegetales.
H. APERTURA A COMENTARIOS DEL PÚBLICO.
Los proyectos de Documentos de Decisión que genere la CONABIA serán
dados a conocer a los fines de recibir comentarios técnicos, no
vinculantes, por parte de cualquier persona humana o jurídica residente
en la REPÚBLICA ARGENTINA.
H.1. PUBLICACIÓN.
El anuncio de la convocatoria a la recepción de
comentarios técnicos no vinculantes, realizada por la SECRETARÍA DE
BIOECONOMÍA del MINISTERIO DE ECONOMÍA, se publicara´ por UN (1) día en
el Boletín Oficial. La convocatoria se mantendrá abierta durante un
periodo de TREINTA (30) días corridos, contados a partir de la
publicación en el Boletín Oficial, en la página web de la citada
Secretaría donde se publicará el proyecto de Documento de Decisión.
Los comentarios deben presentarse a través de la plataforma Trámites a
Distancia (TAD) mediante el trámite “Presentación Ciudadana ante el
Poder Ejecutivo” y dirigidas a la Coordinación de Innovación y
Biotecnología de la Dirección Nacional de Bioeconomía de la SECRETARÍA
DE BIOECONOMÍA del MINISTERIO DE ECONOMÍA. Por excepción, podrán
presentarse en papel ante la Área de Mesa de Entradas de la Dirección
de Gestión Documental de Agricultura, Ganadería y Pesca de la
mencionada Secretaría, sita en la Avenida Paseo Colón Nº 982, Planta
Baja, de la CIUDAD AUTÓNOMA DE BUENOS AIRES.
Cuando los comentarios se basen en hallazgos científicos-técnicos o
datos concretos, deberá´ acompañarse copia de los estudios o
publicaciones originales donde puedan ser corroborados, de lo contrario
se los tendrá´ por infundados. Si se tratase de documentos en idioma
diferente al español, deberán acompañarse las correspondientes
traducciones publicas. Sólo resultarán admisibles los comentarios de
carácter técnico que se circunscriban a las cuestiones que le
corresponde analizar a la CONABIA durante el análisis de riesgo del OGM
vegetal. Toda otra cuestión que no resulte relevante a la convocatoria
se tendrá´ por no presentada. Todos los comentarios serán integrados al
expediente respectivo, sumándose al proceso de evaluación y toma de
decisiones en forma unidireccional, es decir, no se contestara´ a los
proponentes salvo que se requieran aclaraciones o información
adicional.
(Apartado H.I sustituido por art. 1° de la Resolución N° 31/2024
de la Secretaría de Bioeconomía B.O. 28/5/2024. Vigencia: a partir del
día siguiente al de su publicación en el Boletín Oficial.)
H.2. EXAMEN Y CONCLUSIÓN DEL PROCESO.
La CONABIA evaluará el mérito técnico de los comentarios recibidos y,
de considerarlo necesario, revisará el proceso de evaluación o el
Documento de Decisión respectivo, como paso previo a suscribir este
último y elevarlo para consideración de la referida SECRETARÍA DE
ALIMENTOS, BIOECONOMÍA Y DESARROLLO REGIONAL. Asimismo, la mencionada
Coordinación de Innovación y Biotecnología remitirá al interesado una
copia de la versión final del Documento de Decisión.
I. CASOS ESPECIALES
A continuación se proporcionan previsiones para ciertas clases de OGM
vegetales, anticipándose que las mismas podrán ser complementadas por
disposiciones de la citada Coordinación de Innovación y Biotecnología,
surgidas de la orientación adicional que la CONABIA estime pertinente
proporcionar a partir de la evolución de la casuística y la experiencia
acumulada.
I.1. CULTIVOS PROTEGIDOS CONTRA PLAGAS.
La evaluación de riesgo de un OGM vegetal con protección contra plagas
requerirá considerar, caso a caso, la necesidad y contenido de un plan
de manejo y monitoreo para reducir la posibilidad de surgimiento o
incremento poblacional de plagas resistentes, en función de atender a
un interés general por maximizar la vida útil de las tecnologías una
vez que están disponibles.
I.2. EVENTOS CON CONSTRUCCIONES GENÉTICAS IDÉNTICAS O ESENCIALMENTE
SIMILARES.
I.2.1. TRATAMIENTO DIFERENCIADO.
En el caso de eventos que contengan construcciones genéticas idénticas
o esencialmente similares a las incorporadas en otros OGM vegetales que
ya cuenten con evaluación de riesgo concluida con Documento de Decisión
favorable, se dispone de un tratamiento diferenciado para la evaluación
de riesgo. La evaluación se realizará caso por caso, y basará en
establecer la ausencia de riesgos nuevos o incrementados respecto del
OGM vegetal previamente evaluado y con dictamen favorable.
I.2.2. PRESENTACIÓN DE ICP.
A efectos de habilitar el tratamiento diferenciado, los interesados
deberán presentar el caso ante la CONABIA a través de una ICP. La
mencionada ICP deberá indicar, para el evento bajo análisis y el de
referencia, la siguiente información: cultivo modificado, una
representación esquemática del inserto y una descripción de todas las
secuencias insertadas, sean codificantes o no, respetando el orden en
que se encuentran ubicadas en el genoma, e incluyendo a sus respectivos
organismos donantes, sus tamaños en pares de bases y sus funciones en
el OGM vegetal. A su vez, deberán informar sólo para el evento bajo
análisis: método de transformación, el/los mapa/s del/ de los vector/es
y/o secuencias lineales de ADN, y una descripción de todos los
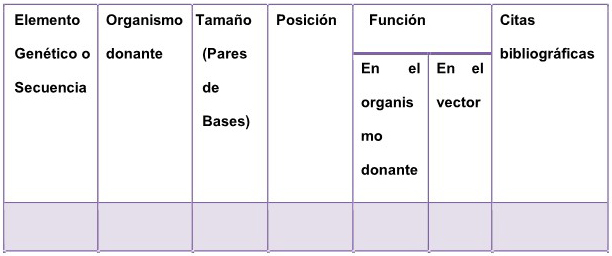
elementos genéticos presentes en este/estos último/s (especificando sus
respectivos organismos donantes, tamaños en pares de bases, posiciones,
funciones en los organismos donantes y en el vector, y las citas
bibliográficas correspondientes).
I.2.3. ANÁLISIS DEL CASO.
La CONABIA evaluará si la construcción es idéntica o esencialmente
similar a la contenida en el OGM vegetal previamente autorizado. En
caso afirmativo, proporcionará respuestas orientativas en relación a la
información necesaria para evaluar que no existen riesgos nuevos o
incrementados respecto del OGM vegetal de referencia, expresada como un
subconjunto de los ítems de la “SOLICITUD DE ANÁLISIS DE RIESGO DE
ORGANISMOS GENÉTICAMENTE MODIFICADOS VEGETALES” que considere
relevantes según el caso.
I.2.4. CULTIVOS EN ETAPA DE DESARROLLO.
En el caso de proyectos que aún se encuentren en etapa de diseño o de
desarrollo, el interesado podrá realizar una consulta preliminar al
solo fin de anticipar si la construcción que pretende utilizar se
hallaría alcanzada por el tratamiento diferenciado. En este supuesto,
la CONABIA realizará un análisis preliminar y proporcionará una
respuesta orientativa. De concretarse, luego la obtención de tales
nuevos cultivos, los mismos deberán someterse al procedimiento
precedente solo a los fines de confirmar que poseen las características
anticipadas en la consulta preliminar.
I.3. ACUMULACIÓN DE EVENTOS.
I.3.1 PRESENTACIÓN DE ACUMULACIONES DE EVENTOS
Para la acumulación de eventos el solicitante deberá presentar una
instancia de consulta previa (ICP) ante la CONABIA y la Coordinación de
Innovación y Biotecnología, donde se describirá el producto a evaluar y
se detallarán cuestiones particulares de la acumulación de eventos.
También se podrán realizar consultas sobre estudios a realizar o
información relevante para el solicitante, entre otras.
De tratarse de una acumulación de eventos en la cual cada evento
individual cuente con Documento de Decisión favorable de la CONABIA, la
presentación de la ICP deberá enfocarse en la evaluación de las
posibles interacciones, como se describe en el punto I.3.2 “Análisis de
la ICP”.
En aquellos casos en que uno o más de los eventos individuales no hayan
sido evaluados por CONABIA, se deberá presentar la “SOLICITUD DE
ANÁLISIS DE RIESGO DE ORGANISMOS GENÉTICAMENTE MODIFICADOS VEGETALES”
para el/los mismo/s. A través de la ICP el solicitante podrá requerir
que en conjunto con la evaluación de el/los evento/s individuales se
evalúe la acumulación de eventos que lo incluyan, para concluir sobre
el acumulado mayor, sus acumulaciones intermedias y sobre el/los
eventos individuales. Para ello, también se deberá presentar la
información sobre las posibles interacciones en la acumulación de
eventos como se describe en el párrafo precedente y se establecen
DOSCIENTOS SESENTA (260) días hábiles como plazo máximo de evaluación,
considerando la sumatoria de los tiempos asignados para la evaluación
de un evento individual y una acumulación de eventos.
Las acumulaciones intermedias de eventos se evaluarán dentro de la
máxima acumulación de eventos presentada.
La ICP para la evaluación de la acumulación de eventos deberá contener
la información necesaria para el análisis que se describe a
continuación:
I.3.2. ANÁLISIS DE LA ICP
El análisis de la ICP hará énfasis en la posible interacción entre los
productos de expresión y/o rasgos combinados, incluyendo datos
específicos para verificar la ausencia de interacciones. El mencionado
análisis se realizará caso por caso, y se basará en el criterio de la
posible existencia de efectos epistáticos entre los genes introducidos
y/o de efectos de interacción entre los productos de expresión de los
transgenes en caminos metabólicos relacionados. Como resultado de este
análisis de interacción, se identificarán los efectos que podrían
generarse sobre el agroecosistema y se evaluará su riesgo. Esta
evaluación se realizará mediante la aplicación de la metodología de
Formulación del Problema, entendiendo por la misma el planteo de las
hipótesis de riesgo correspondientes, su análisis y verificación.
Tanto la referida Coordinación de Innovación y Biotecnología como la
CONABIA podrán requerir a los Solicitantes información y estudios
complementarios a los fines de completar su análisis.
En función del análisis realizado, la citada Coordinación de Innovación
y Biotecnología en conjunto con la CONABIA responderán la ICP
informando al solicitante sobre las cuestiones planteadas (consultas
sobre estudios a realizar o información relevante para el solicitante,
evaluación de la información presentada, entre otras) y como fin
último, concluirán sobre el análisis de riesgo para la liberación al
agroecosistema de la acumulación de eventos presentada. La mencionada
conclusión se plasmará en un Documento de Decisión.
ANEXO II
SOLICITUD DE ANÁLISIS DE RIESGO DE ORGANISMOS GENÉTICAMENTE MODIFICADOS
VEGETALES (OGM VEGETALES).
- INCLUYA A CONTINUACIÓN UN ÍNDICE DETALLADO DE LOS CONTENIDOS
- DETALLE A CONTINUACIÓN LA LISTA DE ABREVIATURAS UTILIZADAS
I - MÓDULO
GENERAL
A. RESUMEN
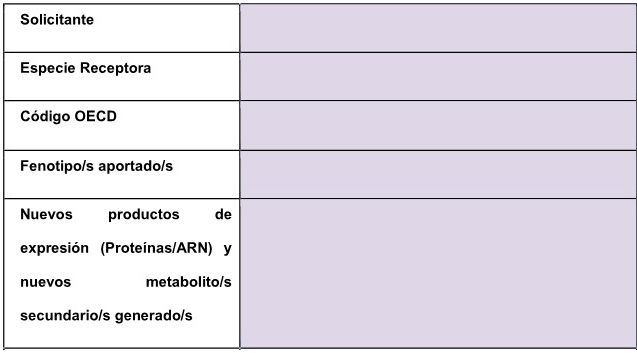
B. INFORMACIÓN GENERAL
1. Datos del Solicitante.
1.1. Representante legal.
1.2. Responsable técnico.
1.3. Domicilio.
2. Remitir los datos de contacto de las Instituciones y personas que
han desarrollado el OGM vegetal, aclarando sus diferentes roles.
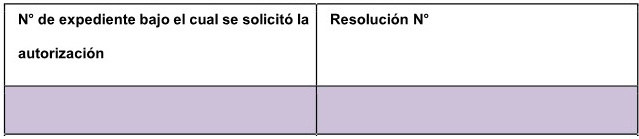
3. Informar los permisos para actividades contenidas y confinadas
obtenidos previamente en el país, si los hubiera.
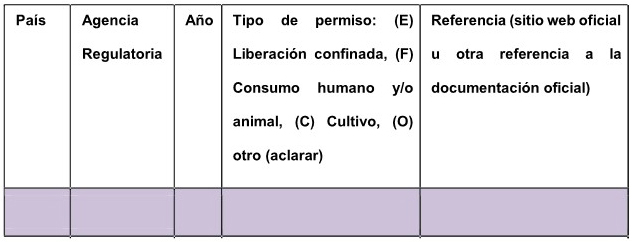
4. Completar el cuadro con los antecedentes de autorización en otros
países.
II -
MÓDULO ESPECIE RECEPTORA
1. Nombre común y científico.
2. Historial de uso y riesgos conocidos.
3. Informar el/los centro/s de origen y centro/s de diversidad genética.
4. Indicar la distribución geográfica en nuestro país y su diversidad
biológica presente en condiciones naturales. A su vez, describir los
hábitats en que puede persistir o proliferar.
5. Describir sus características genéticas.
6. Características fenotípicas.
6.1. Describir su fenología y
morfología.
6.2. Describir sus características reproductivas.
- Biología floral.
- Reproducción sexual y factores que la afectan.
- Informar si existen formas de reproducción asexual.
- Capacidad de dispersión y persistencia de la especie vegetal.
- Factores específicos que afectan la capacidad de dispersión y
supervivencia.
6.3. Informar sobre su invasividad.
7. Informar sobre la posibilidad de cruzamiento con especies
sexualmente compatibles presentes en el país (cultivadas y silvestres)
y una descripción de la posible descendencia, incluyendo su
comportamiento invasivo y/o persistente en el agroecosistema.
8. Remitir información sobre las interacciones con organismos
relevantes para el agro-ecosistema local.
- Plagas.
- Organismos benéficos: (ej. predadores, polinizadores, parasitoides,
descomponedores y simbiontes).
- Incluir información sobre toxicidad, alergenicidad u otro riesgo
hacia otros organismos.
III -
MÓDULO BIOLOGÍA MOLECULAR
A. GENERACIÓN DEL OGM VEGETAL.
A.1. Identificar la variedad, cultivar, ecotipo u espécimen utilizado
como receptor de la modificación genética, incluyendo su lugar de
adquisición o recolección.
A.2. Describir el método de obtención del OGM vegetal.
A.3. Caracterización del o los vector/es y la/las construcción/es
utilizada/s para la obtención del OGM vegetal.
A.3.1. Completar el cuadro con la
descripción de sus elementos.
A.3.2. Remitir el/los mapas del/ de los
vector/es y la/las construcción/es.
A.3.3. Informar la taxonomía, nombre común, lugar de recolección o
adquisición y características del/los organismo/s donante/s.
A.3.4. Informar sobre la patogenicidad, toxicidad y/o alergenicidad de
el/los organismo/s donante/s.
A.3.5. De corresponder informar el historial de uso del organismo
donante.
B. ANÁLISIS MOLECULAR DE LA/S
INSERCIÓN/ES EN EL GENOMA DEL OGM VEGETAL.
B.1. Informar el número de sitios de integración (número de insertos).
B.2. Para cada sitio de integración:
B.2.1. Representar esquemáticamente el inserto y las secuencias
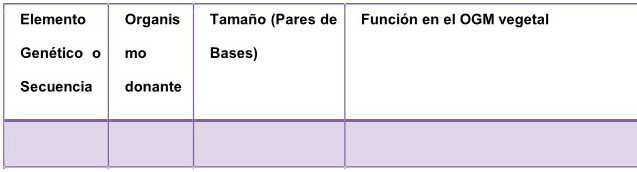
flanqueantes. B.2.2. Completar el cuadro con la descripción de todas
las secuencias insertadas, sean codificantes o no, respetando el orden
en el que se encuentran ubicados en el genoma. De corresponder, incluir
aquellas secuencias nucleotídicas del esqueleto del vector presentes en
el inserto.
Elemento Genético o Secuencia Organismo donante Tamaño (Pares de Bases)
Función en el OGM vegetal
B.2.3. Informar si alguno(s) de los elementos del inserto:
B.2.3.1. Tiene potencial para
duplicarse y/o movilizarse en el genoma del OGM vegetal. Detallar el
mecanismo y su probabilidad de ocurrencia.
B.2.3.2. Está involucrado en la transferencia horizontal de material
genético. Detallar el mecanismo, la probabilidad de ocurrencia y
posibles fenotipos resultantes en dichos organismos.
B.2.4. Informar si se han producido transposiciones, inserciones,
deleciones y/o rearreglos dentro del inserto respecto de su posición
original en el vector.
B.2.5. Remitir información detallada de las secuencias del genoma
vegetal que flanquean el inserto, indicando si se han interrumpido
secuencias codificantes o secuencias regulatorias conocidas. En caso
afirmativo, describir y analizar el (posible) efecto sobre el fenotipo
del OGM Vegetal.
B.2.6. Proporcionar información sobre la estabilidad genética del
inserto.
C. NUEVOS PRODUCTOS EN EL OGM VEGETAL.
C.1. Productos esperados.
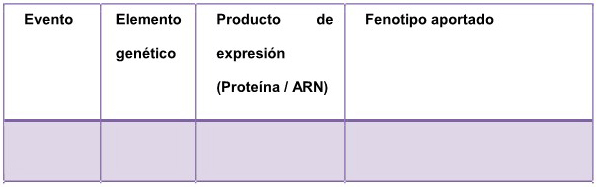
C.1.1. Enumerar, utilizando la
siguiente tabla, los nuevos productos presentes en el OGM vegetal. Esto
incluye toda nueva proteína o ARN (con función diferente o adicional a
actuar como ARN mensajero) y todo metabolito secundario nuevo.
C.1.2 Informar la función molecular y
la actividad biológica de cada uno de los productos mencionados en el
punto anterior.
C.1.3. Detallar los niveles y el sitio de expresión (tejido/órgano) de
los nuevos productos a lo largo del ciclo de vida del OGM vegetal,
según resulte relevante para el análisis de riesgo.
C.1.4. Proporcione toda información disponible sobre la posible
toxicidad y alergenicidad de los nuevos productos expresados. Ello
deberá incluir estudios bioinformáticos de similitud de secuencias con
toxinas y alérgenos conocidos, utilizando bases de datos actualizadas.
C.2. Productos hipotéticos.
C.2.1. Remitir el análisis detallado de
búsqueda de marcos de lectura abiertos generados como consecuencia del
proceso de obtención del OGM vegetal, abarcando al inserto y las
secuencias flanqueantes del genoma vegetal. Indicar cuáles de ellos
podrían generar productos hipotéticos.
C.2.2. Presente estudios bioinformáticos de similitud de secuencias de
los productos hipotéticos con toxinas y alérgenos conocidos, utilizando
bases de datos actualizadas.
C.2.3. Analizar la posibilidad de que los productos hipotéticos tengan
actividad biológica y, de corresponder, su consecuencia en relación a
posibles riesgos.
C.3. Potenciales interacciones de los productos.
C.3.1. Evaluar las posibles
interacciones de el/los producto/s generado/s a partir de la expresión
de las secuencias insertadas en el OGM vegetal con otros procesos
biológicos y otros productos endógenos de la planta. En caso de
corresponder, describir y analizar el (posible) efecto sobre el
fenotipo del OGM vegetal.
D. MÉTODO DE DETECCIÓN.
D.1. Incluir métodos analíticos para eventos incluidos en la solicitud,
declaración de compromiso sobre los insumos correspondientes.
IV -
MÓDULO AGROFENOTÍPICO
A. CARACTERIZACIÓN AGROFENOTÍPICA DEL
OGM VEGETAL Y SU INTERACCIÓN CON OTROS ORGANISMOS.
A.1. Demostrar el fenotipo aportado por la/s modificación/es genética/s
introducida/s en el OGM vegetal.
A.2. Informar sobre el uso previsto del OGM vegetal o sus productos.
A.3. Informar sobre la realización de estudios de poder germinativo y
dormición.
A.4. Informar el comportamiento agrofenotípico del OGM vegetal en
ensayos a campo, obtenidos en condiciones agroecológicas diferentes
entre sí y representativas de las zonas de producción del cultivo.
A.4.1. Características vegetativas y
reproductivas. En aquellos casos que el cultivo tenga otras especies
sexualmente compatibles en el territorio nacional, describir además el
tipo y agentes polinizadores y las características del polen
(morfología, tamaño y viabilidad).
A.4.2. Susceptibilidad a factores de estrés abiótico.
A.4.3. Susceptibilidad a factores de estrés biótico (plagas y
enfermedades).
A.5. Analizar el potencial de invasividad y persistencia del OGM
vegetal y/o de la progenie resultante del cruzamiento con especies
sexualmente compatibles (cultivadas y silvestres).
A.6. Remitir un análisis de la composición centesimal.
B. INTERACCIONES DEL OGM VEGETAL CON
OTROS ORGANISMOS.
B.1. De tratarse de un OGM vegetal con fenotipo de protección contra
plagas:
B.1.1. Analizar los posibles efectos
del mismo sobre organismos no blanco, incluyendo los organismos
benéficos detallados previamente y otros que sería de esperar que
interactúen con el OGM vegetal a partir de su liberación al
agroecosistema para uso comercial.
En caso de presentar ensayos in vitro utilizando productos de expresión
generados en microorganismos recombinantes, fundamentar su equivalencia
con los productos expresados en el OGM vegetal.
B.1.2 De tratarse de un OGM vegetal con fenotipo de protección contra
artrópodos, informar sobre la realización de estudios de impacto y
abundancia de artrópodos en ensayos a campo, detallando las especies o
grupo recolectados.
V - MÓDULO
MANEJO
A.1. Informar si el manejo agronómico del OGM vegetal difiere al de su
homólogo convencional.
A.2. De tratarse de un OGM vegetal con fenotipo de protección contra
plagas, informe sobre la necesidad y contenido de un plan de manejo
agronómico y monitoreo de plagas, para reducir la posibilidad de
surgimiento o incremento poblacional de plagas resistentes.
VI -
MÓDULO EVALUACIÓN DE RIESGO
1. Remitir las hipótesis de riesgo en relación al evento presentado. A
su vez, formular el razonamiento hacia un hipotético efecto adverso y
vincularlo con la información presentada para poder aceptar o rechazar
las hipótesis de riesgo planteadas.
2. Esta información será considerada dentro de otras posibles hipótesis
de riesgo que puedan surgir durante la evaluación de riesgo.
ANEXO III
INFORMACIÓN A PRESENTAR EN UNA INSTANCIA DE CONSULTA PREVIA (ICP) PARA
LA EVALUACIÓN DE EVENTOS ACUMULADOS.
La evaluación se realizará mediante la implementación de Formulación de
Problema. Durante la misma, se evaluarán las hipótesis de riesgo (HDR)
planteadas por el solicitante. El mismo deberá presentar la información
científica que permita responder a las HDR que se planteen durante las
presentaciones de la ICP de los eventos acumulados. Esta información
deberá contemplar los siguientes detalles, según el caso a evaluar:
1. Interacción entre los productos de expresión y/o los genes
introducidos.
1.1 Información sobre posibles interacciones entre los nuevos productos
de expresión teniendo en cuenta los mecanismos de acción, rutas
metabólicas implicadas, conformación espacial y localización a nivel
celular de los mismos.
1.2 Información sobre posibles efectos epistáticos entre los genes
introducidos y, en caso que los hubiera, corroborarlos con estudios
sobre niveles de expresión.
1.3 Bibliografía científica disponible, análisis bioinformático, entre
otros.
2. Si se hubieran identificado posibles interacciones y/o efectos
epistáticos, presentar estudios que permitan confirmarlos y
caracterizarlos (efectos sinérgicos, aditivos, antagónicos o de
silenciamiento derivados de la presencia de las secuencias introducidas
en el evento) y, de corresponder, estudios para evaluar las HDR que
surjan de tales interacciones.
3. Acumulación de eventos con protección contra plagas.
3.1 En aquellas acumulaciones de eventos con protección contra plagas
en que se hayan verificado efectos sinérgicos entre los productos de
expresión, se deberán presentar estudios sobre organismos no blanco o
evidencia científica que permita evaluar los posibles efectos de las
proteínas en combinación.
3.2 Se deberá tener en cuenta lo establecido en el punto I.1 del Anexo
I de la presente medida respecto a “cultivos protegidos contra plagas”
en lo que refiere al manejo de resistencia de plagas.
IF-2020-83640222-APN-SABYDR#MAGYP