Administración
Nacional de Medicamentos, Alimentos y Tecnología Médica
SALUD PUBLICA
Disposición N° 1678/96
Adóptase la categorización de riesgo
de Encefalopatía Bovina (EEB) por país, según Resolución N° 203/96
-SENASA y establécese una categorización de riesgo de materias primas
de rumiantes por eventual transmisión de EEB al hombre.
Bs As., 26/4/96
VISTO el expediente de esta Administración Nacional 1-47-3189/96-9 y la
Disposición 1422/96 de esta administración nacional que estableciera
medidas precautorias como consecuencia de la incertidumbre creada por
los casos de enfermedades humanas tipo " Creutzfeld Jacob" ocurridas en
el Reino Unido eventualmente relacionada con la Encefalopatía
Espongiforme Bovina E.E.B. y en el marco de la resolución del Servicio
de Sanidad Animal N° 203/96, y
CONSIDERANDO:
Que esta Administración Nacional conforme al Decreto 1490/92 ejerce la
fiscalización y el control de los productos terminados y semielaborados
el que incluye el efectuado en aquellos que contienen materias primas
de origen rumiante en la elaboración de cosméticos, medicamentos, y
dispositivos de uso médico y cosméticos en el marco de la Ley de
Medicamentos N° 16.463.
Que las medidas precautorias tomadas por esta administración se basan
en las recomendaciones de organismos internacionales tales como la
Unión Europea, la Organización Mundial de la Salud, la Administración
de Drogas y Alimentos de Estados Unidos de Norteamérica y por el
Servicio Nacional de Sanidad Animal de Argentina.
Que el Servicio Nacional de Sanidad Animal ha efectuado un seguimiento
puntual desde el año 1986, fecha en que se identificó la E.E.B. como
epizootia de la especie bovina y que ha trabajado en el sentido de
aplicar medidas para mantener al ganado libre de la enfermedad.
Que existen recomendaciones de la Administración de Drogas y Alimentos
de Estados Unidos de Norteamérica, de la Unión Europea y de la
Organización Mundial de la Salud sobre los conocimientos al presente de
la seguridad de ciertos productos y derivados de rumiantes que se
incluyen en la elaboración de cosméticos, medicamentos y dispositivos
de uso médico.
Que en especial, con relación a los medicamentos y dispositivos de uso
médico que difieren de otros productos de uso humano, la Organización
Mundial de la Salud, en la reunión llevada a cabo los días 2 y 3 de
abril de 1996 en Ginebra, Suiza, sostuvo que las medidas tendientes a
minimizar el riesgo de transmisión de la E.E.B. desarrollados por la
O.M.S., en 1991, continúan siendo a la fecha aplicables.
Que la aparición en el presente de diez casos de una variante de la
enfermedad de Creutzfeld Jacob acaecida en los últimos seis meses en el
Reino Unido, si bien no está definitivamente relacionada con la E.E.B.,
constituye una evidencia circunstancial que sugiere que la exposición a
E.E.B. puede ser la hipótesis más probable.
Que la incertidumbre sobre la aparición de esta variante de enfermedad
en el hombre hace necesario al presente considerar en los productos
cosméticos, medicamentos y dispositivos de uso médico, la existencia de
un riesgo potencial, y que corresponde instrumentar medidas de
aplicación inmediata.
Que esta administración ve conveniente adecuar en el área de su
incumbencia y sus operatorias, los términos de la Resolución 203/96 del
Servicio Nacional de Sanidad Animal en cumplimiento de su quehacer de
control para garantizar la calidad de cosméticos, medicamentos y
dispositivos de uso médico.
Que la comisión " ad hoc" creada por Disposición ANMAR 1341/96 para
efectuar recomendaciones a esta dirección ha evaluado la documentación
técnica sobre la temática.
Que la Dirección de Asuntos Jurídicos ha tomado la intervención de su
competencia.
Que se actúa en virtud a las atribuciones conferidas por los artículos
3° y 8° del Decreto N° 1490/92.
Por ello,
EL DIRECTOR NACIONAL DE LA ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS, Y TECNOLOGIA MEDICA
DISPONE:
Artículo 1º - Adóptase la categorización de riesgo de EEB por
país establecida por SENASA en Resolución N° 203/96 que se agrega como
ANEXO I a la presente.
Art. 2º - Establécese para
materias primas importadas de origen rumiante destinadas a la
elaboración de cosméticos, medicamentos, y dispositivos de uso médico,
y para las incorporadas en productos importados terminados o
semielaborados la categorización de riesgo sobre la eventual
transmisión de EEB al hombre que se detalla en el Anexo II de la
presente disposición
Art. 3º - A los fines de la
aplicación de lo establecido en los artículos 1º y 2º de la presente
disposición establécese la matriz de decisión de importaciones conforme
riesgo materia prima/país para EEB, según el Anexo III que forma parte
de la presente disposición.
Art. 4º - En aquellos casos en
los cuales la importación de materias primas derivadas de rumiantes
requiriesen una "autorización condicionada", según Anexo III de esta
disposición, los importadores deberán adjuntar: Certificado debidamente
legalizado expedido por la autoridad sanitaria del país de origen, en
el que conste que el producto proviene de animales de establecimientos
en los que nunca se presentó ni sospechó la presencia de EEB. En su
defecto, una declaración jurada, por parte del establecimiento
elaborador de la materia prima, la que deberá contener el origen de la
misma y que ésta proviene de animales de establecimientos en los que
nunca se presentó ni sospechó la presencia de EEB que será
confeccionada en papel con membrete, correspondiente al establecimiento
elaborador de la materia prima.
Art. 5º - Las empresas
elaboradoras de medicamentos, cosméticos y dispositivos de uso médico
que utilicen materia prima de origen rumiante, categorizadas según
Anexo II de la presente disposición serán solidariamente responsables
con el establecimiento declarante por las inexactitudes, falsedades,
errores u omisiones que pudiera contener la declaración jurada
mencionada en el artículo 4º de la presente, y serán pasibles de las
sanciones correspondientes, con los alcances establecidos por la Ley de
Medicamentos N° 16.463 y normas complementarias.
Art. 6º - Las empresas
importadoras que comercialicen cosméticos, medicamentos o dispositivos
de uso médico que hayan sido elaborados con materia prima de origen
rumiante categorizada en el Anexo II de la presente Disposición, serán
solidariamente responsables con el establecimiento declarante por las
inexactitudes, falsedades, errores u omisiones que pudiera contener la
declaración jurada mencionada en el artículo 4º de la presente, y se
hará pasible de las sanciones correspondientes, con los alcances
establecidos por la Ley de Medicamentos N° 16.463 y normas
complementarias.
Art. 7º - Todas las
autorizaciones de importación efectuadas por esta Administración con
anterioridad a la emisión de esta disposición, que correspondieran a
materias primas o productos alcanzados por ella, deberán ser
convalidados en el marco de la presente.
Art. 8º - Sin perjuicio de lo
establecido en los artículos precedentes la comisión "ad hoc" creada
por Disposición 1341/96 asesorará a esta Dirección Nacional sobre las
medidas emergentes que se hicieran necesarias para garantizar la
calidad de los cosméticos, medicamentos y dispositivos de uso médico.
Art. 9º - Deróganse las
Disposiciones A.N.M.A.T. 1411/96 y 1422/96, y toda prescripción
normativa que se oponga a esta disposición a partir de su entrada en
vigencia.
Art. 10. - Las medidas
adoptadas por la presente Disposición, podrán ser modificadas en virtud
de nuevos aportes científicos y regulatorios que varíen la situación
Riesgo - Producto - País.
Art. 11. - Comuníquese a las
Entidades relacionadas con la producción, importación y
comercialización de cosméticos, medicamentos y dispositivos de uso
médico.
Art. 12. - Anótese;
comuníquese a quienes corresponda. Dése a la Dirección Nacional del
Registro Oficial para su publicación; comuníquese a la Administración
Nacional de Aduanas para su implementación inmediata a aprtir de la
publicación en el Boletín Oficial . Cumplido, archívese PERMANENTE.-
Pablo M. Bazerque.
ANEXO I
CATEGORIZACION DE RIESGO DE EEB POR (según Resolución SENASA N° 203/96)
De acuerdo a la situación epidemiológica de cada país respecto a la
encefalopatía espongiforme bovina (EEB) y a la información que sobre la
misma ha recibido el SERVICIO NACIONAL DE SANIDAD ANIMAL, se los ha
clasificado en las siguientes cuatro categorías:
I) CON BROTE EPIDEMIOLOGICO
REINO UNIDO DE GRAN BRETAÑA E IRLANDADEL NORTE
REPUBLICA DE IRLANDA
II) CON RIESGO DE CASOS
A) EN ANIMALES NATIVOS
FRANCIA
SUIZA
PORTUGAL
B) EN ANIMALES NO NATIVOS NO EXISTIENDO INFOMACION POSTERIOR DE LO
ACTUADO CON LOS MISMOS
ALEMANIA
ITALIA
DINAMARCA
OMAN
III) CON SITUACION DESCONOCIDA Y/O EN ESTUDIO
OTROS PAISES NO INCLUIDOS EN LA LISTA Y DE LOS CUALES NO SE HAN
RECIBIDO INFORMES SOBRE SU SITUACION EPIDEMIOLOGICA
IV) LIBRES DE ENFERMEDADES
PAISES DE AMERICA
AUSTRALIA
NUEVA ZELANDIA
(Nota Infoleg: Por art. 1° de la Disposición N° 554/2001
de la Administración Nacional de Medicamentos, Alimentos y Tecnología
Médica B.O. 29/01/2001 se suspende temporariamente la Aplicación de los
Anexos I y III de la presente para los países que se indican a
continuación: Alemania, Bélgica, Dinamarca, España, Francia, Holanda,
Italia, Liechtenstein, Luxemburgo, Portugal, Suiza, Austria, Federación
Rusa, Finlandia, Lituania, Omán, Polonia, República Checa, Suecia)
ANEXO II
CATEGORIZACION DE RIESGO DE MATERIAS PRIMAS DE RUMIANTES POR EVENTUAL
TRANSMISION DE EEB AL HOMBRE
A) MEDICAMENTOS:
1) RIESGO ALTO
Obtenidos a partir de órganos del sistema nervioso central o sus
extractos y/o lisados.
2) RIESGO MEDIO
Obtenidos a partir de lleon, nódulos linfáticos, colon, bazo,
amígdalas, duramadre, glándula pineal, placenta, fluido cerebroespinal,
glándula pituitaria, glándula adrenal o sus extractos y/o
lisados.Colágeno, inyectable.
3) RIESGO BAJO O NO DEMOSTRADO
Obtenidos de: Mucosa nasal, nervio ciático, médula ósea, hígado,
pulmón, páncreas, timo, gelatina, suero fetal o sus extractos y/o
lisados.
Colágeno no inyectable.
Cartílago.
B) DISPOSITIVOS DE USO MEDICO
RIESGO MEDIO: Colágeno o gelatina a incorporar a dispositivos médicos,
para uso intravascular.
C) COSMETICOS
RIESGO BAJO O NO DEMOSTRADO: Colágeno (no inyectable), derivados de
colágeno, líquido amniótico o extractos, líquidos de placenta o
extractos, seroalbúmina, y serocalostrum. Sebo.
RIESGO
ALTO: Extractos biológicos, lisados y materiales obtenidos a partir del
sistema nervioso central, y RIESGO MEDIO: Extractos biológicos, lisados
y materiales obtenidos a partir de: lleon, nódulos linfáticos, colon,
bazo, amígdalas, duramadre, glándula pineal, placenta, fluido
cerebroespinal, glándula pituitaria y adrenal y colágeno inyectable. (Incorporado por art. 1° de la Disposición N° 1872/96 de la Administración Nacional de Medicamentos y Tecnología Médica B.O. 10/05/1996)
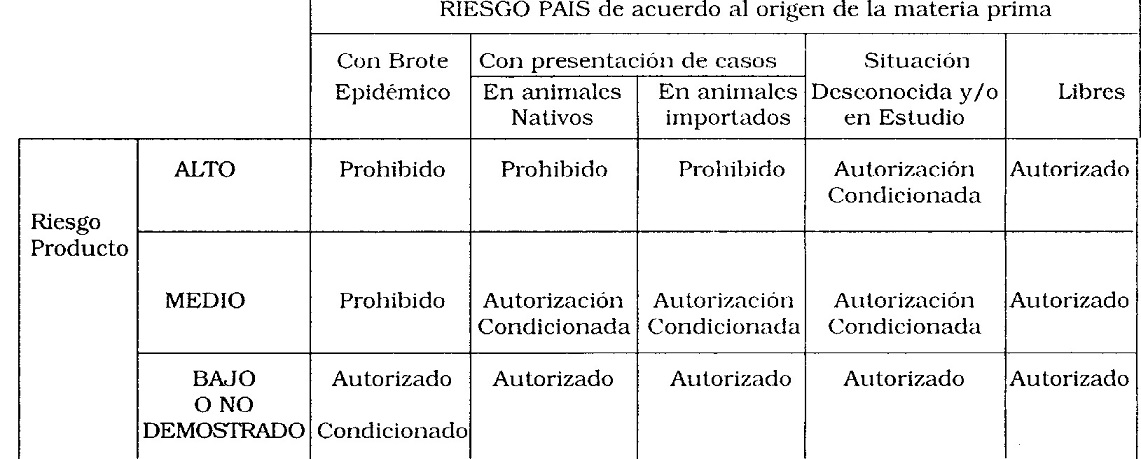
ANEXO III
MATRIZ DE DECISION PARA IMPORTACIONES SEGUN RIESGO PAIS - PRODUCTO PARA
EEB DE APLICACION EN MEDICAMENTOS, ELEMENTOS DE USO MEDICO Y COSMETICO
(Nota Infoleg: Por art. 1° de la Disposición N° 554/2001
de la Administración Nacional de Medicamentos, Alimentos y Tecnología
Médica B.O. 29/01/2001 se suspende temporariamente la Aplicación de los
Anexos I y III de la presente para los países que se indican a
continuación: Alemania, Bélgica, Dinamarca, España, Francia, Holanda,
Italia, Liechtenstein, Luxemburgo, Portugal, Suiza, Austria, Federación
Rusa, Finlandia, Lituania, Omán, Polonia, República Checa, Suecia)