MINISTERIO DE SALUD
Resolución 3437/2021
RESOL-2021-3437-APN-MS
Ciudad de Buenos Aires, 03/12/2021
Visto el Expediente Nº EX -2021-108855058-APN-DD#MS, la Ley 23.660, Ley
23.661, Ley 24.754, Decreto Nº492/95, la Resolución 201/02 del
Ministerio de Salud de la Nación sus ampliatorias y modificatorias y,
CONSIDERANDO:
Que la pubertad es un fenómeno biológico complejo a través del cual se
desarrollan los caracteres sexuales secundarios, se obtiene la
maduración sexual completa y se alcanza la talla adulta.
Que si la causa está dada por la reactivación prematura del generador
de pulsos de GnRH, la condición se conoce como pubertad precoz
verdadera o central (PPC).
Que este fenómeno, está regulado por la secreción y la pulsatilidad de
hormona liberadora de gonadotropinas (GnRH) por parte de las neuronas
hipotalámicas productoras de GnRH que estimulan el aumento de los
niveles de LH y FSH conduciendo al incremento de las concentraciones de
testosterona sérica en el hombre y de estrógenos séricos en la mujer.
Que alguna aceleración en estos mecanismos podría condicionar al
desarrollo de una Pubertad Precoz (PP) con la consiguiente aparición
progresiva de caracteres sexuales a edades tempranas (antes de los 8
años en niñas y 9 años en niños), generando la reactivación prematura
del generador de pulsos de GnRH, la condición se conoce como pubertad
precoz verdadera o central.
Que el mayor impacto de la PPC es la pérdida del potencial de talla
estimada, consecuencia del cierre prematuro epifisario, causada por la
rápida maduración esquelética secundaria a la exposición precoz de las
fisis a los esteroides gonadales, ocasionando una menor altura de la
esperada para sexo y genética del niño.
Que se estima una pérdida en varones de hasta 20 cm de altura y en
mujeres de 12 cm promedio, comparado con la talla adulta normal.
Que otras repercusiones estarían relacionadas con trastornos del ámbito
psicosocial por el desarrollo temprano de caracteres sexuales
secundarios en niños que presentan cierto grado de inmadurez y de
mentalidad infantil acarreando problemas emocionales y de
comportamiento, además de incremento en la frecuencia de otras
situaciones de riesgo como el adelanto en la actividad sexual, riesgo
de abuso sexual, consumo de sustancias tóxicas, trastornos de la
conducta alimentaria y depresión.
Que los niños con Pubertad Precoz Verdadera o Central, en edad más
temprana y con una progresión rápida de la maduración, son los que más
se benefician de la terapia porque tienen una fusión epifisaria
temprana y una talla adulta reducida si no se tratan. Por el contrario,
los niños que se acercan a la edad de la pubertad normal o que tienen
una variante muy lentamente progresiva de la pubertad precoz pueden no
necesitar tratamiento, sobre todo si su estatura adulta sin tratamiento
es concordante con el rango de estatura media de los padres.
Que la Pubertad Precoz Verdadera o Central es considerada una
enfermedad rara o poco frecuente, de claro predominio femenino,
incluida en el listado nacional de enfermedades poco frecuentes con la
codificación Orpha Nº759.
Que el tratamiento se lleva a cabo con los análogos del factor
hipotalámico liberador de gonadotrofinas (aGnRH), compuestos sintéticos
que provienen de modificaciones en la molécula del GnRH endógeno, que
le confieren mayor resistencia a la degradación enzimática, prolongando
su vida media y aumentando su actividad biológica. Éstos producen una
“desensibilización hipofisaria”, al disminuir el número de receptores
hipofisarios de GnRH y la consiguiente disminución en los niveles
circulantes de LH, FSH y esteroides gonadales.
Que esto se traduce en una detección e incluso regresión de los signos
puberales con un aumento de la predicción de la estatura final en los
pacientes con pubertad precoz.
Que dicho tratamiento tiene como objetivo inhibir la secreción gonadal
de esteroides, para así permitir un crecimiento y maduración sexual
normal, dependiendo la decisión de tratar, de múltiples variables, como
la edad de inicio y ritmo puberal, talla adulta estimada e impacto
psicológico del desarrollo sexual prematuro.
Que el tratamiento es indiscutible en formas rápidamente progresivas,
definido en base a criterios clínicos, radiológicos y bioquímicos,
mientras que no siempre se requiere en formas lentamente progresivas.
Que la administración de análogos de la gonadotrofina depende de su
dosificación presentando formulaciones de liberación sostenida de
varios agonistas de GnRH para dosis mensuales, trimestrales o
semestrales.
Que la Administración Nacional de Medicamentos, Alimentos y Tecnología
Médica (ANMAT) informa los productos inscriptos en el Registro de
Especialidades Medicinales (REM), de esa Administración Nacional, con
los Ingredientes Farmacéuticos Activos (IFAs) comercializados al día de
la fecha para el tratamiento de esta condición, detallados en ANEXO I
(IF-2021-112941560-APN-SSMEIE#MS): Leuprolida Acetato / Acetato de
Leuprolida / Leuprolide Acetato y Triptorelina / Triptorelina Pamoato.
Que el Decreto Nº 492 de fecha 26 de septiembre de 1995, determinó que
los beneficiarios de los agentes del Sistema Nacional del Seguro de
Salud (SNSS) comprendidos en el artículo 1° de la ley 23.660, tendrán
derecho a recibir las prestaciones médicos asistenciales que se
establezcan en el programa médico-asistencial, el cual es aprobado por
el Ministerio de Salud de la Nación a través de la ex Secretaria de
Políticas de Salud y Regulación Sanitaria.
Que dicho programa, denominado Programa Médico Obligatorio (PMO), se
encuentra actualmente contemplado en la Resolución N° 201/02 del
MINISTERIO DE SALUD, sus modificatorias y complementarias, por medio de
la cual se establece el catálogo mínimo de prestaciones básicas
esenciales que deben brindar los Agentes del Seguro de Salud, como
también todas las entidades comprendidas en el artículo 1° de la Ley N°
26.682.
Que para el supuesto de enfermedades poco frecuentes, el Art. 6º de la
Ley 26.689 establece que “Las obras sociales enmarcadas en las leyes
23.660 y 23.661, la Obra Social del Poder Judicial de la Nación, la
Dirección de Ayuda Social para el Personal del Congreso de la Nación,
las entidades de medicina prepaga y las entidades que brinden atención
al personal de las universidades, así como también todos aquellos
agentes que brinden servicios médicos asistenciales a sus afiliados
independientemente de la figura jurídica que posean, deben brindar
cobertura asistencial a las personas con EPF, incluyendo como mínimo
las prestaciones que determine la autoridad de aplicación”.
Que en dicho marco, resulta necesario incorporar en el PMO que deben
brindar los Agentes del Seguro de Salud y Entidades de Medicina Prepaga
a los medicamentos para el tratamiento de la Pubertad Precoz Central.
Que ha tomado la intervención propia de su competencia el PROGRAMA DE
ENFERMEDADES POCO FRECUENTES, dependiente de la DIRECCIÓN DE COBERTURAS
DE MEDICAMENTOS ESPECIALES Y DE ALTO PRECIO, la DIRECCIÓN NACIONAL DE
MEDICAMENTOS Y TECNOLOGÍA SANITARIA, la SUBSECRETARÍA DE MEDICAMENTOS E
INFORMACIÓN ESTRATÉGICA, así como la SECRETARÍA DE ACCESO A LA SALUD.
Que la DIRECCIÓN GENERAL DE ASUNTOS JURÍDICOS ha tomado la intervención de su competencia.
Que la medida es adoptada en el marco de las atribuciones acordadas por
el artículo 18 del Decreto Nº 486/02, el artículo 8 del Anexo I del
Decreto Nº 987/03, art. 1 del Decreto 492/95, la Ley de Ministerios N°
22.520, modificatorias y complementarias.
Por ello,
LA MINISTRA DE SALUD
RESUELVE:
ARTÍCULO 1°- Incorpórese en el punto 7 apartado 3, del Anexo I de la
Resolución N° 201/02 del Ministerio de Salud, sus ampliatorias y
modificatorias, que forma parte integrante del PROGRAMA MÉDICO
OBLIGATORIO (PMO), a los análogos de la gonadotrofina: Leuprolida
Acetato - también conocido como Leuprolide acetato o Acetato de
leuprolida- Triptorelina y Triptorelina pamoato, detallados en el ANEXO
I que, identificado como IF-2021-112941560-APN-SSMEIE#MS, forma parte
integrante de la presente con cobertura al CIEN POR CIENTO 100% para
los pacientes bajo tratamiento de Pubertad Precoz Central.
ARTÍCULO 2 °- Incorpórese en el Anexos III de la Resolución N° 201/02
del Ministerio de Salud sus ampliatorias y modificatorias, los
principios activos Leuprolida Acetato - también conocido como
Leuprolide acetato o Acetato de leuprolida- Triptorelina y Triptorelina
pamoato, en las formas farmacéuticas y presentaciones que se detallan
en el Anexo I de la presente Resolución.
ARTÍCULO 3° - Incorpórese en el Anexos IV de la Resolución N° 201/02
del Ministerio de Salud sus ampliatorias y modificatorias, los
principios activos Leuprolida Acetato - también conocido como
Leuprolide acetato o Acetato de leuprolida- Triptorelina y Triptorelina
pamoato, en las formas farmacéuticas y presentaciones que se detallan
en el Anexo I de la presente Resolución.
ARTÍCULO 4°- La presente medida comenzará a regir a partir del día siguiente de su publicación en el Boletín Oficial.
ARTICULO 5°- Comuníquese, publíquese, dese a la Dirección Nacional del Registro Oficial y oportunamente archívese.
Carla Vizzotti
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la edición web del BORA -www.boletinoficial.gob.ar-
e. 06/12/2021 N° 93747/21 v. 06/12/2021
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
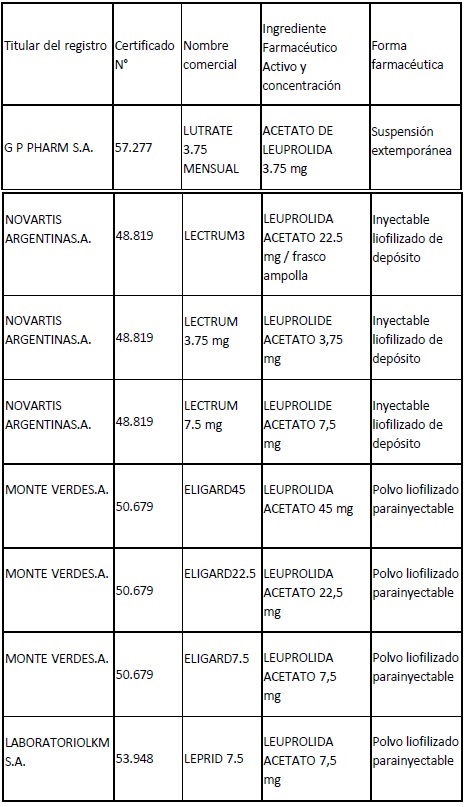
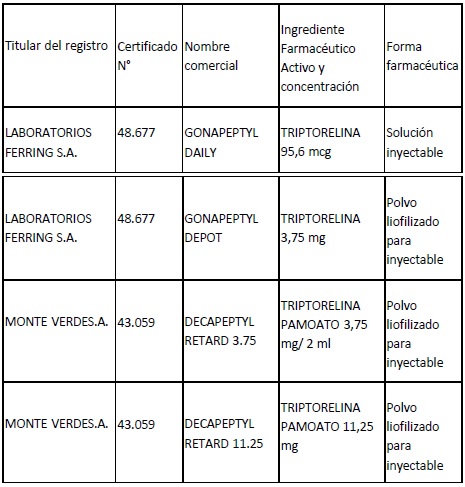
ANEXO I. Productos inscriptos en el
Registro de Especialidades Medicinales (REM) con los Ingredientes
Farmacéuticos Activos (IFAs) comercializados al día de la fecha:
Con el IFA Leuprolida Acetato / Acetato de Leuprolida / Leuprolide Acetato:
IF-2021-112941560-APN-SSMEIE#MS