MINISTERIO DE SALUD
Resolución 2820/2022
RESOL-2022-2820-APN-MS
Ciudad de Buenos Aires, 14/11/2022
VISTO el EX-2022-106587308- -APN-DD#MS, la Ley Nº 23.753 y sus
modificatorias, el Decreto Nº 1.286 del 6 de agosto de 2014, la
Resolución Nº 1.156 del 23 de julio de 2014 del MINISTERIO DE SALUD, la
Resolución Nº 423 del 14 de noviembre de 2018 y su Resolución
rectificatoria Nº 764 del 12 de diciembre de 2018, ambas de la entonces
SECRETARÍA DE GOBIERNO DE SALUD, y
CONSIDERANDO:
Que por Ley Nº 23.753 se asigna competencia al MINISTERIO DE SALUD DE
LA NACIÓN para coordinar, junto a las autoridades sanitarias de todo el
país, la planificación de acciones tendientes a asegurar a las personas
con diabetes los medios terapéuticos que requieran para su tratamiento,
así como los medios para su control evolutivo.
Que mediante la Ley N° 26.914 se incorpora a la Ley N° 23.753 el
artículo 5°, por el que se dispone que la autoridad de aplicación debe
establecer las “Normas de Provisión de Medicamentos e Insumos”, las que
deberán ser revisadas y actualizadas como mínimo cada dos años a fin de
poder incluir en la cobertura los avances farmacológicos y tecnológicos
que resulten de aplicación en la terapia y promuevan una mejora en la
calidad de vida a personas con diabetes.
Que el Decreto N° 1.286/2014 señala que deberán disponerse las medidas
necesarias para garantizar a las personas con diabetes el
aprovisionamiento de los medicamentos y reactivos de diagnóstico para
autocontrol que se estimen como elementos indispensables para un
tratamiento adecuado, según lo establecido por las normas técnicas
aprobadas por autoridad competente en el orden nacional, y que su
financiación corresponde a la Seguridad Social, a la medicina privada
y, en caso de pacientes carentes de dichas coberturas, a cargo del
gobierno de la jurisdicción.
Que mediante la Resolución Nº 423/2018 de la ex SECRETARÍA DE GOBIERNO
DE SALUD se aprobó la actualización de las “NORMAS DE PROVISIÓN DE
MEDICAMENTOS E INSUMOS PARA PERSONAS CON DIABETES” (ANEXO I), pasando a
integrar el Sistema de Prestaciones Médicas Obligatorias (PMO), y el
“MODELO DE CERTIFICADO PARA LA ACREDITACION DE PERSONAS CON DIABETES”
(ANEXO II) que todos los Agentes del SISTEMA NACIONAL DEL SEGURO DE
SALUD enmarcados en las Leyes N° 23.660 y N° 23.661, las Entidades de
Medicina Prepaga (Ley N° 26.682), el INSTITUTO NACIONAL DE SERVICIOS
SOCIALES PARA JUBILADOS Y PENSIONADOS (Ley N° 19.032), la OBRA SOCIAL
DEL PODER JUDICIAL DE LA NACIÓN, la DIRECCION DE AYUDA SOCIAL PARA EL
PERSONAL DEL CONGRESO DE LA NACIÓN, el INSTITUTO DE OBRA SOCIAL DE LAS
FUERZAS ARMADAS y las OBRAS SOCIALES UNIVERSITARIAS (Ley N° 24.741)
pueden expedir a través de sus efectores.
Que en relación a la certificación para la acreditación de persona con
diabetes, se ha tenido en cuenta que la condición de enfermedad crónica
no caduca, se realizará al momento del diagnóstico y seguirá vigente
mientras el paciente revista su condición de tal.
Que los ANEXOS I y II mencionados anteriormente fueron rectificados por
la Resolución Nº 764/2018 de la ex SECRETARIA DE GOBIERNO DE SALUD.
Que por otra parte, revisiones sistemáticas y metaanálisis de ensayos
clínicos demostraron que la Educación Diabetológica para el Automanejo
(EDAM) mejora el control glucémico y reduce las complicaciones y
mortalidad, por lo que resulta un insumo esencial para ser incorporado.
Que las guías de práctica clínica de alta calidad metodológica
recomiendan la EDAM debido a que permite mejorar la adherencia al
tratamiento y el control glucémico, dotar a las personas de
conocimientos para el autocuidado y reducir las complicaciones y la
mortalidad, entre otros.
Que la EDAM es un proceso colaborativo y estructurado destinado a
facilitar el desarrollo de los conocimientos, habilidades y cambios de
actitud que se requieren para el autocontrol exitoso de la diabetes
mellitus (DM).
Que dicho concepto se fundamenta en considerar de manera integral el
cuidado de la diabetes, consistiendo en una educación estructurada para
las personas con DM o sus cuidadores, para el caso de que las personas
con DM no puedan realizar su autocuidado.
Que, en tal sentido, se ha evaluado y definido a la EDAM para su incorporación al PMO.
Que considerando las modificaciones realizadas a la Ley Nº 23.753 a
partir del dictado de la Ley Nº 26.914, la DIRECCIÓN NACIONAL DE
ABORDAJE INTEGRAL DE ENFERMEDADES NO TRANSMISIBLES ha elaborado una
propuesta de actualización a las Normas de Provisión de Medicamentos e
Insumos, la cual fue tratada y consensuada en las reuniones de la
COMISIÓN PERMANENTE ASESORA DE DIABETES celebradas los días 6 y 27 del
mes de septiembre de 2022.
Que la SUBSECRETARÍA DE ESTRATEGIAS SANITARIAS y la SECRETARÍA DE ACCESO A LA SALUD han prestado la debida conformidad.
Que la DIRECCION GENERAL DE ASUNTOS JURIDÍCOS ha tomado la intervención de su competencia.
Que la presente medida se dicta en uso de las facultades conferidas por
la Ley de Ministerios Nº 22.520 (T.O. Decreto N° 438/1992), sus
modificatorias y complementarias, y el artículo 5° del Decreto N°
1286/2014.
Por ello,
LA MINISTRA DE SALUD
RESUELVE:
ARTÍCULO 1°.- Déjanse sin efecto las Resoluciones N° 423/2018 y N° 764/2018, ambas de la ex SECRETARÍA DE GOBIERNO DE SALUD.
ARTÍCULO 2°.- Apruébase la actualización de las “NORMAS DE PROVISION DE
MEDICAMENTOS E INSUMOS PARA PERSONAS CON DIABETES” que como ANEXO I
(IF-2022-117115865-APN-DNAIENT#MS) forma parte de la presente norma y
pasará a integrar el Sistema de Prestaciones Médicas Obligatorias.
ARTÍCULO 3º.- Apruébase el nuevo “MODELO DE CERTIFICADO PARA LA
ACREDITACION DE PERSONAS CON DIABETES” que como ANEXO II
(IF-2022-117117186-APN-DNAIENT#MS) forma parte de la presente norma.
Esta certificación se hará al momento del diagnóstico y seguirá vigente
mientras el paciente revista el carácter de enfermo crónico.
ARTÍCULO 4º.- Apruébase e incorpórase al Programa Médico Obligatorio la
provisión de Programas de Educación Diabetológica para el Automanejo
para todas las personas con diabetes mellitus o las personas cuidadoras
de las mismas, según corresponda, los que se estructurarán y dictarán
de acuerdo a lo establecido en el ANEXO III
(IF-2022-117118173-APN[1]DNAIENT#MS) que forma parte de la presente
medida.
ARTÍCULO 5º.- Las Obras Sociales nacionales, las Entidades de Medicina
Prepaga, el INSTITUTO NACIONAL DE SERVICIOS SOCIALES PARA JUBILADOS Y
PENSIONADOS, la OBRA SOCIAL DEL PODER JUDICIAL DE LA NACIÓN, la
DIRECCION DE AYUDA SOCIAL PARA EL PERSONAL DEL CONGRESO DE LA NACIÓN,
el INSTITUTO DE OBRA SOCIAL DE LAS FUERZAS ARMADAS y las OBRAS SOCIALES
UNIVERSITARIAS deberán establecer los procedimientos administrativos
necesarios a fin de garantizar la provisión de medicamentos e insumos y
la Educación Diabetológica para el Automanejo acorde a lo estipulado en
los respectivos ANEXOS I y III de la presente norma.
ARTÍCULO 6°.- Invítase a las jurisdicciones provinciales y a la CIUDAD
AUTONOMA DE BUENOS AIRES a instrumentar los mecanismos necesarios
tendientes a garantizar la cobertura a las personas con diabetes
mellitus que no estén comprendidas en el Sistema Nacional de Seguro de
Salud.
ARTÍCULO 7°.- Comuníquese, publíquese, dese a la DIRECCIÓN NACIONAL DEL REGISTRO OFICIAL y archívese.
Carla Vizzotti
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la edición web del BORA -www.boletinoficial.gob.ar-
e. 16/11/2022 N° 93283/22 v. 16/11/2022
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
ANEXO I
Normas de Provisión de Medicamentos e Insumos para Personas con Diabetes Mellitus.
Las modificaciones a la norma precedente contenidas en este reglamento
están basadas en una búsqueda exhaustiva, selección y análisis crítico
de la evidencia proveniente de Guías de Práctica Clínica, revisiones
sistemáticas y metaanálisis de alta calidad metodológica referentes a
la temática, valorando especialmente la efectividad clínica y seguridad
de las personas con diabetes mellitus.
Glosario
AMG: automonitoreo glucémico
ARAII: antagonistas de los receptores de la angiotensina II
DM1: diabetes mellitus tipo 1
DM2: diabetes mellitus tipo 2
EDAM: educación diabetológica para el automanejo
HbA1c: hemoglobina glicosilada A1c
iDPP4: inhibidores de la dipeptidil peptidasa 4
IECA: inhibidores de la enzima convertidora de angiotensina
IFGe: índice de filtrado glomerular estimado
ISCI: infusor subcutáneo continuo de insulina
iSGLT2: inhibidor del receptor del cotransportador sodio-glucosa tipo 2
MG-i: sistema de monitoreo de glucosa intermitente o flash
NPH: Neutral Protamine Hagedorn.
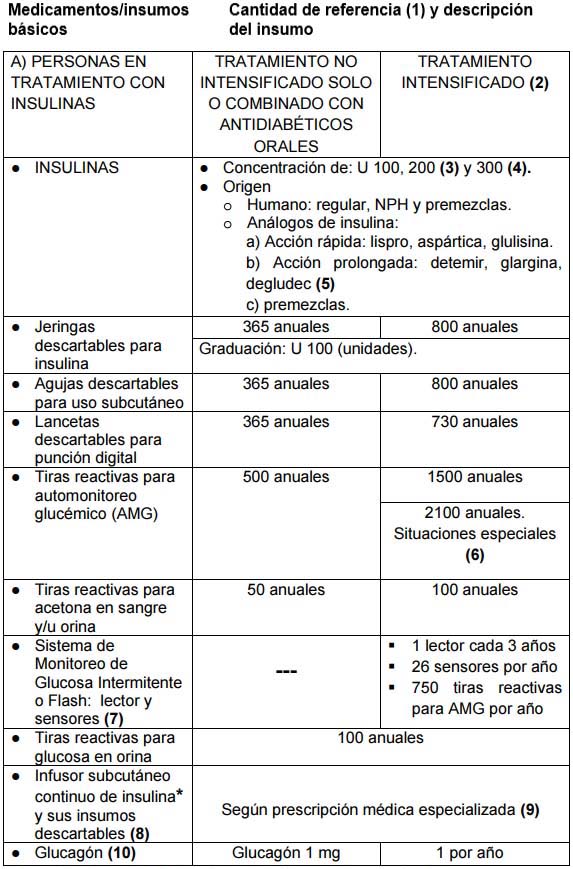
MEDICAMENTOS E INSUMOS COMPRENDIDOS:
* también denominado bomba de infusión continua de insulina
(1) Cantidades de referencia: son
aquellas establecidas para dar respuesta adecuada a la gran mayoría de
las personas con diabetes en los diferentes esquemas terapéuticos
recomendados. Pueden ser modificadas ante casos particulares
debidamente documentados mediante historia clínica y registro semanal
de glucemias.
(2) Tratamiento intensificado:
consiste en administración de insulina basal (NPH dos a tres veces al
día, insulina detemir dos veces al día o insulina glargina/degludec una
vez al día), más insulina adicional de acción rápida en relación a las
ingestas (insulina regular o análogos rápidos), o infusor subcutáneo
continuo de insulina. El tratamiento intensificado será indicado por
médico/a especializado/a
(9).
(3) Insulina lispro U200: solamente
si el precio por unidad de insulina lispro de la concentración U200 no
supera el precio por unidad de insulina lispro de concentración U100.
(4) Insulina glargina U300: solamente
en personas con DM1 si el precio por unidad de insulina glargina de la
concentración U300 no supera el precio por unidad de insulina glargina
de concentración U100.
(5) Insulina degludec: personas
con DM1 que presenten hipoglucemias nocturnas con insulina glargina y/o
detemir, habiéndose evaluado previamente: técnica de inyección, sitios
de inyección, habilidades de autocontrol, conocimiento y habilidades de
autogestión, estilo de vida, dificultades psicológicas y psicosociales,
posibles causas orgánicas como la gastroparesia.
Deberán presentar la indicación acompañada de un resumen de historia
clínica del médico/a especializado/a que incluya el registro de las
hipoglucemias y la evaluación de los criterios mencionados previamente.
(6) Situaciones especiales:
tratamiento intensificado con riesgo frecuente de hipoglucemias o
infusor subcutáneo continuo de insulina o gestantes con diabetes
pregestacional o gestacional con insulina o mujer con diabetes que
planifica su embarazo.
(7) Sistema de Monitoreo de Glucosa Intermitente o Flash (MG-i):
ante indicación expresa y fundamentada de médico/a especializado/a y
entrenado/a en el manejo de la tecnología. Su otorgamiento deberá ser
evaluado y aprobado por la auditoría de la entidad que corresponda,
utilizando como referencia los siguientes criterios:
Personas con Diabetes Mellitus tipo 1 que presenten todas las siguientes condiciones en forma simultánea:
1. estar bajo tratamiento intensificado con insulina (2) durante por lo menos 6 meses,
2. realizar 6 o más AMG por día, durante por lo menos los últimos 3 meses,
3. haber recibido educación diabetológica para el automanejo (EDAM) y realizar adecuadamente conteo de hidratos de carbono,
4. tener capacidad de realizar las tareas necesarias para el uso de
esta tecnología en forma segura y efectiva, por parte de la persona con
DM1 o su cuidador,
5. compromiso a utilizar el MG-i por lo menos el 70% del tiempo,
6. a las anteriores debe sumarse al menos una de las siguientes:
❖ requerir la realización de 6 o más AMG por día para conseguir la meta individualizada de control glucémico (HbA1c),
❖ presentar uno o más episodios por año de hipoglucemia nivel 3
(hipoglucemia asociada a disfunción cognitiva severa que requiere ayuda
externa) sin causa obvia prevenible,
❖ padecer hipoglucemias nocturnas a pesar del refuerzo de EDAM y haber descartado causas obvias prevenibles,
❖ pérdida de la sensibilidad en los pulpejos de los dedos por el uso
frecuente de la medición de glucosa capilar afectando el desempeño en
su actividad laboral (ejemplo músicos) o personas con discapacidad
visual que leen Braille.
Criterios de suspensión del MG-i, uno o más de los siguientes:
• Cuando la persona con DM1 lo desea.
• Ante reacciones cutáneas asociadas al adhesivo del sensor u otros efectos adversos causados por el dispositivo.
• Paciente que no utilice el sistema al menos el 70% del tiempo, medido a través de las lecturas del sensor.
• Si la tasa de ocurrencia de hipoglucemias nivel 3 y/u otras
complicaciones graves sean iguales o mayores a la tasa del año previo
al inicio del uso del dispositivo.
• Si el/la paciente utiliza un número de tiras de glucemia capilar similar al que venía usando antes de facilitarle el sensor.
Nota: la persona con Diabetes
Mellitus tipo 1 beneficiaria del MG-i requiere continuar con la
cobertura de 750 tiras reactivas para automonitoreo glucémico (AMG) por
año.
(8) Infusor subcutáneo continuo de insulina (ISCI) (también denominado bomba de infusión continua de insulina):
ante indicación expresa y fundamentada de médico/a especializado/a y
entrenado/a en el manejo de la tecnología. No prescribir por nombre
comercial. Su otorgamiento deberá ser evaluado y aprobado por la
auditoría de la entidad que corresponda, utilizando como referencia los
Lineamientos Técnicos para la prescripción de los ISCI del Ministerio
de Salud de la Nación, los cuales serán publicados en la página web
oficial del mismo.
(9) Prescripción médica especializada:
Médicos/as especialistas en Endocrinología y/o Nutrición, y aquellos
especialistas en Clínica Médica, Medicina General y Pediatría, que
acrediten capacitación en Diabetes (Especialización Universitaria a
través de carreras de especialización y/o maestrías, capacitación en
sociedades científicas afines).
(10) Glucagón: Glucagón 1 mg en
personas con diagnóstico de DM1. Uno por año. Se autorizará la
cobertura del glucagón más de una vez al año si la persona con DM1
confirma su utilización a través de resumen de historia clínica del
profesional tratante.
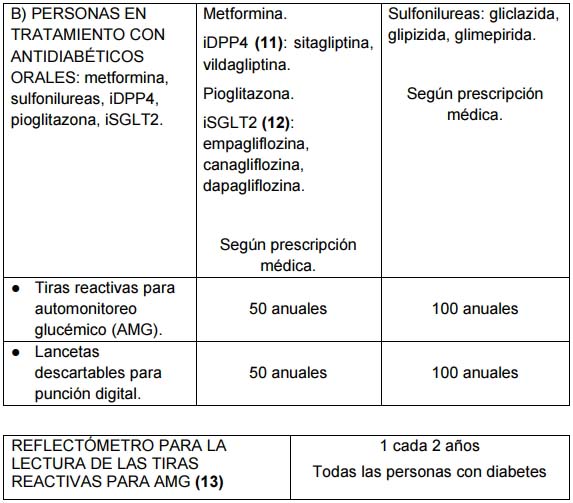
(11) Sitagliptina o Vildagliptina (gliptinas o iDPP-4):
1. En personas adultas con DM2 como tratamiento complementario de la metformina cuando la persona presente
todos estos criterios simultáneamente:
• No logre la meta de HbA1c con dosis máxima tolerada de metformina (con 3 a 6 meses de tratamiento documentado).
• No tenga contraindicaciones para la utilización de iDPP-4.
• Los valores de HbA1 c no superen en más del 1 % del valor meta.
• Presente riesgo aumentado de hipoglucemia.
2. En personas adultas con DM2 como tratamiento alternativo a la metformina cuando la persona presente
todos estos criterios simultáneamente:
• Contraindicaciones para el uso de la metformina.
• No tenga contraindicaciones para la utilización de iDPP-4.
• Sus valores de HbA1 c no superen en más del 1 % del valor meta.
• Presente riesgo aumentado de hipoglucemia.
(12) Empaglifloziona, Canagliflozina o Dapagliflozina (iSGLT2)
en personas adultas con DM2 que no alcancen meta individualizada de
HbA1c con el tratamiento antidiabético instaurado y que además
presenten:
• enfermedad cardiovascular establecida y/o
• nefropatía diabética en tratamiento con IECA o ARAII.
Nota: a los fines de implementar la cobertura se considera:
• enfermedad cardiovascular establecida: antecedentes de infarto agudo
de miocardio, angina crónica estable diagnosticada por prueba
provocadora de isquemia con ejercicio o fármacos, cirugía de
revascularización miocárdica o angioplastia previa, y/o internación por
angina inestable con cambios en el ECG y/o marcadores serológicos
(troponina).
• nefropatía diabética: índice de filtrado glomerular estimado igual o
menor a 60 ml/min y/o presencia de albuminuria mayor a 30 mg/g por más
de 3 meses.
(13) Incluye reflectómetro
parlante en aquellas personas con DM y discapacidad visual. La
prescripción de los mismos no podrá efectuarse por nombre comercial.
PROCEDIMIENTOS PROPUESTOS PARA EL SUMINISTRO DE MEDICAMENTOS Y OTROS INSUMOS
Las obras sociales y las empresas de medicina prepaga establecerán los
procedimientos administrativos necesarios a fin de garantizar la
provisión de medicamentos e insumos de la presente norma a las personas
con diabetes comprendidas en dichos subsistemas. Para aquellas no
pertenecientes a estas dos modalidades de cobertura anterior, cada
jurisdicción provincial y la Ciudad Autónoma de Buenos Aires podrán
instrumentar los mecanismos necesarios teniendo en cuenta el domicilio
de la persona con diabetes, el diagnóstico con certificado médico
otorgado por establecimiento público o servicio asistencial estatal en
que tendrá que estar registrado y al cual concurriría para control y
tratamiento. Dicho procedimiento estará a cargo de profesionales
habilitados por la autoridad competente. Dicho certificado deberá
contener los datos correspondientes al formulario de acreditación para
personas con diabetes (Anexo II).
Cancelación de beneficios: la cancelación de los beneficios a que se
refiere la presente normativa operará en los siguientes casos: a.
Renuncia del titular del beneficio. b. Radicación del beneficiario
fuera del país. c. Abandono del control médico periódico regular en el
establecimiento donde esté registrado. d. Incompatibilidad con otros
beneficios.
IF-2022-117115865-APN-DNAIENT#MS

ANEXO II:
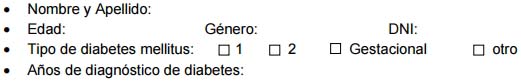
MODELO DE CERTIFICADO PARA LA ACREDITACIÓN DE LA CONDICION DE PERSONA CON DIABETES MELLITUS
DATOS FILIATORIOS.
DATOS DEL EXAMEN FÍSICO.
COMPLICACIONES.
COMORBILIDAD.
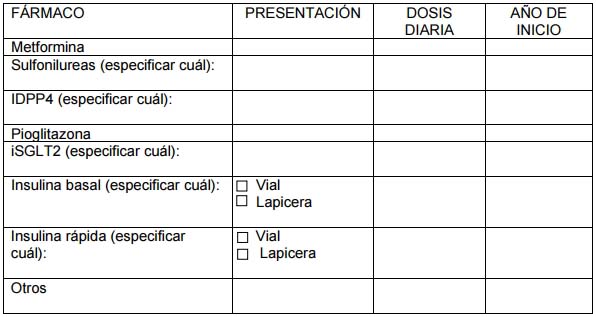
DATOS REFERIDOS AL TRATAMIENTO.
EXAMENES (últimos 12 meses)
Abreviaturas:
• IMC: índice de masa corporal.
• RD: retinopatía diabética.
• RDNP: retinopatía diabética no proliferativa.
• RDP: retinopatía diabética proliferativa.
IF-2022-117117186-APN-DNAIENT#MS

ANEXO III
Características de los programas de Educación Diabetológica para el Automanejo (EDAM)
• Destinatarios: personas con diabetes mellitus (DM) o sus cuidadores
(padre, madre o cualquier persona que se encuentre con la
responsabilidad de cuidados del paciente con diabetes) en el caso que
la persona con DM no pueda realizar su autocuidado.
• Formato: individual o grupal, o bien combinación de ambos.
• Modalidad: participativa, interactiva.
• Currículum estructurado con objetivos generales y específicos que deberá incluir:
o conocimiento de la DM y factores de riesgo cardiovasculares,
o estilo de vida saludable (actividad física, alimentación saludable,
no fumar, ambientes libres de humo, reducción y control del peso,
reducción del consumo de alcohol y otros),
o tratamiento farmacológico,
o técnica de automonitoreo glucémico (a quienes lo requieran),
o técnica de aplicación de insulina (cuando corresponda),
o prevención, detección y tratamiento de hipoglucemias,
o prevención, detección y tratamiento de complicaciones agudas y crónicas,
o cuidados de los pies,
o adherencia al tratamiento farmacológico y no farmacológico,
o plan de vacunación,
o situaciones especiales (manejo de la DM en días de enfermedad, viajes, etc.),
o conteo de hidratos de carbono, utilización de infusor subcutáneo
continuo de insulina y otras tecnologías, en quienes corresponda.
• Duración de la EDAM:
o inicial: 10 horas, en todas las
personas con DM independientemente del tipo. Deberá realizarse
preferentemente dentro del primer año del diagnóstico,
o en cualquier momento sea cual fuere el tiempo de evolución de la enfermedad en aquellas personas que no la hayan recibido.
o refuerzo: 2 horas/año. En las personas con DM que:
✓ presenten DM tipo 1 o
✓ presenten mal control metabólico o
✓ en quienes se realicen cambios en el tratamiento.
o conteo de hidratos de carbono,
utilización de infusor subcutáneo continuo de insulina, otras
tecnologías: pueden requerir mayor carga horaria inicial y de refuerzo.
• Perfil de personas educadoras:
o Profesionales Médicos, Licenciados en Nutrición, Licenciados en
Enfermería, Agentes Sanitarios, Enfermeros Profesionales, Técnicos
Superiores en Enfermería y Enfermeros Universitarios que asistan a
personas con diabetes en su práctica clínica cotidiana y cuenten con
capacitación específica en EDAM, y
o Médicos especialistas en Endocrinología y/o Nutrición, y
o Médicos especialistas en Clínica Médica, Medicina General y/o
Familiar y Pediatría, que acrediten capacitación en Diabetes
(Especialización Universitaria a través de carreras de especialización
y/o maestrías, capacitación en sociedades científicas afines).
IF-2022-117118173-APN-DNAIENT#MS