ADMINISTRACIÓN
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
Disposición 9465/2022
DI-2022-9465-APN-ANMAT#MS
Ciudad de Buenos Aires, 23/11/2022
VISTO: las Disposiciones ANMAT Nº 3185/99 con sus complementarias y
modificatorias, 5040/06 y sus modificatorias, 758/09, 6677/10 con sus
complementarias y modificatorias, 4132/12,4133/12, 1918/13, 5068/19,
9944/19, 4540/20, 5640/22, el EX-2021-88047862-APN-DERM#ANMAT, y
CONSIDERANDO:
Que por DI-2020-4540-APN-ANMAT#MS se creó la Comisión Asesora en
Bioequivalencia-Biodisponibilidad.
Que entre sus funciones se encuentra la de aconsejar la incorporación
de ingredientes farmacéuticos activos para estudios de Bioequivalencia
y/o Biodisponibilidad, de Equivalencia in-vitro y Bioexenciones, y
establecer las pautas de actualización de los cronogramas que
oportunamente se establezcan; como así también coordinar la confección
de un listado, con actualización permanente, de los principios activos
sobre los que se hayan efectuado estudios de Bioequivalencia y/o
Biodisponibilidad y proponer la inclusión del mismo en la página Web de
la ANMAT, así como los productos de referencia que deban ser utilizados
para la aceptación de los estudios (conf. art. 4°, inc. c y d de la
Disposición ANMAT N° 4540/20)
Que por Disposición ANMAT Nº 3185/99 se aprobaron recomendaciones para
la realización de estudios de bioequivalencia de medicamentos de riesgo
sanitario significativo y se estableció un cronograma de implementación
gradual en consideración a los antecedentes internacionales en la
materia.
Que en la aludida Disposición se establecen los métodos idóneos para
demostrar equivalencia In Vivo y equivalencia In Vitro.
Que mediante disposiciones posteriores, la ANMAT ha ido incorporando
ingredientes farmacéuticos activos a la obligatoriedad de demostración
de estudios de bioequivalencia.
Que el grado de desarrollo alcanzado actualmente por el sistema
fiscalizador de nuestro país incluye el diseño y presentación de
protocolos de investigación en farmacología clínica, cuyos requisitos
se encuentran establecidos por la Disposición ANMAT N° 6677/10, que
aprueba el Régimen de Buena Práctica Clínica para Estudios en
Farmacología Clínica.
Que por la Disposición ANMAT Nº 5040/06 se aprueba el Régimen de Buenas
Práctica para la realización de Estudios de Biodisponibilidad y
Bioequivalencia.
Que por la Disposición ANMAT Nº 4133/12 se establece que solo se
deberán presentar resultados de estudios de bioequivalencia cuando los
mismos se hallen comprendidos dentro del intervalo de confianza del 90%
de 0,80-1,25 tanto para Concentración Máxima como para Área Bajo la
Curva.
Que por la Disposición ANMAT N° 1918/13 se establecen los criterios de
selección de una especialidad medicinal como producto de referencia
para estudios de Bioequivalencia y Equivalencia in vitro.
Que por la Disposición ANMAT N° 9944/19 se establecen los requisitos y
condiciones que deben cumplir los Centros Clínicos para ser autorizados
a realizar Estudios de Farmacología Clínica de Bioequivalencia.
Que por la Disposición ANMAT N° 758/09 se adoptaron los Criterios de
Bioexencion de Estudios de Bioequivalencia basados en la Clasificación
Biofarmacéutica para las formas farmacéuticas sólidas orales de
liberación inmediata, con alcance para algunos de los principios
activos establecidos en la Disposición ANMAT N° 3185/99 como de riesgo
intermedio y los que en un futuro se vayan incorporando, así como las
exigencias que se deberán cumplir para demostración de Bioexención.
Que por la Disposición ANMAT N° 4132/12 se incorporó a la exigencia de
demostración de bioequivalencia, establecida en la Disposición ANMAT N°
3185/99, a todas las concentraciones de una especialidad medicinal de
forma farmacéutica sólida oral que contenga alguno de los IFAs con
requerimiento de bioequivalencia,
Que en el mercado local existen especialidades medicinales que
contienen IFAs que pueden ser tomados como referencia para la
realización de estos estudios.
Que en tal sentido la Comisión Asesora en
Bioequivalencia-Biodisponibilidad mediante
IF-2022-56165065-APN-DERM#ANMAT se ha expedido al respecto aconsejando
la inclusión de nuevos IFAs a la exigencia de realización de estudios
de Bioequivalencia y/o Biodisponibilidad.
Que asimismo brinda información sobre los Productos de Referencia para
estos IFAs.
Que el Instituto Nacional de Medicamentos y la Dirección de Asuntos
Jurídicos han tomado la intervención de su competencia.
Que se actúa en virtud de las facultades conferidas por el Decreto Nº
1490/92 y sus modificatorios.
Por ello,
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACIÓN NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
DISPONE:
ARTÍCULO 1º.- Incorpóranse a la exigencia de realización de estudios de
Bioequivalencia establecida por la Disposición ANMAT Nº 3185/99, a los
siguientes Ingredientes Farmacéuticos Activos (IFAs):
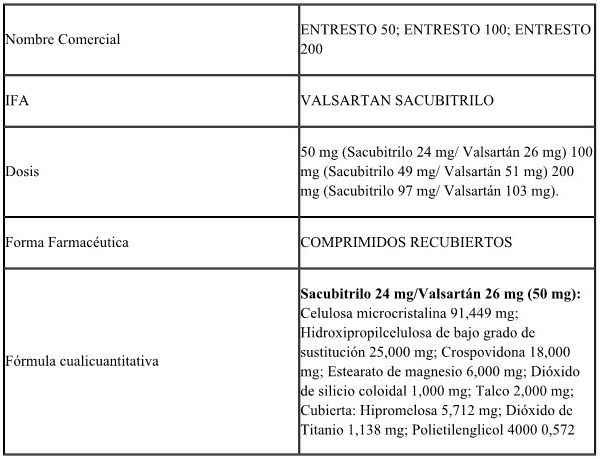
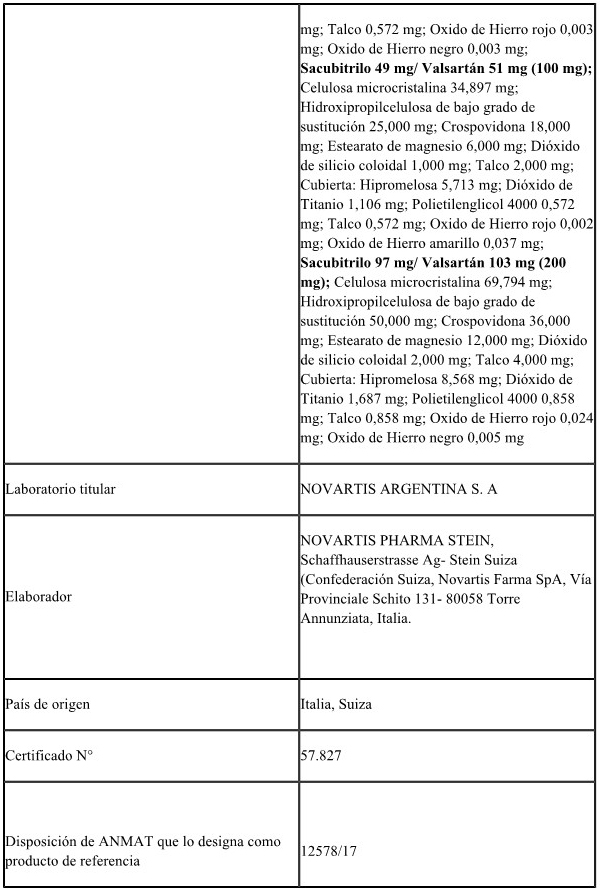
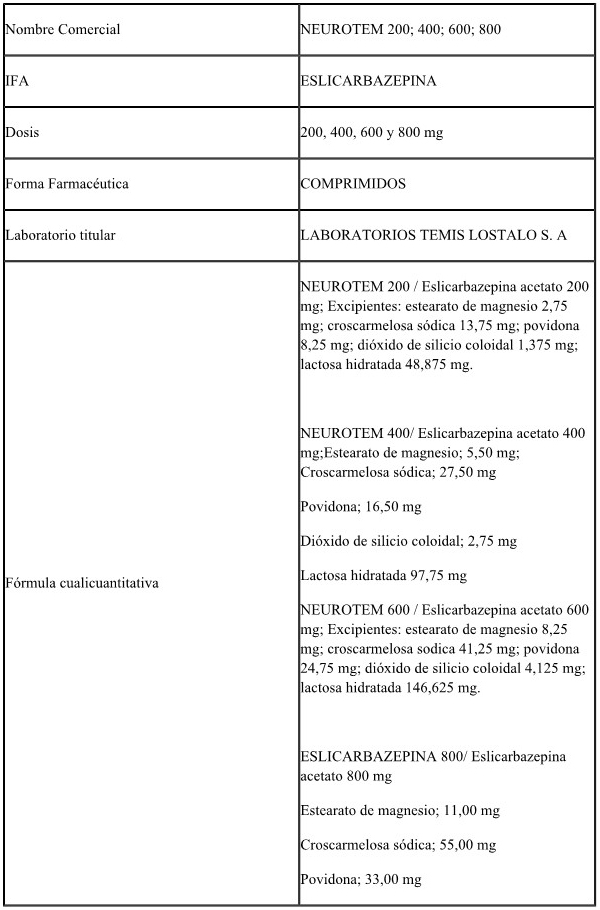
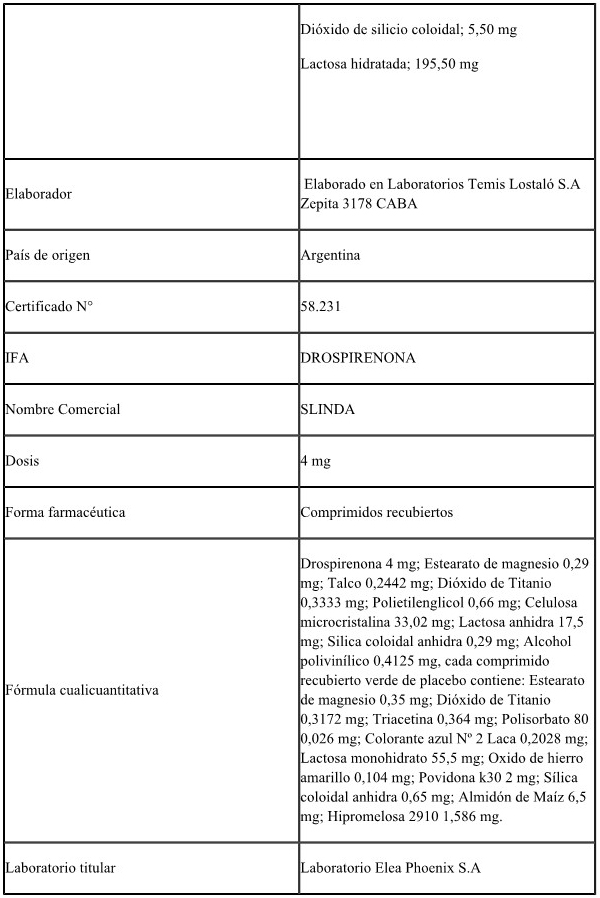
VALSARTAN-SACUBITRILO, ESLICARBAZEPINA, DROSPIRENONA y FINGOLIMOD.
ARTÍCULO 2º.- Establécense como productos de referencia a los
enumerados en el Anexo I (IF-2022-23116724-APN-DERM#ANMAT) que forma
parte integrante de la presente disposición.
ARTÍCULO 3º.- Para los laboratorios titulares de especialidades
medicinales con bioequivalencia demostrada para una de sus
concentraciones y que posean más de una concentración comercializada,
deberán cumplimentar las Disposiciones ANMAT Nº 758/09 y N° 4132/12, o
las que en un futuro las complementen o reemplacen, presentando los
protocolos de solicitud de bioexención para todas las concentraciones,
según Disposición ANMAT Nº 5068/19, o la que en un futuro la
complementeo reemplace.
ARTÍCULO 4°.-La presente disposición entrará en vigencia a partir del
día siguiente al de su publicación en el Boletín Oficial.
ARTÍCULO 5°.- Dése a la Dirección Nacional del Registro Oficial para su
publicación. Dése a la Dirección de Gestión de Información Técnica, al
Instituto Nacional de Medicamentos, a la Dirección de Evaluación y
Registro de Medicamentos y a la Dirección de Relaciones
Institucionales. Comuníquese a las Cámaras de la industria farmacéutica
CILFA, CAEME, COOPERALA, CAPGEN, CAPEMVEL ySAFyBI. Cumplido archívese.
Manuel Limeres
NOTA: El/los Anexo/s que integra/n este(a) Disposición se publican en
la edición web del BORA -www.boletinoficial.gob.ar-
e. 25/11/2022 N° 96393/22 v. 25/11/2022
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
ANEXO I
PRODUCTOS DE REFERENCIA PARA ESTUDIOS DE BIOEQUIVALENCIA