ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
Disposición 1387/2023
DI-2023-1387-APN-ANMAT#MS
Ciudad de Buenos Aires, 15/02/2023
VISTO el Expediente EX-2022-108784196-APN-DGA#ANMAT del registro de
esta Administración Nacional de Medicamentos, Alimentos y Tecnología
Médica; y
CONSIDERANDO
Que en las actuaciones citadas en el VISTO la Dirección de Evaluación y
Gestión de Monitoreo de Productos para la Salud (DVPS), informa informa
por IF-2023-09226439-APN-DVPS#ANMAT acerca de una comunicación recibida
de la firma St. Jude Medical Argentina S.A. dando a conocer el extravío
de productos médicos, en circunstancias de su traslado por devolución
al depósito de la firma titular de registro.
Que la Dirección de Evaluación y Gestión de Monitoreo de Productos para
la Salud (DVPS) recibió una comunicación de la firma St. Jude Medical
Argentina S.A. informando respecto del extravío de productos médicos,
en circunstancias de su traslado por devolución al depósito de la firma
titular de registro.
Que según se detalla en el informe confeccionado por el director
técnico, se trata de productos individualizados unívocamente mediante
un número de serie, lo que permite su identificación.
Que a continuación se mencionan las generalidades de los productos
involucrados: 1. Válvula cardiaca biológica Aortica, modelo EPIC, PM
961-106, están indicadas para pacientes que requieran reemplazo de una
válvula cardiaca aortica nativa enferma, dañada o con funcionamiento
defectuoso; 2. Válvula cardiaca biológica Aortica, modelo EPIC supra,
PM 961-106, están indicadas para pacientes que requieran reemplazo de
una válvula cardiaca aortica nativa enferma, dañada o con
funcionamiento defectuoso; 3. Válvula cardiaca biológica Mitral, modelo
EPIC, PM 961-106, están indicadas para pacientes que requieran
reemplazo de una válvula cardiaca aortica nativa enferma, dañada o con
funcionamiento defectuoso;
4. Válvula cardiaca Mecánica Mitral, modelo MECJ, PM 961-110, indicada
para reposición de válvula cardiaca mitral o aortica enferma, dañada o
defectuosa; 5. Válvula cardiaca Mecánica Aortica, modelo AECJ, PM
961-110, indicada para reposición de válvula cardiaca mitral o aortica
enferma, dañada o defectuosa; 6. Anillo para anuloplastía Tailor TARP,
PM 961-138, indicada para reparación de una válvula mitral o tricúspide
enferma o dañada debido a una enfermedad valvular congénita o
adquirida; 7. Oclusor Amplatzer Cribriforme 9 ASD-MF 025M, PM 961-171,
indicado para cierre de comunicaciones interauriculares
multifenestradas por vía percutánea; 8. Sistema de liberación Amplatzer
Torqvue 9-ITV07F45/80, PM 961-189, indicado para ser empleado durante
la implantación de un dispositivo oclusor Amplatzer; 9. Válvula
cardiaca biológica de porcino de bajo perfil Aortica TRIFECTA, PM
961-190, indicada para reemplazo de una válvula aortica afectada,
dañada o con mal funcionamiento; 10. Amplatzer Cardiaco plug amulet
9-ACP2-010-034, PM 961-201, autorizado para prevenir la embolización de
trombos en la orejuela auricular; 11. Oclusor de conducto Amplatzer
9-PDA2-05-06, PM 961-211, dispositivo de oclusión percutáneo para el
cierre no quirúrgico del conducto arterioso persistente.
12. FLEXNAV™ DELIVERY SYSTEM FNAV-DS-LG, PM 961-239, válvula cardiaca
transcateter indicada en pacientes con estenosis grave y sintomática de
la válvula aortica en los que se considere que existe riesgo alto para
el tratamiento quirúrgico; 13. Conducto valvulado Aortico MOD. CAVGJ –
514, PM 961-39, está indicado para reemplazar válvulas cardiacas
aorticas nativas o protésicas y aortas ascendentes en mal estado.
Que cabe poner de resalto que todos los productos pertenecen a la clase
de riesgo IV y solo están autorizados para ser utilizado por
profesionales y en instituciones sanitarias.
Que las constancias documentales agregadas al expediente permiten corroborar los hechos motivo de la presente.
Que atento las circunstancias detalladas, toda vez que los productos
médicos denunciados, identificados con un serial único, se encuentran
fuera del control de su titular y se desconoce el estado actual, no
puede asegurarse su calidad y seguridad, el uso de las unidades de
mención revisten peligro para la salud de los pacientes.
Que, por lo tanto, a fin de proteger a eventuales adquirentes y
usuarios de los productos involucrados, la Dirección de Evaluación y
Gestión de Monitoreo de Productos para la Salud (DVPS) sugiere:
prohibir los productos médicos detallados en el
IF-2023-09226439-APN-DVPS#ANMAT y notificar a las autoridades
jurisdiccionales.
Que con relación a la medida sugerida esta Administración Nacional
resulta competente en virtud de las atribuciones conferidas por el
artículo 8 inciso ñ del Decreto Nº 1490/92.
Que la Dirección de Evaluación y Gestión de Monitoreo de Productos para
la Salud y la Coordinación de Sumarios han tomado la intervención de su
competencia.
Que se actúa en ejercicio de las facultades conferidas por el Decreto Nº 1490/92 y sus modificatorias.
Por ello,
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
DISPONE:
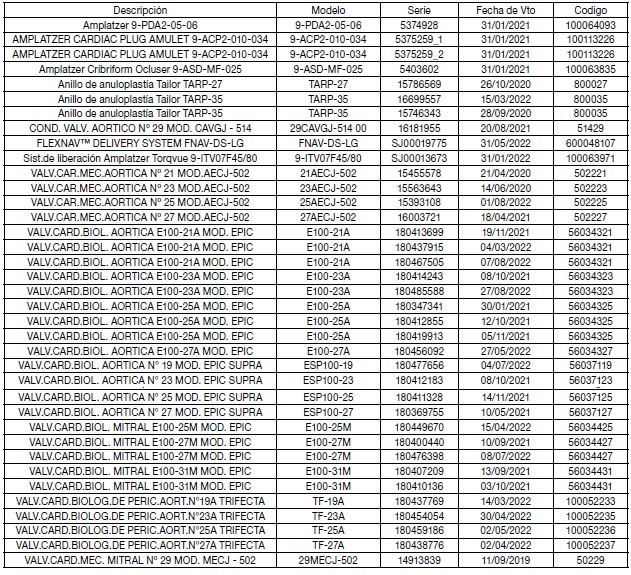
ARTÍCULO 1°: Prohíbese el uso, comercialización y distribución en todo
el territorio nacional de los productos médicos detallados en el
siguiente cuadro:
ARTÍCULO 2º: Regístrese. Dése a la Dirección Nacional de Registro
Oficial para su publicación en el Boletín Oficial. Comuníquese a las
autoridades sanitarias provinciales, a la del Gobierno de la Ciudad
Autónoma de Buenos Aires y a quienes corresponda. Comuníquese a la
Dirección de Evaluación y Gestión de Monitoreo de Productos para la
Salud. Comuníquese la prohibición dispuesta a la Dirección de Gestión
de Información Técnica a sus efectos. Cumplido, gírese a la
Coordinación de Sumarios a los efectos.
Manuel Limeres
e. 17/02/2023 N° 8767/23 v. 17/02/2023