ANEXO
II
PROTOCOLOS
Y DOCUMENTOS DE ADOPCIÓN DEL MÉTODO
Los laboratorios deberán enviar a la Dirección de Evaluación de Calidad
del INSTITUTO NACIONAL DE SEMILLAS (INASE), los protocolos utilizados
que se correspondan con el alcance que pretenden habilitar (ver Anexo
III de la presente resolución).
Cada protocolo aplicado para los análisis que se realizan en el
laboratorio deberá haber sido ensayado de manera previa a su
aplicación, debido a que es necesario que el laboratorio demuestre que
domina el ensayo y lo realiza correctamente.
Como evidencia de esto, el Director Técnico deberá elaborar un
Documento de adopción del método,
conteniendo los siguientes puntos:
- Objetivo y alcance del ensayo.
- Ítem a ensayar.
- Detalle de insumos, reactivos, materiales de referencia y
acondicionamiento de las muestras.
- Listado de equipamiento necesario para su aplicación (Anexo I-D).
- Parámetros a evaluar:
1) Repetibilidad: proximidad
entre los resultados de mediciones sucesivas del mismo objeto valorado,
realizadas bajo las mismas condiciones de medición (aplicación de un
mismo procedimiento, a un mismo objeto, por el mismo analista, en
intervalos cortos de tiempo, con el mismo equipamiento, instrumental,
en el mismo lugar).
2) Reproducibilidad:
proximidad entre los resultados de mediciones de un mismo objeto
valorado, realizadas bajo distintas condiciones de medición (aplicación
de un mismo objeto valorado a diferentes analistas, distinto
equipamiento, intervalos largos de tiempo).
3) Límite de detección:
menor concentración de analito en una muestra de ensayo que puede ser
confiablemente distinguida del blanco.
4) Robustez:
capacidad de un método analítico para que los resultados no se vean
afectados por variaciones deliberadas en los parámetros del
procedimiento.
5) Especificidad/Selectividad:
aseguran la confiabilidad de la medición del analito en presencia de
interferencias.
6) Intervalo de
trabajo/Linealidad: el ámbito de trabajo de un método analítico
es el intervalo entre los niveles más bajo y más alto de
concentraciones que ha sido demostrado que puede ser determinado con la
precisión y la exactitud requeridas para una determinada matriz.
- Resultados obtenidos.
- Personas que desarrollaron los ensayos.
- Conclusiones, criterios de aceptación o rechazo del ensayo.
El Documento de adopción del método deberá incluir la evidencia
empírica y todos los pasos para llevar a cabo todo el ensayo hasta la
obtención del resultado final, debiendo incluir en el protocolo la
forma correcta para controlar el ensayo.
Se deberá presentar un protocolo con su respectivo Documento de
adopción del método para cada patógeno a determinar.
Además, cada vez que se introduzca un cambio en el protocolo o en
instalaciones/equipos/insumos que afecten al desarrollo de ensayos, el
laboratorio deberá redactar un nuevo Documento de adopción del método y
cumplimentar lo establecido en el Artículo 13 de la presente resolución.
Los criterios a tener en cuenta para generar un nuevo Documento de
adopción del método son los siguientes, entre otros:
1. - Incorporación de equipos (aun cuando el equipo sea idéntico a uno
preexistente).
2. - Modificación en el método de procesamiento de la muestra.
3. - Modificación de los protocolos de extracción de ácidos nucleicos.
4. - Modificación en los reactivos/insumos (marca y/o tipo).
5. - Modificación en la visualización y análisis de datos y resultados.
PRESENTACIÓN
- Requisitos de Forma
Tanto los protocolos como sus Documentos de adopción del método deberán
ser presentados ante la Dirección de Evaluación de Calidad del INASE
debiendo constar, además de las especificaciones técnicas anteriormente
mencionadas, todos los datos identificatorios del laboratorio y del
Director Técnico para su correcta individualización como, asimismo,
cada una de sus hojas numeradas, selladas y firmadas por el Director
Técnico.
IF-2023-128685093-APN-INASE#MEC
ANEXO
III
NORMAS DE
FUNCIONAMIENTO DE LABORATORIOS DE ANÁLISIS FITOSANITARIOS DE PLANTAS DE
VIVERO DE VID Y/O SUS PARTES
DISPOSICIONES
GENERALES
GENERALIDADES:
El alcance de la presente normativa es referente a los diagnósticos
obligatorios de enfermedades transmitidas por injerto a las distintas
categorías y subcategorías de plantas de vid según se detalla en el
Anexo II de la Resolución N° RESOL-2018-199- APN-INASE#MPYT. Los
laboratorios deberán contar con las condiciones ambientales, físicas y
de equipamiento necesarias para el desarrollo de sus tareas, y podrán
realizar sólo los ensayos para los cuales el INSTITUTO NACIONAL DE
SEMILLAS (INASE) los haya habilitado.
Dichos ensayos deberán estar documentados en protocolos con sus
respectivos Documentos de adopción del método. Estos documentos tendrán
que ser presentados ante la Dirección de Evaluación de Calidad del
INASE para su aprobación.
Asimismo, se recomienda que se tengan en cuenta las normas de higiene y
seguridad y aquellas referidas al descarte seguro de residuos del
laboratorio.
El Director Técnico deberá capacitar a los analistas dejando constancia
de dicha capacitación en el legajo del personal.
INSTALACIONES:
El área del laboratorio y cada una de sus dependencias deben ser
compatibles con el volumen de muestras que se procesen y con el
personal disponible. Se debe establecer una separación eficaz entre
zonas vecinas cuando se desarrollen en ellas actividades incompatibles
de forma que el acceso y el uso de todos los sectores sea definido y
controlado. Estos sectores deberán estar detallados en un croquis que
será presentado al momento de la solicitud de habilitación (Anexo I-A).
En función del o los análisis para los cuales el laboratorio desee
estar habilitado será necesario disponer de:
• Sector de recepción e ingreso de muestras (independiente de los demás
sectores).
• Sector de acondicionamiento y preparación de muestras.
• Sector para el análisis mediante DAS-ELISA.
• Sector para el análisis mediante técnicas moleculares (deberá
disponer de espacios adecuados de manera de evitar la contaminación
cruzada).
• Sector para almacenamiento de insumos y reactivos.
• Sector para almacenamiento de materiales de vidrio y plástico.
• Sector para el lavado de material.
• Sector de archivo de muestras.
• Sector de oficina.
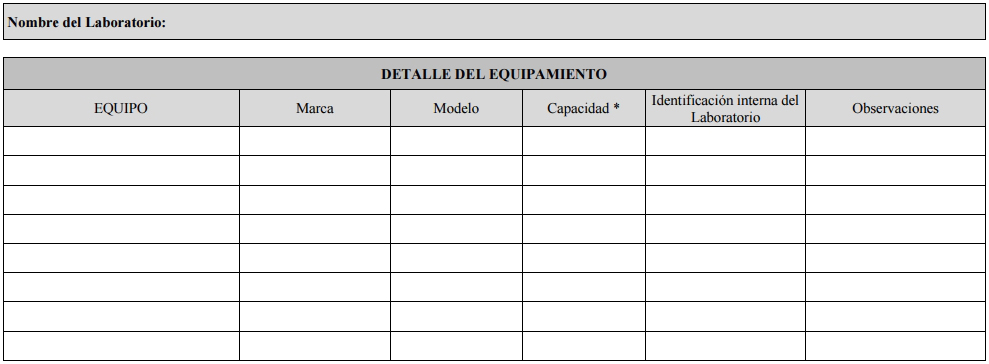
EQUIPAMIENTO:
El laboratorio deberá estar provisto de todos los insumos y equipos
necesarios para la correcta ejecución de los ensayos. Cada equipo
tendrá una ficha técnica que contenga toda la información necesaria del
mismo, así como las reparaciones, mantenimientos y calibraciones
realizadas. Todos los equipos deberán ser mantenidos en adecuado estado
de funcionamiento, debiendo para ello elaborarse un plan de
mantenimiento/verificación de los mismos.
MATERIALES DE REFERENCIA:
El laboratorio deberá contar con el material de referencia adecuado
para conducir los ensayos, el cual será identificado con las
características técnicas que se consideren relevantes.
PROCEDIMIENTOS, REGISTROS Y DOCUMENTOS:
El laboratorio establecerá y mantendrá un sistema documental en el que
consten los siguientes registros:
• Protocolo/s de análisis para el cual/los cuales ha solicitado la
habilitación.
• Documento de adopción del método para cada análisis.
• Registro de ingreso de muestras.
• Registro de análisis de virus (incluye boletín interno de análisis,
lecturas de lector ELISA, salidas del equipo de PCR, fotografías de
geles de agarosa, según corresponda).
• Registro de materiales de referencia.
• Registro de pruebas periódicas de dilución de anticuerpos utilizados
en la técnica de ELISA.
• Registro de equipos (listado de equipos, plan de
mantenimiento/control de equipos, registros de controles, fichas
técnicas).
• Registro de reactivos (facturas y/o remitos, fichas informativas que
acompañan a los reactivos).
• Certificados de análisis emitidos.
Registro de ingreso de muestras: se
registrarán en él todas las muestras que ingresen al laboratorio, se
haya emitido certificado o no (muestras de control interno de calidad,
particulares, entrenamiento, test de referencia, muestras de
fiscalización y otras), con número correlativo que corresponderá al
número de diagnóstico de la misma. Los campos mínimos obligatorios que
deben ser completados son: número de muestra y/o de diagnóstico, fecha
de recepción, remitente, procedencia u origen, categoría, código
otorgado por el muestreador, análisis solicitados, fecha de inicio y
final del análisis, fecha de emisión y número del certificado de
análisis.
Registro de análisis: se
elaborará un registro de análisis por patógeno/técnica y uno por cada
muestra. El mismo será identificado con el mismo número de ingreso que
posee la muestra en el registro de ingreso de muestras.
El registro de análisis deberá contar con la siguiente información:
número de ingreso de la muestra, análisis solicitados/virus analizados,
fecha de inicio y finalización del análisis, resultados obtenidos,
metodología utilizada, datos e identificación del analista (si las
etapas fueran desarrolladas por distintos analistas, cada uno indicará
la etapa que le corresponda mediante firma y aclaración o sus
iniciales). Se recomienda dejar un espacio para anotar observaciones
que hubiera del ensayo.
Material de Referencia: el
laboratorio deberá contar con los testigos positivos y sanos adecuados
para conducir los ensayos.
Reactivos: los distintos
reactivos empleados en los análisis de rutina deberán estar rotulados
con: fecha de apertura del envase y fecha de vencimiento. Si se trata
de soluciones preparadas en el laboratorio, como buffers, en el rótulo
se indicarán los siguientes datos: nombre de la solución, fecha de
preparación, fecha de vencimiento, nombre del analista que preparó la
misma y otros campos que pudieran corresponder (por ejemplo: pH).
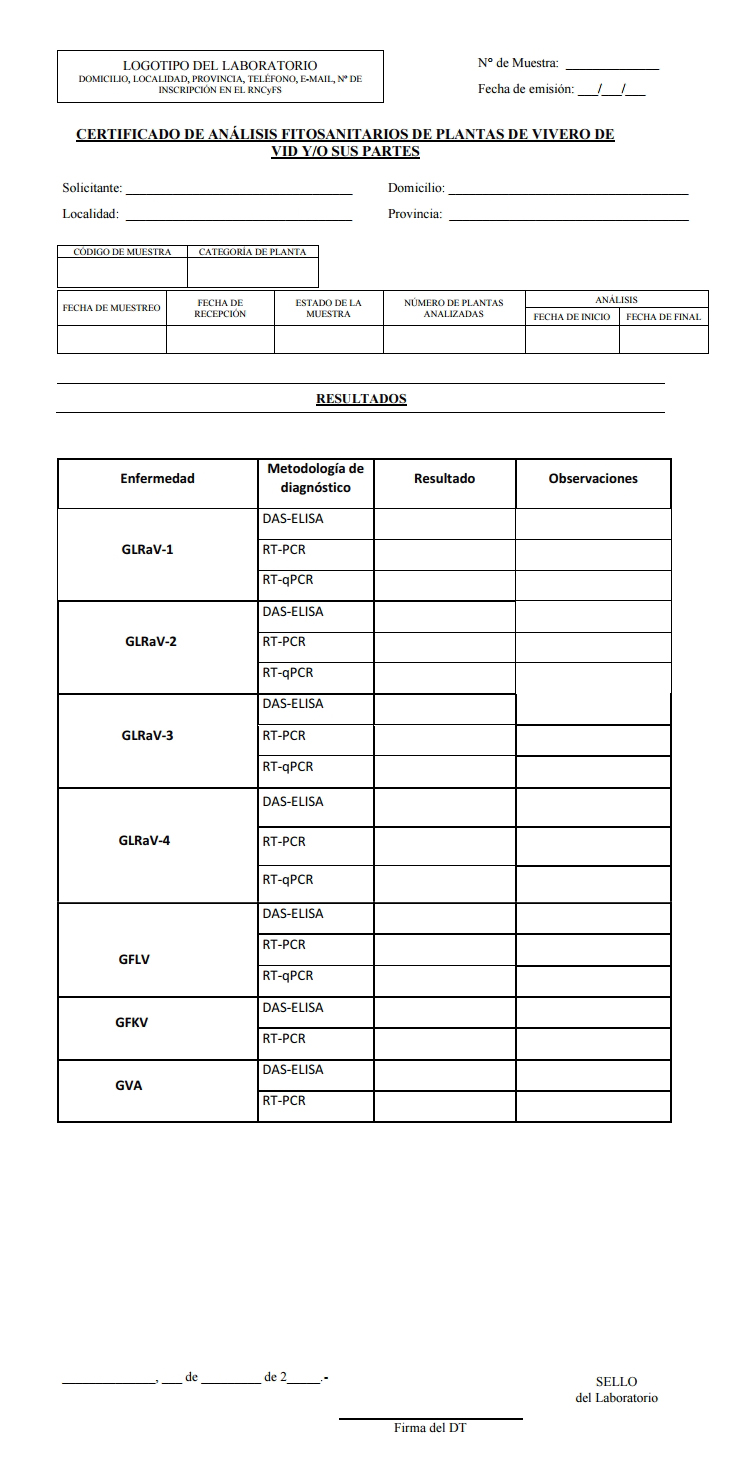
Informe de los resultados: los
resultados de los ensayos solicitados se informarán en el "Certificado
de análisis fitosanitarios de plantas vivero de vid y/o sus partes"
(Anexo IV).
Los resultados serán de tipo cualitativo y se informarán como:
Detectado / No detectado.
Expresión
de los resultados en el certificado:
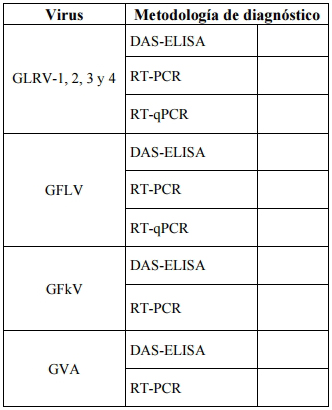
En el campo "Metodología" se debe marcar con una cruz la metodología
empleada para cada análisis realizado.
En el campo “Resultados” se deberá indicar lo siguiente:
- Si el objetivo a determinar no fue detectado, se deberá indicar “No
detectado”.
- Si el objetivo a determinar fue detectado, se deberá indicar
“Detectado”.
- Si no se ha ensayado un determinado patógeno, deberá indicarse "No
ensayado".
- En el campo "Observaciones", podrán indicarse aclaraciones, de ser
necesario.
Archivo de
Registros y Documentos:
Todos los registros, documentos y certificados emitidos deberán
guardarse por un plazo de CINCO (5) años y deberán estar a disposición
del equipo auditor.
MUESTRAS PARA ANÁLISIS:
Se deberán procesar la cantidad de plantas que se indican en el Anexo
II de la Resolución N° RESOL-2018-199-APN-INASE#MPYT.
Una vez que ingresan al laboratorio, las muestras recibidas deben ser
identificadas con su respectivo número de ingreso y procesarse en el
menor tiempo posible para evitar alteraciones en la calidad de las
mismas.
Muestras para análisis:
En el caso de muestras foliares, al momento del ingreso al laboratorio,
deben almacenarse en bolsas plásticas bien cerradas, a 4°C por un
tiempo que no supere los CINCO (5) días. En el caso de muestras de
sarmientos, pueden almacenarse en bolsas plásticas bien cerradas y a
temperatura ambiente por un tiempo que no supere los CINCO (5) días.
Para períodos más prolongados, las muestras pueden acondicionarse, de
manera de conservar su capacidad propagativa, con papel húmedo en
bolsas plásticas bien cerradas con un fungicida de amplio espectro como
preservante en dosis adecuada. Los paquetes acondicionados se
almacenarán a 4°C hasta su uso y en un tiempo no mayor a los TRES (3)
meses.
Las muestras quedarán a total disposición del INASE durante VEINTE (20)
días corridos después de entregado el correspondiente certificado de
análisis, lapso durante el cual deberán mantenerse en condiciones
adecuadas de temperatura y humedad y protegidas de contaminaciones.
TÉCNICAS DE
LABORATORIO
DETECCIÓN
DE VIRUS MEDIANTE DAS-ELISA
Equipamiento obligatorio:
• Micropipetas de rango apropiado para desarrollar el protocolo.
• Peachímetro rango de pH de 0 a 14, resolución 0,01, error +/- 0,1.
• Estufa de cultivo de temperatura regulable.
• Balanzas analíticas, capacidad para pesar 120 gr, precisión 0,001 gr.
• Heladera y Freezer (-20 °C).
• Equipo para producción de agua destilada o similar (o en su defecto
deberá contar con agua destilada).
• Lector de microplacas (espectrofotómetro 405 nm).
Técnica:
El laboratorio deberá enviar el protocolo, que dependerá de la marca
comercial del kit utilizado, junto con el Documento de adopción del
método. Los mismos serán evaluados por la Dirección de Evaluación de
Calidad del INASE.
Se deberán tener en cuenta las siguientes consideraciones:
• Época de realización:
Para muestras de tejido
herbáceo:
- GFLV y GFkV: se analizará en muestras
colectadas entre los meses de octubre y noviembre, al principio de la
temporada de crecimiento.
- GVA, GLRaV 1, GLRaV 2, GLRaV 3 y GLRaV 4: se analizarán sobre
muestras colectadas entre los meses de marzo y abril, a finales de la
temporada de crecimiento.
Para muestras de tejido
leñoso:
Todos los patógenos considerados podrán analizarse sobre muestras
leñosas colectadas a partir del mes de marzo hasta el momento de poda
invernal.
• Prueba de diluciones de anticuerpos: se realizará cada vez que se
abre un nuevo lote de anticuerpos y deberá emplearse un testigo
positivo de baja concentración.
• El número de testigos a emplear por placa, será como mínimo, el
siguiente:
- testigos positivos (enfermos): DOS
(2). Uno de la menor concentración posible tal que se distinga del
testigo sano (positivo débil) y otro de una concentración mayor.
- testigos negativos (sanos): TRES (3).
- blanco (buffer): UNO (1).
Interpretación de los resultados:
El tiempo de lectura variará según la calidad de las placas y de los
anticuerpos empleados. Se podrá hacer una lectura preliminar a los
TREINTA (30) minutos y la lectura final a los SESENTA (60) minutos.
Se considerarán positivas a aquellas muestras cuyas lecturas de
absorbancia a una longitud de onda de 405 nm (A 405) arrojen un valor
mayor al doble de los controles sanos, o mayor al promedio del valor de
la lectura de los controles sanos más un valor de 0,1 de absorbancia.
Todas las muestras con valores de absorbancia menores a lo expresado
serán consideradas sanas.
En caso de lecturas donde el cálculo arroje interpretaciones dudosas o
confusas, la interpretación final de los resultados quedará a criterio
del Director Técnico.
DETECCIÓN
DE VIRUS MEDIANTE TÉCNICAS MOLECULARES
Equipamiento:
• Micropipetas de rango apropiado para
desarrollar el protocolo.
• Termociclador para PCR o para qPCR, según corresponda.
• Heladera (4°C) y Freezer (-20°C).
• Balanza analítica con resolución 0,001gr.
• Sistema de molienda de material vegetal.
• Centrífuga refrigerada.
• Agitador vórtex.
• Cuba electroforética, camas y peines para geles de electroforesis.
• Cámara fotográfica o dispositivo para tomar fotos.
• Transiluminador.
• Espectrofotómetro para cuantificar ácidos nucleicos.
Técnica:
El laboratorio deberá enviar los siguientes protocolos:
- Protocolo de extracción de RNA.
- Protocolo de síntesis de cDNA.
- Protocolo de PCR.
También, deberá enviar el respectivo Documento de adopción del método,
el cual será evaluado por la Dirección de Evaluación de Calidad del
INASE.
Además, se tendrá que cumplir con las siguientes consideraciones:
-Para detectar los distintos patógenos mediante RT-PCR y RT-qPCR
deberán utilizarse únicamente los cebadores que se detallan en la
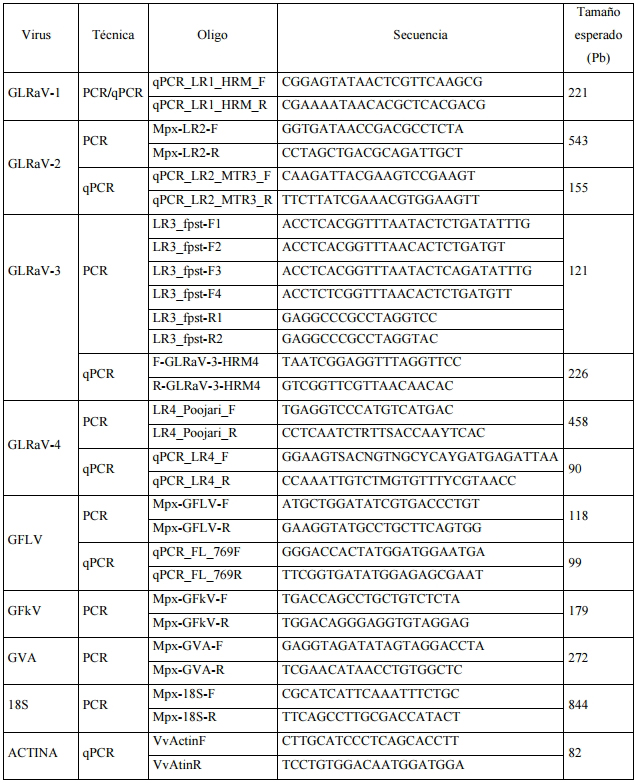
Tabla 1. No se permite utilizar
otros cebadores que no estén incluidos en dicha tabla.
-Las detecciones son de tipo CUALITATIVO.
Tabla 1: Cebadores específicos para
detectar los distintos virus mediante RT-PCR y RT- qPCR.
GLRaV1,2,3 y 4:
Grapevine
leafroll-associated virus 1, 2, 3 y 4; GFLV:
Grapevine fan-leaf virus; GVA:
Grapevine virus A; GFkV:
Grapevine fleck virus; 18S y
Actina: controles endógenos.
Interpretación de los resultados:
En el caso de las detecciones mediante RT-PCR o PCR convencional, la
aparición en el gel de una banda a la altura esperada (tamaño de
fragmento esperado) indica la presencia del patógeno en la muestra. La
ausencia de banda indica que el patógeno analizado no fue detectado en
esa muestra. La banda debe observarse en el control positivo (enfermo)
y no observarse en el control negativo (sano). Para la estimación del
tamaño del amplicón, la banda se debe comparar con el marcador de peso
molecular y, además, con el control positivo.
Por otro lado, en el caso de determinaciones mediante RT-qPCR, la
muestra se considerará positiva cuando:
- La temperatura de Melting en la cual ocurre el pico, se encuentre
dentro del rango establecido por el laboratorio.
- Cuando el valor de Ct obtenido se encuentre dentro del rango
establecido por el laboratorio.
Tanto el rango de Tm como el rango de Ct serán establecidos y
demostrados/validados por el laboratorio en el Documento de adopción
del método que el mismo presentó al momento de la habilitación.
Cualquier cambio en los reactivos que pudiera modificar los rangos de
Tm y Ct de las muestras positivas, el laboratorio deberá realizar una
nueva validación y presentar su correspondiente Documento de adopción
del método.
IF-2023-128685042-APN-INASE#MEC
ANEXO
IV
IF-2023-128684972-APN-INASE#MEC