INSTITUTO
NACIONAL DE SEMILLAS
Resolución 798/2023
RESOL-2023-798-APN-INASE#MEC
Ciudad de Buenos Aires, 05/12/2023
VISTO el Expediente N° EX-2023-132775133-APN-DA#INASE del Registro del
INSTITUTO NACIONAL DE SEMILLAS, organismo descentralizado en la órbita
de la SECRETARÍA DE AGRICULTURA, GANADERÍA Y PESCA del MINISTERIO DE
ECONOMÍA y la Resolución N° RESOL-2023-744-APN-INASE#MEC de fecha 13 de
noviembre de 2023 del INSTITUTO NACIONAL DE SEMILLAS, y
CONSIDERANDO:
Que la Ley de Semillas y Creaciones Fitogenéticas N° 20.247 establece
como objetivo garantizar la identidad y calidad de las semillas.
Que la calidad de las semillas también involucra a los aspectos
relacionados con la sanidad de las mismas.
Que resulta de interés contar con una normativa referente a la
habilitación y funcionamiento de laboratorios de análisis de patología
de semilla físico-botánica que certificarán su sanidad.
Que la presente normativa permitirá reconocer la capacidad técnica de
los laboratorios de análisis de patología de semilla físico-botánica
contando con el seguimiento y control técnico del INSTITUTO NACIONAL DE
SEMILLAS, organismo descentralizado en la órbita de la SECRETARÍA DE
AGRICULTURA, GANADERÍA Y PESCA del MINISTERIO DE ECONOMÍA, en relación
con las metodologías de ensayo y equipamiento que los laboratorios
utilizarán para la identificación de patógenos en semillas.
Que la presente norma complementa la Resolución N°
RESOL-2023-744-APN-INASE#MEC de fecha 13 de noviembre de 2023 del
INSTITUTO NACIONAL DE SEMILLAS.
Que, debido a las características técnicas y diversidad de los ensayos
fitosanitarios existentes, la habilitación por parte de los
laboratorios para esta resolución es de carácter optativo a excepción
de los laboratorios que deseen habilitarse para determinar Ascochyta
rabiei en la especie garbanzo.
Que las condiciones que debe reunir un laboratorio y las normas para su
funcionamiento dependen de los análisis y del material que pretenda
analizar.
Que, a los fines de homogenizar los resultados de los ensayos de cada
laboratorio, es necesaria la adecuación de la metodología de análisis e
interpretación de los mismos.
Que por el Artículo 1° de la Resolución N° RESOL-2023-180-APN-INASE#MEC
de fecha 4 de abril de 2023 del INSTITUTO NACIONAL DE SEMILLAS,
organismo descentralizado en la órbita de la SECRETARÍA DE AGRICULTURA,
GANADERÍA Y PESCA del MINISTERIO DE ECONOMÍA, y su respectivo Anexo I,
se crean categorías que contemplan a los laboratorios.
Que la Dirección de Evaluación de Calidad, dependiente de la Dirección
Nacional de Desarrollo de Semillas y Creaciones Fitogenéticas, la
Dirección de Fiscalización, dependiente de la Dirección Nacional de
Articulación Federal y la Dirección de Asuntos Jurídicos del INSTITUTO
NACIONAL DE SEMILLAS, han tomado la intervención técnica que les
compete.
Que la COMISIÓN NACIONAL DE SEMILLAS creada por la Ley de Semillas y
Creaciones Fitogenéticas N° 20.247, ha aprobado la nueva conformación
del Comité Técnico de Patología de Semilla botánica según surge del
Acta N° 494 en su reunión de fecha 14 de junio de 2022.
Que la COMISIÓN NACIONAL DE SEMILLAS, se ha pronunciado favorablemente
según surge del Acta Nº 508, en su reunión de fecha 14 de noviembre de
2023.
Que la Dirección de Asuntos Jurídicos del INSTITUTO NACIONAL DE
SEMILLAS, ha tomado la intervención de su competencia.
Que la suscripta es competente para dictar el presente acto, en virtud
de lo establecido en los Artículos 8º y 9º del Decreto Nº 2.817 de
fecha 30 de diciembre de 1991, ratificado por la Ley Nº 25.845.
Por ello,
LA PRESIDENTA DEL DIRECTORIO DEL INSTITUTO NACIONAL DE SEMILLAS
RESUELVE:
ARTÍCULO 1°.- Apruébanse las NORMAS DE FUNCIONAMIENTO DE LABORATORIOS
DE ANÁLISIS DE PATOLOGÍA DE SEMILLA FÍSICO-BOTÁNICA, que como Anexo I
(IF-2023-143481768-APN-INASE#MEC), Anexo II
(IF-2023-143482430-APN-INASE#MEC) y Anexo III
(IF-2023-143483271-APN-INASE#MEC) forman parte integrante de la
presente resolución.
El alcance de la presente resolución abarca a los laboratorios que
analicen muestras de semilla físico-botánica con el fin de informar el
resultado de los análisis efectuados a un tercero, y, que, en forma
optativa, deseen inscribirse en el INSTITUTO NACIONAL DE SEMILLAS,
organismo descentralizado en la órbita de la SECRETARÍA DE AGRICULTURA,
GANADERÍA Y PESCA del MINISTERIO DE ECONOMÍA.
ARTÍCULO 2°.- Para comenzar el proceso de habilitación técnica del
laboratorio, el interesado deberá presentar una nota solicitando la
habilitación y los siguientes formularios debidamente completados:
Solicitud de Habilitación (Anexo I-A), Alcance de la habilitación
(Anexo I-B), Término de Compromiso del Director Técnico (Anexo I-C),
Listado de Analistas (Anexo I-D), Detalle del Equipamiento (Anexo I-E),
ante la Dirección de Evaluación de Calidad, dependiente de la Dirección
Nacional de Desarrollo de Semillas y Creaciones Fitogenéticas del
INSTITUTO NACIONAL DE SEMILLAS.
Toda documentación que no cumpla con los requisitos de fondo y de forma
exigidos en la presente norma será devuelta (de ser identificable su
autor) o desechada y se tendrá por nunca presentada.
ARTÍCULO 3°.- La habilitación del laboratorio de análisis de patología
de semilla físico-botánica estará condicionada a la aceptación de la
información presentada por el interesado, al título profesional del
postulante al cargo de Director Técnico y la capacitación específica
del mismo, a la disponibilidad del equipamiento mencionado en el Anexo
II de la presente resolución, a la aprobación de la auditoría de
habilitación, y al cumplimiento de los criterios y requisitos que el
INSTITUTO NACIONAL DE SEMILLAS establezca como necesarios.
ARTÍCULO 4°.- El postulante al cargo de Director Técnico deberá contar
con título universitario oficial no menor de CUATRO (4) años con
incumbencia profesional o grados superiores de educación (con
incumbencia en la materia) y formación avalada por una institución de
referencia, por ejemplo instituciones académicas o personas referentes
con trayectoria en el área, y experiencia acreditable en el área
técnica correspondiente al alcance de la habilitación solicitada. Al
inicio de los trámites deberá presentar fotocopia del título
profesional habilitante y de la matrícula profesional -de
corresponder-, junto a un currículum vitae actualizado y firmado, con
sus respectivos comprobantes.
De considerarlo necesario y bajo su entera responsabilidad podrá
nombrar un Reemplazante Autorizado. Para esta designación deberá
presentar debidamente completado ante la Dirección de Evaluación de
Calidad, dependiente de la Dirección Nacional de Desarrollo de Semillas
y Creaciones Fitogenéticas del INSTITUTO NACIONAL DE SEMILLAS, la
Designación de Reemplazante Autorizado (Anexo I-F), firmado por el
autorizado y endosado por el Director Técnico.
ARTÍCULO 5°.- El Reemplazante Autorizado y los analistas deberán tener,
por parte del Director Técnico, una capacitación y un entrenamiento
acorde al alcance de la habilitación.
ARTÍCULO 6°.- La Dirección de Evaluación de Calidad, llevará a cabo la
auditoría de habilitación y el control de los laboratorios inscriptos,
estando obligado el Director Técnico a estar presente en las auditorías
y a brindar al INSTITUTO NACIONAL DE SEMILLAS toda la documentación que
se requiera.
ARTÍCULO 7°.- La falta de envío de las propuestas de acciones
correctivas para el levantamiento de no conformidades encontradas en la
auditoría dentro del plazo establecido por el auditor, hará pasible al
laboratorio de la aplicación de lo previsto por el Artículo 17.
ARTÍCULO 8º.- Una vez obtenida la habilitación técnica otorgada por la
Dirección de Evaluación de Calidad, el interesado deberá proceder a su
inscripción ante el Registro Nacional de Comercio y Fiscalización de
Semillas (RNCyFS) dentro de los TREINTA (30) días de notificada la
aprobación técnica por parte de la Dirección de Evaluación de Calidad.
La habilitación del laboratorio se mantendrá vigente mientras el
laboratorio cumpla los requisitos de la presente normativa, el pago de
la anualidad y toda otra normativa complementaria del INSTITUTO
NACIONAL DE SEMILLAS.
ARTÍCULO 9°.- En los casos que existan resultados cuestionados por las
personas que solicitaron el servicio, los mismos corresponderán a la
órbita de derecho privado, por lo que se deberán resolver entre el
afectado y el laboratorio que hubiese realizado el servicio.
ARTÍCULO 10.- Los certificados emitidos por los laboratorios
habilitados tendrán validez en el orden nacional y deberán ser
confeccionados considerando los campos mínimos requeridos en el Anexo
II de la presente resolución y según el alcance de habilitación. Para
ser válidos, los certificados emitidos deberán contener sello y firma
del Director Técnico quien se hará responsable del contenido de los
mismos. Deberán estar debidamente completados no pudiendo contener
borrones ni enmiendas ni ser completados a mano. Bajo responsabilidad
del Director Técnico podrán ser firmados por el Reemplazante Autorizado
designado.
ARTÍCULO 11.- La Dirección de Evaluación de Calidad podrá solicitar a
los laboratorios copia firmada de los certificados emitidos y de
cualquier registro asociado a estos.
ARTÍCULO 12.- Todos los laboratorios habilitados deberán participar de
los ensayos interlaboratorios organizados por la Dirección de
Evaluación de Calidad. Conjuntamente a lo anterior, la Dirección de
Evaluación de Calidad podrá convocar tanto a los Directores Técnicos
como a los analistas a jornadas, talleres o cursos de capacitación y
actualización que estipule como obligatorios.
ARTÍCULO 13.- Toda modificación en la situación del laboratorio en
cuanto a domicilio, instalaciones, Director Técnico, equipamiento o
reactivos que afecten al desarrollo de ensayos, deberá comunicarse en
forma fehaciente a la Dirección de Evaluación de Calidad, dentro de los
TREINTA (30) días corridos de producida la modificación. La
modificación no surtirá efecto hasta recibir la conformidad por parte
de la Dirección de Evaluación de Calidad, es decir, el laboratorio no
podrá realizar análisis ni emitir certificados hasta recibir la
conformidad por parte de la Dirección de Evaluación de Calidad. Otros
cambios en los datos suministrados en cualquiera de los Anexos
presentados en el momento de la habilitación deberán ser informados
mediante la presentación de un nuevo Anexo actualizado al momento de la
auditoría o a requerimiento de la Dirección de Evaluación de Calidad.
ARTÍCULO 14.- Para que proceda el cambio de Director Técnico, el nuevo
postulante al cargo deberá presentar toda la documentación requerida en
los Artículos 2° y 4º, además de cumplir con los requisitos
establecidos en la presente resolución. La presentación de la
documentación no implica la designación automática del postulante en el
cargo de Director Técnico, por lo que el laboratorio no podrá emitir
certificados suscritos por el postulante hasta recibir la conformidad
por parte de la Dirección de Evaluación de Calidad. En casos de
acefalía en la Dirección Técnica, el laboratorio no podrá emitir
certificados.
ARTÍCULO 15.- Los laboratorios de análisis de patología de semilla
físico-botánica podrán habilitarse para realizar todos o algunos de los
ensayos mencionados en el Anexo I-B, lo que definirá el alcance del
laboratorio.
ARTÍCULO 16.- El Certificado de Habilitación Técnica emitido por la
Dirección de Evaluación de Calidad deberá estar expuesto al público
junto a la constancia de inscripción del Registro Nacional de Comercio
y Fiscalización de Semillas (RNCyFS).
ARTÍCULO 17.- El INSTITUTO NACIONAL DE SEMILLAS podrá advertir,
apercibir, suspender o dar de baja la habilitación técnica y/o la
inscripción del laboratorio en función de la ponderación de la gravedad
de las siguientes faltas:
a) Incumplimiento de deberes y obligaciones emergentes de la presente
norma.
b) Impedir la realización de auditorías, o que en las mismas se
detecten reiteradas irregularidades, o ante el no levantamiento de las
“no conformidades” detectadas dentro del plazo estipulado por el
INSTITUTO NACIONAL DE SEMILLAS.
c) Falsedad en la información y datos suministrados.
ARTÍCULO 18.- Los conceptos y casos no previstos en la presente
normativa serán evaluados y resueltos por el INSTITUTO NACIONAL DE
SEMILLAS.
ARTÍCULO 19.- Regístrese, comuníquese, publíquese, dese a la Dirección
Nacional del Registro Oficial y oportunamente archívese.
Silvana Babbitt
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la
edición web del BORA -www.boletinoficial.gob.ar-
e. 06/12/2023 N° 99722/23 v. 06/12/2023
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
ANEXO
I-A
SOLICITUD
DE HABILITACIÓN
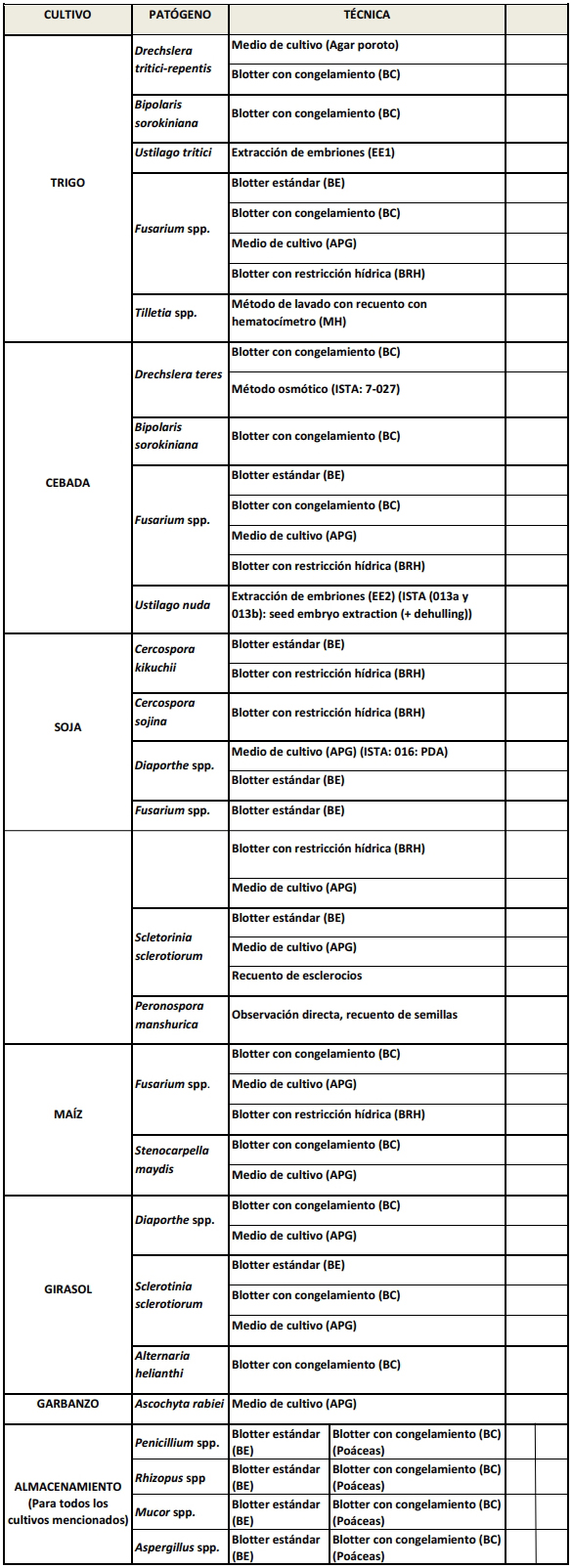
| DATOS DEL LABORATORIO DE ANÁLISIS DE
PATOLOGÍA DE SEMILLA FÍSICO-BOTÁNICA |
| DATOS DEL
SOLICITANTE (RESPONSABLE LEGAL) |
(Firma y aclaración del Responsable legal)
ANEXO
I-B
| ALCANCE DE LA HABILITACIÓN: (marcar con una
"X" las técnicas que requiera habilitación) |
El abajo firmante solicita que el alcance de la habilitación a otorgar
sea:
El presente formulario será válido una vez firmado por el Director
Técnico.
ANEXO
I-C
TÉRMINO
DE COMPROMISO DEL POSTULANTE A DIRECTOR TÉCNICO
El abajo firmante declara asumir la entera responsabilidad técnica y
administrativa de todos los procesos efectuados por el laboratorio para
el cual se postula como Director Técnico, una vez inscripto en el
Registro Nacional de Comercio y Fiscalización de Semillas (RNCyFS) del
INSTITUTO NACIONAL DE SEMILLAS, comprometiéndose a ejecutar la tarea de
Director Técnico de acuerdo con Resolución N°
y con toda la
legislación complementaria y directrices establecidas por el mencionado
Instituto Nacional.
El presente formulario será válido una vez firmado por el Director
Técnico.
ANEXO
I-D
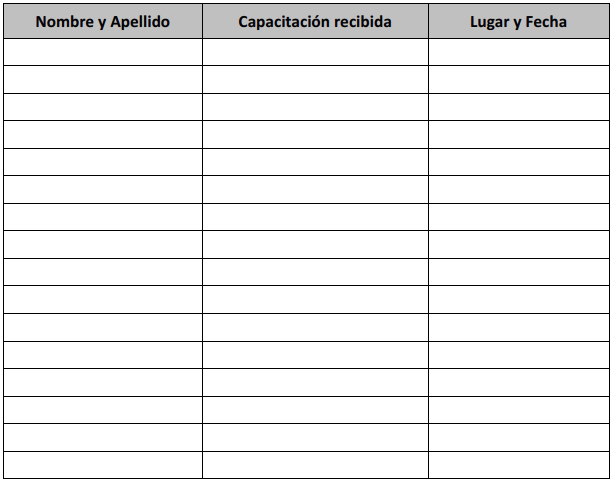
Cantidad de Analistas autorizados para ejecutar las técnicas dentro del
alcance de la habilitación:
Fecha:
El presente formulario será válido una vez firmado por el Director
Técnico.
ANEXO
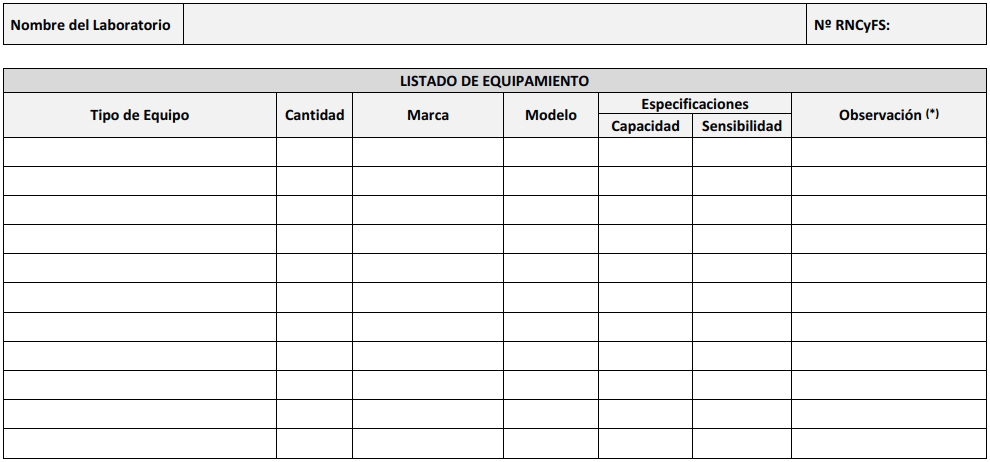
I-E
(*) Para las cámaras de germinación deberá indicar las temperaturas de
uso del equipo y si es alterna o constante.
Fecha:
El presente formulario será válido una vez firmado por el Director
Técnico.
ANEXO
I-F
| DESIGNACIÓN DE REEMPLAZANTE AUTORIZADO |
Quien suscribe_________________________________________________________
D.N.I.: _________________________ en mi carácter de Director Técnico de
Laboratorio de
Análisis__________________________________________________ N° de
Inscripción en el RNCyFS:____________, designo como Reemplazante
Autorizado a ______________________________,
D.N.I.:______________________, declarando asumir la entera
responsabilidad técnica por las tareas desarrolladas en el ejercicio de
sus funciones. -
Se adjunta curriculum vitae actualizado del autorizado para su
aprobación y fotocopia de D.N.I. -
La presente designación expira en el momento en que la Dirección de
Evaluación de Calidad del INSTITUTO NACIONAL DE SEMILLAS reciba la
Carta de Anulación por mí firmada y/o por parte del Responsable de la
empresa o por la finalización del ejercicio de mis funciones como
Director Técnico. -
Fecha:
(Sello y Firma del Reemplazante Autorizado)
El presente formulario será válido una vez firmado por el Director
Técnico.
IF-2023-143481768-APN-INASE#MEC
ANEXO
II
NORMAS DE
FUNCIONAMIENTO DE LABORATORIOS DE ANÁLISIS DE PATOLOGÍA DE SEMILLA
FÍSICO-BOTÁNICA
GENERALIDADES
El alcance de la presente normativa es referente a las técnicas para el
diagnóstico de patógenos mencionados en el Anexo I-B, que se
transportan y/o transmiten a través de la semilla físico-botánica de
las especies citadas en dicho Anexo.
Los laboratorios que deseen habilitarse para estos ensayos deberán
enviar, a la Dirección de Evaluación de Calidad del INSTITUTO NACIONAL
DE SEMILLAS (INASE), toda la documentación mencionada en los Artículos
2° y 4°. Además, deberán contar con las condiciones ambientales,
físicas y de equipamiento necesarias para el desarrollo de sus tareas.
Para realizar los ensayos deberán emplear las metodologías mencionadas
en el Anexo I-B y los protocolos indicados en el Anexo III.
Asimismo, se recomienda que se tengan en cuenta las normas de higiene y
seguridad y aquellas referidas al descarte seguro de residuos del
laboratorio.
INSTALACIONES
El área del laboratorio y cada una de sus dependencias deben ser
compatibles con el volumen de muestras que se procesen y con el
personal disponible. Se debe asegurar que el acceso y el uso de todas
las áreas donde se efectúen análisis estén controladas apropiadamente y
que la entrada de personas ajenas al laboratorio sea restringida, de
manera que no se vea afectada la calidad de los análisis ni la
confidencialidad de la información. Se deberá establecer una separación
eficaz entre zonas vecinas cuando se desarrollen en ellas actividades
incompatibles de forma que el acceso y el uso de todos los sectores sea
definido y controlado, evitando comprometer la calidad de los análisis
principalmente como consecuencia de contaminación cruzada. Los sectores
del laboratorio estarán detallados en un croquis en escala que deberá
presentarse al momento de la solicitud de habilitación.
EQUIPAMIENTO E INSUMOS
El laboratorio deberá estar provisto de todos los insumos y equipos
necesarios para la correcta ejecución de los ensayos para los cuales
está habilitado.
Cada equipo deberá tener una ficha técnica que contenga toda la
información necesaria del mismo, así como las reparaciones,
mantenimientos y calibraciones realizadas.
Todos los equipos deberán ser mantenidos en adecuado estado de
funcionamiento, debiendo para ello elaborarse un plan de
mantenimiento/verificación de los mismos.
Equipamiento mínimo requerido (de
acuerdo al alcance solicitado):
• Microscopio óptico.
• Microscopio estereoscópico.
• Peachímetro rango de pH de 0 a 14, resolución 0,01, error +/- 0,1.
• Estufa de cultivo o cámara con luz y temperatura regulable.
• Balanzas analíticas, capacidad para pesar 120 gr., precisión 0,001 gr.
• Heladera y Freezer (-20 °C).
• Equipo para producción de agua destilada o similar (o agua destilada).
• Autoclave u olla a presión.
• Flujo laminar o recinto con tubo germicida.
• Centrífuga.
• Tamices (3.5, 2 y 1 mm de abertura).
• Hematocímetro.
• Agitador magnético.
• Cámara fotográfica.
• Implementos necesarios para realizar la división de la muestra.
Reactivos:
Los distintos reactivos empleados en los análisis de rutina deberán
estar rotulados con: fecha de apertura del envase y fecha de
vencimiento. Si se trata de soluciones preparadas en el laboratorio
(como buffers), el rótulo deberá tener los siguientes datos: nombre de
la solución, fecha de preparación, fecha de vencimiento, pH y nombre
del analista que preparó la misma.
MATERIALES DE REFERENCIA
El laboratorio deberá contar con bibliografía para la identificación de
patógenos en semilla físico-botánica (Claves taxonómicas, Manuales de
identificación específicos, citas mencionadas en los protocolos del
Anexo III).
Asimismo, se recomienda que el laboratorio arme su colección de
referencia (semillas positivas para los patógenos dentro del alcance de
la habilitación), con muestras de análisis que fueron dando positivas.
El INASE podrá solicitar que se utilicen dichas semillas para la
realización de alguno de los análisis en las auditorías.
Además, el laboratorio deberá contar con las Reglas ISTA vigentes
(Capítulos 2 y 3).
PROCEDIMIENTOS, REGISTROS Y DOCUMENTOS
El laboratorio deberá mantener un sistema documental en el que consten
los siguientes registros:
• Protocolos de análisis.
• Libro de ingreso de muestras.
• Boletín de análisis.
• Fotos de los análisis realizados donde se evidencien los resultados
informados en el certificado.
• Certificados de análisis emitidos (copia electrónica o impresa).
• Registro de reactivos (facturas y/o remitos, fichas informativas que
acompañan a los reactivos).
• Registro de equipos (listado de equipos, plan de mantenimiento,
registros de controles, fichas técnicas).
Los registros no deben tener borrones. Cuando se detecten errores, los
mismos deben ser salvados, no debiendo ser borrados, ni quedar
ilegibles, ni eliminados y el valor correcto debe ser escrito al margen
del error a salvar. Todas las alteraciones a los registros deben ser
firmadas o visadas por la persona que realice la corrección.
Todos los registros, documentos y certificados emitidos deberán
guardarse por un plazo de CINCO (5) años.
Libro de ingreso de muestras:
se registrarán todas las muestras que ingresen al laboratorio, se haya
emitido certificado o no, con número correlativo (muestras de control
interno de calidad, particulares, entrenamiento, test de referencia,
ensayos interlaboratorios y otras). Los campos mínimos obligatorios que
debe contener este registro y que deben ser completados son: número de
muestra o número de análisis, fecha de ingreso o de recepción de la
muestra, remitente (solicitante), especie, análisis solicitados, fecha
de emisión del certificado de análisis y observaciones.
Boletín de análisis: cada uno
de los análisis realizados por el laboratorio debe estar respaldado por
un Boletín de análisis. El Boletín de análisis deberá contar con la
siguiente información: número de muestra o número de análisis, especie,
identificación de los analistas involucrados, fecha de inicio y
finalización del análisis (cuando sea aplicable). La información
relativa a los análisis realizados (metodologías y resultados parciales
y finales) debe ser registrada en forma clara y legible. Asimismo, se
deberán tomar y almacenar fotos de los análisis realizados donde se
evidencien los resultados informados en el certificado.
Informe de los resultados: los
resultados de los análisis efectuados se informarán en el "
Certificado de Sanidad de Semilla
Físico-Botánica".
Sólo podrán emitirse para los patógenos y técnicas de acuerdo al
alcance de la habilitación. Los mismos deben contener como mínimo los
siguientes datos:
Nombre del solicitante, Especie, Fecha de recepción de la muestra,
Fecha de finalización de los análisis, Número de análisis, Fecha de
emisión del certificado de análisis, nombre científico del patógeno,
número de semillas analizadas y el método de diagnóstico utilizado
(incluyendo cualquier pretratamiento físico o químico realizado en el
laboratorio sobre la muestra de trabajo, que precede a la incubación,
realizado sólo para facilitar el análisis).
En caso de resultado negativo (patógeno no detectado), el resultado
debe informarse como "no detectado". En caso de resultado positivo, se
deberá indicar "detectado" como así también el porcentaje de semillas
infectadas y la suma de las mismas, que indica la carga fúngica total.
Los certificados no pueden presentar borrones ni enmiendas y deben
contener la correcta transcripción de los datos referentes a la muestra
analizada. Para ser válidos deben contener el nombre y firma del
Director Técnico y el membrete del laboratorio junto con el número de
inscripción en el Registro Nacional de Comercio y Fiscalización de
Semillas (RNCyFS).
MUESTRAS PARA ANÁLISIS
Para ser remitida, la muestra debe ser envasada de manera que no se
altere el estado de sanidad de las semillas.
Una vez que ingresan al laboratorio, las muestras recibidas deben ser
identificadas con su respectivo número de ingreso y deben ser
mantenidas antes de la ejecución del análisis en condiciones adecuadas
de manera de evitar eventuales alteraciones en la calidad de las
mismas, debiendo ser analizadas lo antes posible.
Cuando la muestra de trabajo sea una parte de la muestra recibida, la
reducción debe realizarse usando técnicas apropiadas y equipos limpios
(para evitar la contaminación cruzada) y en buenas condiciones, acorde
a los métodos permitidos para análisis sanitarios estipulados por ISTA
en el Capítulo 2 de las Reglas.
Los análisis se deberán realizar sobre semilla pura, de acuerdo a la
definición de semilla pura correspondiente al género que se analiza,
según el Capítulo 3 de las Reglas ISTA.
La cantidad de semilla a utilizar será de DOSCIENTAS (200) a
CUATROCIENTAS (400) semillas para el análisis de todos los patógenos
según el Anexo III, a excepción de:
- OCHOCIENTAS (800) semillas para el
caso de Cercospora sojina, debido a que este patógeno se suele
presentar con incidencias menores al CUATRO POR CIENTO (4%).
- 100-120 g, conteniendo 2000-4000 semillas para Ustilago tritici y
Ustilago nuda
- 50 g de semilla libre de soros o aglomeraciones de teliosporas para
Tilletia spp. Después de su análisis, la muestra deberá ser almacenada
en un lugar fresco y seco, con el fin de que los cambios en las
características de la calidad de las semillas analizadas sean mínimos y
poder repetir el análisis en caso de ser necesario. Deben guardarse en
un archivo de semillas por el término de SEIS (6) meses contados a
partir de su ingreso al laboratorio. La temperatura de conservación no
debe superar los 20°C, con una tolerancia de + 3°C para variaciones
eventuales. De ser necesario se deberán realizar tratamientos contra
insectos, roedores y otros cuidados, para asegurar la conservación de
las muestras.
AUDITORÍA DE VERIFICACIÓN INICIAL Y
AUDITORÍAS DE SEGUIMIENTO
Las auditorías de verificación inicial son actividades desarrolladas
por la Dirección de Evaluación de Calidad para habilitar un
laboratorio. Asimismo, se realizarán auditorías de seguimiento para
verificar el cumplimiento de los requisitos de la presente normativa.
La Dirección de Evaluación de Calidad acordará y comunicará al
laboratorio la fecha de realización de la auditoría. El Director
Técnico del laboratorio debe estar presente en el momento de la
realización de las mismas.
Luego de cada auditoría, la Dirección de Evaluación de Calidad emitirá
un informe en el cual se establecerá el plazo para efectuar las
acciones correctivas de las no conformidades detectadas.
ENSAYOS INTERLABORATORIOS
Son actividades desarrolladas por la Dirección de Evaluación de Calidad
o quien ésta designe, con el objetivo de evaluar el desempeño de los
laboratorios. La Dirección de Evaluación de Calidad podrá solicitar el
envío de muestras del archivo de semillas de los laboratorios, cada una
de las cuales debe estar acompañada de las copias de los Certificados
correspondientes, y copia de sus respectivos boletines de análisis y
fotografías que evidencien los resultados, de ser requeridos. Los
resultados de los análisis interlaboratorios serán comunicados al
laboratorio evaluado, para que efectúe las acciones correctivas en caso
de corresponder.
IF-2023-143482430-APN-INASE#MEC
ANEXO
III
MÉTODO
BLOTTER TEST CON CONGELAMIENTO SOBRE PAPEL
Aplicable para detectar
Fusarium spp
. en trigo, cebada y maíz;
Drechslera tritici-repentis y
Bipolaris sorokiniana de trigo y
cebada;
Drechslera teres en cebada;
Stenocarpella maydis en maíz;
Diaporthe
spp., Sclerotinia sclerotiorum
y
Alternaria helianthi en
girasol; y
hongos de almacenamiento (
Penicillium
spp.,
Rhizopus spp., Mucor spp.,
y Aspergillus spp) en el caso de las Poáceas.
Procedimiento
Preparar bandejas plásticas para microondas (se recomienda utilizar de
16x20x5 cm) (ver Nota 1) con CUATRO (4) hojas de papel de germinación y
40 ml de agua destilada estéril (ADE) como sustrato. Separar de la
muestra un mínimo de DOSCIENTAS (200) semillas (verificar en el Anexo
II qué cantidad de semillas debe utilizarse en cada caso) y proceder a
la desinfección superficial con hipoclorito de sodio al 1% de cloro
activo (ver Nota 2) durante 1-2 minutos, luego realizar DOS (2)
enjuagues sucesivos con agua destilada estéril durante 1 minuto cada
uno, y finalmente orear las semillas sobre papel de filtro
esterilizado. Sembrar en las bandejas en diseño 10x5 semillas. Mover
las bandejas cuidadosamente. Incubar 24 h a temperatura constante de 20
°C ± 2 °C para trigo y cebada, o de 23-25 °C ± 1 °C para soja, maíz y
girasol (8 h de luz y 16 h de oscuridad), seguido de 24 h a -20 °C, y
luego SIETE (7) días a temperatura constante de 20 °C ± 2 °C para trigo
y cebada, o de 23-25 °C ± 1 °C para soja, maíz y girasol en ciclos
alternados de OCHO (8) h de luz y DIECISÉIS (16) h de oscuridad (ver
Nota 3).
Observar la macromorfología en forma directa y bajo lupa binocular con
aumento de 20-40X y la micromorfología, al microscopio óptico (ver Nota
4) con aumento de 200-400X, aunque algunas lupas permiten ver diversas
microestructuras. De esta manera será posible la identificación de los
patógenos. Se calcula la incidencia como el porcentaje de semillas que
presentan el patógeno.
Nota 1: Una variante es sembrar en placas de
Petri. Su uso facilita la
observación bajo lupa ya que la placa entra completa en el campo visual.
Nota 2: Para preparar la solución de hipoclorito
de sodio al 1% de
cloro activo a partir de lavandina comercial, tener en cuenta la
concentración inicial que figura en el envase y hacer la dilución
correspondiente. El porcentaje de cloro activo decrece rápidamente en
solución, por lo tanto, la solución de NaClO debe guardarse en
oscuridad y usarse dentro de los TRES (3) días de su preparación. Es
posible verificar la concentración de cloro usando tiras reactivas para
cloro.
Nota 3: Los tubos de luz para la incubación
pueden ser fluorescentes, LED o NUV.
Nota 4: Para realizar el preparado se podría
utilizar portaobjeto y
cubreobjeto o bien, portaobjeto y un trozo de cinta adhesiva
transparente, utilizando agua como líquido de montaje.
Referencias
Scandiani M.M., Luque A.G. 2009. Manual: identificación de Patógenos en
Semilla de Soja. Suplemento Especial N° 2. Análisis de semillas. 148 p.
ISSN 1852-5024.
Mathur S.B., Kongsdal O. 2003. Common Laboratory Seed Health Testing
Methods for Detecting Fungi. ISTA. 1° ed. 425 pp.
Machado J.C., Langerak C.J., Jaccoud-Filho D.S. 2002. Seed-borne fungi:
A Contribution to Routine Seed Health Analysis. ISTA. 134 pp.
Limonard T. 1966. A modified blotter test for seed health. Neth. J. Pl.
Path. 72:319-321.
MÉTODO
BLOTTER TEST ESTÁNDAR SOBRE PAPEL
Aplicable para detectar
Fusarium
spp. en trigo, cebada y soja,
Cercospora kikuchii y
Diaporthe spp. en soja,
Sclerotinia sclerotiorum
en soja y girasol, y hongos de almacenamiento (
Penicillium spp.,
Rhizopus spp.,
Mucor spp., y
Aspergillus spp).
Procedimiento
Preparar bandejas plásticas para microondas (se recomienda utilizar de
16x20x5 cm) (ver Nota 1) con CUATRO (4) hojas de papel de germinación y
entre 80 a 90 ml de agua destilada estéril (ADE) como sustrato. El
volumen de ADE puede variar según la semilla a analizar. Separar de la
muestra un mínimo de DOSCIENTAS (200) semillas (verificar en el Anexo
II qué cantidad de semillas debe utilizarse en cada caso). En este
momento se puede optar por realizar una desinfección previa, de acuerdo
al objetivo. En caso de elegir esta opción, proceder a la desinfección
superficial con hipoclorito de sodio al 1% de cloro activo (ver Nota 2)
durante 1-2 minutos, luego realizar DOS (2) enjuagues sucesivos con ADE
durante 1 minuto cada uno, y finalmente orear las semillas sobre papel
de filtro esterilizado. Sembrar en las bandejas con un diseño 10x5
semillas. Mover las bandejas cuidadosamente para evitar que las
semillas se corran o desordenen tocándose unas con otras. Incubar SIETE
(7) días a temperatura constante de 20 °C ± 2 °C para trigo y cebada, o
de 23-25 °C ± 1 °C para soja, maíz y girasol, en ciclos alternados de
OCHO (8) h de luz y DIECISÉIS (16) h de oscuridad (ver Nota 3).
Observar la macromorfología en forma directa y bajo lupa binocular con
aumento de 20-40X y la micromorfología, al microscopio óptico (ver Nota
4) con aumento de 200-400X aun cuando algunas lupas permiten ver
algunas microestructuras como microesclerocios, acérvulas,
esporodoquios, peritecios, picnidios, etc. De esta manera será posible
la identificación de los patógenos. Se calcula la incidencia como el
porcentaje de semillas que presentan el patógeno.
Nota
1: Una variante es sembrar en placas de Petri. Su uso facilita
la observación bajo lupa ya que la placa entra completa en el campo
visual.
Nota
2: Para preparar la solución de hipoclorito de sodio al 1% de
cloro activo a partir de lavandina comercial, tener en cuenta la
concentración inicial que figura en el envase y hacer la dilución
correspondiente. El porcentaje de cloro activo decrece rápidamente en
solución, por lo tanto, la solución de NaClO debe guardarse en
oscuridad y usarse dentro de los TRES (3) días de preparación. Es
posible verificar la concentración de cloro usando tiras reactivas para
cloro.
Nota
3: Los tubos de luz para la incubación pueden ser fluorescentes,
LED o NUV.
Nota
4: Para realizar el preparado se podría utilizar portaobjeto y
cubreobjeto o bien, portaobjeto y un trozo de cinta adhesiva
transparente, utilizando agua como líquido de montaje.
Referencias
Scandiani M.M., Formento A.N., Luque A.G. 2021. identificación de
patógenos en Semillas de Trigo. 1a ed. adaptada. Vicente López,
Syngenta. 160 p. ISBN 978-987-45623-2-6.
Scandiani M.M., Formento A.N., Luque A.G. 2021. identificación de
patógenos en Semillas de Maíz. 1a ed. adaptada. Vicente López,
Syngenta. 228 p. ISBN 978-987-45623-3-3.
Carmona M.A., Reis E.M. 2019. Patología de semillas de trigo y cebada.
Detección, epidemiología y manejo. 1a ed. ampliada. Vicente López,
Marcelo Aníbal Carmona. 152 p. ISBN 978-987-783¬154-2.
Scandiani M.M., Luque A.G. 2009. Manual: identificación de Patógenos en
Semilla de Soja. Suplemento Especial N° 2. Análisis de semillas. 148 p.
ISSN 1852-5024.
MÉTODO
BLOTTER TEST CON RESTRICCIÓN HÍDRICA
Aplicable para detectar
Cercospora
kikuchii,
Cercospora sojina
y
Fusarium spp. en soja,
trigo, cebada y maíz.
Procedimiento
Preparar bandejas plásticas para microondas (se recomienda utilizar de
16x20x5 cm) (ver Nota 1) con CUATRO (4) hojas de papel de germinación y
40 ml de solución de NaCl (sal de mesa en concentración 11,81 g/l agua
destilada, presión osmótica -1 Mpa) como sustrato. Separar de la
muestra un mínimo de DOSCIENTAS (200) semillas (verificar en el Anexo
II qué cantidad de semillas debe utilizarse en cada caso) y proceder a
la desinfección superficial con hipoclorito de sodio al 1% de cloro
activo (ver Nota 2) durante 1-2 minutos, luego realizar DOS (2)
enjuagues sucesivos con agua destilada estéril durante 1 minuto cada
uno, y finalmente orear las semillas sobre papel de filtro
esterilizado. Sembrar en las bandejas en diseño 10x5 semillas. Mover
las bandejas cuidadosamente. Incubar SIETE (7) días a temperatura
constante de 20 °C ± 2 °C para trigo y cebada, o de 23-25 °C para soja,
maíz y girasol, en ciclos alternados de OCHO (8) h de luz y DIECISÉIS
(16) h de oscuridad (ver Nota 3).
Observar en forma directa y bajo lupa binocular con aumento de 20x-40X
la macromorfología y al microscopio óptico (ver Nota 4) con aumento de
200-400X la micromorfología, aunque algunas lupas permiten ver
microestructuras. De esta manera será posible la identificación de los
patógenos. Se calcula la incidencia como el porcentaje de semillas que
presentan el patógeno.
Nota
1: Una variante es sembrar en placas de Petri. Su uso facilita
la
observación bajo lupa ya que la placa entra completa en el campo visual.
Nota
2: Para preparar la solución de hipoclorito de sodio al 1% de
cloro activo a partir de lavandina comercial, tener en cuenta la
concentración inicial que figura en el envase y hacer la dilución
correspondiente. El porcentaje de cloro activo decrece rápidamente en
solución, por lo tanto, la solución de NaClO
debe guardarse en oscuridad y usarse dentro de los TRES (3) días de
preparación. Es posible verificar la concentración de cloro usando
tiras reactivas para cloro.
Nota
3: Los tubos de luz para la incubación pueden ser fluorescentes,
LED o NUV.
Nota
4: Para realizar el preparado se podría utilizar portaobjeto y
cubreobjeto o bien, portaobjeto y un trozo de cinta adhesiva
transparente, utilizando agua como líquido de montaje.
Referencias
Machado J. da C., Oliveira J.A., Vieira M. das G., Alves M. de C. 2003.
Controle da germinação de sementes de soja em testes de sanidade pelo
uso da restrição hídrica. Revista Brasileira de Sementes 25(2): 77-81.
Scandiani M.M., Luque A.G. 2009. Manual: Identificación de Patógenos en
Semilla de Soja. Suplemento Especial N° 2. Análisis de semillas. 148
pp. ISSN 1852-5024.
MÉTODO
DE EXTRACCIÓN DEL EMBRIÓN PARA LA DETERMINACIÓN DE Ustilago tritici
Este test se emplea para la detección del "carbón volador del trigo”
Ustilago tritici. Aplicable
para detectar los patógenos que se
encuentran infectando las semillas como micelio durmiente en el embrión
de la semilla. Se considera que el tamaño conveniente para una muestra
de trabajo es de unos 100-120 g, conteniendo 2000-4000 semillas. La
muestra debe ser extraída al azar y debe ser representativa del lote.
Se examinan un mínimo de MIL (1000) embriones.
Procedimiento
La muestra de trabajo se sumerge en un litro de solución de NaOH al 5%
recientemente preparado (ver Nota 1) conteniendo 0,2 g de azul de
Tripan (ver Nota 2), donde se deja por unas 22-24 h a aproximadamente
20 °C. Luego de este período de extracción, se lava la muestra con agua
corriente o agua caliente para facilitar la liberación de los
embriones. Para separar los restos de las semillas de los embriones se
utiliza una batería de TRES (3) tamices (3.5, 2 y 1 mm de abertura).
Esta extracción debe ser realizada con gran cuidado, pues los embriones
de trigo son muy delicados y hay que evitar la rotura del escutelo. Una
vez separados los embriones, estos son suspendidos en un líquido de
partes iguales (1+1+1) de ácido láctico, glicerina y agua destilada. En
estas condiciones, los embriones flotan mientras que las impurezas
acompañantes bajan y son fácilmente removidas. Este proceso se repite
varias veces hasta obtener una muestra de embriones razonablemente
limpia. Luego se clarifican transfiriéndolos a un vaso de precipitados
con ácido láctico libre de agua, se hierven durante unos TREINTA (30)
segundos, y se escurren. Para la observación se utiliza glicerina como
líquido de montaje; los embriones totalmente inmersos en el líquido de
montaje son dispuestos en líneas para facilitar el examen y el conteo
(Figura 1). Se examina cuidadosamente cada embrión bajo lupa con
aumento de 18-25X con iluminación transmitida (desde abajo). El ataque
puede manifestarse en distintos grados, desde la presencia de unas
pocas hifas cortas hasta la invasión completa de los tejidos del
escutelo (Figura 2). Se cuentan
los embriones infectados y el total de embriones revisados.
El
porcentaje de carbón se calcula sobre el total de embriones contados
(no sobre el total de embriones de la muestra).
Figura
1: Montaje de embriones en glicerina para observación en lupa.
Foto: Astiz Gasso M.M.
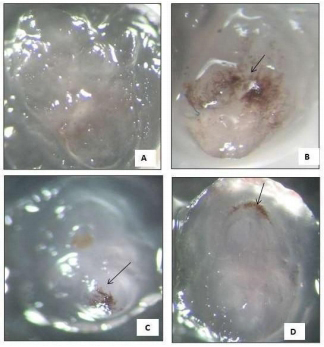
Figura
2: A.- Embrión de trigo sin presencia del hongo; B,C,D: Muestras
positivas con presencia de las hifas del hongo Ustilago tritici en
diferentes zonas del embrión de trigo (Fotos M.M. Astiz Gassó).
Nota
1: Una solución de NaOH menos concentrada o una temperatura
menor hacen dificultosa la extracción.
Nota
2: El azul de tripano o de tripán colorea de azul el micelio
presente en los embriones infectados, ya que el micelio de U. tritici
no puede detectarse sin el agregado de un colorante.
Referencias
Rennie W.J., Seaton R.D. 1975. Loose smut of barley. The embryo test as
a means of assessing loose smut infection in seed stocks. Seed Science
and Technology 3: 697-709.
Khanzada A.K., Rennie WJ., Mathur S.B., Neergaard P. 1980. Evaluation
of two routine embryo test procedures for assessing the incidence of
loose smut infection in seed samples of wheat (
Triticum aestivum). Seed
Science and Technology 8(3):363-370.
TÉCNICAS
PARA LA DETECCIÓN DE Ustilago nuda
Estos métodos son aplicables para detectar
Ustilago nuda en semillas de
cebada. La muestra de trabajo consiste en 100-120 gramos, conteniendo
2000-4000 semillas. La muestra debe ser extraída al azar y debe ser
representativa del lote. Se examinan un mínimo de MIL (1000) embriones.
1. Método de extracción del embrión
Este método se puede utilizar para detectar
Ustilago nuda en semillas
de cebada no tratadas y en semillas a las que se les ha aplicado un
tratamiento químico.
Procedimiento
Sumergir las semillas en un litro de solución acuosa recién preparada
de hidróxido de sodio (NaOH) al 5 %, y mantener a 20 °C durante
VEINTICUATRO (24) h (ver Nota 1). Después de embeber, toda la muestra
debe transferirse a un recipiente adecuado y ser lavada con agua tibia
para separar los embriones, los que aparecen a través de los
pericarpios reblandecidos. Recolectar los embriones en un tamiz con
malla de 1 mm; se pueden usar tamices adicionales de mayor tamaño para
recolectar trozos de endosperma y paja. Transferir los embriones a una
mezcla de cantidades iguales de glicerol y agua, en la cual se puede
realizar una separación adicional de embriones y paja. Luego,
transferir los embriones a un vaso de precipitados que contenga 50 ml
de solución de ácido láctico (con o sin azul de metileno, ver Nota 2),
y limpiarlos manteniendo la solución de ácido láctico en el punto de
ebullición durante aproximadamente CINCO (5) min en una campana de
extracción. Transferir los embriones a glicerol fresco para su
evaluación: el escutelo se vuelve más transparente cuando los embriones
se dejan en glicerol durante 1-2 h, lo que facilita la evaluación.
Examinar los embriones bajo lupa con aumento de 16X-25X con una
adecuada iluminación, para observar el micelio característico de
U.
nuda: de aproximadamente de 3 pm de grosor, de color marrón
dorado, y visible
sin tinción (Figura 1). El grado de infección puede variar desde la
presencia de unos pocos filamentos de hifas cortas hasta la completa
invasión de los tejidos del escutelo. Ocasionalmente, otros hongos
distintos de
U. nuda se
presentan en el escutelo, pero generalmente son
de color más oscuro y bastante distintos. Cuando las paredes de las
células se decoloran, pueden confundirse con el micelio de
U. nuda,
pero esto puede verificarse mediante un examen con aumento de 50X o
mayor (Figura 2).
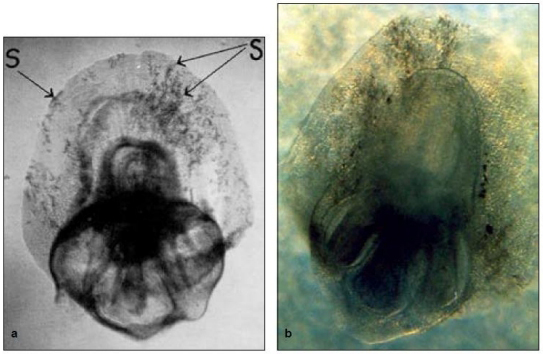
Figura
1. Embrión infectado, micelio del carbón (S) en el escutelo.
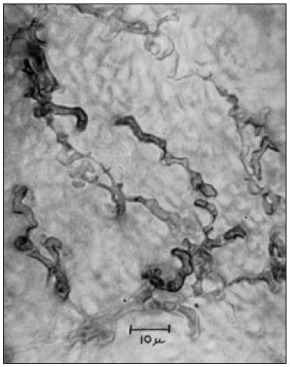
Figura
2. Micelio del carbón en el escutelo.
2. Método de descascarado y extracción
embrionaria
Este método difiere del método de extracción del embrión previamente
desarrollado (Método 7-013a de las Reglas ISTA 2023) en la técnica de
extracción del embrión y en el procedimiento usado para la limpieza de
los embriones para examinar el micelio de
Ustilago. Los dos métodos
producen resultados equivalentes (ISTA, 2011). Este método no ha sido
validado para la determinación de
U.
nuda en semilla tratada, por lo
que los tratamientos a la semilla podrían afectar el desempeño.
Procedimiento
a) Descascarado
Poner la muestra de trabajo en un vaso de precipitado de vidrio con
ácido sulfúrico (H
2SO
4) 25-37% hasta que las semillas estén cubiertas.
Incubar en una estufa a 75 °C por CINCUENTA (50) min o hasta que las
semillas se pongan de un color marrón mediano. Luego quitar
cuidadosamente la solución de H
2SO
4. Enjuagar las semillas vertiendo
agua en el vaso de precipitados, mezclar cuidadosamente, y eliminar el
agua. Agregar agua nueva y remover las cáscaras que se sueltan al
agitar con fuerza con una varilla. Remover las cáscaras eliminando
cuidadosamente el agua. Si aún quedan cáscaras, añadir nuevamente agua
y usar un mezclador eléctrico de mano a baja velocidad (máximo TRES (3)
min), o bien continuar agitando. Repetir el procedimiento hasta que se
eliminen todas las cáscaras. Tener cuidado de no perder ningún grano
(semilla pelada).
b) Extracción del embrión
Colocar los granos drenados en un contenedor con solución de NaOH-NaCl.
Incubar durante la noche (aproximadamente 15 h) a 22 °C ± 3 °C. Agitar
la mezcla suavemente para soltar los embriones de los granos. Verter
los embriones sueltos, los cuales flotan en la parte superior del
líquido, en el vaso de precipitado. Repetir el procedimiento hasta que
todos los embriones estén liberados. Para asegurarse de que no queden
embriones restantes, poner los granos disueltos en la parte superior de
un tamiz grueso combinado con un tamiz fino. El tamiz grueso debe tener
una malla de aproximadamente 2,4 mm, suficiente para dejar pasar los
embriones, pero retener los restos de grano. El tamiz fino debe tener
una malla de 1 mm. Si hay algún embrión en el tamiz de abajo, añadir
éstos al vaso de precipitado. Usando un tamiz fino, drenar la solución
de NaOH-NaCl de los embriones y enjuagar con agua corriente por
aproximadamente DIEZ (10) seg. Si hay una gran cantidad de paja con los
embriones, agregar agua y remover la paja flotante. Drenar los
embriones, ponerlos en un vaso de precipitados y cubrirlos con ácido
láctico (con o sin solución de azul de metileno, ver Nota 2). Incubar
durante la noche en una estufa a 75 °C ± 5 °C. Usando un tamiz fino,
drenar el ácido láctico de los embriones. Los embriones pueden ponerse
más
transparentes al ser lavados con etanol o al ser cubiertos por algunos
minutos con etanol 95 %. Finalmente, cubrir los embriones con solución
de glicerol-etanol (95 %) (1:2) o glicerol puro. Examinar los embriones
bajo lupa con aumento de 16-25X con una adecuada iluminación, para
observar el micelio característico de
U. nuda, como fue descripto para
el método de extracción del embrión (Método 7-013a de las Reglas ISTA
2023).
Nota
1: Una solución más débil de NaOH o una temperatura más baja
dificulta la extracción.
Nota
2: Por cada 1000 ml de ácido láctico, se agregan 0,16 g de azul
de metileno.
Referencias
ISTA, 2011. Alternative embryo extraction procedure to 7-013b
Ustilago
nuda/Hordeum vulgare. Method Validation Reports. International
Seed
Testing Association, Bassersdorf, Switzerland.
Métodos 7-013a y 7-013b de las Reglas ISTA (2023).
MÉTODO
DE DETECCIÓN DE Drechslera teres
EN SEMILLAS DE CEBADA
Aplicable para detectar
Drechslera
teres en semillas de cebada. Este
método no ha sido validado para la determinación del patógeno en
semillas tratadas, por lo que los tratamientos a la semilla podrían
afectar el desempeño del método. El tamaño mínimo de muestra debe ser
CUATROCIENTAS (400) semillas.
Procedimiento
Colocar las semillas en bandejas o placas abiertas, en una capa
delgada, y calentar por DOS (2) h en una estufa a 90 °C para reducir el
crecimiento de saprófitos. Para preparar el sustrato, sumergir
rápidamente papel de filtro en solución de azúcar (170 g de azúcar por
litro de agua desionizada o agua del grifo (ver Nota 1) y drenar el
exceso de solución. Perforar 50 o 100 huecos en el papel de filtro, y
colocar el papel de filtro perforado en una placa con una tapa
transparente de cierre hermético. Sembrar las semillas sobre el papel,
una semilla por pocillo, sembrada a mano o mediante una aspiradora de
conteo (si se dispone de una). Incubar las muestras por siete días,
alternando períodos de luz brillante (al menos 4000 lux) de 16 a 26 °C
± 2 °C con períodos de oscuridad de 8 h a 22 °C ± 2 °C. Se debe incubar
una muestra de semillas control con un nivel de infección conocido,
bajo las mismas condiciones que las muestras de análisis u otro control
adecuado. Finalmente, sacar las semillas y verter solución de NaOH al 1
% sobre el papel de filtro. Se utilizan aproximadamente 15 ml para un
papel con CINCUENTA (50) pocillos, y el doble de esa cantidad para un
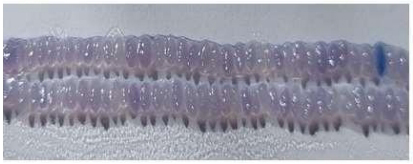
papel con CIEN (100) pocillos. El pigmento de color rojo ladrillo
cambiará inmediatamente a un color violeta. Contar las manchas
pigmentadas de color violeta bajo una lámpara de aumento. Las manchas
muy tenues (es decir, las manchas más pequeñas sin color violeta
distintivo) no deben ser registradas (Figuras 1-3). Comparar con el
control positivo (material de referencia).
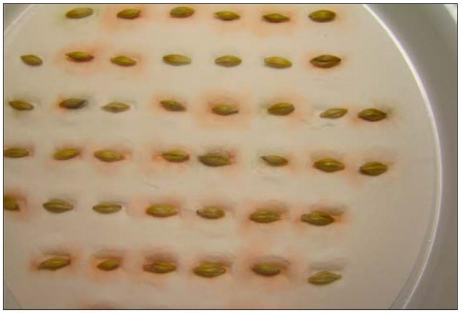
Figura
1. Una placa luego de la incubación de las semillas.
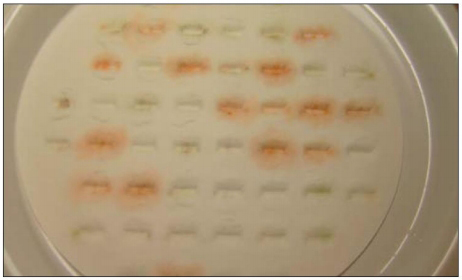
Figura
2. Una placa luego de remover las semillas incubadas, antes de
agregar la solución de NaOH.
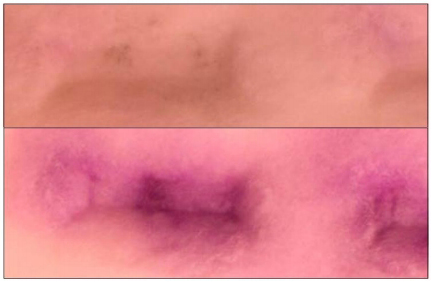
Figura
3. Ampliación de manchas visibles en los papeles secantes, luego
de agregar la solución de NaOH. Manchas tenues que no se registran
(arriba) y manchas normales a ser registradas (abajo).
NOTA
1: El agua destilada no es adecuada, debido a cierta hidrólisis
del azúcar que produce acidificación. La solución de azúcar no debe ser
almacenada por más de una semana, y la temperatura durante el
almacenamiento no debe exceder los 25 °C. Si hay alguna sospecha de
crecimiento de microorganismos, la solución de azúcar no debe ser
utilizada.
Referencias
Método 7-027 de las Reglas ISTA (2023).
PROTOCOLOS
DE PREPARACIÓN DE MEDIOS DE CULTIVO (MC) *
1. AGAR POROTO LIMA (LBA)
Aplicable para la detección de Drechslera
tritici-repentis en semillas de
trigo.
Preparación
Procedimiento para UN (1) litro
1. Agregar CINCUENTA (50) g de porotos lima y OCHOCIENTOS (800) ml de
agua destilada en un Erlenmeyer de MIL (1000) ml.
2. Tindalizar por TREINTA (30) min.
3. Filtrar recogiendo el sobrenadante.
4. Llevar a volumen con agua destilada y calentar el agua a 60 °C.
5. Agregar de a poco el agar agar con agitación. Una técnica es tomar
una alícuota de DOSCIENTOS (200) ml de líquido en un frasco con tapa,
agregar 1/5 de los sólidos, cerrar la tapa, agitar y reincorporar al
resto del líquido. Repetir la operación hasta introducir la totalidad
del agar.
6. Mantener el calentamiento por VEINTE (20) minutos con agitación
periódica. Se recomienda el uso de una varilla de vidrio.
7. Llenar CUATRO (4) frascos de TRESCIENTOS CINCUENTA (350) ml con la
totalidad del medio producido, dejando las tapas a medio cerrar.
8. Esterilizar por autoclave durante VEINTE (20) minutos a 121°C.
9. Una vez frío, abrir el autoclave y cerrar fuerte los frascos.
10. Registrar los frascos con el nombre "Medio poroto lima” y la fecha
de preparación.
11. Almacenar en el lugar adecuado.
2. AGAR PAPA GLUCOSADO
Aplicable para detectar
Fusarium
spp. en trigo, cebada, soja y maíz;
Diaporthe spp. y Scletorinia
sclerotiorum en soja y girasol;
Stenocarpella maydis en maíz y
Ascochyta rabiei en garbanzo.
El medio agar papa glucosado (APG) se puede preparar utilizando agar
papa dextrosa comercial (39 g de agar papa dextrosa en 1000 cm3 de agua
destilada), o de manera casera partiendo de un extracto de papas, agar
agar y glucosa.
Preparación del extracto de papa UN
(1) litro:
Cortar DOSCIENTOS (200) g de papas peladas en cubos de 1 cm3. Colocar
en un vaso de precipitado con SEISCIENTOS (600) ml de agua destilada.
Hervir por TREINTA (30) minutos y luego filtrar con un paño. Lavar el
sobrenadante con DOSCIENTOS (200) ml de agua destilada. Llevar a MIL
(1000) ml con agua destilada.
Preparación del medio agar papa
glucosado (APG) al 2 % UN (1) litro:
Calentar UN (1) litro de extracto de papa a 60 °C. Pesar VEINTE (20) g
de agar agar y VEINTE (20) g de glucosa, y mezclar los sólidos.
Agregarlos de a poco al extracto de papa, con agitación. Esterilizar
por autoclave durante VEINTE (20) min a 121 °C.
Para obtener APG en otros porcentajes (por ej., al 1%), únicamente se
debe modificar de manera acorde la cantidad de agar agar que se agrega
a la preparación (por ej., pesar 10 g de agar agar para obtener APG al
1%).
3. PROCEDIMIENTO
Preparar grupos compuestos por un mínimo de DOSCIENTAS (200) semillas
(verificar en el Anexo II qué cantidad de semillas debe utilizarse en
cada caso). Realizar una desinfección superficial con una solución de
hipoclorito de sodio (NaClO) al 0,1% (ver Nota 1) durante 1-2 min.
Luego enjuagar con agua desmineralizada estéril durante 1 min. Dejar
secar en papel de filtro
estéril. Una vez secas, las semillas se siembran en placas de Petri de
vidrio de 9 cm conteniendo el medio de cultivo elegido. Incubar a la
temperatura de crecimiento establecida/ideal para la especie durante
CINCO (5) a SIETE (7) días en ciclos de luz y oscuridad (la duración de
las etapas de luz y oscuridad varía según la especie). Después de la
incubación, las semillas se observan bajo una lupa estereoscópica (60X)
en búsqueda de picnidios. Se debe confirmar la presencia de conidios,
observando bajo un microscopio óptico (400X).
Especificaciones por especie:
Ascochyta
rabiei en semillas de
garbanzo.
Se preparan placas de Petri con aproximadamente 18 ml de medio de
cultivo APG al 1,7% (200 g de papas peladas y cortadas, 20 g dextrosa,
17 g agar, 1000 cm3 agua destilada). Se siembran las semillas, y se
incuban a 21 °C +/- 1 °C durante siete días en ciclos de luz: oscuridad
de 12 h.
Diaporthe
spp. en semillas de soja.
Método validado para análisis de Sanidad de Semillas 7-016 de las
Reglas ISTA (2023). Variación: uso de agar papa dextrosa acidificada
(APDA) (McGee, 1992).
Preparar y autoclavar medio APG como fue explicado anteriormente. Dejar
enfriar a 50 °C aproximadamente, y ajustar el pH a 4,5 con ácido
láctico 85 % estéril. Si se sospecha que el ácido láctico está
contaminado, esterilizar mediante filtración. Verter en placas (22 ml
por placa de Petri de 9 cm) y dejar solidificar a temperatura ambiente
(aproximadamente a 22 °C) durante VEINTICUATRO (24) horas antes de
usar. Las placas preparadas pueden ser almacenadas a temperatura
ambiente o a 4 °C hasta TRES (3) semanas.
Nota
1: Para preparar la solución de hipoclorito de sodio al 0,1% de
cloro activo a partir de lavandina comercial, tener en cuenta la
concentración inicial que figura en el envase y hacer la dilución
correspondiente. El porcentaje de cloro activo decrece rápidamente en
solución, por lo tanto, la solución de NaClO
debe guardarse en oscuridad y usarse dentro de los TRES (3) días de
preparación. Es posible verificar la concentración de cloro usando
tiras reactivas para cloro.
* Aclaración: como alternativa podrán
utilizarse los medios de cultivo que se comercializan listos para usar.
Referencias
McGee D.C. 1992. Soybean diseases: A reference source for seed
technologists. APS Press, St. Paul, MN. 151 p.
Sautua F.J., Casey S.A., Zapata R.L., Scandiani M.M., Carmona M.A.
2019. A comparison of methods for the detection of
Ascochyta rabiei in
chickpea seeds.
Summa
Phytopathologica, v.45, n.2, p.197-199.
TÉCNICAS
PARA LA DETERMINACIÓN DE Tilletia
spp.
Aplicable para detectar los patógenos
Tilletia
controversa, T. laevis y
T. tritici que se encuentran infectando las semillas a través de
esporas adheridas externamente a la superficie de la semilla.
1. Inspección Directa
Los granos carbonudos infectados con
Tilletia
controversa son globosos
y duros, en cambio aquellos que presentan
T. laevis y T.
tritici son
pulverulentos y de forma similar a la semilla sana. Usualmente no
aparecen en la semilla limpia. Las teliosporas adheridas a las semillas
(que causan el cepillo negro y el típico olor a pescado debido a la
trimetilamina) solo pueden observarse en semillas con alto grado de
infestación. Se ha encontrado que CINCO (5) mg de soros (aglomeraciones
de teliosporas) contienen aproximadamente UN MILLÓN (1.000.000) de
esporas.
2. Método del Filtrado
Es otro método descripto en la hoja de trabajo del ISTA que permite
determinar
presencia
de las esporas en la muestra y por inferencia en
el lote, pero que no cuantifica, por lo que solo nos limitaremos a
nombrarlo.
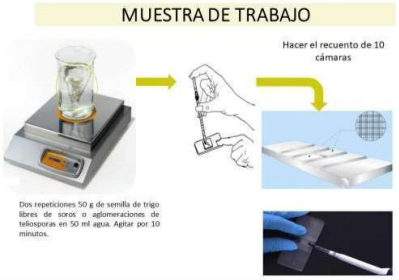
3. Método del Hematocímetro (Pirson,
1978)
Muestra de trabajo
CINCUENTA (50) g de semilla libre de soros o aglomeraciones de
teliosporas.
Lavado
Se agitan las semillas en un erlenmeyer con CINCUENTA (50) ml de agua
conteniendo 0,1 % de detergente en forma intermitente con agitador
magnético, durante unos DIEZ (10) min. Si se espera un bajo nivel de
contaminación, la suspensión debe concentrarse. Para esto, se
centrifuga a 1800 rpm por
CUATRO (4) min (Figura 1), luego se extrae con una pipeta el líquido
sobrenadante (menos 0,3 ml), sin agitar el fondo del tubo para no
remover el pellet formado. El sedimento se resuspende agregando 0,2 ml
de agua o líquido de montaje ácido láctico + glicerol + agua destilada
(1+1+1).
Examen
se llenan ambas mitades del hematocímetro. Esto se debe hacer desde el
margen del cubreobjetos hasta llenar el espacio entre el cubreobjetos y
la cámara, evitando que caigan gotas sobre las acanaladuras (según el
tipo de hematocímetro que se esté usando). Inmediatamente colocar el
cubreobjetos, cuidando que no queden burbujas y que la gota no se
derrame ni se salga de la zona de conteo, ya que el excedente
arrastraría las esporas generando un dato erróneo. Una vez que el
espacio se encuentre correctamente lleno, las esporas dejarán de
moverse. Se requiere un manipuleo rápido y cuidadoso para evitar la
sedimentación de las esporas. El campo de conteo que se debe utilizar
depende del tamaño de las esporas o conidios del hongo con el que se
esté trabajando. Si estos son grandes, lo más convenientes es contar en
los cuadrados de las esquinas (A, B, C, D) más el cuadro del centro E.
Con un aumento de 250 - 400X se cuentan las esporas dentro de todo el
cuadrado del hematocímetro (Figura 2). Este procedimiento se repite
hasta contar DIEZ (10) veces las cámaras, y luego se calcula el
promedio. Si se encuentran esporas solo fuera del cuadrado, se registra
como "menos de 1” y no 0.
El número de esporas por g de semilla se calcula de la siguiente manera:
Si la suspensión fue concentrada por centrifugación el número de
esporas calculado por gramo de semilla debe ser corregido, y el número
de esporas por gramo de semilla encontrado en los aglomerados de
esporas debe ser agregado.
CÁMARAS DE RECUENTO GLOBULAR
1. Cámara
Fuchs-Rosental: la
superficie de cada grilla es de 16 mm2 y
está dividida en DIECISÉIS (16) cuadraditos de 1 mm de lado, cada uno
de los cuales a su vez está dividido en CUATRO (4) cuadraditos de 0,25
mm de lado. El volumen que se lee en cada uno de estos cuadraditos
menores es de 0,0625 mm2 (= 0,25 mm x 0,25 mm). Esta superficie se
multiplica por la altura de la columna de líquido (= “Tiefe” en
alemán): 0,0625 mm2 x 0,2 mm = 0,01250 mm3. Con lo cual,
si contamos
las esporas presentes en 80 cuadraditos (es decir, 5 cuadrados
grandes), estaremos leyendo la cantidad presente en 0,01250 x 80 = 1
mm3. Estos valores de altura de columna y superficie pueden
leerse
impresos en la cámara.
2. Cámara de
Neubauer: tiene
grillas divididas en NUEVE (9) cuadrados
de 1 mm2. Los centrales tienen más subdivisiones que los de los
extremos, y la columna tiene una altura de 0,1 mm. También en esta
pueden leerse impresos los valores de altura (Tiefe = 0,100 mm) y
superficie: 0,0025 mm2 y 0,0625 mm2.
Figura
1: Preparación de muestra de semillas de trigo.
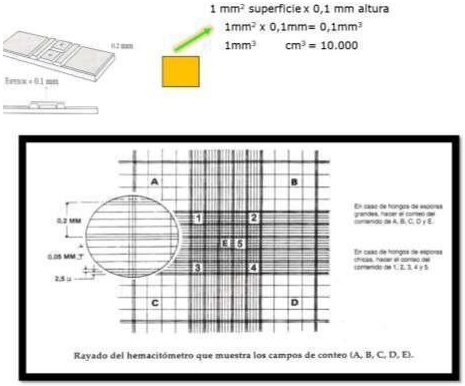
Figura
2: Recuento de esporas con hematocímetro.
Identificación y morfología de las
teliosporas de las especies de Tilletia
Las teliosporas de
T. laevis
(= T.
foetida; Figura 3) son
de color
castaño oliváceo, a veces muy claras o casi hialinas, globosas,
subglobosas y muy irregulares, de 19-25 μ de Ø, con episporio grueso y
liso. Células estériles hialinas, globosas o subglobosas, de 12-18 μ de
Ø, lisas o ligeramente reticuladas. Su cantidad varía con los
ejemplares y formas fisiológicas, desde muy escasas a abundantes.
Figura
3: Teliosporas de T. laevis.
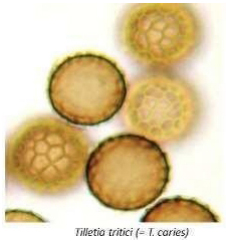
Las teliosporas de
T. tritici
(=
T. caries; Figura 4) son
de color
castaño a castaño oscuro, globosas u ovaladas de 14-25 μ de Ø, con
episporio reticulado con celdillas de 1-1,5 μ de Ø, a veces con aspecto
cerebroide y de profundidad variable. Células hialinas estériles y
globosas de 10-18 μ de Ø, con episporio no muy grueso.
Figura
4: Teliosporas de T. tritici.
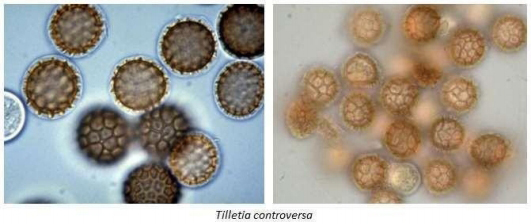
Las teliosporas de
T. controversa
(Figura 5) son de color castaño
oscuro, castaño amarillento o amarillento, globosas, subglobosas o
irregulares, de 19-30 μ de Ø incluyendo la membrana hialina que la
rodea; episporio reticulado de celdillas penta o hexagonales
irregulares de 3-3,5 μ x 1,5-3 μ de Ø de profundidad; encerrados en una
membrana hialina que sobrepasa el diámetro de las teliosporas o a veces
tan estrecha que resulta imperceptible si no se observa con lente de
inmersión
Figura
5: Teliosporas de T.
controversa (dwarf bunt of wheat).
Referencias
Pirson H. 1978. A simple method for the detection of bunt and covered
smut spores as contaminants on cereal seeds. Working group on temperate
climate cereals. In the Report on the sixteenth International Workshop
on Seed Pathology. Karlsruhe: ISTA-PDC, 54-57.
IF-2023-143483271-APN-INASE#MEC