SERVICIO
NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
Resolución 45/2024
RESOL-2024-45-APN-PRES#SENASA
Ciudad de Buenos Aires, 09/01/2024
VISTO el Expediente N° EX-2023-107378528- -APN-DGTYA#SENASA; la Ley N°
27.233; el Decreto N° DECTO-2019-776-APN-PTE del 19 de noviembre de
2019; la Decisión Administrativa N° DA-2018-1881-APN-JGM del 10 de
diciembre de 2018; las Resoluciones Nros. 555 del 8 de septiembre de
2006 de la ex-SECRETARÍA DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS,
38 del 3 de febrero de 2012 del entonces MINISTERIO DE AGRICULTURA,
GANADERÍA Y PESCA y su modificatoria, 740 del 13 de julio de 1999 y
RESOL-2021-153-APN-PRES#SENASA del 30 de marzo de 2021, ambas del
SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, y
CONSIDERANDO:
Que por la Ley N° 27.233 se declara de interés nacional la sanidad de
los animales y los vegetales, así como la prevención, el control y la
erradicación de las enfermedades y de las plagas que afecten la
producción silvoagropecuaria nacional, la flora y la fauna, la calidad
de las materias primas producto de las actividades silvo-agrícolas,
ganaderas y de la pesca, así como también la producción, la inocuidad y
la calidad de los agroalimentos, los insumos agropecuarios específicos
y el control de los residuos químicos y contaminantes químicos y
microbiológicos en los alimentos y el comercio nacional e internacional
de dichos productos y subproductos.
Que dicha declaración comprende todas las etapas de la producción
primaria, elaboración, transformación, transporte, comercialización y
consumo de agroalimentos, y el control de los insumos y productos de
origen agropecuario que ingresen al país.
Que, asimismo, mediante el Artículo 3° de la citada ley se establece la
responsabilidad primaria e ineludible de los actores de la cadena
agroalimentaria, de velar y responder por la sanidad, inocuidad,
higiene y calidad de su producción, de conformidad a la normativa
vigente, extendiendo esa responsabilidad a quienes produzcan, elaboren,
fraccionen, conserven, depositen, concentren, transporten,
comercialicen, expendan, importen o exporten animales, vegetales,
alimentos, materias primas, aditivos alimentarios, material
reproductivo, alimentos para animales y sus materias primas, productos
de la pesca y otros productos de origen animal y/o vegetal, que actúen
en forma individual, conjunta o sucesiva, en la cadena agroalimentaria.
Que el Artículo 5° de la referida norma dispone que el SERVICIO
NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA (SENASA) es la autoridad
de aplicación y el encargado de planificar, ejecutar y controlar el
desarrollo de las acciones previstas en la citada ley.
Que, a tal fin, por su Artículo 6° se faculta al mentado Servicio
Nacional a establecer los procedimientos y sistemas para el control
público y privado de la sanidad y la calidad de los animales y
vegetales y del tráfico federal, importaciones y exportaciones de los
productos, subproductos y derivados de origen animal y vegetal, estos
últimos en las etapas de producción, transformación y acopio, que
correspondan a su jurisdicción, productos agroalimentarios,
fármaco-veterinarios y fitosanitarios, fertilizantes y enmiendas,
adecuando los sistemas de fiscalización y certificación
higiénico-sanitaria actualmente utilizados.
Que la Triquinosis es una zoonosis ampliamente extendida, causada por
la ingestión de carne cruda o poco cocida de cerdos destinados al
consumo o de animales de la fauna silvestre infectados por larvas del
parásito “Trichinella spp.”.
Que, oportunamente, mediante la Resolución N° 740 del 13 de julio de
1999 del mencionado Servicio Nacional se establece la técnica
diagnóstica de digestión artificial para la investigación del parásito
“Trichinella spiralis” en las carnes porcinas como metodología de
referencia.
Que a través de la Resolución Nº 555 del 8 de septiembre de 2006 de la
ex-SECRETARÍA DE AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS se aprueba
el Programa de Control y Erradicación de Triquinosis Porcina en la
REPÚBLICA ARGENTINA, cuyos objetivos son prevenir la ocurrencia de
casos de triquinosis humana y controlar la enfermedad en los cerdos
domésticos.
Que la mentada Resolución Nº 555/06 prevé bases de prevención y control
que apuntan a la regulación de la tenencia de cerdos, al análisis de
digestión artificial en faena comercial y domiciliaria, a la educación
para profesionales, productores y consumidores, a la intervención
oficial en establecimientos sospechosos y a la gestión de basurales y
control de roedores.
Que, asimismo, mediante la precitada resolución se establece que la
Dirección Nacional de Sanidad Animal del referido Servicio Nacional
queda facultada para dictar las normas técnicas o administrativas
complementarias que correspondan para el mejor cumplimiento de las
medidas sanitarias mencionadas, así como también para modificar las
técnicas de diagnóstico, dictar las pautas de interpretación y todas
aquellas que hagan al mejor cumplimiento de lo dispuesto en ella.
Que, de conformidad con lo previsto en la Decisión Administrativa N°
DA-2018-1881-APN-JGM del 10 de diciembre de 2018, la Dirección General
de Laboratorios y Control Técnico del SENASA tiene como responsabilidad
primaria el entender, en su carácter de Laboratorio de Referencia
Nacional e Internacional en sanidad animal, protección vegetal e
inocuidad alimentaria, en el control analítico de: alimentos,
productos, subproductos y derivados de origen animal y/o vegetal,
drogas, plaguicidas, fertilizantes y enmiendas de uso agrícola,
vacunas, productos biológicos de uso agrícola y veterinario, alimentos
para animales, tejidos y fluidos, pasturas, tierras, aguas, envases,
aditivos alimentarios, productos conexos, determinación de plagas y
enfermedades de los vegetales y de los animales, formulando,
proponiendo y evaluando los métodos, programas, normas específicas e
investigaciones aplicadas.
Que, por su parte, a través de la Resolución Nº
RESOL-2021-153-APN-PRES#SENASA del 30 de marzo de 2021 del referido
Servicio Nacional se mantiene el Sistema Nacional de Vigilancia
Epidemiológica de enfermedades animales, incluyendo a la Infección por
“Trichinella spp.” entre las enfermedades de notificación obligatoria.
Que los avances más recientes registrados en investigaciones sobre la
técnica de diagnóstico señalan la necesidad de asegurar la calidad de
los resultados de dicho análisis.
Que la ORGANIZACIÓN MUNDIAL DE SANIDAD ANIMAL (OMSA), en el Manual de
Estándares para Test Diagnósticos y Vacunas, recomienda muestras de un
peso mínimo de CINCO GRAMOS (5 g) de músculo de cada porcino faenado,
en los análisis de muestras agrupadas en faena de rutina.
Que las recomendaciones de la OMSA, de la COMISIÓN INTERNACIONAL SOBRE
TRIQUINELOSIS (ICT) y de la UNIÓN EUROPEA (UE) hacen necesario
modificar y actualizar la técnica diagnóstica vigente actualmente.
Que, dada la materia técnica y las competencias del SENASA, la aludida
Dirección General resulta ser la autoridad para establecer
modificaciones a la técnica diagnóstica de digestión artificial para la
investigación y el análisis del parásito “Trichinella spp.” en las
carnes porcinas como metodología de referencia.
Que las Direcciones Nacionales de Sanidad Animal y de Inocuidad y
Calidad Agroalimentaria, y la Dirección General de Laboratorios y
Control Técnico han tomado la debida intervención.
Que la Dirección de Asuntos Jurídicos ha tomado la intervención que le
compete.
Que el suscripto es competente para dictar la presente medida de
conformidad con lo dispuesto en el Artículo 8º, incisos e) y f), del
Decreto Nº 1.585 del 19 de diciembre de 1996 y sus modificatorios.
Por ello,
EL PRESIDENTE DEL SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
RESUELVE:
ARTÍCULO 1°.- Técnica Diagnóstica de Digestión Artificial para la
investigación del parásito “Trichinella spp.”. Se establece la Técnica
Diagnóstica de Digestión Artificial para la investigación del parásito
“Trichinella spp.” en las carnes porcinas para consumo, de acuerdo con
los siguientes pesos de las muestras musculares:
Inciso a) Faena de Porcinos No Sospechosos de Triquinelosis:
Apartado I) diagnóstico individual: muestra de VEINTE GRAMOS (20 g) de
músculo;
Apartado II) diagnóstico en muestras agrupadas: muestras de CINCO
GRAMOS (5 g) de músculo cada una hasta completar CIEN GRAMOS (100 g)
totales, formado por un grupo de VEINTE (20) muestras agrupadas (pool).
Subapartado 1) el peso mínimo del pool debe ser de VEINTE GRAMOS (20 g)
[(CUATRO) muestras de CINCO GRAMOS (5 g) cada una];
Subapartado 2) el peso máximo del pool no debe exceder los CIENTO
QUINCE GRAMOS (115 g) [se podrá agregar hasta TRES (3) muestras de
CINCO GRAMOS (5) cada una];
Subapartado 3) en todos los casos se debe respetar la proporción de los
reactivos utilizados según el tamaño de la muestra.
Inciso b) Faena de Porcinos Sospechosos de Triquinelosis:
considerándose sospechoso cuando en el documento que ampare el
transporte del animal al frigorífico figure, en el apartado de
observaciones, la leyenda “Faena controlada”.
Apartado I) diagnóstico individual: muestra de VEINTE GRAMOS (20 g) de
músculo;
Apartado II) diagnóstico en muestras agrupadas: muestras de DIEZ GRAMOS
(10 g) de músculo hasta completar CIEN GRAMOS (100 g) totales, formado
por un grupo de DIEZ (10) muestras agrupadas.
ARTÍCULO 2°.- Especificaciones. Los análisis contemplados en el
artículo precedente se deben realizar conforme a las especificaciones
que se indican en el Anexo (IF-2023-151497643-APN-DGLYCT#SENASA), que
forma parte integrante de la presente resolución.
ARTÍCULO 3°.- Autoridad de Aplicación. La Dirección General de
Laboratorios y Control Técnico del SENASA será la autoridad de
aplicación para modificar las técnicas de diagnóstico para la
investigación y el análisis del parásito “Trichinella spp.”, y para
dictar las normas técnicas complementarias de la presente resolución.
ARTÍCULO 4°.- Artículo 14 de la Resolución N° 555 del 8 de septiembre
de 2006 de la ex-SECRETARÍA DE AGRICULTURA, GANADERÍA, PESCA Y
ALIMENTOS. Sustitución. Se sustituye el texto del Artículo 14 de la
citada Resolución N° 555/06 por el siguiente:
“ARTÍCULO 14.- La Dirección Nacional de Sanidad Animal del SERVICIO
NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA queda facultada para
dictar las normas técnicas o administrativas complementarias que
correspondan para el mejor cumplimiento de las medidas sanitarias
mencionadas, y para dictar las pautas de interpretación y todas
aquellas que hagan al mejor cumplimiento de la presente resolución.”.
ARTÍCULO 5°.- Anexo. Aprobación. Se aprueba la “Técnica de Digestión
Artificial” que, como Anexo (IF-2023-151497643-APN-DGLYCT#SENASA),
forma parte integrante de la presente resolución.
ARTÍCULO 6°.- Derogación. Se deroga el Numeral 25.2. del Anexo I de la
Resolución N° 555 del 8 de septiembre de 2006 de la ex-SECRETARÍA DE
AGRICULTURA, GANADERÍA, PESCA Y ALIMENTOS.
ARTÍCULO 7°.- Abrogación. Se abroga la Resolución Nº 740 del 13 de
julio de 1999 del SERVICIO NACIONAL DE SANIDAD Y CALIDAD
AGROALIMENTARIA.
ARTÍCULO 8°.- Incumplimiento. Sanciones. El incumplimiento o las
transgresiones a la presente norma será pasible de las sanciones
establecidas en el Capítulo V de la Ley Nº 27.233 y su Decreto
Reglamentario N° DECTO-2019-776-APN-PTE del 19 de noviembre de 2019,
sin perjuicio de las acciones preventivas que pudieran adoptarse en
virtud de lo dispuesto en la Resolución Nº 38 del 3 de febrero de 2012
del entonces MINISTERIO DE AGRICULTURA, GANADERÍA Y PESCA y su
modificatoria, o la que en el futuro la reemplace.
ARTÍCULO 9°.- Incorporación. Se incorpora la presente resolución al
Libro Tercero, Parte Quinta, Título III, Capítulo II, del Índice
Temático del Digesto Normativo del SERVICIO NACIONAL DE SANIDAD Y
CALIDAD AGROALIMENTARIA, aprobado por la Resolución Nº 401 del 14 de
junio de 2010 y su complementaria N° 325 del 1 de junio de 2011, ambas
del citado Servicio Nacional.
ARTÍCULO 10.- Vigencia. La presente resolución entra en vigencia a
partir de su publicación en el Boletín Oficial.
ARTÍCULO 11.- Comuníquese, publíquese, dese a la DIRECCIÓN NACIONAL DEL
REGISTRO OFICIAL y archívese.
Pablo Cortese
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la
edición web del BORA -www.boletinoficial.gob.ar-
e. 11/01/2024 N° 1182/24 v. 11/01/2024
(Nota
Infoleg:
Los anexos referenciados en la presente norma han sido extraídos de la
edición web de Boletín Oficial)
ANEXO
(Articulo 5°)
TÉCNICA DE DIGESTIÓN ARTIFICIAL
1. TOMA DE MUESTRAS:
1.1. Tomar UNA (1) muestra, de
aproximadamente CUARENTA Y CINCO GRAMOS (45 g), en uno de los pilares
del diafragma, en la zona de transición entre la parte muscular y la
parte tendinosa; si no hubiere pilar del diafragma, como alternativa
puede tomarse la misma cantidad de muestra de la parte del diafragma
situada cerca de las costillas o del esternón, de la musculatura de la
base de la lengua, de los músculos masticadores o de la musculatura
abdominal.
1.2. Las muestras deben liberarse de restos de aponeurosis, grasa y
tendones.
1.3. Las muestras deben ser rotuladas e identificadas unívocamente.
2. CONSERVACIÓN DE LAS MUESTRAS:
2.1. Las muestras que no sean
procesadas en el dia de la extracción deben ser mantenidas en
condiciones de refrigeración [entre DOS GRADOS CENTÍGRADOS (2 °C) y
OCHO GRADOS CENTÍGRADOS (8 °C)] que ralentizan la descomposición pero
evitan la congelación; en estas condiciones podrán ser procesadas hasta
CUATRO (4) dias posteriores a la toma de muestra.
2.2. Solo se aceptarán muestras congeladas en caso de que provengan de
un brote, debiendo modificarse, en consecuencia, el tiempo de
sedimentación.
3. INSTRUMENTAL Y REACTIVOS:
3.1. Cuchillo, bisturí y pinzas para la
toma de muestras.
3.2. Bandejas numeradas, con tapa, divididas en VEINTE (20) cuadrados,
también numerados, que puedan contener, cada uno, muestras de músculo
de CUARENTA Y CINCO GRAMOS (45 g), aproximadamente.
3.3. Máquina picadora de carne (manual o eléctrica).
3.4. Agitador magnético provisto de una placa térmica de temperatura
controlada.
3.5. Barra magnética (recubierta de teflón) de aproximadamente la mitad
del diámetro de la base del vaso de precipitados que se utilice.
3.6. Ampolla cónica de vidrio de separación de una capacidad adecuada.
3.7. Soporte con anillos y fijación.
3.8. Tamiz de acero inoxidable de DIEZ CENTÍMETROS (10 cm) a DOCE
CENTÍMETROS (12 cm) de diámetro, con malla, cuyo tamaño debe ser de
aproximadamente CIENTO SETENTA Y SIETE MICRONES (177 μm).
3.9. Embudo de vidrio de diámetro interior mínimo de DOCE CENTÍMETROS
(12 cm), destinados a recibir el tamiz.
3.10. Vaso de precipitado de vidrio de TRES LITROS (3 l).
3.11. Probeta de vidrio graduada de CINCUENTA MILILITROS (50 ml) de
capacidad.
3.12. Pipeta de vidrio de DIEZ MILILITROS (10 ml).
3.13. Propipeta automática o de goma o bomb a de vacío.
3.14. Triquinoscopio, lupa estereoscópica o microscopio que disponga de
una iluminación adecuada y aumento suficiente para la correcta
visualización del parasito.
3.15. Papel de aluminio.
3.16. Ácido Clorhídrico, calidad analítica.
3.17. Pepsina: UNO EN DIEZ MIL (1:10.000) unidades UNITED STATES PHARMACOPEIA AND NATIONAL
FORMULARY (USP-NF); correspondiente a UNO EN DOCE MIL QUINIENTAS
(1:12.500) unidades BRITISH
PHARMACOPOEIEA (BP); correspondiente a DOS MIL (2.000) unidades
FEDERACIÓN INTERNACIONAL DE FARMACIA (FIP) o pepsina líquida
estabilizada, con una concentración mínima de SEISCIENTAS SESENTA (660)
unidades de la FARMACOPEA EUROPEA por MILILITRO (ml).
3.18. Tiras indicadoras de poder de hidrogeno (pH), rango UNO (1) a
CATORCE (14).
3.19. Agua destilada.
3.20. Balanza granataria [sensibilidad máxima CERO COMA UN GRAMOS (0,1
g)].
3.21. Termómetro apto para el rango de trabajo.
3.22. Placas de Petri grabada en cuadrados de DIEZ MILÍMETROS (10 mm)
por DIEZ MILÍMETROS (10 mm).
3.23. Cubeta para el cómputo de larvas (en caso de utilización de un
triquinoscopio).
4. MÉTODO:
Procedimiento de Digestión Artificial para CIEN GRAMOS (100 g) de
músculo:
4.1. PREPARACIÓN DEL LÍQUIDO DE
DIGESTIÓN:
4.1.1. A un vaso de precipitado de TRES
LITROS (3 l) que contenga DOS LITROS (2 l) de agua destilada,
precalentada a una temperatura de CUARENTA Y CINCO GRADOS CENTÍGRADOS
(45 °C), con un margen de tolerancia de más o menos UN GRADO CENTÍGRADO
(1 °C), añadirle ONCE MILILITROS (11 ml) de ácido clorhídrico al
TREINTA Y SIETE POR CIENTO (37 %). Pueden utilizarse otras
formulaciones del ácido siempre y cuando la concentración final de la
solución de digestión sea CERO COMA DOS POR CIENTO (0,2 %); a modo de
ejemplo, VEINTIÚN MILILITROS (21 ml) de ácido clorhídrico al DIECINUEVE
POR CIENTO (19 %).
4.1.2. Colocar una barra magnética en el vaso, y este en la placa
precalentada del agitador magnético para comenzar la agitación.
4.1.3. Añadir DIEZ GRAMOS (10 g), con un margen de tolerancia de más o
menos CERO COMA DOS GRAMOS (0,2 g), de pepsina o TREINTA MILILITROS (30
ml), con un margen de tolerancia de más o menos CERO COMA CINCO
MILILITROS (0,5 ml), de pepsina líquida.
4.1.4. Picar el total de la carne que conformará la muestra de CIEN
GRAMOS (100 g). En caso de utilizar picadora eléctrica se debe evitar
un excesivo procesado que pudiera destruir las larvas presentes.
4.1.5. Trasvasar cuantitativamente la carne picada al vaso de
precipitados de TRES LITROS (3 l) que contiene el agua, el ácido
clorhídrico y la pepsina.
4.1.6. Verificar el pH en el rango UNO (1) a DOS (2).
4.1.7. Cubrir el vaso de precipitados con una hoja de aluminio.
4.2. DIGE STIÓN, FILTRADO Y SEDIMENTACIÓN:
4.2.1. Agitar el líquido de digestión a
una velocidad suficiente para que se forme un remolino profundo sin
salpicaduras manteniendo una temperatura constante de CUARENTA Y CINCO
GRADOS CENTÍGRADOS (45 °C), con un margen de tolerancia de más o menos
UN GRADO CENTÍGR ADO (1 °C), durante CUARENTA Y CINCO (45) a SESENTA
(60) minutos (hasta que se digiera la totalidad de la carne).
4.2.2. Filtrar el líquido de digestión a través del tamiz de CIENTO
SETENTA Y SIETE MICRONES (177 pm) y recoger el filtrad o en la ampolla
cónica de decantación.
4.2.3. Se considera satisfactorio el proceso de digestión si no queda
más del CINCO POR CIENTO (5 %) del peso de la muestra inicial sin
digerir (se observa en el tamiz).
4.2.4. Dejar sedimentar el líquido de digestión en la ampolla cónica de
decantación TREINTA (30) minutos. Si el tiempo de sedimentación es
menor a TREINTA (30) minutos, es posible que no todas l as larvas se
hayan asentado y no se recu peren en el sedimento recolectado. El
tiempo de sedimentación para muestras de músculo congelado debe
extenderse hasta SESENTA (60) minutos debido a la posible existencia de
larvas muertas que sedimentan a menor velocidad.
4.2.5. Transcurridos los TREINTA (30) minutos, abrir el robinete y
recolectar CUARENTA MILILITROS (40 ml) del líquido de digestión
rápidamente (flujo libre) en una probeta de CINCUENTA MILILITROS (50
ml).
4.2.6. Dejar reposar el extracto de CUARENTA MILILITROS (40 ml) durante
DIEZ (10) minutos y luego aspirar superficialmente TREINTA MILILITROS
(30 ml) de líquido sobrenadante, sin alterar el sedimento, dejan do así
un volumen de DIEZ MILILITROS (10 ml).
4.2.7. Puede ocurrir que este líquido requiera ser clarificado para su
observación, en cuyo caso se procederá de la siguiente manera: agregar
agua destilada a los DIEZ MILILITROS (10 ml) que quedaron en la probeta
hasta recuperar el volumen de CUARENTA MILILITROS (40 ml); dejar
reposar durante DIEZ (10) minutos y aspirar superficialmente TREINTA
MILILITROS (30 ml) del líquido sobrenadante, dejando un volumen final
de DIEZ MILILITROS (10 ml). Repetir este proceso hasta obtener una
solución suficientemente límpida.
4.2.8. La muestra de DIEZ MILILITROS (10 ml) del sedimento restante se
debe verter en una placa de Petri o en una cubeta para el recuento de
larvas.
4.2.9. Enjuagar la probeta graduada con DIEZ MILILITROS (10 ml) de agua
destilada que se agregarán a la muestra en observación obteniend o as í
un volumen de VEINTE MILILITROS (20 ml) para la lectura.
4.2.10. Los líqui dos de digestión deberán observarse en el momento. Si
los líquidos de digestión no se examinan en el plazo de TREINTA (30)
minutos siguientes a su preparación, se deberán clarificar, conforme a
lo descripto.
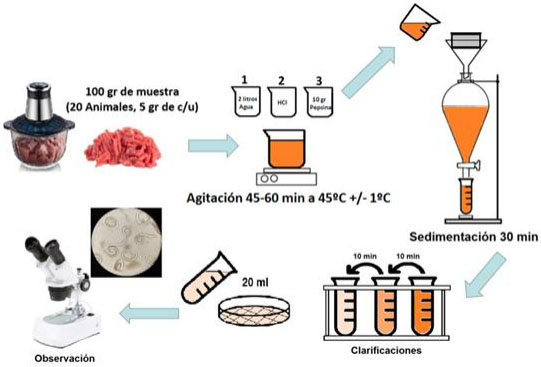
4.3. ESQUEMA TÉCNICA DIGESTIÓN ARTIFICIAL
5. RESULTADOS:
5.1. La presencia de UNA (1) larva es
indicativa de resultado positivo, debiéndose informar la cantidad de
larvas por gramo. Ante la ausencia de estas el resultado se informará
como NO DETECTADO (ND)
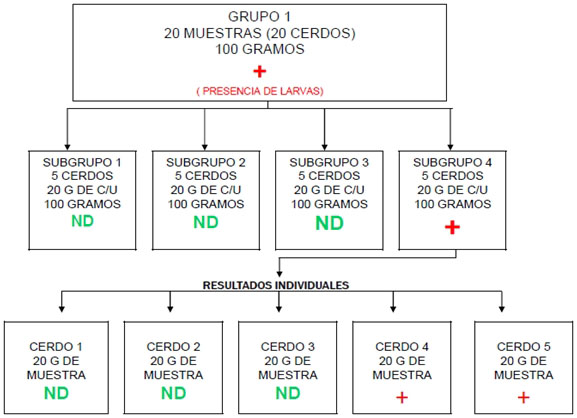
5.2. En caso de resultado positivo del análisis de un pool, se deberá
tomar una muestra de VEINTE GRAMOS (20 g) de cada cerdo, agrupándolas
en grupos de a CINCO (5) cerdos para ser examinadas por el método
arriba descripto.
5.3. Los grupos que resultaran positivos de esta última observación se
deberán analizar abriéndolos y examinando individualmente cada animal
utilizando VEINTE GRAMOS (20 g) de muestra de cada uno.
MARCHA DE LA TECNICA LUEGO DE UNI
RESULTADO GRUPAL POSITIVO EN PORCINOS
6. ASEGURAMIENTO DE LA CALIDAD DEL ENSAYO:
6.1. Las balanzas y termómetros
utilizados deben estar calibrados con trazabilidad metrológica en el
rango de trabajo.
6.2. Al validar la metodología se debe asegurar un límite de detección
del método de UNA (1) larva cada CIEN GRAMOS (100 g) de muestra.
6.3. Inactivación de Larvas de “
Trichinella
spp.”:
6.3.1. Superficies y material de
laboratorio: según concentración comercial del reactivo, deben
prepararse las siguientes soluciones:
6.3.1.1. Hipoclorito de Sodio CINCUENTA
Y CINCO GRAMOS POR LITRO (55 g/l): preparar una solución al TREINTA POR
CIENTO (30 %) [TRESCIENTOS MILILITROS (300 ml) de Hipoclorito de Sodio
por cada SETECIENTOS MILILITROS (700 ml) de agua].
6.3.1.2. Hipoclorito de Sodio CIENTO DIEZ GRAMOS POR LITRO (110 g/l):
preparar una solución al QUINCE POR CIENTO (15 %) [CIENTO CINCUENTA
MILILITROS (150 ml) de Hipoclorito de Sodio por cada OCHOCIENTOS
CINCUENTA MILILITROS (850 ml) de agua].
6.3.1.3. El tiempo de contacto requerido es de QUINCE (15) minutos.
Posteriormente se debe proceder al lavado del material.
6.3.2. Solución de digestión:
6.3.2.1. Por cada SETECIENTOS
MILILITROS (700 ml) de solución de digestión incorporar TRESCIENTOS
MILILITROS (300 ml) de Hipoclorito de Sodio; CINCUENTA Y CINCO GRAMOS
POR LITRO (55 g/l) o CINCUENTA Y CINCO GRAMOS POR CENTILITRO (55 g/cl).
6.3.2.2. Por cada OCHOCIENTOS CINCUENTA MILILITROS (850 ml) de solución
de digestión incorporar CIENTO CINCUENTA MILILITROS (150 ml) de
Hipoclorito de Sodio; CIENTO DIEZ GRAMOS POR LITRO (110 g/l) o CIENTO
DIEZ GRAMOS POR CENTILITRO (110 g/cl).
6.3.2.3. El tiempo de contacto requerido es de TREINTA (30) minutos.
6.4. Vasos de precipitados, probetas, embudos y ampollas de decantación
no deben ser de material plástico y/o teflón, para evitar la adherencia
de las larvas a la superficie del recipiente.
6.5. Cualquier modificación a la técnica detallada en la presente
disposición deberá ser aprobada por la Dirección General de
Laboratorios y Control Técnico del SERVICIO NACIONAL DE SANIDAD Y
CALIDAD AGROALIMENTARIA.
6.6. Toda otra especie susceptible a la enfermedad (con excepción del
equino) podrá ser analizada utilizando la presente metodología, previa
validación de esta para la matriz correspondiente.
IF-2023-151497643-APN-DGLYCT#SENASA