SECRETARÍA DE CALIDAD EN SALUD
Y
SECRETARÍA DE BIOECONOMÍA
Resolución Conjunta 2/2024
RESFC-2024-2-APN-SCS#MS
Ciudad de Buenos Aires, 12/08/2024
VISTO el Expediente N° EX-2020-45899023- -APN-DLEIAER#ANMAT; y
CONSIDERANDO:
Que la empresa PB LEINER ARGENTINA S.A. solicitó a la Comisión Nacional
de Alimentos (CONAL) la incorporación del componente colágeno
hidrolizado al Código Alimentario Argentino (CAA).
Que la Resolución Conjunta N° 3 de fecha 19 de diciembre de 2020 de la
SECRETARÍA DE CALIDAD EN SALUD del MINISTERIO DE SALUD y de la
ex-SECRETARÍA DE ALIMENTOS, BIOECONOMÍA Y DESARROLLO REGIONAL del
ex-MINISTERIO DE AGRICULTURA, GANADERÍA Y PESCA, referida a suplementos
dietarios, modificó el Artículo 1381 del CAA y estableció la
posibilidad de autorizar otros ingredientes con rol fisiológico para
esa categoría de productos.
Que la Resolución Nº 563 de fecha 31 de agosto de 2017 del SERVICIO
NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA (SENASA), organismo
descentralizado en la órbita del ex – MINISTERIO DE AGROINDUSTRIA,
incorporó al producto colágeno hidrolizado al Numeral 19.16 del
Capítulo XIX del Decreto Nº 4.238 del 19 de julio de 1968, Reglamento
de Inspección de Productos, Subproductos y Derivados de Origen Animal,
estableciendo las mismas especificaciones, requerimientos y
limitaciones que para el colágeno.
Que en cuanto a los antecedentes normativos internacionales, la Agencia
Nacional de Vigilancia Sanitaria (ANVISA) de Brasil incluye al colágeno
hidrolizado en su Anexo I, dentro de la lista de constituyentes
autorizados para su uso en suplementos alimenticios.
Que por otra parte, el Ministerio de Salud de Canadá lo clasifica como
producto natural para la salud y lo incluye dentro de las sustancias
autorizadas para su utilización en suplementos alimenticios.
Que atento a los antecedentes mencionados, la CONAL acordó incluir al
colágeno hidrolizado al CAA, en el Artículo 1417 del Capítulo XXII
“Misceláneos” como ingrediente para utilizar en suplementos dietarios.
Que en el proyecto de resolución conjunta tomó intervención el Consejo
Asesor de la Comisión Nacional de Alimentos (CONASE) y se sometió a
Consulta Pública.
Que la CONAL ha intervenido, expidiéndose favorablemente.
Que los Servicios Jurídicos Permanentes de los organismos involucrados han tomado la intervención de su competencia.
Que se actúa en virtud de las facultades conferidas por los Decretos
Nros. 815 del 26 de julio de 1999 y 50 del 19 de diciembre de 2019 y
sus modificatorios.
Por ello,
EL SECRETARIO DE CALIDAD EN SALUD
Y
EL SECRETARIO DE BIOECONOMÍA
RESUELVEN:
ARTÍCULO 1°.- Sustitúyese el Artículo 1417 del Código Alimentario
Argentino, el que quedará redactado de la siguiente manera: “Artículo
1417: Los ingredientes/productos que a continuación se listan deberán
responder a las características que se establecen en cada caso:
1. CLORURO DE POTASIO
Identificación y pureza según lo establecido en JECFA, FCC y/o UE.
Usos: como ingrediente para utilizarlo en reemplazo parcial o total del
cloruro de sodio (NaCl) en todas las categorías de alimentos en cuya
definición se establezca un límite máximo de contenido de sodio o como
aditivo en los casos en que la normativa vigente así lo permita.
2. ISOMALTO OLIGOSACÁRIDOS
Con la denominación de Jarabe de isomalto-oligosacáridos o IMO jarabe,
se entiende el producto obtenido mediante hidrólisis enzimática
controlada del almidón de maíz, y que consiste principalmente de
oligómeros de isomaltosa, panosa, isomaltotriosa, e isomaltotetraosa
conectados por uniones alfa 1-6 glicosídicas no digeribles.
Características: Líquido claro, viscoso y ligeramente dulce. Extracto seco, mín.: 78% p/p
Azúcares (mono y disacáridos): máx. 46% p/p (sobre sustancia seca)
Oligosacáridos de 3 a 6 unidades: mín. 30% p/p (sobre sustancia seca)
Oligosacáridos de más de 7 unidades: mín. 20% p/p (sobre sustancia seca)
Cenizas (sobre sustancia seca), máx.: 0,2% p/p
Dióxido de azufre total, máx.: 40 mg/kg
Arsénico como As, máx.: 1 mg/kg
Cobre como Cu, máx.: 5 mg/kg
Plomo como Pb, máx.: 2 mg/kg
Este producto se rotulará: “Jarabe de isomalto-oligosacáridos”.
Con la denominación de jarabe de isomalto-oligosacáridos deshidratado o
jarabe de IMO deshidratado, se entiende el producto obtenido mediante
hidrólisis enzimática controlada del almidón de maíz, y que consiste
principalmente de oligómeros de isomaltosa, panosa, isomaltotriosa, e
isomaltotetraosa conectados por uniones alfa 1-6 glicosídicas no
digeribles, del que se ha separado la casi totalidad del agua.
Características: Polvo blanco, higroscópico, soluble en agua.
Humedad, máx.: 5% p/p
Azúcares (mono y disacáridos): máx. 46% p/p (sobre sustancia seca)
Oligosacáridos de 3 a 6 unidades: mín. 30% p/p (sobre sustancia seca)
Oligosacáridos de más de 7 unidades: mín. 20% p/p (sobre sustancia seca)
Cenizas (sobre sustancia seca), máx.: 0,2% p/p
Dióxido de azufre total, máx.: 40 mg/kg
Arsénico como As, máx.: 1 mg/kg
Cobre como Cu, máx.: 5 mg/kg
Plomo como Pb, máx.: 2 mg/kg
Este producto se rotulará: “Jarabe de isomalto-oligosacáridos deshidratado o jarabe de IMO deshidratado”.
3. TREHALOSA
Sinónimos: alfa, alfa -trehalosa
Definición: Disacárido no reductor consistente en dos moléculas de
glucosa unidas por un puente alfa -1,1-glucosídico. Se obtiene del
almidón mediante un proceso enzimático en varios pasos.
Se presenta como dihidrato.
Nombre químico: alfa -D-glucopiranosila -D-glucopiranósido, dihidrato
Número CAS: 6138-23-4 (dihidrato)
Fórmula química: C12 H22 O11 · 2H2O (dihidrato)
Peso molecular: 378,33 (dihidrato)
Descripción: Casi inodoro, cristales blancos o casi blancos de sabor dulce.
Características
Solubilidad: Soluble en agua, apenas soluble en etanol.
Rotación específica: [alfa] D20 + 199° (solución acuosa al 5%).
Punto de fusión: 97°C (dihidrato)
Pureza: No menos del 98% de materia seca.
Pérdida por desecación: No Más del 1,5% (60° C, 5 h).
Cenizas totales: No más del 0,05%.
Plomo: No más de 1 mg/kg.
Método de determinación: Contenido en el Anexo de la Decisión de la
Comisión de las Comunidades Europeas Nº 721, de fecha 25 de septiembre
de 2001.
Uso: en productos en los que se sustituyen los ingredientes tipificados en el presente código.
Leyendas:
“La trehalosa en una fuente de glucosa”
“El consumo de más de 50 g de trehalosa produce efecto laxante. Una porción de este producto contiene...g de trehalosa”.
4. ISOMALTULOSA
Con la denominación de isomaltulosa, se entiende el producto obtenido
mediante isomerización enzimática de la sacarosa, y que consiste
principalmente de glucosa y fructosa unidas por un enlace glucosídico
alfa 1-6.
Características: sustancia blanca o incolora, cristalina, dulce, leve olor específico de isomaltulosa.
Isomaltulosa: no menos de 98% p/p (sobre sustancia seca).
Agua: máx. 6% p/p.
Otros sacáridos: máx. 2% p/p (sobre sustancia seca).
Cenizas: máx. 0,01% p/p (sobre sustancia seca).
Plomo como Pb: máx. 0,1 mg/kg (sobre sustancia seca).
Metodología de análisis: FCC
Este producto se rotulará: “Isomaltulosa”.
5. L - CARNITINA
Identificación y pureza según lo establecido en FCC.
Uso: como ingrediente para utilizar en suplementos dietarios, fórmulas infantiles y alimentos para propósitos médicos.
6. CARNITINA (Clorhidrato)
Identificación y pureza según lo establecido en FCC.
Uso: como ingrediente para utilizar en suplementos dietarios, fórmulas infantiles y alimentos para propósitos médicos.
7. HIERRO ELECTROLÍTICO
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.
8. HIERRO (II) FUMARATO
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.
9. HIERRO (III) PIROFOSFATO
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.
10. HIERRO (II) LACTATO
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.
11. HIERRO (II) SULFATO
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios y alimentos fortificados.
12. TAURINA
Identificación y pureza según lo establecido en FCC, FDA, USP y otras Farmacopeas.
Uso: como ingrediente para utilizar en la elaboración de bebidas
analcohólicas con cafeína y taurina, y en la elaboración de fórmulas
infantiles.
13. COLÁGENO
Se entiende por colágeno, el subproducto concentrado y seco obtenido a
partir de las siguientes materias primas: cartílagos, tendones, huesos,
trozos de cuero, fascias, aponeurosis y productos de la pesca.
El producto se denominará Colágeno, si la materia prima no fue sometida a ningún proceso de hidrólisis.
Deberán cumplir con los siguientes requisitos:
a) No contener más de 2% de cenizas
b) No contener menos de 15% de nitrógeno
c) Salmonella: ausencia en 25 gramos
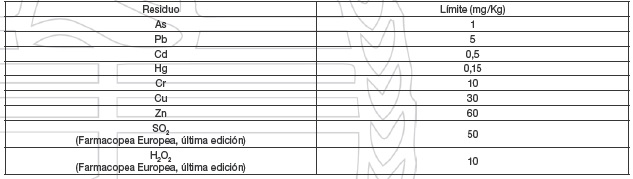
Límites de residuos.
Los límites de residuos permitidos quedan establecidos por el siguiente cuadro:
En la elaboración solo se permite el empleo de materia prima procedente
de animales que no hayan sufrido ninguna restricción por parte de la
Inspección Veterinaria. Se deberá declarar la especie animal de origen
de la materia prima utilizada.
Para la elaboración de los productos queda prohibida la utilización de
cueros y pieles que hayan sido sometidos a procesos de curtido,
independientemente de si se completó dicho proceso. A efectos de su
definición, se entiende por curtido el endurecimiento de pieles
mediante agentes endurecedores vegetales, sales de cromo u otras
sustancias como sales de aluminio, sales férricas, sales silíceas,
aldehídos y quinonas u otros agentes endurecedores sintéticos.
14. COLÁGENO HIDROLIZADO
Se entiende por colágeno hidrolizado, el subproducto concentrado, seco
y sometido a procesos de hidrólisis tales que no presenta propiedades
de formar gel en solución acuosa; obtenido a partir de las siguientes
materias primas: cartílagos, tendones, huesos, trozos de cuero,
fascias, aponeurosis y productos de la pesca. El producto deberá
cumplir con los mismos requisitos y condiciones de elaboración, así
como los límites de residuos del colágeno definido en el presente
artículo.
Uso: como ingrediente para utilizar en suplementos dietarios.
15. LUTEÍNA
Identificación y pureza según lo establecido en FCC y/o USP y/o otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios.
16. ZEAXANTINA
Identificación y pureza según lo establecido en FCC y/o USP y/o otras
Farmacopeas. Uso: como ingrediente para utilizar en suplementos
dietarios.
17. RESVERATROL
Identificación y pureza según lo establecido en FCC y/o USP y/o otras
Farmacopeas. Uso: como ingrediente para utilizar en suplementos
dietarios.
18. COENZIMA Q10
Identificación y pureza según lo establecido en FCC y/o USP y/o otras
Farmacopeas. Uso: como ingrediente para utilizar en suplementos
dietarios.
19. LICOPENO
Identificación y pureza según lo establecido en FCC y/o USP y/o otras Farmacopeas.
Uso: como ingrediente para utilizar en suplementos dietarios.
20. ß-HIDROXI-ß-METILBUTIRATO (HMB)
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
ID máximo: la ingesta diaria establecida por el elaborador no debe superar los 3 g por día.
Uso: como ingrediente para utilizar en suplementos dietarios.
21. BETA- ALANINA (ß-ALA)
Identificación y pureza según lo establecido en FCC, USP y otras Farmacopeas.
ID máximo: 2 g dividido en porciones o ingestas unitarias de no más de 300 mg.
Uso: como ingrediente para utilizar en suplementos dietarios”.
ARTÍCULO 2°.- La presente resolución entrará en vigencia a partir del día siguiente al de su publicación en el BOLETÍN OFICIAL.
ARTÍCULO 3°.- Comuníquese, publíquese, dese a la DIRECCIÓN NACIONAL DEL REGISTRO OFICIAL y archívese.
Leonardo Oscar Busso - Sergio Iraeta
e. 14/08/2024 N° 53479/24 v. 14/08/2024