MERCOSUR/GMC/RES. N° 04/24
REQUISITOS ZOOSANITARIOS DE LOS
ESTADOS PARTES DEL MERCOSUR PARA LA IMPORTACIÓN DE SEMEN BOVINO Y
BUBALINO CONGELADO (DEROGACIÓN DE LAS RESOLUCIONES GMC N° 49/14 Y 42/18)
VISTO: El Tratado de Asunción,
el Protocolo de Ouro Preto, la Decisión N° 06/96 del Consejo del
Mercado Común y las Resoluciones N° 45/14, 49/14 y 42/18 del Grupo
Mercado Común.
CONSIDERANDO:
Que, por Resolución GMC N° 49/14, se aprobaron los requisitos
zoosanitarios de los Estados Partes para la importación de semen bovino
y bubalino congelado, los cuales fueron modificados por la Resolución
GMC N° 42/18.
Que, por Resolución GMC N° 45/14, se aprobaron los requisitos
zoosanitarios adicionales de los Estados Partes para la importación de
semen y embriones de rumiantes con relación a la enfermedad de
Schmallenberg.
Que es necesario revisar la Resolución GMC N° 49/14, de acuerdo con las
recientes modificaciones de la normativa internacional de referencia de
la Organización Mundial de Sanidad Animal (OMSA).
Que es necesario contar con requisitos zoosanitarios de los Estados
Partes del MERCOSUR para la importación, así como con un modelo de
certificado veterinario internacional para la exportación de semen
bovino y bubalino congelado a los Estados Partes.
EL GRUPO MERCADO COMÚN
RESUELVE:
Art. 1 - Aprobar los "Requisitos zoosanitarios de los Estados Partes
del MERCOSUR para la importación de semen bovino y bubalino congelado"
y el modelo de Certificado Veterinario Internacional (CVI), que constan
como Anexos I y II, respectivamente, y forman parte de la presente
Resolución.
Art. 2 - Los Estados Partes indicarán, en el ámbito del Subgrupo de
Trabajo N° 8 "Agricultura" (SGT N° 8), los organismos nacionales
competentes para la implementación de la presente Resolución.
Art. 3 - Derogar las Resoluciones GMC N° 49/14 y 42/18.
Art. 4 - Esta Resolución deberá ser incorporada al ordenamiento jurídico de los Estados Partes antes del 07/X/2024.
CXXX GMC - Asunción, 10/IV/24.
ANEXO I
REQUISITOS ZOOSANITARIOS DE LOS ESTADOS PARTES DEL MERCOSUR PARA LA IMPORTACIÓN DE SEMEN BOVINO Y BUBALINO CONGELADO
CAPÍTULO I
DEFINICIONES
Art. 1 - A los fines de la presente Resolución, se entiende por:
- Centro de Colecta y Procesamiento de Semen (CCPS): los
establecimientos autorizados por la autoridad veterinaria del país
exportador que posean bovinos o bubalinos dadores de semen, o que
reciban dicho material para procesamiento y que reúnan las condiciones
estipuladas en el Código Sanitario para los Animales Terrestres de la
Organización Mundial de Sanidad Animal (OMSA) y donde se ejecuten los
procedimientos de colecta, procesamiento y almacenamiento de semen.
- Veterinario autorizado del CCPS: el veterinario reconocido por la
autoridad veterinaria para desempeñarse como responsable técnico del
CCPS.
CAPÍTULO II
DE LA CERTIFICACIÓN
Art. 2 - Toda importación de semen bovino y bubalino debe estar
acompañada del Certificado Veterinario Internacional (CVI), expedido
por la autoridad veterinaria del país exportador, que certifique el
cumplimiento de los requisitos zoosanitarios que constan en la presente
Resolución.
2.1 - El CVI debe ser previamente acordado entre el país exportador y
el Estado Parte importador de acuerdo con lo establecido en el Anexo II
de la presente Resolución.
2.2 - El CVI debe ser redactado, al menos, en el idioma del Estado Parte importador.
Art. 3 - El CVI tendrá una validez para el ingreso al Estado Parte
importador de hasta sesenta (60) días contados a partir de la fecha de
su emisión.
Art. 4 - Las pruebas de diagnóstico deben ser realizadas de acuerdo con
el Manual de las Pruebas de Diagnóstico y de las Vacunas para los
Animales Terrestres de la OMSA en laboratorios oficiales, acreditados o
reconocidos por la autoridad veterinaria del país exportador.
Art. 5 - Las vacunas deben ser elaboradas de acuerdo con el Manual de
las Pruebas de Diagnóstico y de las Vacunas para los Animales
Terrestres de la OMSA y deben ser aprobadas por la autoridad competente
del país exportador.
Art. 6 - La colecta de muestras para la realización de las pruebas de
diagnóstico establecidas en la presente Resolución debe ser supervisada
por un veterinario oficial o por el veterinario autorizado del CCPS.
Art. 7 - El país o zona de origen del semen a ser exportado que sea
reconocido por la OMSA como libre; o el país, zona, compartimento o el
establecimiento de origen del semen que cumpla con las condiciones del
Código Sanitario para los Animales Terrestres de la OMSA para ser
considerado libre de alguna de las enfermedades para las cuales se
requieran pruebas de diagnóstico o vacunaciones, puede ser exceptuado
de la realización de esas pruebas. En ambos casos, debe contar con el
reconocimiento de dicha condición por el Estado Parte importador y
tales certificaciones deben estar incluidas en CVI.
Art. 8 - El Estado Parte importador que cumpla con lo establecido en
los capítulos correspondientes del Código Sanitario para los Animales
Terrestres de la OMSA para ser considerado libre, o que posea un
programa oficial de prevención, control o erradicación para cualquier
enfermedad que afecte a la especie, se reserva el derecho de solicitar
medidas de mitigación adicionales con el objetivo de prevenir el
ingreso de esa enfermedad al país.
Art. 9 - El Estado Parte importador y el país exportador pueden acordar
otros procedimientos sanitarios que otorguen garantías equivalentes o
superiores a las previstas en la presente Resolución.
Art. 10 - El país o zona de origen del semen a ser exportado, además de
las exigencias establecidas en la presente Resolución, debe cumplir con
los requisitos zoosanitarios adicionales de los Estados Partes para la
importación de semen y embriones de rumiantes con relación a la
enfermedad de Schmallenberg, según lo establecido en la Resolución GMC
N° 45/14, sus modificatorias y/o complementarias.
CAPÍTULO III
INFORMACIÓN ZOOSANITARIA
Art. 11 - Con respecto a Perineumonía Contagiosa Bovina (PCB):
11.1 - El país o zona exportadora debe ser reconocido oficialmente por
la OMSA como libre o el país, zona o compartimento exportador debe
cumplir con lo establecido en el capítulo correspondiente del Código
Sanitario para los Animales Terrestres de la OMSA para ser considerado
libre y dicha condición debe ser reconocida por el Estado Parte
importador.
11.2 - Los dadores deben permanecer desde su nacimiento o durante por
lo menos los últimos seis (6) meses en un país, zona o compartimento
libre de PCB.
Art. 12 - Con respecto a Fiebre Aftosa (FA):
12.1 - El país o zona exportadora debe ser reconocido oficialmente por
la OMSA como libre con o sin vacunación o el compartimento debe ser
reconocido como libre por el Estado Parte importador.
12.2 - En el caso de que el país, zona o compartimento exportador sea libre de Fiebre Aftosa sin vacunación:
12.2.1 - Los dadores no deben manifestar ningún signo clínico de Fiebre
Aftosa el día de la colecta del semen ni durante los treinta (30) días
posteriores a dicha colecta; y
12.2.2 - Los dadores deben permanecer por lo menos durante los tres (3)
meses anteriores a la colecta de semen en un país, zona o compartimento
libre de Fiebre Aftosa en los cuales no se aplica la vacunación.
12.3 - En el caso de que el país o zona exportadora sea libre de Fiebre Aftosa con vacunación:
12.3.1 - Los dadores no deben haber manifestado ningún signo clínico de
Fiebre Aftosa el día de la colecta de semen ni durante los treinta (30)
días posteriores a dicha colecta; y
12.3.2 - Los dadores deben permanecer en un país o una zona libre de
Fiebre Aftosa donde se aplique la vacunación, por lo menos durante los
tres (3) meses anteriores a la colecta de semen. En caso de que el
semen sea destinado a una zona o compartimento libre sin vacunación,
los dadores deben, además:
12.3.2.1 - ser vacunados por lo menos dos (2) veces y la última vacuna
debe ser administrada en un plazo no mayor a seis (6) meses ni menor a
un (1) mes antes de la colecta de semen a ser exportado, salvo que se
demuestre la inmunidad protectora durante más de seis (6) meses; o
12.3.2.2 - resultar negativos a las pruebas de detección de anticuerpos
contra el virus de la Fiebre Aftosa a las que fueron sometidos a partir
de los veintiún (21) días posteriores a la colecta de semen a ser
exportados.
12.3.3 - El semen debe ser almacenado en el país de origen durante, por
lo menos, los treinta (30) días posteriores a su colecta y ningún
animal presente en el establecimiento en el que permanecieron los
animales dadores debe haber manifestado signos clínicos de Fiebre
Aftosa durante ese período.
Art. 13 - Con respecto a Fiebre del Valle del Rift (FVR):
13.1 - El país exportador debe cumplir con las recomendaciones de la
OMSA para ser considerado libre de FVR y esta condición debe ser
reconocida por la autoridad veterinaria del Estado Parte importador; o
13.2 - Los dadores no deben haber manifestado ningún signo clínico de
FVR durante los catorce (14) días anteriores y los catorce (14) días
posteriores a la colecta del semen, y deben:
13.2.1 - haber sido vacunados contra la FVR por lo menos catorce (14) días antes de la colecta; o
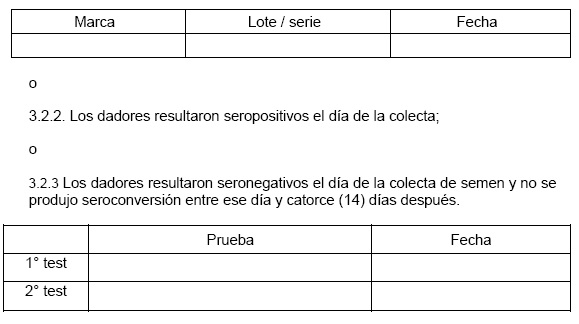
13.2.2 - ser seropositivos el día de la colecta; o
13.2.3 - ser seronegativos el día de la colecta y que no haya ocurrido
seroconversión entre ese día y en los catorce (14) días posteriores.
Art. 14 - Con respecto a Dermatosis Nodular Contagiosa (DN):
14.1 - El país exportador debe cumplir con las recomendaciones de la
OMSA para ser considerado libre de DN y esta condición debe ser
reconocida por el Estado Parte importador. Los dadores no deben haber
presentado ningún signo clínico de la enfermedad el día de la colecta y
deben haber permanecido en ese país o zona por lo menos durante los
veintiocho (28) días anteriores a la colecta; o
14.2 - El semen a ser exportado debe ser sometido a una prueba de detección del agente por PCR, y los dadores:
14.2.1 - No deben haber manifestado ningún signo clínico de DN el día
de la colecta del semen ni durante los veintiocho (28) días posteriores
y deben haber permanecido durante los sesenta (60) días anteriores a la
colecta en un CCPS en el cual no haya ocurrido ningún caso de DN
durante ese período, y deben:
14.2.1.1 - ser vacunados regularmente de acuerdo con las
recomendaciones del fabricante, siendo la última vacunación dentro de
los sesenta (60) días previos a la primera colecta del semen a ser
exportado y deben presentar anticuerpos contra el virus de la DN
treinta (30) días después de la vacunación; o,
14.2.1.2 - ser sometidos, con resultado negativo, a una prueba de virus
neutralización o ELISA para la detección de DN, al menos, cada
veintiocho (28) días durante el período de colecta del semen y veintiún
(21) días después de la última colecta de semen a ser exportado y,
además deben ser sometidos, con resultado negativo, a pruebas de PCR, a
partir de muestras de sangre tomadas al principio y al final del
período de colecta y por lo menos cada veintiocho (28) días durante
este período.
Art. 15 - Con respecto a Lengua Azul (LA):
15.1 - El país o zona exportadora debe cumplir con las recomendaciones
de la OMSA para ser considerado libre de LA y esta condición debe ser
reconocida por la autoridad veterinaria del Estado Parte importador; o
15.2 - Los dadores del semen a ser exportado no deben haber manifestado
ningún signo clínico de LA el día de la colecta del semen, y deben:
15.2.1 - ser sometidos a una prueba de Inmunodifusión en Gel de Agar
(AGID), virus neutralización o c-ELISA (ELISA de competición) contra el
grupo del virus de la LA entre veintiocho (28) y sesenta (60) días
después de cada colecta del semen a ser exportado, o
15.2.2 - ser sometidos, con resultado negativo, a pruebas de
identificación del agente, realizadas a partir de las muestras de
sangre tomadas al principio, al final y durante todo el periodo de
colecta del semen a ser exportado. Para el caso de aislamiento del
virus, las muestras debieron tomarse por lo menos cada siete (7) días,
o para PCR, por lo menos cada veintiocho (28) días, o
15.2.3 - ser sometidos, con resultado negativo, a una prueba de
aislamiento viral o qRT-PCR (prueba cuantitativa en tiempo real) en
muestras de cada partida de semen a ser exportado, considerando como
partida a la colecta de un mismo dador en una misma fecha.
Art. 16 - Con respecto a Tuberculosis y a Brucelosis:
16.1 - Para ingresar al CCPS, los toros y animales excitadores deben
provenir de establecimientos en los cuales no haya habido notificación
de ocurrencia de estas enfermedades en los últimos noventa (90) días
previos al ingreso y deben haber resultado negativo a las pruebas de
diagnóstico realizadas dentro de los sesenta (60) días previos al
ingreso, para las siguientes enfermedades:
16.1.1 - Tuberculosis: Prueba intradérmica anocaudal PPD (derivado
proteico purificado) bovina o intradérmica cervical simple con PPD
bovina o comparada con PPD bovina y aviar.
16.1.2. - Brucelosis: Antígeno Acidificado Tamponado (Rosa de Bengala o
BPA) o Fluorescencia Polarizada o I-ELISA. Los animales positivos al
test Antígeno Acidificado Tamponado (Rosa de Bengala o bPa) podrán ser
sometidos a Fijación de Complemento o 2-mercaptoetanol o test de
I-ELISA o Fluorescencia Polarizada, con resultado negativo, o
16.1.3 - Los animales que proceden de establecimientos libres de esas
enfermedades de acuerdo con un programa sanitario oficial vigente en el
país de origen están exentos de las pruebas descriptas en los numerales
16.1.1 y 16.1.2.
16.2 - Durante el período de aislamiento en el CCPS, los toros y
animales excitadores deben ser sometidos, con resultado negativo, a las
siguientes pruebas diagnósticas:
16.2.1 - Brucelosis: Antígeno Acidificado Tamponado (Rosa de Bengala o
BPA) o Fluorescencia Polarizada o I-ELISA. Los animales con resultado
positivo al test Antígeno Acidificado Tamponado (Rosa de Bengala o BPA)
podrán ser sometidos a Fijación de Complemento o 2-mercaptoetanol o
test de I-ELISA o Fluorescencia Polarizada, con resultado negativo.
16.2.2 - Tuberculosis: Prueba intradèrmica anocaudal con PPD bovina o
intradèrmica cervical simple con PPD bovina o comparada con PPD bovina
y aviar. La prueba se debe efectuar al menos sesenta (60) días después
de la prueba realizada en el rebaño de origen.
16.3 - Los dadores residentes del CCPS deben dar resultado negativo a
las pruebas previstas en los numerales 16.2.1 y 16.2.2 al menos una vez
cada doce (12) meses.
Art. 17 - Con respecto a Tricomonosis (
Trichomonas foetus):
17.1 - Los dadores residentes del CCPS deben ser sometidos a una prueba
de cultivo, con resultado negativo, al menos una vez cada doce (12)
meses; y
17.2 - Los dadores de menos de seis (6) meses de edad o que, desde esa
edad, permanecieron siempre en un grupo del mismo sexo antes del
aislamiento previo, deben ser sometidos, con resultado negativo, a una
prueba de cultivo realizada a partir de una muestra prepucial; o
17.3 - Antes de su ingreso al CCPS, los dadores de más de seis (6)
meses de edad que estuvieron o hayan podido estar en contacto con
hembras antes del aislamiento previo deben ser sometidos, con resultado
negativo, a tres (3) pruebas de cultivo realizadas con una (1) semana
de intervalo entre ellas, a partir de una muestra prepucial.
Art. 18 - Con respecto a Campilobacteriosis Genital Bovina (
Campylobacter foetus veneralis):
18.1 - Los dadores residentes del CCPS deben ser sometidos, con
resultado negativo, a una prueba de cultivo o a una prueba de
inmunofluorescencia realizada a partir de una muestra prepucial, al
menos una vez cada doce (12) meses; y
18.2 - Antes de su ingreso al CCPS, los dadores de menos de seis (6)
meses de edad o que, desde esa edad, permanecieron siempre en un grupo
del mismo sexo antes del aislamiento previo, deben ser sometidos, con
resultado negativo, a una prueba de cultivo o inmunofluorescencia
realizada a partir de una muestra prepucial; o
18.3 - Antes de su ingreso al CCPS, los dadores de más de seis (6)
meses de edad que estuvieron o hayan podido estar en contacto con
hembras antes del aislamiento previo deben ser sometidos, con resultado
negativo, a tres (3) pruebas de cultivo o inmunofluorescencia
realizadas con una semana de intervalo entre ellas, a partir de una
muestra prepucial.
Art. 19 - Con respecto a Diarrea Viral Bovina (DVB):
19.1 - Los dadores de semen a ser exportado, residentes del CCPS, deben
haber sido sometidos, con resultado negativo, a una prueba de
aislamiento viral o a una prueba de ELISA para la detección de
antígeno; o
19.2 - Una muestra de semen congelado de cada partida a ser exportada
debe ser sometida a la prueba de RT-PCR o aislamiento viral, con
resultado negativo, considerando como partida a la colecta del semen de
un mismo dador en una misma fecha.
Art. 20 - Con respecto a Rinotraqueítis Infecciosa Bovina (IBR):
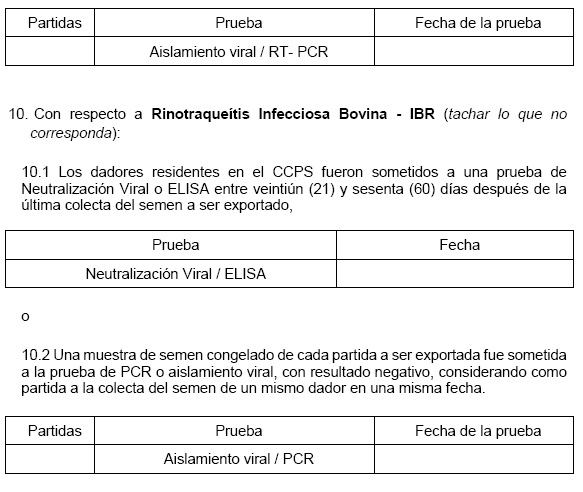
20.1 - Los dadores residentes en el CCPS deben ser sometidos a una
prueba de Neutralización Viral o ELISA entre veintiún (21) y sesenta
(60) días después de la última colecta del semen a exportar, o
20.2 - Una muestra de semen congelado de cada partida a ser exportada
debe ser sometida a la prueba de PCR o aislamiento viral, con resultado
negativo, considerando como partida a la colecta del semen de un mismo
dador en una misma fecha.
CAPÍTULO IV
DEL CENTRO DE COLECTA Y PROCESAMIENTO DE SEMEN (CCPS)
Art. 21 - El CCPS debe estar registrado, ser aprobado por la autoridad
veterinaria del país de origen y cumplir con las condiciones
establecidas en el capítulo correspondiente del Código Terrestre de la
OMSA aplicables a las "Condiciones generales de higiene en los centros
de toma y tratamiento de semen" y sus actualizaciones.
Art. 22 - El semen debe ser colectado y procesado bajo la supervisión del veterinario autorizado del CCPS.
Art. 23 - En el CCPS no se debe haber registrado la ocurrencia de
enfermedades trasmisibles por semen entre los noventa (90) días previos
a la primera colecta y los treinta (30) días posteriores a la última
colecta del semen a ser exportado.
CAPÍTULO V
DE LOS DADORES DE SEMEN
Art. 24 - Los animales dadores de semen deben haber nacido y
permanecido en forma ininterrumpida en el país exportador hasta la
colecta del semen a ser exportado. Cuando se trate de dadores
importados, estos deben proceder de un país con igual o superior
condición sanitaria que el país exportador y deben haber permanecido en
el país exportador los últimos sesenta (60) días previos a la colecta
del semen a ser exportado. La importación de dadores debe haber
cumplido con lo establecido en la presente Resolución para la
enfermedad de Schmallenberg, Perineumonía Contagiosa Bovina, Dermatosis
Nodular Contagiosa, Fiebre Aftosa y Fiebre del Valle del Rift.
Art. 25 - Antes de ingresar al CCPS, los dadores de semen y los
animales excitadores deben haber permanecido en una instalación de
aislamiento durante al menos treinta (30) días. Los animales residentes
que salieren del CCPS deben cumplir con este período nuevamente para su
reingreso.
Art. 26 - Los dadores que sean trasladados directamente entre CCPS
aprobados oficialmente por la autoridad veterinaria del país exportador
pueden ser exceptuados del período de aislamiento preingreso, siempre y
cuando:
a) las condiciones sanitarias establecidas en la presente Resolución hayan sido cumplidas.
b) las pruebas de diagnóstico realizadas en el CCPS de origen se encuentren vigentes.
c) el transporte de los dadores sea directo entre ambos CCPS, sin
transitar por zonas de condiciones sanitarias inferiores o bajo
restricciones sanitarias.
d) los dadores no mantengan contacto con otros animales susceptibles a las enfermedades que afectan a la especie.
e) el vehículo haya sido lavado y desinfectado previamente al transporte.
Art. 27 - Los dadores no deben ser utilizados en monta natural durante
toda su permanencia en el CCPS, incluyendo el período de aislamiento
preingreso mencionado en el Artículo 25.
Art. 28 - Los dadores deben mantenerse bajo supervisión del veterinario
oficial o del veterinario autorizado del CCPS y no deben presentar
evidencias clínicas de enfermedades transmisibles por semen el día de
la colecta y, por lo menos, los treinta (30) días posteriores a la
colecta del semen a ser exportado.
CAPÍTULO VI
DE LA COLECTA, PROCESAMIENTO Y ALMACENAMIENTO DEL SEMEN
Art. 29 - El semen debe ser colectado, procesado y almacenado de
acuerdo con las recomendaciones establecidas en el capítulo
correspondiente del Código Sanitario de los Animales Terrestres de la
OMSA.
Art. 30 - Los productos a base de huevos utilizados como diluyentes del
semen deben ser originarios de un país, zona o compartimento libre de
Influenza Aviar (IA) de notificación obligatoria ante la OMSA y de
enfermedad de Newcastle (NC) de acuerdo con las recomendaciones de la
OMSA, o deben ser huevos SPF (Specific Pathogen Free), o deben ser
sometidos a un tratamiento térmico que inactive el virus de la IA y NC.
Art. 31 - En caso de utilizarse leche en el procesamiento del semen,
esta debe ser originaria de un país o zona reconocida por la OMSA como
libre de Fiebre Aftosa (FA) con o sin vacunación, o debe ser sometida a
un tratamiento térmico que inactive el virus de la FA.
Art. 32 - El semen debe ser acondicionado en forma adecuada, almacenado
en contenedores criogénicos limpios y desinfectados o de primer uso y
las pajuelas identificadas individualmente, incluyendo la fecha de
colecta. El material debe estar bajo responsabilidad del veterinario
autorizado del CCPS hasta el momento del precintado.
Art. 33 - El semen destinado a exportación a un Estado Parte solo puede
ser almacenado con otro de condición sanitaria equivalente y el
nitrógeno líquido utilizado en el contenedor criogénico debe ser de
primer uso.
Art. 34 - El semen solamente puede ser exportado a partir de los
treinta (30) días posteriores a su colecta. Durante ese período, no
debe registrarse ninguna evidencia clínica de enfermedades
transmisibles en el CCPS ni en los dadores.
CAPÍTULO VII
DEL PRECINTADO
Art. 35 - El contenedor criogénico del semen a ser exportado debe estar
precintado en forma previa a su salida del CCPS bajo la supervisión del
Servicio Veterinario Oficial o autorizado por ese Servicio y el número
de precinto debe constar en el Certificado Veterinario Internacional
correspondiente.
Art. 36 - La autoridad veterinaria del país exportador debe verificar
la integridad de los contenedores criogénicos del semen y de los
precintos correspondientes dentro de las setenta y dos (72) horas
previas a la exportación o en el punto de salida del país exportador.
ANEXO II
MODELO DE CERTIFICADO VETERINARIO
INTERNACIONAL PARA LA EXPORTACIÓN DE SEMEN BOVINO Y BUBALINO CONGELADO
A LOS ESTADOS PARTES DEL MERCOSUR
IV. IDENTIFICACIÓN DEL SEMEN
V. INFORMACIÓN ZOOSANITARIA
El Veterinario Oficial abajo firmante certifica que:
1. Con relación a
Perineumonía Contagiosa Bovina -
PCB (
tachar lo que no corresponda):
1.1 En cuanto a la condición sanitaria:
1.1.1 El país o zona exportadora es reconocido oficialmente por la Organización Mundial de Sanidad Animal (OMSA) como libre; o
1.1.2 El país, zona o compartimento exportador cumple con lo
establecido en el capítulo correspondiente del Código Sanitario para
los Animales Terrestres de la OMSA para ser considerado libre de PCB y
dicha condición fue reconocida por el Estado Parte importador.
1.2 Los dadores permanecieron desde su nacimiento o durante, por lo
menos, los últimos seis (6) meses en un país, zona o compartimento
libre de PCB.
2. Con relación a
Fiebre Aftosa - FA (
tachar lo que no corresponda):
2.1 El país o zona exportadora es reconocido oficialmente por la OMSA
como libre con o sin vacunación o el compartimento fue reconocido como
libre por el Estado Parte importador.
2.2 El país, zona o compartimento exportador es libre de FA sin vacunación:
2.2.1 Los dadores no manifestaron ningún signo clínico de FA el día de
la colecta del semen ni durante los treinta (30) días posteriores a
dicha colecta; y
2.2.2 Los dadores permanecieron durante por lo menos los tres (3) meses
anteriores a la colecta de semen en un país, zona o compartimento libre
de FA en el cual no se aplica la vacunación.
2.3 El país o zona exportadora es libre de FA con vacunación:
2.3.1 Los dadores no manifestaron ningún signo clínico de FA el día de
la colecta de semen ni durante los treinta (30) días posteriores a
dicha colecta; y
2.3.2 Los dadores permanecieron en un país o una zona libre de FA en el
cual se aplica la vacunación, durante por los menos los tres (3) meses
anteriores a la colecta de semen.
En caso de que el semen sea destinado a una zona o compartimento libre sin vacunación, además:
2.3.2.1 Los dadores fueron vacunados por lo menos dos (2) veces y la
última vacuna fue administrada en un plazo no mayor a seis (6) meses ni
menor a un (1) mes antes de la colecta de semen a ser exportado, salvo
que se demuestre la inmunidad protectora durante más de seis (6) meses;
2.3.3 El semen se almacenó en el país de origen durante, por lo menos,
los treinta (30) días posteriores a su colecta, y ningún animal
presente en el
establecimiento en el que permanecieron los animales dadores manifestó
signos clínicos de FA durante ese período.
3. Con respecto a
Fiebre del Valle del Rift - FVR (t
achar lo que no corresponda):
3.1 El país exportador cumple con las recomendaciones de la OMSA para
serconsiderado libre de FVR y esta condición fue reconocida por la
autoridad
veterinaria del Estado Parte importador; o
3.2 Los dadores no presentaron ningún signo clínico de FVR durante los
catorce (14) días anteriores y los catorce (14) días posteriores a la
colecta del semen; y
3.2.1 Los dadores fueron vacunados contra la FVR por lo menos catorce (14) días antes de la colecta;
4. Con respecto a
Dermatosis Nodular Contagiosa - DN (
tachar lo que no corresponda):
4.1 El país exportador cumple con las recomendaciones de la OMSA para
ser considerado libre de DN y esta condición fue reconocida por el
Estado Parte importador. Los animales no presentaron ningún signo
clínico de la enfermedad el día de la colecta, y permanecieron en ese
país o zona por lo menos los veintiocho (28) días anteriores a la
colecta; o
4.2 El semen exportado fue sometido a una prueba de detección del
agente por PCR y los dadores no manifestaron ningún signo clínico de DN
el día de la colecta del semen ni durante los veintiocho (28) días
posteriores y permanecieron durante los sesenta (60) días anteriores a
la colecta en un CCPS en el que no ocurrió ningún caso de DN durante
ese período, y
4.2.1 Los dadores fueron vacunados regularmente de acuerdo con las
recomendaciones del fabricante, siendo la última vacunación dentro de
los sesenta (60) días previos a la primera colecta del semen a ser
exportado y demostraron la presencia de anticuerpos contra el virus de
la DN treinta (30) días después de la vacunación;
o,
4.2.2. Los dadores fueron sometidos, con resultado negativo, a una
prueba de Virus Neutralización o ELISA para la detección de DN al menos
cada veintiocho (28) días durante el período de colecta del semen a ser
exportado y veintiún (21) días después de la última colecta de semen a
ser exportado y, además, fueron sometidos con resultado negativo a la
prueba de PCR, a partir de muestras de sangre tomadas al principio y al
final del período de colecta y por lo menos cada veintiocho (28) días
durante este período.
5. Con respecto a
Lengua Azul - LA (
tachar lo que no corresponda):
5.1 El país o zona exportadora cumple con las recomendaciones de la
OMSA para ser considerado libre de LA y esta condición fue reconocida
por la autoridad veterinaria del Estado Parte importador; o
5.2 Los dadores del semen a ser exportado no manifestaron ningún signo clínico de LA el día de la colecta del semen, y
5.2.1 Los dadores fueron sometidos a una prueba de Inmunodifusión en
Gel de Agar (AGID), Virus Neutralización (VN) o c-ELISA (ELISA de
competición) contra el grupo del virus de la LA entre veintiocho (28) y
sesenta (60) días después de cada colecta del semen a ser exportado,
o
5.2.2 Los dadores resultaron negativos a pruebas de identificación del
agente, que se efectuaron a partir de las muestras de sangre tomadas al
principio, al final y durante todo el período de colecta de semen a
exportar. Para el caso de aislamiento del virus, las muestras fueron
tomadas por lo menos cada siete (7) días, o para PCR, por lo menos cada
veintiocho (28) días,
6. Con respecto a
Tuberculosis y a
Brucelosis (
tachar lo que no corresponda):
6.1 Los toros y animales excitadores que ingresaron al CCPS procedieron
de establecimientos en los cuales no hubo notificación de ocurrencia de
estas enfermedades en los últimos noventa (90) días y en las pruebas de
diagnóstico realizadas dentro de los sesenta (60) días previos al
ingreso, los animales obtuvieron resultados negativos para:
6.1.1. Tuberculosis: Prueba intradèrmica anocaudal PPD (derivado
proteico purificado) bovina o intradèrmica cervical simple con PPD
bovina o comparada con PPD bovina y aviar.
6.1.2. Brucelosis: Antígeno Acidificado Tamponado (Rosa de Bengala o
BPA) o Fluorescencia Polarizada o I-ELISA. Los animales positivos al
test Antígeno Acidificado Tamponado (Rosa de Bengala o BPA) fueron
sometidos a Fijación de Complemento o 2-mercaptoetanol o Test de
I-ELISA o Fluorescencia Polarizada con resultado negativo.
O
6.1.3. Los animales proceden de establecimientos libres de esas
enfermedades de acuerdo con un programa sanitario oficial vigente en el
país de origen,
quedando exentos de la realización de las pruebas descriptas en los numerales 6.1.1 y 6.1.2.
6.2 Durante el período de aislamiento en el CCPS, fueron sometidos con resultado negativo a las siguientes pruebas diagnósticas:
6.2.1 Los toros y animales excitadores:
6.2.1.1 Brucelosis: Antígeno Acidificado Tamponado (Rosa de Bengala o
BPA) o Fluorescencia Polarizada o I-ELISA. Los animales positivos al
test Antígeno Acidificado Tamponado (Rosa de Bengala o BPA) fueron
sometidos a Fijación de Complemento (FC) o 2-mercaptoetanol o test de
I-ELISA o Fluorescencia Polarizada con resultado negativo.
6.2.1.2 Tuberculosis: Prueba intradérmica anocaudal con PPD bovina o
intradérmica cervical simple con PPD bovina o comparada con PPD bovina
y aviar. La misma fue realizada no menos de sesenta (60) días después
de la prueba realizada en el rebaño de origen.
6.3 Los dadores residentes del CCPS resultaron negativo, al menos una
vez cada doce (12) meses, a las pruebas descriptas en los numerales
6.2.1.1. y 6.2.1.2.
7. Con respecto a
Tricomonosis (
Trichomonas foetus) (
tachar lo que no corresponda):
7.1 Los dadores residentes del CCPS dieron resultado negativo, al menos una vez cada doce (12) meses, a una prueba de cultivo; y
7.2 Los dadores de menos de seis (6) meses de edad o que, desde esa
edad, permanecieron siempre en un grupo del mismo sexo antes del
aislamiento previo, dieron resultado negativo en una prueba de cultivo
realizada a partir de una muestra prepucial; o
7.3 Antes de su ingreso al CCPS, los dadores de más de seis (6) meses
de edad que estuvieron o hayan podido estar en contacto con hembras
antes del aislamiento previo dieron resultado negativo en tres (3)
pruebas de cultivo realizadas con una (1) semana de intervalo entre
ellas, a partir de una muestra prepucial.
8. Con respecto de
Campilobacteriosis Genital Bovina (Campylobacter foetus veneralis) (
tachar lo que no corresponda):
8.1 Los dadores residentes del CCPS dieron resultado negativo, al menos
una vez cada doce (12) meses, a una prueba de cultivo o a una prueba de
inmunofluorescencia indirecta realizada a partir de una muestra
prepucial; y
8.2 Antes de su ingreso al CCPS, los dadores de menos de seis (6) meses
de edad o que, desde esa edad, permanecieron siempre en un grupo del
mismo sexo antes del aislamiento previo, dieron resultado negativo en
una prueba de cultivo o inmunofluorescencia indirecta realizada a
partir de una muestra prepucial; o
8.3 Antes de su ingreso al CCPS, los dadores de más de seis (6) meses
de edad que estuvieron o hayan podido estar en contacto con hembras
antes del aislamiento previo dieron resultado negativo a tres pruebas
de cultivo o inmunofluorescencia indirecta realizadas con una semana de
intervalo entre ellas, a partir de una muestra prepucial.
o
9.2 Una muestra de semen congelado de cada partida a ser exportada fue
sometida a la prueba de RT-PCR o aislamiento viral, con resultado
negativo, considerando como partida a la colecta del semen de un mismo
dador en una misma fecha.
11. Con respecto a la
Enfermedad de Schmallenberg:
Nota: Debe ser incluida en forma detallada la certificación que
contemple los requisitos zoosanitarios adicionales de los Estados
Partes para la importación de semen y embriones de rumiantes con
relación a dicha enfermedad según lo establecido en la Resolución GMC
N° 45/14, sus modificatorias y/o complementarias.
VI. DEL CENTRO DE COLECTA Y PROCESAMIENTO DE SEMEN (CCPS)
Nota: Debe incluirse información detallada de conformidad con lo
dispuesto en el Capítulo IV de la Resolución GMC N° 04/24
correspondiente al "Centro de Colecta y Procesamiento de Semen''.
VII. DE LOS DADORES DEL SEMEN
Nota: Debe incluirse información detallada de conformidad con lo
dispuesto en el Capítulo V de la Resolución GMC N° 04/24
correspondiente a los "Dadores del Semen''.
VIII. DE LA COLECTA, PROCESAMIENTO Y ALMACENAMIENTO DEL SEMEN
Nota: Debe incluirse información detallada de conformidad con lo
dispuesto en el Capítulo VI de la Resolución GMC N° 04/24
correspondiente a la "Colecta, Procesamiento y Almacenamiento del
Semen''.
IX. DEL PRECINTADO
El contenedor criogènico del semen a ser exportado fue precintado en
forma previa a su salida del CCPS bajo la supervisión del Servicio
Veterinario Oficial o autorizado por ese Servicio y el número de
precinto consta en el presente Certificado Veterinario Internacional.
La autoridad veterinaria del país exportador verificó la integridad de
los contenedores criogénicos del semen y de los precintos
correspondientes dentro de las setenta y dos (72) horas previas a la
exportación o en el punto de salida del país exportador.
El presente Certificado Veterinario Internacional tiene una validez de
sesenta (60) días corridos a partir de su fecha de emisión.
Lugar de Emisión:........................................................................ Fecha
Nombre y Firma del Veterinario Oficial:.......................................
Sello del Servicio Veterinario Oficial:........................................
IF-2024-107497003-APN-DNCYAI#MEC