ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
Decisión Administrativa 22/2003
Apruébase la estructura organizativa del primer nivel operativo del citado organismo descentralizado dependiente de la Secretaría de Políticas, Regulación y Relaciones Sanitarias del Ministerio de Salud.
Bs. As., 14/3/2003
VISTO el Expediente N° 1-47-12313/02-1, la Decisión Administrativa N° 434 del 12 de diciembre de 1996 y el Decreto N° 357 del 21 de febrero de 2002 y sus modificaciones, y
CONSIDERANDO:
Que por la Decisión Administrativa N° 434/96 se aprobó la estructura organizativa de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
Que por el decreto citado en el Visto y sus modificaciones, se aprobó el organigrama de aplicación de la Administración Pública Nacional Centralizada hasta el nivel de Subsecretaría, estableciéndose sus competencias.
Que este último decreto, en su artículo 19, establece la obligación de presentar a la JEFATURA DE GABINETE DE MINISTROS la propuesta de estructura de primer nivel operativo aplicando una importante reducción con relación a lo vigente, con el objeto de contribuir con ahorros en la actual situación de emergencia.
Que la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA ha dado cumplimiento a la normativa mencionada en el considerando precedente.
Que ha tomado intervención la SUBSECRETARIA DE LA GESTION PUBLICA de la JEFATURA DE GABINETE DE MINISTROS.
Que la presente medida se dicta en ejercicio de las facultades conferidas por el artículo 100 de la CONSTITUCION NACIONAL y por el artículo 16, inciso 12) de la Ley de Ministerios (texto ordenado por Decreto N° 438/92) y sus modificaciones.
Por ello,
EL JEFE DE GABINETE DE MINISTROS
DECIDE:
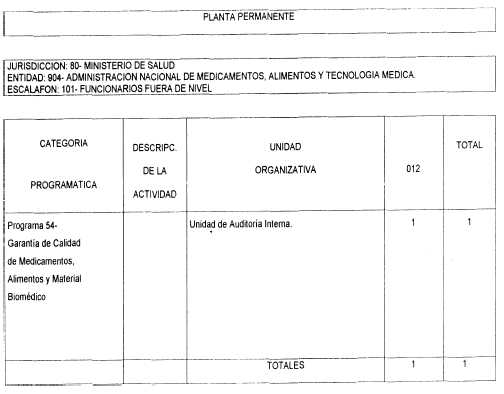
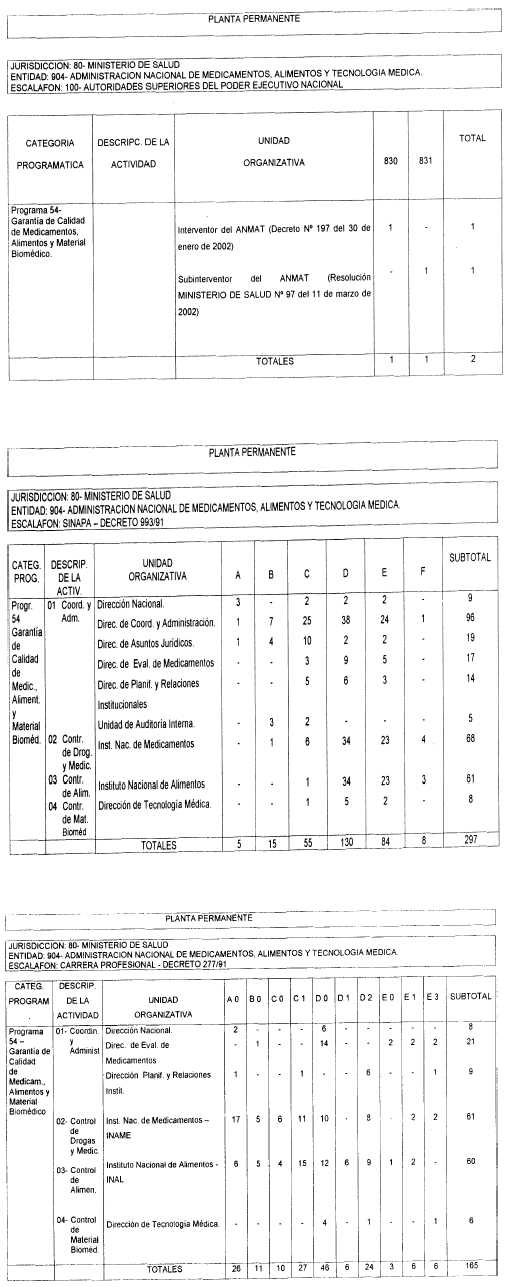
Artículo 1° — Apruébase la estructura organizativa del primer nivel operativo de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, organismo descentralizado dependiente de la SECRETARIA DE POLITICAS, REGULACION Y RELACIONES SANITARIAS del MINISTERIO DE SALUD, de acuerdo al Organigrama, Objetivos, Responsabilidad Primaria y Acciones y Dotación, que como Anexos I, II y III forman parte integrante de la presente decisión administrativa.
Art. 2° — Derógase la Decisión Administrativa N° 434/96.
Art. 3° — En un plazo de TREINTA (30) días, la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, deberá elevar a la SUBSECRETARIA DE LA GESTION PUBLICA dependiente de la JEFATURA DE GABINETE DE MINISTROS, para su evaluación, la estructura organizativa correspondiente al segundo nivel operativo, en concordancia con lo establecido por el Decreto N° 1545 del 31 de agosto de 1994 reglamentado por la Resolución de la ex-SECRETARIA DE LA FUNCION PUBLICA N° 422 del 13 de septiembre de 1994.
Art. 4° — Establécese que hasta tanto se aprueben las unidades de nivel inferior a las aprobadas por la presente, conservarán su vigencia las unidades existentes a la fecha, con la asignación de los suplementos que les correspondiere.
Art. 5° — El gasto que demande el cumplimiento de la presente medida será atendido con los créditos asignados a la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, organismo descentralizado del MINISTERIO DE SALUD.
Art. 6° — Comuníquese, publíquese, dése a la DIRECCION NACIONAL DEL REGISTRO OFICIAL y archívese. — Alfredo N. Atanasof. — Ginés M. González García.
ANEXO I
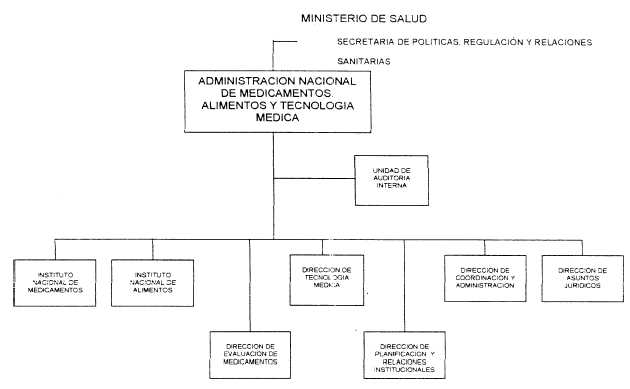
ANEXO II
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
OBJETIVOS
Realizar las acciones conducentes al registro, control, fiscalización y vigilancia de la sanidad y calidad de los productos, substancias, elementos, procesos, tecnologías y materiales que se consumen o utilizan en la medicina, alimentación y cosmética humana y del contralor de las actividades y procesos que median o están comprendidos en estas materias.
Aplicar y velar por el cumplimiento de las disposiciones legales, científicas, técnicas y administrativas comprendidas dentro del ámbito de sus competencias.
UNIDAD DE AUDITORIA INTERNA
RESPONSABILIDAD PRIMARIA:
Realizar exámenes integrales de las actividades, procesos y resultados de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA de manera de asegurar niveles continuos de eficacia, eficiencia y economía en la gestión.
ACCIONES:
1. Elaborar el ciclo de auditoría y los planes anuales de auditoría que lo conforman.
2. Evaluar el cumplimiento de las políticas, planes y procedimientos determinados por la autoridad superior.
3. Tomar conocimiento en forma integral de los actos administrativos, evaluando aquellos de significativa trascendencia económica.
4. Verificar el cumplimiento de los niveles presupuestarios de la normativa legal vigente.
5. Constatar la confiabilidad de los antecedentes utilizados en la elaboración de los informes de Auditoría.
6. Comunicar a la autoridad superior y a la SINDICATURA GENERAL DE LA NACION los resultados de los informes practicados y de las sugerencias o recomendaciones que se efectúen.
7. Efectuar el seguimiento de las recomendaciones u observaciones realizadas.
8. Informar a la SINDICATURA GENERAL DE LA NACION sobre temas que sean requeridos en lo atinente al desarrollo de actividades de la Unidad de Auditoría Interna.
9. Evaluar los cambios que se produzcan en el esquema presupuestario del Organismo y su incidencia en la formulación de planes.
10. Apreciar el comportamiento técnico-profesional en el desarrollo de las acciones de la Unidad, evaluando los rendimientos individuales y los resultados por programas.
INSTITUTO NACIONAL DE MEDICAMENTOS
RESPONSABILIDAD PRIMARIA:
Registrar y controlar las drogas, medicamentos, reactivos y elementos de diagnóstico, cosméticos y otros productos de uso y aplicación en medicina humana mediante estudios farmacotécnicos, biológicos, farmacológicos básicos y toxicólogos, como así también de las actividades, procesos y tecnologías que se realicen en función de la elaboración, fraccionamiento, importación y/o exportación, depósito y comercialización de dichos productos, a fin de asegurar a la población el consumo y uso de elementos de calidad comprobada.
ACCIONES:
1. Realizar los análisis y estudios destinados a controlar la composición, calidad, eficacia e inocuidad de drogas, medicamentos, productos para diagnóstico y otros productos usados en medicina humana.
2. Establecer normativas y especificaciones técnicas que deban reunir las drogas, medicamentos, cosméticos y productos usados en medicina humana.
3. Armonizar las metodologías de validación para facilitar la aceptación y reconocimiento de las mismas en todo el país tanto por la industria como por parte de los organismos de control.
4. Asesorar en los aspectos de su competencia a personal y/o instituciones públicas y/o privadas.
5. Entender, en el ámbito de su competencia, en los trámites de evaluación de solicitudes de inscripción en el registro, modificación y reinscripción de especialidades medicinales en cumplimiento de la Ley N° 16.463, decretos y disposiciones reglamentarias y modificatorios.
6. Fiscalizar los establecimientos dedicados a la elaboración, importación, fraccionamiento y/o comercialización de productos de su competencia.
7. Vigilar la legitimidad de los productos que se comercializan y son competencia de este organismo, a través del Programa de Pesquisa de Medicamentos Ilegítimos.
8. Entender en las acciones relacionadas con la elaboración, importación y/o exportación, fraccionamiento, comercialización y dispensación de psicotrópicos y estupefacientes.
9. Establecer y organizar la redacción, revisión y actualización permanente de la farmacopea argentina.
INSTITUTO NACIONAL DE ALIMENTOS
RESPONSABILIDAD PRIMARIA:
Registrar y controlar en el ámbito de competencia de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA los alimentos acondicionados incluyendo sus insumos, los productos de uso doméstico y los materiales en contacto con los alimentos, como así también las actividades, procesos y tecnologías, detectando los efectos adversos derivados de su consumo o utilización, como la presencia en los mismos de residuos o substancias nocivas para la salud humana.
ACCIONES:
1. Promover la salud de la población, asegurando la inocuidad de los productos alimenticios, insumos, los materiales en contacto directo con los alimentos y los productos de uso doméstico.
2. Controlar y fiscalizar la sanidad y calidad de los alimentos acondicionados para su venta al público, de elaboración nacional o importados, destinados para ser consumidos en el mercado interno y/o externo de acuerdo a la normativa vigente.
3. Controlar y fiscalizar los establecimientos que elaboren, fraccionen y almacenen productos alimenticios destinados al consumo humano.
4. Controlar y fiscalizar la distribución, el transporte y la comercialización de los productos alimenticios destinados al consumo humano.
5. Evaluar y gestionar las solicitudes de autorización de alimentos, insumos específicos, aditivos, colorantes, materiales en contacto con los alimentos, productos de uso domestico y de los establecimientos que los elaboran, fraccionan y almacenan.
6. Otorgar y cancelar las autorizaciones de importación y exportación de alimentos, insumos, aditivos específicos, colorantes, materiales en contacto con alimentos y productos de uso doméstico.
7. Coordinar con las autoridades provinciales, municipales y del Gobierno de la CIUDAD AUTONOMA DE BUENOS AIRES, las acciones necesarias para el mejor cumplimiento del Código Alimentario Argentino.
8. Promover normas nacionales e internacionales referidas a la legislación alimentaria para su estudio, armonización y adecuación a los efectos de ser incorporadas al Código Alimentario Argentino.
9. Promover la realización de estudios comparativos de nuevas metodologías técnicas para ser probadas y adecuadas para su posterior incorporación a la metodología analítica oficial.
10. Diseñar, proponer y ejecutar acciones y programas de prevención y control para asegurar la inocuidad de los productos bajo su competencia, advirtiendo públicamente sobre la utilización y el consumo de los alimentos que puedan afectar la salud humana.
11. Formular y recibir denuncias sobre incumplimientos de las disposiciones establecidas en el Código Alimentario Argentino y aplicar las sanciones correspondientes de acuerdo a las normas vigentes.
12. Promover la implementación de programas y campañas tendientes a fiscalizar el cumplimiento del Código Alimentario Argentino y prevenir las Enfermedades Trasmitidas por los Alimentos, por sí o en coordinación con los demás organismos del MINISTERIO DE SALUD, las Autoridades Competentes provinciales o del Gobierno de la CIUDAD AUTONOMA DE BUENOS AIRES.
13. Mantener una efectiva red de comunicación e intercambio con las delegaciones del INSTITUTO NACIONAL DE ALIMENTOS y con los organismos provinciales y municipales competentes.
14. Brindar cooperación técnica-administrativa a los organismos provinciales y municipales relacionados con la calidad y el control de los alimentos.
DIRECCION DE TECNOLOGIA MEDICA
RESPONSABILIDAD PRIMARIA:
Controlar, fiscalizar y vigilar la calidad de los productos médicos como así también las actividades, procesos y tecnologías que se realicen en función de la elaboración, fraccionamiento, importación y/o exportación y depósito de dichos productos a fin de asegurar a la población la utilización de productos médicos de comprobada calidad, eficacia y seguridad.
ACCIONES:
1. Elaborar y proponer normas técnicas relativas a la elaboración, importación y/o exportación y depósito de productos médicos.
2. Proponer y organizar, en función de la normativa aplicable, la creación de registros y otros procedimientos que se consideren necesarios, reglamentando e instrumentando su funcionamiento.
3. Adoptar, ante la detección de cualquier factor de riesgo relacionado con la calidad, eficacia y seguridad de los productos médicos, las medidas más oportunas y adecuadas para proteger la salud de la población.
4. Fiscalizar los establecimientos dedicados a la elaboración, importación, fraccionamiento y/o comercialización de productos de su competencia.
5. Fiscalizar adecuada y razonablemente el cumplimiento de las normas relacionadas con la calidad, eficacia y seguridad de los productos médicos.
6. Armonizar las metodologías de validación para facilitar la aceptación y reconocimiento de las mismas en todo el país tanto por la industria como por parte de los organismos de control.
7. Asesorar en los aspectos de su competencia a personal y/o instituciones públicas y/o privadas.
8. Generar y fiscalizar un sistema de laboratorios idóneos y confiables con capacidad para realizar análisis y estudios destinados a controlar la calidad, seguridad y eficacia de los productos médicos.
9. Participar mediante procesos apropiados con representantes de otros países en la armonización de requerimientos regulatorios para los productos médicos y promover los procesos de reconocimiento mutuo.
DIRECCION DE EVALUACION DE MEDICAMENTOS
RESPONSABILIDAD PRIMARIA:
Realizar las acciones tendientes a la evaluación clínica de los medicamentos en el trámite de inscripción en el registro y en la post comercialización.
ACCIONES:
1. Entender, en el ámbito de su competencia, en los trámites de evaluación de solicitudes de inscripción en el registro, modificación y reinscripción de especialidades medicinales en cumplimiento de la Ley N° 16.463, decretos y disposiciones reglamentarias y modificatorias.
2. Entender en la autorización de realización de ensayos clínicos y de bioequivalencia en el país.
3. Proponer textos de prospectos normatizados de acuerdo a la información nacional e internacional disponible.
4. Entender en la asignación de la condición de venta de medicamentos de acuerdo a la normativa vigente y a criterios internacionalmente aceptados.
5. Entender en la aprobación, ampliación y restricción de las indicaciones terapéuticas de los principios activos.
6. Entender en las actividades de farmacovigilancia realizando la recopilación, el análisis y el registro de los efectos indeseables que aparezcan durante la etapa de comercialización de los medicamentos, drogas, cosméticos y todo otro producto de aplicación en medicina humana.
7. Proponer en función de la normativa aplicable la creación de registros y otros dispositivos y procedimientos que se consideren necesarios, reglamentando, instrumentando y operativizando su funcionamiento.
8. Entender en la importación y exportación de medicamentos exentos de la obligatoriedad de inscripción en el registro de acuerdo a lo establecido en el Decreto N° 150 del 20 de enero de 1992.
9. Mantener actualizada la información referida al listado nacional de medicamentos, como asimismo las altas y bajas que se produzcan, conforme lo indiquen las áreas competentes de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
DIRECCION DE PLANIFICACION Y RELACIONES INSTITUCIONALES
RESPONSABILIDAD PRIMARIA:
Entender en la propuesta y coordinación de los programas transversales de la Organización, como así también en la evaluación de los mismos diseñando y proponiendo mecanismos de comunicación y difusión tendientes a mantener informada a la población acerca del quehacer del Organismo.
ACCIONES:
1. Proponer y comunicar una vez aprobados, los lineamientos para la formulación de los programas transversales del Organismo.
2. Coordinar el diseño y evaluación de los mismos compatibilizando las propuestas de las distintas áreas e informando a las autoridades del Organismo, los resultados obtenidos y las acciones en ejecución.
3. Definir, implementar y promover estrategias y acuerdos que permitan desarrollar programas de investigación, capacitación, docencia y promoción comunitaria para optimizar las acciones de ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
4. Diseñar, proponer y generar convenios con instituciones públicas y privadas implementando sistemas y programas que propendan a la optimización de las acciones para el mejor cumplimiento de los objetivos de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, contemplando mecanismos que posibiliten la organización, ejecución y fiscalización de los mismos.
5. Establecer acuerdos con entidades de distintos niveles y ámbitos para fortalecer la capacidad de control de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
6. Establecer vínculos con organizaciones intermedias, públicas o privadas, de reconocido prestigio y representativas de la comunidad, a fin de conocer sus necesidades y expectativas tendiente a una cultura de prevención que minimice las acciones correctivas.
7. Establecer un fluido intercambio de información con entidades similares, nacionales o extranjeras, y organismos multilaterales vinculados con el área.
8. Implementar programas de divulgación de las acciones de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, dirigidos a la población en general y a sectores especiales que se definan como de interés particular.
9. Definir contenidos y pautas generales para la difusión de temas de salud vinculados con medicamentos, alimentos y tecnología médica.
10. Difundir la información pertinente a los cambios de legislación que ocurran respecto a los temas que competen a la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
11. Definir, proponer y generar estudios de evaluación económica de medicamentos y de tecnologías aplicados a la salud.
DIRECCION DE COORDINACION Y ADMINISTRACION
RESPONSABILIDAD PRIMARIA:
Efectuar la gestión económico-financiera, contable, patrimonial y de servicios del Organismo, como así también las cuestiones relativas a la administración de los recursos humanos y organizacionales.
ACCIONES:
1. Asistir a la Dirección Nacional con el diseño de la política presupuestaria del Organismo y en la evaluación de su cumplimiento.
2. Elaborar el Presupuesto Anual y el cálculo de recursos para su funcionamiento, como así también el Programa Anual de Actividades y Trabajos.
3. Efectuar las registraciones dispuestas por la Ley de Administración Financiera y de los Sistemas de Control del Sector Público Nacional N° 24.156.
4. Entender en la aplicación de los regímenes laborales pertinentes al personal del Organismo, selección, capacitación y evaluación del desempeño del personal, como así también la liquidación de sus remuneraciones y en los aspectos atinentes a la gestión organizacional.
5. Entender en la organización, registro y actualización de la información relacionada con los recursos humanos del Organismo.
6. Entender en la implementación y seguimiento de las políticas relativas a las Tecnologías de la Información, incluyendo la informática, las telecomunicaciones, la telefonía, las redes, los sistemas de información y las tecnologías asociadas, fijadas por la jurisdicción, conforme a las normas vigentes en la Administración Pública Nacional.
7. Compatibilizar, evaluar y llevar a cabo los distintos requerimientos de las dependencias del Organismo vinculados con la adquisición y contratación de bienes y servicios.
8. Coordinar y supervisar el cumplimiento del control y registración de los bienes patrimoniales del Organismo, su actualización y aplicación de las normativas que correspondan.
9. Coordinar el ingreso, egreso y archivo de la documentación administrativa, como así también la protocolización de los actos administrativos que emite la Dirección Nacional del Organismo.
DIRECCION DE ASUNTOS JURIDICOS
RESPONSABILIDAD PRIMARIA:
Entender en los asuntos relativos a la legislación general e instrumentación normativa en la que tiene competencia el Organismo, como así también en el perfeccionamiento de las disposiciones legales y reglamentarias, en el control de legitimidad y legalidad de los actos y procedimientos administrativos. Representar y asesorar jurídicamente a la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
ACCIONES:
1. Ejercer el control de la legalidad y legitimidad de los actos administrativos.
2. Representar a la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, en los juicios en que dicho organismo sea parte como actor o demandado por intermedio de los apoderados que designe al efecto con relación a los derechos y obligaciones de que pueda ser titular, pudiendo transigir, comprometer en árbitros, prorrogar jurisdicciones, desistir de apelaciones y renunciar a prescripciones adquiridas, contestar los oficios judiciales y remitirlos a los que deben intervenir en su diligenciamiento y realizar todos aquellos actos necesarios tendientes a iniciar, proseguir y concluir juicios.
3. Asesorar en forma permanente en los aspectos legales a las distintas áreas de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
4. Atender a las actividades derivadas de la presentación de recursos y denuncias administrativas.
5. Entender en la producción de normas jurídicas para el mejor desarrollo de las actividades sobre medicamentos, alimentos y tecnología médica.
6. Instruir los sumarios administrativos-disciplinarios y los sumarios por contravenciones a la legislación respecto de la cual la ADMINISTRACION NACIONAL DE MEDICAMENTOS. ALIMENTOS Y TECNOLOGIA MEDICA, es organismo de aplicación.
ANEXO III