ANEXO III
(Anexo sustituido por art. 9° de la Resolución N° 843/2025
del Servicio Nacional de Sanidad y Calidad Agroalimentaria B.O.
4/11/2025. Vigencia: a partir del día de su publicación en el Boletín
Oficial.)
REGISTRO DE PRODUCTOS FITOSANITARIOS
Los productos fitosanitarios que se elaboren o formulen en la REPÚBLICA
ARGENTINA o en otros países y no cuenten con el registro y la
aprobación de uso agrícola por Autoridades Competentes del listado de
países o grupos de países que se detallan en el Anexo IV deberán estar
aprobados y registrados en el Registro Nacional de Productos
Fitosanitarios, dependiente del SERVICIO NACIONAL DE SANIDAD Y CALIDAD
AGROALIMENTARIA (SENASA) cumpliendo con lo establecido en el presente
Anexo.
Los interesados que deseen registrar los productos deberán presentar un
formulario de solicitud de registro dependiendo del tipo de producto a
registrar, a través de la plataforma SIG-Trámites o la que en el futuro
la reemplace, y la documentación correspondiente según el tipo de
producto.
El SENASA procederá a evaluar la información presentada y expedirse en un plazo no mayor a CIENTO OCHENTA (180) días hábiles.
A los efectos de la presente norma los productos a registrar estarán
encuadrados en DOS (2) categorías dependiendo del tipo de producto a
registrar:
SUSTANCIAS ACTIVAS: se entiende por sustancia activa al componente
principal de un producto fitosanitario que tiene la capacidad de
ejercer un efecto biológico. Esta puede ser grado técnico nueva o
equivalente.
SUSTANCIAS ACTIVAS NUEVAS: se considera sustancia activa grado técnico nueva a la que no ha sido registrada en el país.
En los casos en que se desee registrar este tipo de sustancias se
deberá proceder al registro completo detallado en los apartados I a VI.
SUSTANCIAS ACTIVAS EQUIVALENTES: se considera sustancia activa
equivalente cuando su equivalencia ha sido demostrada respecto de otras
ya registradas en el país.
Las sustancias activas de diferentes fabricantes o de diferentes procesos de síntesis del mismo fabricante son equivalentes si:
- La sustancia activa tiene una concentración declarada mayor o igual a la de la referencia.
- El máximo nivel de impurezas no relevantes no se incrementa por más
del CINCUENTA POR CIENTO (50 %) (relativo al máximo nivel en la
referencia), o el nivel absoluto no se incrementa en más del CERO COMA
TRES POR CIENTO PESO EN PESO (0,3 %p/p), considerando el que represente
el mayor nivel de incremento.
- No se presentan nuevas impurezas mayores a CERO COMA UNO POR CIENTO PESO EN PESO (0,1 %p/p).
- No se encuentran impurezas relevantes por encima de los límites
establecidos en la Resolución N° 481 del 27 de octubre de 2014 del
citado Servicio Nacional y sus modificatorias, o en las
especificaciones de la Organización de las Naciones Unidas para la
Alimentación y la Agricultura (FAO).
En los casos en que se desee registrar este tipo de sustancias activas
equivalentes, se deberán cumplimentar los apartados detallados en los
puntos I a III.
PRODUCTO FORMULADO: se entiende por producto formulado a la mezcla de
sustancias activas y otras sustancias, que cumple la función de
proteger a las plantas contra plagas, enfermedades y malezas.
Los coadyuvantes incluidos como componentes de una formulación no serán
pasibles de registro, pero deberán usarse para la elaboración o
fabricación de productos fitosanitarios aquellos que no se encuentren
alcanzados en la Resolución N° RESOL-2019-32-APN-PRES#SENASA del 17 de
enero de 2019 del mencionado Servicio Nacional, o la que en un futuro
la reemplace.
A fin de realizar la inscripción de fitosanitarios al registro, los
requerimientos para las diferentes categorías son los siguientes:
A - SUSTANCIAS ACTIVAS
I - INFORMACIÓN ADMINISTRATIVA
Formulario de solicitud de registro, dependiendo del tipo de producto a
registrar, firmado por el Apoderado o Representante Legal y el
Responsable Técnico con incumbencia profesional en la materia.
Patrones: en caso de que el SENASA así lo requiera para control, la
empresa registrante deberá aportar los patrones analíticos de la
sustancia activa e impurezas, en las condiciones que establezca la
Dirección General de Laboratorios y Control Técnico (DGLCyT) del SENASA.
Hoja de Datos de Seguridad: de acuerdo con la versión del Manual de las
Naciones Unidas del Sistema Globalmente Armonizado de Clasificación y
Etiquetado de Productos Químicos (SGA), adoptada en la presente norma.
Informes técnicos de análisis de riesgo toxicológico y ecotoxicológico
de nuevos principios activos de uso agrícola, firmados por los equipos
interdisciplinarios de profesionales independientes especializados en
toxicología y ecotoxicología del SENASA.
Si se desea registrar una sustancia activa grado técnico equivalente
que se produzca en el país o que se importe desde países no incluidos
en el Anexo IV, para acreditar dicha equivalencia se deberá presentar
ante el SENASA el formulario de solicitud de registro, junto con toda
la documentación técnica y administrativa requerida.
II - GENERALIDADES
Protocolos y estudios de Productos Fitosanitarios
Los estudios biológicos para la producción de datos toxicológicos y
ecotoxicológicos y los laboratorios que realicen propiedades físicas y
químicas, y determinaciones analíticas de residuos de principios
activos en matrices vegetales y ambientales con fines de registro,
revalidación, revaluación o monitoreo de productos fitosanitarios,
deberán incluir la documentación respaldatoria correspondiente al
monitoreo de Buenas Prácticas de Laboratorio (BPL), desarrolladas por
la Organización para la Cooperación y el Desarrollo Económico (OCDE),
emitida por un Organismo de Acreditación de reconocimiento
internacional. Asimismo, los ensayos de residuos de principios activos
deberán encuadrarse en la Directiva OCDE sobre aplicación de las BPL
para los estudios de campo.
Los protocolos de los estudios biológicos para la producción de datos
toxicológicos y de propiedades físicas y químicas y las determinaciones
analíticas de residuos de principios activos deben realizarse mediante
los protocolos correspondientes a los organismos y cuerpos normativos
que protocolizan ensayos y procedimientos de laboratorio para la
obtención de datos con fines de registro, a saber:
APVMA: AUSTRALIAN PESTICIDES AND VETERINARY MEDICINES AUTHORITY
• CIPAC: COLLABORATIVE INTERNATIONAL PESTICIDES ANALYTICAL COUNCIL
• EEC/EU: EUROPEAN ECONOMIC COMMUNITY/EUROPEAN UNION
• EFSA: EUROPEAN FOOD SAFETY AUTHORITY
• EPA: UNITED STATES ENVIRONMENTAL PROTECTION AGENCY
• EURACHEM: EUROPEAN COLLABORATION ON CHEMICAL MEASUREMENT
• FDA: UNITED STATES FOOD AND DRUG ADMINISTRATION
• FFDCA: FEDERAL FOOD DRUG AND COSMETIC ACT
• FIFRA: FEDERAL INSECTICIDE, FUNGICIDE AND RODENTICIDE ACT
• ISO: INTERNATIONAL STANDARD ORGANIZATION
• IUPAC: INTERNATIONAL UNION OF PURE AND APPLIED CHEMISTRY
• OECD: ORGANIZATION FOR ECONOMIC COOPERATION AND DEVELOPMENT
• OMS: WORLD HEALTH ORGANIZATION
• OPPTS: OFFICE OF PREVENTION, PESTICIDES AND TOXIC SUBSTANCES
Otros protocolos provenientes de organismos o cuerpos normativos
diferentes a los que figuran en el presente Manual deberán ser
consultados previamente al SENASA.
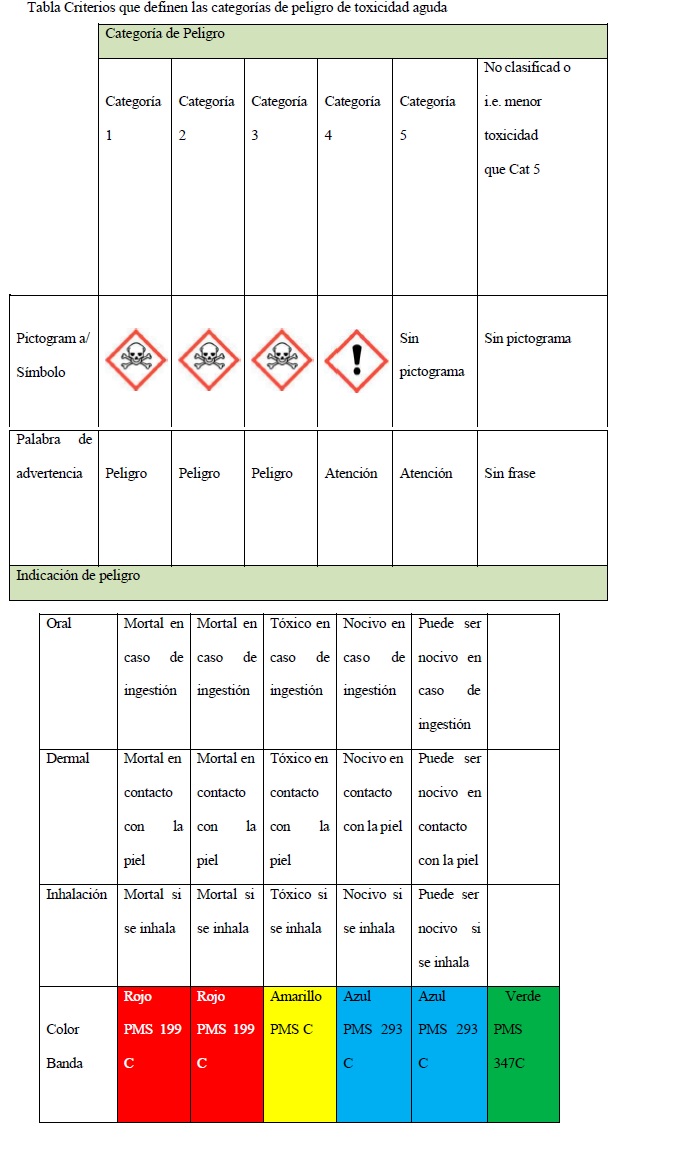
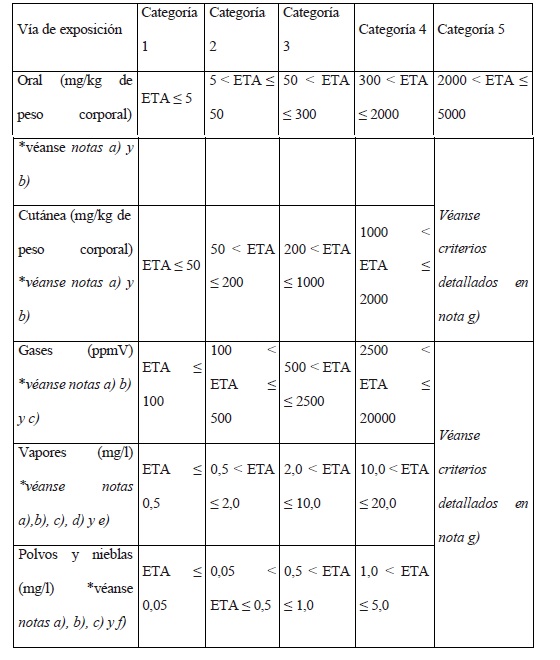
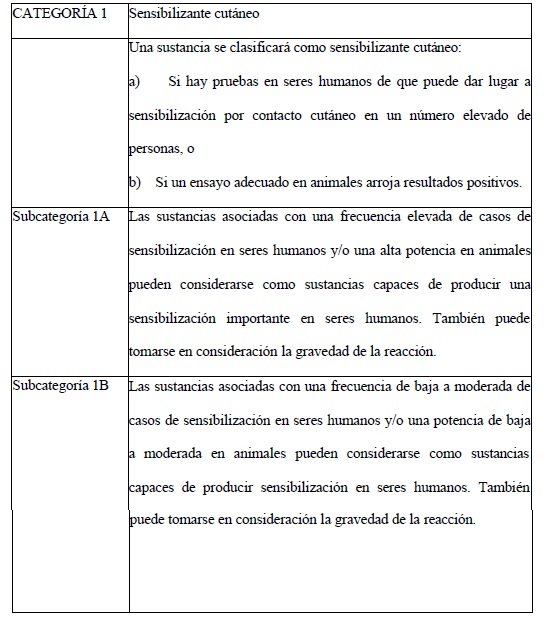
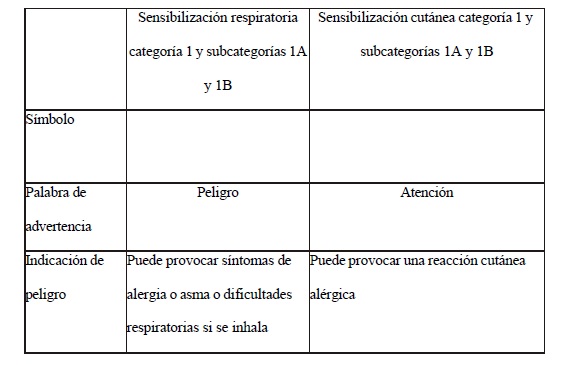
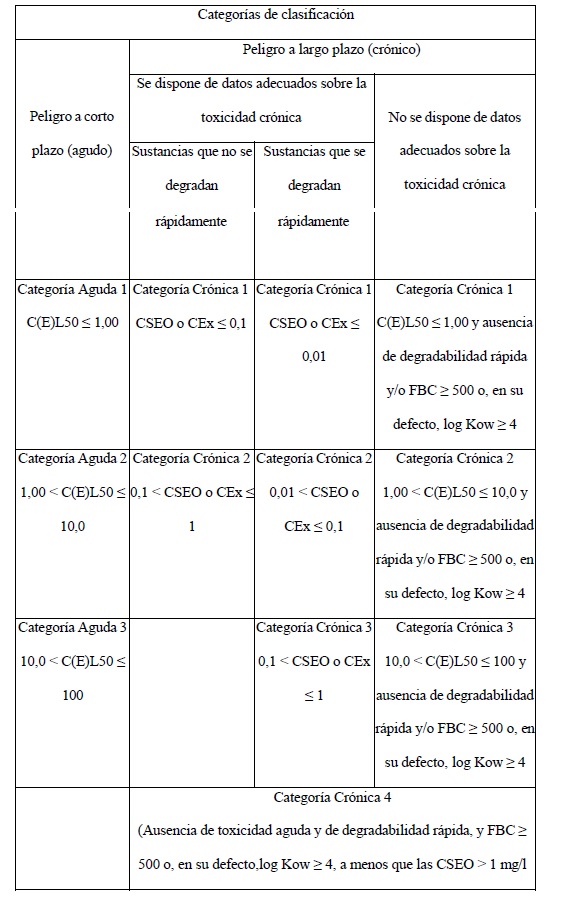
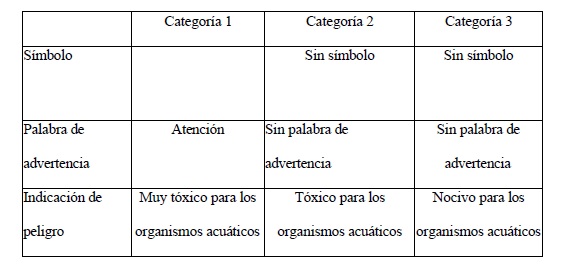
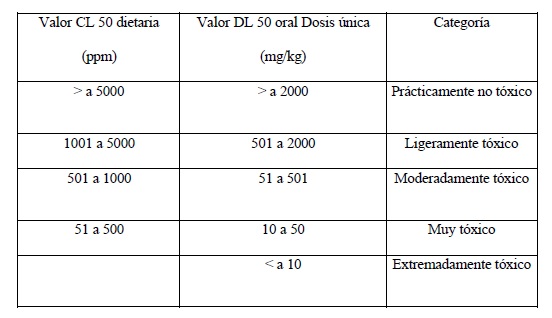
Clasificación toxicológica
Se adoptará como clasificación toxicológica la del Sistema Globalmente
Armonizado de Clasificación y Etiquetado de Productos Químicos
(SGA/GHS), utilizando para tal fin la información sobre toxicología en
mamíferos y no mamíferos de la sustancia activa o del producto
formulado, según corresponda.
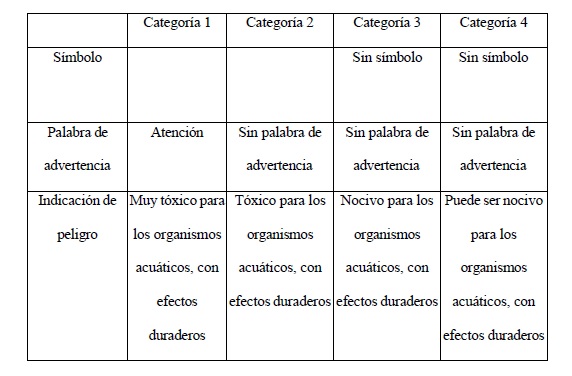
A los fines de comunicar el peligro en los marbetes de productos
fitosanitarios y las hojas de datos de seguridad de estos, se deberá
proceder de acuerdo con los criterios definidos en la Versión
ST/SG/AC.10/30/Rev.9 del Manual de las Naciones Unidas del Sistema
Globalmente Armonizado de Clasificación y Etiquetado de Productos
Químicos (SGA), y en función de la normativa de etiquetado de productos
fitosanitarios vigente en la REPÚBLICA ARGENTINA, versión revisable al
efecto del presente manual cada CINCO (5) años.
Accesibilidad de la información de registro
La información confidencial y los datos de pruebas serán provistos por
el registrante, distinguiendo claramente entre qué es información
confidencial y qué son datos de pruebas, considerando: Información
confidencial: la información correspondiente a la identidad,
composición, proceso de síntesis, proceso de formulación y otros
secretos industriales y comerciales.
Datos de pruebas: datos de ensayos toxicológicos, ecotoxicológicos, de residuos y propiedades físicas y químicas.
Respecto a la información confidencial o a los datos no divulgados
requeridos para su evaluación, el SENASA tomará las medidas necesarias
para su salvaguarda contra todo uso comercial deshonesto y evitar que
dicha información sea revelada o transferida. A tales efectos, el
SENASA se encargará de proveer las instalaciones y los medios
necesarios para garantizar la seguridad y una adecuada gestión de la
información.
A tal fin, la información confidencial y los datos no publicados
recibidos serán resguardados informáticamente en los sistemas que
disponga especialmente el SENASA, y será proporcionada a los técnicos
evaluadores a tal fin, no pudiendo estos efectuar copias ni totales ni
parciales, ni compartir dicha información o darla a conocer a terceros.
Los técnicos evaluadores (funcionarios internos o auxiliares) dejarán
constancia escrita de que aceptan las condiciones de confidencialidad
en que deberán manejar el material informativo que se les provea, bajo
declaración jurada.
Concluida la evaluación, la información confidencial y los datos no
publicados serán resguardados siguiendo las medidas de seguridad
dispuestas. El SENASA podrá disponer su entrega al administrado para
que éste los tenga en guarda. En este último caso, la información
confidencial y los datos no publicados deben estar disponibles en el
caso que el SENASA lo solicite.
La información confidencial de las sustancias activas grado técnico
consideradas de referencia para la determinación de equivalencia quedan
en guarda del SENASA y no están alcanzadas por lo dispuesto en el
párrafo previo respecto de su entrega al administrado.
Cuando los datos de ensayos y pruebas sobre seguridad y eficacia,
resguardados en el Organismo, hubieran caído en el dominio público en
cualquier país por la publicación de cualquiera de los datos
protegidos, la presentación de todos o parte de estos datos en medios
científicos o académicos o por cualquier otro medio de publicación,
entonces estos dejarán de ser archivados mediante las medidas de
seguridad dispuestas por el SENASA.
Los expedientes técnicos de registro son reservados de acuerdo con el
marco previsto en el Artículo 38 del Decreto N° 1.759 del 3 de abril de
1972, sus modificatorios y complementarios. Su vista queda reservada al
personal y los auxiliares de este Servicio Nacional afectados al
procedimiento de registro, y a las personas fehacientemente autorizadas
por el administrado titular del registro.
El SENASA utilizará la información suministrada del modo antes descrito
a los efectos de los registros de productos fitosanitarios, observando
el marco legal que impone la Ley N° 24.766 y normas complementarias.
Quedan expresamente exceptuados de la confidencialidad:
a) Nombre, contenido y origen de principios activos en productos
formulados, establecimientos elaboradores y empresas registrantes.
b) Métodos y recomendaciones de transporte, almacenaje, tratamientos de incendio y otros riesgos.
c) Medios de disposición de envases.
d) Procedimientos de descontaminación.
e) Primeros auxilios y ayuda médica en caso de daño a las personas.
f) Método de análisis de residuos.
g) Método de análisis de las impurezas de importancia toxicológica o ecotoxicológica (denominadas de declaración obligatoria).
h) La información contenida en la Hoja de Datos de Seguridad.
i) Toda información que haya caído en el dominio público.
Quienes requieran la información referida en los incisos f) y g),
deberán hacerlo mediante nota, expresando el motivo del requerimiento,
la que será registrada y archivada.
El personal afectado a los procedimientos de registro de productos
fitosanitarios se encuentra comprendido en los mandatos de los
Artículos 3°, 12 y 13 de la Ley N° 24.766, por lo que deberá abstenerse
de usar y de revelar sin causa justificada o sin consentimiento del
registrante la información en cuestión, bajo apercibimiento de las
sanciones que la misma norma prevé.
III - INFORMACIÓN CONFIDENCIAL (tanto para sustancias activas nuevas, como equivalentes)
a.-
Certificado de Origen, el cual debe ser original y emitido por el establecimiento elaborador.
Debe incluir:
Identificación de la sustancia activa.
Contenido mínimo declarado porcentaje PESO EN PESO (p/p).
Nombre y localización del establecimiento elaborador.
Clave o número con el que la Autoridad Competente del país de origen identifica al establecimiento.
Nombre y dirección de la empresa que registrará el producto ante
SENASA. En caso de que no figure esta información se deberá remitir una
nota emitida por el establecimiento elaborador donde conste la
autorización para realizar el registro del producto en el país.
b -
Declaración de composición cuali-cuantitativa firmada por el establecimiento elaborador o por la empresa registrante con carácter de declaración jurada.
Debe incluir:
Nombre químico según criterios internacionales [Unión Internacional de
Química Pura y Aplicada (IUPAC) o Chemical Abstract Service (CAS)] y
número CAS (cuando esté disponible) de la sustancia activa y sus
impurezas asociadas.
Concentración mínima de la sustancia activa.
Concentración máxima de cada impureza mayor o igual a CERO COMA UNO POR CIENTO PESO EN PESO (0,1 %p/p).
Concentración máxima de impurezas relevantes: el límite establecido por
la normativa vigente y de no existir, el límite de detección del método
utilizado.
La fracción no identificada de la sustancia activa no podrá superar el
DOS POR CIENTO (2 %) por lote y deberá componerse solo de impurezas con
concentración inferior al CERO COMA UNO POR CIENTO PESO EN PESO (0,1
%p/p), excluyendo impurezas relevantes.
La concentración declarada se basará en el análisis de muestras
representativas de al menos CINCO (5) lotes de síntesis, asegurando que
en todos los casos la concentración obtenida sea igual o superior al
límite inferior establecido.
La concentración mínima de sustancia activa se determinará mediante un
análisis estadístico, por ejemplo, la media menos TRES (3) desvíos
estándar. Si el valor declarado es inferior, deberá justificarse el
criterio estadístico o la razón para su reducción.
La concentración máxima de impurezas se obtendrá con un análisis
similar, tomando la media más TRES (3) desvíos estándar. Si el valor
declarado es superior, deberá explicarse el criterio utilizado o la
justificación del aumento.
c -
Estudio y cuantificación en CINCO (5) lotes
Debe presentarse un estudio completo de al menos CINCO (5) lotes de
síntesis independientes, realizado por un laboratorio conforme a las
Buenas Prácticas de Laboratorio (BPL), debidamente firmado y fechado.
Si los sponsors del estudio no coinciden con la empresa registrante,
deberá incluirse una autorización para el uso de la información.
El reporte debe contener:
Índice de contenidos.
Nombre y localización del establecimiento elaborador.
Cuadro resumen de resultados.
Métodos de análisis con todas las ecuaciones necesarias para reproducir los cálculos.
Resultados, incluyendo cromatogramas representativos de cada lote, del blanco y de los patrones analíticos.
En caso de usar curvas de calibración, los gráficos con títulos, ejes (con magnitudes y unidades) y ecuación de la recta.
Datos en formato de cuadro para reproducir cálculos, dentro del informe
o como anexo. Cromatogramas con encabezado (fecha, hora, descripción) y
reporte (áreas y tiempos de retención). Certificados de análisis de los
patrones utilizados.
Certificados de análisis de los lotes analizados, emitidos y firmados
por el fabricante, incluyendo nombre y dirección del establecimiento
elaborador, fecha de elaboración y vencimiento. Si la dirección no
figura en el certificado, deberá presentarse una declaración jurada con
dicha información.
Certificado BPL del Laboratorio.
Además, el análisis de impurezas debe realizarse en los mismos lotes de síntesis, incorporando:
Un
screening con detector
universal para visualizar impurezas en concentraciones menores a CERO
COMA UNO POR CIENTO PESO EN PESO (0,1 % p/p), ajustado a la impureza
significativa de menor concentración.
Certificados de estándares con reporte de cuantificación e
identificación. En caso de patrones secundarios, cuantificación contra
el patrón primario y su certificado de análisis. Si se utilizan
patrones de sustancias análogas, deberá presentarse una justificación
técnica demostrando la analogía molecular.
d -
Análisis de identidad de la sustancia activa e impurezas
La identidad de la sustancia activa deberá confirmarse mediante
determinaciones analíticas que permitan establecer fehacientemente su
estructura química y, si corresponde, su configuración molecular. Para
uno de los CINCO (5) lotes analizados, se presentarán al menos DOS (2)
espectros entre: Espectroscopía Infrarroja (IR), Resonancia Magnética
Nuclear (RMN) y Espectrometría de Masas (MS). Se incluirá una discusión
clara y concisa sobre la interpretación de los espectros, demostrando
la identidad de la sustancia activa en grado técnico o comparándolos
con los espectros del estándar analítico.
Asimismo, la identidad de todas las impurezas, o de grupos de impurezas
relacionadas, deberá ser demostrada mediante análisis espectrométricos,
espectroscópicos y/o químicos que permitan identificarlas
inequívocamente. Cada impureza deberá estar identificada en al menos
UNO (1) de los CINCO (5) lotes analizados, presentando un espectro de
masa o, en caso de contar con patrones, una comparación de espectros
espectroscopia ultravioleta-visible (UV-vis) y tiempos de retención. Se
acompañará la información con explicaciones claras y concisas que
justifiquen la identificación de cada impureza o grupo de impurezas
relacionadas.
e -
Métodos de análisis
El registrante debe proveer los métodos analíticos utilizados para la
determinación, tanto de la sustancia activa como de las impurezas.
Deberán incluir la descripción completa y los parámetros de validación
respectivos (especificidad, linealidad, recuperación, precisión,
límites de detección y de cuantificación en el caso de las impurezas).
Además de lo especificado en los contenidos mínimos establecidos en el
ítem 3, el reporte debe incluir cromatogramas representativos
correspondientes a cada uno de los parámetros estudiados.
f-
Proceso de síntesis
Debe proveerse la siguiente información emitida y firmada por el fabricante o la empresa registrante:
Nombre y localización del establecimiento elaborador que interviene en el proceso.
Caracterización general del proceso: deberá consistir en una
descripción completa y detallada de cada una de las etapas que
constituyen el proceso, incluyendo en forma explícita las reacciones
químicas que tienen lugar en cada una de ellas y sus condiciones de
presión y temperatura. Cuando corresponda, incluir otros parámetros
controlados [por ejemplo, potencial de hidrógeno (pH), humedad,
etcétera]. Detallar los criterios usados para dar por finalizada cada
etapa de reacción.
Diagrama de flujo.
Identificación de todos los reactivos usados en el proceso, con las especificaciones requeridas.
Descripción de los equipos usados y sus características.
g.-
Justificación de la presencia de impurezas
El fabricante deberá suministrar la explicación pertinente sobre el
origen y la formación de las impurezas que pueden estar presentes en el
producto final, especificando la estructura molecular y el nombre
químico para cada una de ellas. Debe indicar las reacciones químicas
que describen su formación, las que deben estar sustentadas en
mecanismos reconocidos y probados, y compatibles con las reacciones que
constituyen el proceso de síntesis.
Si el SENASA considera que una impureza declarada, o que sea probable
que esté presente en el grado técnico puede ser considerada relevante,
deberá solicitar a la empresa registrante que remita la discusión que
fundamente su condición así como la concentración en que puede
encontrarse.
En caso de que el sistema de vigilancia post registro de activos
demuestre inconsistencias entre la información declarada y los análisis
efectuados por la Dirección de Agroquímicos y Biológicos (DAyB) en las
muestras oficiales, el SENASA se reserva el derecho de solicitar
documentación adicional o dar de baja el registro.
h
Sobre los efectos tóxicos en especies mamíferas (solo para sustancias activas equivalentes)
Si la evaluación de equivalencia química determina la presencia de
nuevas impurezas relevantes o impurezas excedidas respecto a la
referencia, el registrante deberá justificar dichas impurezas conforme
a los procedimientos establecidos y presentar un test de mutagénesis
junto con un informe toxicológico. Este deberá demostrar que los
efectos subcrónicos y/o crónicos no son significativamente superiores a
los de la sustancia parental, pudiendo basarse en estudios de
relaciones cuantitativas estructura-actividad (QSAR) en DOS (2)
parámetros toxicológicos crónicos relevantes.
Para evaluar los posibles efectos dañinos que deben consignarse en la
etiqueta elemental del grado técnico y en la Hoja de Datos de
Seguridad, se tomará como referencia la información de la sustancia
parental una vez establecida la equivalencia, en concordancia con la
versión adoptada por la Autoridad Competente del Sistema Globalmente
Armonizado de Clasificación y Etiquetado de Productos Químicos (SGA) de
las Naciones Unidas.
IV - CUERPO TÉCNICO
SOBRE LAS PROPIEDADES FÍSICAS Y QUÍMICAS:
Aspecto
Estado físico
Color
Densidad
Presión de vapor
Solubilidad en agua
Solubilidad en disolventes orgánicos
Punto de inflamación
Propiedades oxidantes
Potencial de hidrógeno (pH), si la sustancia activa grado técnico es soluble o dispersable en agua.
Para el caso de sustancias activas grado técnico equivalentes, el cuerpo técnico debe incluir también la siguiente información:
SOBRE LA IDENTIDAD:
Fabricante.
Nombre común: aceptado por la Organización Internacional de Estandarización (ISO), o equivalente (si está disponible).
Nombre químico: aceptado o propuesto por IUPAC o CAS (si está disponible).
Número CAS, CIPAC y/o número de código experimental.
Fórmula empírica, peso molecular.
Fórmula estructural.
Grupo químico.
Concentración de sustancia activa.
SOBRE LOS ASPECTOS RELACIONADOS A SU USO.
1. Organismos nocivos controlados.
2. Modo de acción sobre los organismos nocivos y sobre las plantas.
3. Ámbito de aplicación previsto.
4. Condiciones fitosanitarias y ambientales para ser usado.
SOBRE LOS MÉTODOS ANALÍTICOS (para la determinación de residuos en
cultivos tratados, subproductos de origen vegetal, alimentos
procesados, suelo y agua)
Se incluirá la tasa de recuperación y los límites de sensibilidad metodológica.
Estos métodos serán requeridos si los usos propuestos para el producto requieren el establecimiento de una tolerancia.
Métodos analíticos para la determinación en el aire: Estos serán
requeridos para productos volátiles. Métodos analíticos para la
determinación en tejidos y fluidos animales o humanos: Estos métodos
serán requeridos cuando las plantas tratadas se destinen a la
alimentación animal.
V- RESIDUOS EN PRODUCTOS TRATADOS (ÚNICAMENTE REQUERIDO PARA SUSTANCIAS
ACTIVAS DE GRADO TÉCNICO NUEVAS y AMPLIACIONES DE NUEVO USO)
Los estudios serán requeridos si los usos propuestos exigen el
establecimiento de una tolerancia. El cálculo del Límite Máximo de
Residuos (LMR) se realizará utilizando la calculadora de la OCDE,
basada en los datos disponibles.
a. Metabolismo en Vegetales (para sustancias activas nuevas)
Debe identificarse la degradación y reacción de metabolitos en plantas
o productos tratados. Se requiere un estudio de metabolismo en un
cultivo representativo de cada categoría o grupo de cultivos para los
que se propone el uso, conforme a las Directrices de la OCDE u otras
reconocidas. Para extrapolar el metabolismo a todos los grupos, se
realizarán estudios en al menos TRES (3) de las CINCO (5) categorías de
cultivos; si los resultados son comparables, no serán necesarios
estudios adicionales.
b. Comportamiento de Residuos (para sustancias activas nuevas y
ampliaciones de uso en nuevos cultivos, incremento de dosis, reducción
del tiempo de carencia)
Para usos que requieran la fijación de tolerancias, se realizarán
ensayos de residuos en cultivos para establecer un LMR. Estos estudios
deberán cumplir con Buenas Prácticas de Laboratorio (BPL) en sus fases
analíticas y de campo. En caso de requerirse estudios locales, la fase
de campo deberá realizarse en la REPÚBLICA ARGENTINA con certificación
BPL.
Para aquellos usos que requieran la fijación de tolerancias, se
requerirán ensayos de residuos en cultivos a fin de establecer un
Límite Máximo de Residuos para el cultivo o grupo de cultivos para el
que se requiera autorizar el uso de la sustancia activa.
Los estudios de residuos de productos fitosanitarios deben ser
realizados por entidades que hayan certificado el cumplimiento de
Buenas Prácticas de Laboratorio (BPL), tanto en sus fases analíticas,
como de campo.
Para aquellos casos en los que se requiera
un número mínimo de estudios de residuos locales, la fase de campo deberá realizarse en el territorio Argentino por entidades que hayan certificado el cumplimiento de BPL.
El plan de ensayos deberá ajustarse a este Manual y los ensayos de
campo en Argentina deberán emplear variedades representativas en la
región evaluada. Para ensayos realizados en la misma campaña, los lotes
experimentales deben distanciarse al menos VEINTE (20) kilómetros y
tener un desfase de QUINCE (15) días.
Los ensayos deben respetar la práctica agrícola crítica indicada en la
etiqueta del producto formulado: dosis máxima, número de aplicaciones,
intervalo entre aplicaciones y período de carencia. Previa
justificación técnica, se aceptará una variación en más o en menos de
un VEINTICINCO POR CIENTO (±25 %) en un parámetro de la práctica
agrícola crítica y el criterio de proporcionalidad de la dosis máxima,
siguiendo directrices de la OCDE.
Cuando se requieran curvas de degradación, estas deberán incluir al
menos TRES (3) puntos y abarcar el período de carencia. Si el residuo
es menor al Límite de Cuantificación (LOQ), no será necesario realizar
curvas de degradación.
Los ensayos destinados a establecer un periodo de seguridad (usos en
postcosecha), no requerirán curvas de disipación, pero las muestras
deben tomarse dentro del período de seguridad propuesto. El producto
formulado utilizado en el ensayo debe caracterizarse bajo principios
BPL, con Certificado de Análisis incluido en el informe. Las muestras
deben analizarse en un máximo de TREINTA (30) días tras la recolección;
en caso contrario, deberá presentarse un estudio de estabilidad de la
molécula y sus metabolitos en una matriz representativa.
Productos exentos de fijación de LMR:
• Tratamiento de semillas y órganos de propagación no destinados al consumo.
• Aplicaciones en cultivos florales, ornamentales o áreas no cultivadas.
• Arbusticidas de acción tópica, preservadores de madera y hormiguicidas no aplicables al vegetal.
• Feromonas, atractivos, repelentes, rodenticidas y coadyuvantes.
• Biocontroladores
• Otros productos definidos con base técnica y científica.
c. Residuos en Cultivos Rotacionales (Nuevas sustancias activas - Condicionalmente Requeridos)
Si la sustancia activa se usa en cultivos anuales y sus metabolitos
persisten en el suelo, pueden exigirse estudios de metabolismo en
cultivos de rotación.
Si estos estudios indican residuos de la sustancia activa o metabolitos
MAYOR A CERO COMA CERO UN MILIGRAMOS POR KILOGRAMO (> 0,01 mg/kg) en
alimentos o MAYOR O IGUAL A CERO COMA CERO CINCO MILIGRAMOS POR
KILOGRAMO (
> 0,05 mg/kg) en forrajes, se seguirán directrices de la OCDE. Se aceptarán estudios realizados en otros países.
VI - EFECTOS TÓXICOS EN ESPECIES MAMÍFERAS. (ÚNICAMENTE REQUERIDO PARA SUSTANCIAS ACTIVAS DE GRADO TÉCNICO NUEVAS)
Se deberá aplicar un enfoque basado en toda la información disponible
(peso de la evidencia) para determinar si un estudio estándar, un
estudio con parámetros adicionales o un método alternativo al uso de
animales, permite evaluar adecuadamente el peligro para la salud humana
o justificar una exención de estudios específicos.
Los estudios deberán seguir las
Test Guidelines y Guidance Documents de la OCDE u otros reconocidos internacionalmente.
a - TOXICIDAD AGUDA
Se requerirá el estudio de toxicidad oral aguda (DL50 oral) en todos
los casos, excepto cuando la sustancia activa de grado técnico sea un
gas o altamente volátil.
El estudio de toxicidad cutánea aguda (DL50 cutánea) será obligatorio
al momento de la inscripción definitiva, salvo que el producto
formulado sea un gas, altamente volátil o corrosivo para la piel, o
presente un pH inferior a DOS (2) o superior a ONCE COMA CINCO (11,5).
El estudio de toxicidad aguda por inhalación (LC50 inhalación) será
requerido cuando la sustancia activa de grado técnico tenga una presión
de vapor superior a 10-2 Pa a 20 °C, sea un polvo con una proporción
significativa de partículas con diámetro menor a 50 p,m [más del UNO
POR CIENTO (1 %) en peso] o se incluya en productos en polvo o que se
apliquen por pulverización.
El estudio de irritación cutánea in vivo no deberá realizarse cuando la
sustancia activa de grado técnico sea un gas o altamente volátil, sea
corrosiva para la piel, presente un pH inferior a DOS (2) o superior a
ONCE COMA CINCO (11,5), cuente con información suficiente que permita
clasificarla como corrosiva para la piel o irritante ocular, o haya
sido clasificada como muy tóxica por vía dérmica.
El estudio de irritación ocular será obligatorio, salvo que la
sustancia activa de grado técnico sea corrosiva o severamente irritante
para la piel, presente un pH inferior a DOS (2) o superior a ONCE COMA
CINCO (11,5) o haya sido clasificada como muy tóxica por vía dérmica.
El estudio de sensibilización cutánea será requerido, excepto cuando la sustancia activa sea un sensibilizante conocido.
En cuanto a la mutagenicidad, será obligatorio realizar un estudio
in vitro
en el momento del registro experimental. Si la empresa registrante no
dispone de estudios toxicológicos in vivo, podrá presentar estudios
alternativos in vitro, in silico u otros métodos reconocidos por
autoridades regulatorias internacionales con convergencia normativa
entre la REPÚBLICA ARGENTINA, para el registro de productos
fitosanitarios. En estos casos, deberá solicitarse su aceptación
mediante una nota con una justificación técnico-científica del uso de
dichos estudios.
b - TOXICIDAD SUBCRÓNICA (corto plazo/medio plazo)
- Cuando esté disponible, se deberán comunicar los estudios de
toxicidad oral acumulativa con una duración de VEINTIOCHO (28) días.
- El estudio de toxicidad oral a corto plazo en roedores deberá
realizarse con una duración de NOVENTA (90) días, utilizando ratas como
especie de prueba, salvo que se justifique el uso de otra especie. Para
no roedores, se deberá presentar un estudio de toxicidad de NOVENTA
(90) días en perros. En ambos casos, deberán evaluarse el potencial
neurotóxico, los efectos inmunotóxicos, la genotoxicidad a través de la
formación de micronúcleos y los posibles efectos sobre el sistema
hormonal.
- El estudio de toxicidad inhalatoria con exposición repetida durante
VEINTIOCHO (28) o NOVENTA (90) días será requerido condicionalmente
para sustancias activas volátiles con una presión de vapor superior a
10“2 Pascales, cuando sea necesario para refinar
la evaluación del
riesgo ocupacional.
El estudio de toxicidad dérmica con administración repetida durante
VEINTIÚN (21), VEINTIOCHO (28) o NOVENTA (90) días será requerido
condicionalmente para el refinamiento de la evaluación del riesgo
ocupacional, en caso de que los estudios de toxicología aguda dérmica o
los valores por defecto de penetración dérmica no sean suficientes para
su determinación.
c - TOXICIDAD CRÓNICA A LARGO PLAZO Y CARCINOGENICIDAD.
Se requerirá un estudio de toxicidad oral a largo plazo y un estudio de
carcinogenicidad a largo plazo de la sustancia activa, utilizando ratas
como especie de prueba; cuando sea posible, estos estudios se
combinarán.
Las duraciones mínimas de estudio aceptables son:
Estudio de carcinogenicidad en ratones: 18 meses.
Estudio combinado toxicidad oral a largo plazo y carcinogenicidad en ratas: 12 - 24 meses.
Se requerirá un segundo estudio de carcinogenicidad de la sustancia
activa utilizando ratón como especie de ensayo, a menos que pueda
justificarse científicamente que no es necesario. En tales casos, se
pueden utilizar modelos alternativos de carcinogenicidad
validados científicamente.
Se deben remitir los datos experimentales, incluyendo la determinación
del posible mecanismo de carcinogenicidad implicado y su relevancia
para los seres humanos, cuando se considere que el modo de acción de la
carcinogenicidad no es genotóxico.
d.- MUTAGENICIDAD
Los estudios de mutagenicidad in vitro deberán realizarse según
corresponda, incluyendo al menos uno de los siguientes ensayos: ensayo
bacteriano para mutación genética, prueba combinada para aberraciones
cromosómicas estructurales y numéricas en células de mamífero, o prueba
de mutación genética en células de mamíferos.
Los estudios de mutagenicidad in vivo en células somáticas solo serán requeridos si al menos uno de los estudios
in vitro
arroja un resultado positivo. En tal caso, deberá realizarse al menos
un estudio in vivo que evalúe específicamente el efecto de
genotoxicidad identificado en los ensayos in vitro. Si se requiere un
estudio de micronúcleos in vivo, este podrá integrarse dentro de un
estudio de dosis repetida.
La necesidad de estudios in vivo en células germinales se evaluará caso
por caso, en función de los resultados obtenidos en células somáticas,
considerando la toxicocinética de la sustancia, su uso y la exposición
anticipada.
e - EFECTOS SOBRE LA REPRODUCCIÓN
Para evaluar los efectos sobre la reproducción, se recomienda la
realización de un estudio combinado de toxicidad reproductiva en ratas,
utilizando un estudio de dos generaciones o de una generación extendida
como protocolo base. Este estudio deberá incluir criterios adicionales
de valoración y evaluaciones funcionales en animales inmaduros.
Los estudios de toxicidad del desarrollo serán obligatorios y deberán realizarse en ratas y conejos por vía oral.
f - METABOLISMO EN MAMÍFEROS
Se deberán realizar estudios in vitro comparativos del metabolismo de
la sustancia activa entre
especies animales y humanos.
Los estudios in vivo en mamíferos deberán proporcionar información
sobre la cinética de la sustancia activa y sus metabolitos en especies
relevantes, considerando:
Una dosis oral única en niveles de dosis baja y alta.
Una dosis intravenosa o, si está disponible, una dosis oral única con evaluación de la excreción biliar en nivel de dosis baja.
Una dosis repetida.
Para el refinamiento de la evaluación de riesgo ocupacional, podrá
requerirse un estudio de penetración dérmica in vitro en piel humana a
fin de determinar la biodisponibilidad por vía dérmica.
Asimismo, deberá incluirse una descripción detallada de las rutas metabólicas de la sustancia activa y sus metabolitos.
g - ESTUDIOS DE NEUROTOXICIDAD EN ROEDORES
Los estudios serán condicionalmente requeridos a partir de un enfoque
basado en el peso de la evidencia, considerando que:
La sustancia causa efectos neurológicos en animales adultos (es decir,
signos clínicos de neurotoxicidad, neuropatología, alteraciones
funcionales o de comportamiento).
La sustancia causa efectos neurológicos en animales en desarrollo,
después de la exposición pre y posnatal (es decir, malformaciones del
sistema nervioso o neuropatía, cambios de peso cerebral en la
descendencia, alteraciones funcionales o de comportamiento en la
descendencia). la sustancia evoque un mecanismo que está asociado con
efectos adversos sobre el desarrollo del sistema nervioso, en
comparación con neurotóxicos conocidos, respuestas de neurorreceptores
o neurotransmisores alterados.
Se recomienda el uso de un enfoque combinado que utilice el estudio de
reproducción de DOS (2) generaciones en roedores o de UNA (1)
generación extendida, como protocolo básico para la evaluación de
efectos de neurotoxicidad y evaluaciones funcionales
en animales inmaduros.
h- OTROS ESTUDIOS TOXICOLÓGICOS
Cuando los metabolitos de la sustancia activa generados en plantas,
productos animales, suelo o agua subterránea difieran de aquellos
identificados en los estudios toxicológicos en animales, o se detecten
en bajas proporciones en estos últimos, se requerirán estudios
adicionales. La necesidad de estos estudios se evaluará caso por caso,
considerando la cantidad y la estructura química del metabolito en
relación con la sustancia parental.
En lo que respecta a la
Información Médica Obligatoria, se deberá presentar información sobre: Diagnóstico y síntomas de intoxicación.
Observaciones sobre sensibilización y alergización.
Efectos tóxicos de los metabolitos provenientes de vegetales tratados.
Información médica complementaria, cuando esté disponible.
Elaboración de una ficha médica definitiva.
i - INFORMACIÓN CON RESPECTO A LA SEGURIDAD
Se deberán establecer procedimientos específicos para la destrucción de
la sustancia activa y su descontaminación, así como la evaluación de
posibles métodos de recuperación, neutralización e incineración
controlada, indicando las condiciones en que debe realizarse.
Asimismo, deberá detallarse la depuración de aguas y los métodos
recomendados para la manipulación, almacenamiento, transporte y
respuesta ante incendios o derrames, incluyendo información sobre los
productos de reacción y gases de combustión generados en caso de
incendio. Finalmente, se deberá proporcionar información sobre los
equipos de protección individual adecuados para minimizar los riesgos
asociados a la exposición a la sustancia activa.
j.- EVALUACIÓN TOXICOLÓGICA
Para la identificación de peligros, deberá determinarse el Nivel de
Efecto Adverso No Observable (NOAEL) con base en los estudios más
representativos de los escenarios de uso del producto en Argentina,
tanto para la evaluación de riesgos ocupacionales como dietarios. Se
considerará el estudio toxicológico crónico más sensible y
representativo de la vía de exposición evaluada.
En la evaluación de riesgo dietario, deberá establecerse la Ingesta
Diaria Admisible (IDA) con base en el NOAEL del estudio toxicológico de
largo plazo más sensible y representativo por vía oral, aplicando un
factor de incertidumbre técnicamente justificado. Además, salvo prueba
científica en contrario, deberá definirse una Dosis de Referencia Aguda
(ARfD) basada en estudios de corto plazo por vía oral.
Asimismo, deberá realizarse la clasificación de peligros a la salud y
de los peligros físicos de la sustancia activa conforme a la versión
adoptada por la Autoridad Competente del Sistema Globalmente Armonizado
de Clasificación y Etiquetado de Productos Químicos (SGA) de las
Naciones Unidas.
Definición del Residuo en Material Tratado:
Deberá proporcionarse la definición de residuos con fines de análisis de riesgo y monitoreo.
La inclusión de metabolitos o productos de degradación en la definición
para evaluación del riesgo dependerá de su perfil toxicológico y su
magnitud, cuando superen el DIEZ POR CIENTO (10 %) del total de
residuos radioactivos.
Para la definición de residuos con fines de monitoreo, debe ser
inequívoca y simple, preferentemente basada en un único compuesto
(generalmente el compuesto parental), para todas las commodities.
Evaluación de la Exposición y Caracterización del Riesgo Dietario:
La evaluación del riesgo dietario, tanto crónico como agudo, se
realizará conforme a metodologías internacionalmente aceptadas,
considerando los ensayos de residuos supervisados para la sustancia
activa, los valores de referencia toxicológicos (IDA y ARfD) y las
estadísticas de consumo de la población argentina o una dieta
representativa de la región.
Se considerará aceptable la exposición alimentaria crónica cuando la
Ingesta Diaria Estimada Nacional sea inferior al CIEN POR CIENTO (100
%) de la IDA. De igual manera, la exposición alimentaria aguda será
aceptable si la Ingesta Nacional Estimada de corto plazo es menor al
CIEN POR CIENTO (100 %) de la ARfD.
Evaluación de la Exposición y Caracterización del Riesgo Laboral:
La evaluación de la exposición podrá basarse en estudios específicos o
estimaciones mediante datos genéricos y modelos de simulación aceptados
internacionalmente. Los escenarios de exposición deberán considerar las
prácticas laborales, el uso y disponibilidad del equipo de protección
personal, en concordancia con la práctica agrícola recomendada en la
etiqueta.
El criterio de aceptabilidad del riesgo estará determinado por el
Margen de Exposición (MOE), calculado como el cociente entre el NOAEL y
la exposición estimada. Un MOE superior a CIEN (100) se considerará
como riesgo aceptable.
En aquellos casos en que el valor de CIEN (100) pueda variar asociado a
razones como relevancia de un estudio de ruta específica, ausencia de
NOAEL u otras causas atendibles y válidas, deberá justificarse y
validarse científicamente si se utiliza otro valor como límite de
preocupación diferente a CIEN (100).
Período de Reingreso al Lote Tratado:
Cuando corresponda, se deberá realizar una evaluación de riesgo para el
trabajador de reingreso al lote tratado. Para su determinación, deberán
presentarse datos sobre toxicidad aguda dérmica, potencial irritante
dérmico y ocular, y sensibilización dérmica del principio activo o del
producto formulado.
VII - EFECTOS TÓXICOS SOBRE OTRAS ESPECIES (ÚNICAMENTE REQUERIDO PARA SUSTANCIAS ACTIVAS DE GRADO TÉCNICO NUEVAS).
Los estudios deberán realizarse conforme a las Test Guidelines y
Guidance Documents de la OCDE u otras referencias internacionalmente
reconocidas.
Para evaluar los efectos en aves, se deberán realizar estudios de
toxicidad oral aguda, toxicidad dietaria subcrónica y efectos en la
reproducción, utilizando especies validadas como faisán, codorniz o
pato silvestre.
En cuanto a peces, se requerirá la evaluación de toxicidad aguda y
crónica en especies como trucha arco iris o carpa, así como estudios de
bioacumulación, los cuales serán exigidos de manera condicional para
sustancias con un Log Kow superior a TRES (3).
Para invertebrados acuáticos, se deberá evaluar la toxicidad aguda y crónica en
Daphnia magna.
Asimismo, se evaluarán los efectos en organismos acuáticos mediante
estudios sobre el crecimiento de algas, utilizando Selenastrum
capricornutum u otra especie validada, y la inhibición del crecimiento
de plantas acuáticas, tomando como referencia Lemna sp.
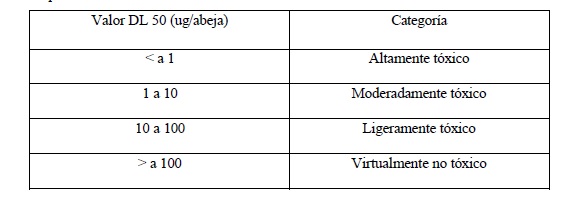
El impacto sobre invertebrados terrestres deberá analizarse mediante
estudios de toxicidad aguda y crónica en abejas. Para las abejas
adultas, se evaluará la toxicidad oral y por contacto (DL50); mientras
que la toxicidad oral aguda en larvas y los estudios crónicos en
adultos y larvas se determinará será requerido condicionalmente cuando
la sustancia activa sea sistémica en el vegetal y presente un DL50
inferior a ONCE (11) miligramos/abeja. Quedan exceptuados los
formulados de uso exclusivo en poscosecha, invernáculos o cebos.
Además, se deberá evaluar la toxicidad aguda en artrópodos benéficos en especies validadas como
Aphidius rhopalosiphi,
Chrysoperla carnea u
Orius laevigatus. Para lombrices de tierra, se evaluará la toxicidad aguda y el impacto en la reproducción en
Eisetia foetida u otra especie validada.
Asimismo, se analizarán los efectos sobre colémbolos en el suelo, particularmente en
Folsomia candida y
Folsomia fimetaria, mediante estudios de reproducción.
Finalmente, se evaluará la toxicidad en microorganismos del suelo,
enfocándose en aquellos involucrados en procesos de nitrificación.
VIII - EFECTOS SOBRE EL MEDIO ABIÓTICO (ÚNICAMENTE REQUERIDO PARA SUSTANCIAS ACTIVAS DE GRADO TÉCNICO NUEVAS).
Comportamiento en el suelo.
Se requerirán estudios en al menos TRES (3) tipos de suelos patrón. Las
evaluaciones deben conducirse considerando concentraciones de la
sustancia equivalentes a la práctica agrícola crítica que se quiere
registrar. Los suelos patrón deben ser representativos de los suelos
agrícolas, pueden incluir uno de textura gruesa, otro de textura franca
y otro de textura fina.
Se debe determinar la tasa de degradación, hasta el NOVENTA POR CIENTO
(90%), y vías de degradación incluida la identificación de: Procesos
que intervienen; Metabolitos y productos de degradación (Degradación
Aeróbica y Anaeróbica/ Fotólisis); Absorción y desorción y movilidad de
la sustancia activa y si es relevante, de sus metabolitos; Magnitud y
naturaleza de los residuos remanentes.
Comportamiento en el agua y en el aire.
Se debe determinar la tasa de degradación, hasta el NOVENTA POR CIENTO (90%), y vías de degradación. Biodegradación.
m - EVALUACIÓN DE RIESGO AMBIENTAL
Formulación del problema:
En función del patrón de uso y las formulaciones representativas a
registrar, se deben determinar grupos potenciales de especies no blanco
que podrían estar expuestas y requerir evaluación de riesgo.
Evaluación de la exposición ambiental
El destino ambiental de una sustancia química dependerá del patrón de
uso definido en la formulación del problema, por ende se deben
considerar tanto los factores, como el método de aplicación, los
cultivos objetivo, la época del año en que se propone la aplicación de
la sustancia activa y el área geográfica en la que se utilizará.
Como producto final se deberá definir la concentración ambiental
estimada (CAE), definida como la cantidad de sustancia activa y sus
metabolitos toxicológicamente relevantes en agua, suelo o sedimento y
aire, como resultado del uso propuesto. En ausencia de modelos de
exposición locales, se podrán utilizar los procedimientos desarrollados
por la Agencia de Protección Ambiental de Estados Unidos (US-EPA).
La evaluación de riesgos ambientales será desarrollada como un proceso
escalonado, de diferentes fases de refinamiento de la información,
tendiente a reducir la incertidumbre en la toma de decisiones.
Para nuevas sustancias activas, las fases serán:
Fase 1: Estudios de laboratorio estándar requeridos en esta norma:
propiedades fisicoquímicas, destino ambiental, toxicidad aguda y/o
crónica. En esta fase de la evaluación de riesgos, se utiliza el
llamado enfoque de 'peor caso', el cual combina los valores más altos
de exposición (máxima biodisponibilidad), con los niveles más altos de
toxicidad (especie sensible).
Fase 2: Modelos de estimación de la distribución y degradación
ambiental del compuesto parental y sus metabolitos toxicológicamente
relevantes en suelo, agua y aire. La elección estará determinada por
las propiedades individuales y los usos de una sustancia. En ausencia
de modelos de exposición locales, se deberán utilizar los
procedimientos de estimación ambiental predicha desarrollados por la
Agencia de Protección Ambiental de Estados Unidos (US-EPA).
Fase 3: Estudios de semi-campo o de campo simulados, en caso de que el
riesgo de un producto no pueda evaluarse suficientemente luego de las
fases de evaluación 1 y 2, particularmente para sustancias que son
relativamente persistentes o exhiben una alta movilidad. Se deberá
acordar con la Autoridad Competente el protocolo a utilizar.
Caracterización del riesgo
Como procedimiento para integrar los resultados del análisis de la
exposición con los efectos ecotoxicológicos adversos potenciales, puede
utilizarse el método determinístico que utilice la aproximación de los
COCIENTES DE RIESGO (RQ), calculados como el cociente entre los CAE y
los valores de ecotoxicidad aguda o crónica, según corresponda. Sin
embargo, pueden aplicarse otras metodologías aceptadas
internacionalmente, a fin de establecer perfil ecotoxicológico de la
sustancia en estudio.
DECLARACION DE NUEVOS ESTABLECIMIENTOS ELABORADORES
La solicitud de registro de una sustancia activa grado técnico
registrada previamente por el solicitante, proveniente de un nuevo
establecimiento elaborador debe realizarse mediante la presentación de
la información y documentación requerida en el presente Anexo, Título
“III. INFORMACIÓN CONFIDENCIAL (para sustancias activas nuevas y
equivalentes)”.
La Autoridad Competente puede dar curso a la gestión de la solicitud,
aprobación y registro una vez admitida la presentación de la
información y documentación requerida.
B - PRODUCTOS FORMULADOS:
Además de los productos formulados de síntesis este registro también contempla los siguientes supuestos:
Los formulados que entre sus componentes contengan productos sintéticos
solos o en mezcla con sustancias de origen biológico que por su forma
de uso generen una respuesta en la conducta o en la fisiología del
organismo plaga que se desee controlar, de aquí en adelante serán
llamados semioquímicos.
Los formulados que contengan bactericidas, fungicidas y/o insecticidas
destinados a prevenir, detener y/o eliminar el ataque de bacterias,
hongos y/o insectos que afecten a las maderas en sus distintas formas y
serán denominados de aquí en adelante preservadores para la madera.
Los formulados que sean producidos en base a agentes microbianos de
ocurrencia natural, o introducidos en el ambiente, para la prevención
y/o el control de organismos considerados plaga de la agricultura;
sustancias bioquímicas (extractos de origen vegetal, animal o
microbiológico). Invertebrados para el control biológico de plagas de
la agricultura.
En los casos que se desee inscribir un producto formulado, se deberá
presentar la documentación descrita a continuación. dada la diversidad
de características asociadas al origen, naturaleza y aptitud de uso,
los y preservadores de madera serán tratados en el apartado de LOS
REQUISITOS Y PROCEDIMIENTOS DE PRODUCTOS DE TRATO DIFERENCIADO (PTD).
I - INFORMACIÓN ADMINISTRATIVA
Formulario de solicitud de registro dependiendo el tipo de formulado
firmado por el Apoderado o Representante Legal y el Responsable Técnico
con incumbencia profesional en la materia.
Proyecto de marbete según normativa vigente.
Hoja de Datos de Seguridad, de acuerdo a la versión del Manual de las
Naciones Unidas del Sistema Globalmente Armonizado de Clasificación y
Etiquetado de Productos Químicos (SGA), adoptada en la presente norma.
Patrones: en caso de que el SENASA así lo requiera, a los fines de
control y vigilancia, la empresa registrante deberá aportar los
patrones y metodología analítica de la/s sustancia/s activa/s, en las
condiciones que establezca la Dirección General de Laboratorios y
Control Técnico (DGLCyT) del SENASA.
Sistema de gestión de envases vacíos aplicado en cumplimiento de la Ley vigente.
Formulario II (condicionalmente requerido).
Autorización a terceros a hacer uso del registro de un principio activo
grado técnico para el registro de un producto formulado.
II - INFORMACIÓN CONFIDENCIAL
a.- Certificado de Origen del producto formulado.
El Certificado de Origen debe ser original y emitido por el establecimiento elaborador.
Para establecimientos no ubicados en la REPÚBLICA ARGENTINA, para cada uno de los orígenes a registrar.
Debe incluir:
Identificación de la/s sustancia/s activa/s; Concentración declarada
para cada sustancia activa Tipo de formulación armonizada; Nombre y
domicilio real del establecimiento formulador.
b. - Declaración de composición cuali-cuantitativa del producto
formulado firmada por el establecimiento elaborador o por la empresa
registrante con carácter de declaración jurada y que deberá
contener:
Nombre químico según criterios internacionales (IUPAC o CAS) y número
CAS (cuando está disponible) de la/s sustancia/s activa/s y demás
componentes.
Contenido nominal de la(s) sustancia(s) activa(s), en base CIEN POR
CIENTO (100 %) de pureza, expresado en porcentaje en masa (% p/p) para
los formulados sólidos o gaseosos, y en porcentaje masa/volumen (% p/v)
para los formulados líquidos.
Contenido nominal, naturaleza química y función específica de cada uno de los componentes restantes incluidos en la formulación.
Tipo de formulación armonizada de acuerdo con la Norma IRAM 12074.
Se presentará una sola declaración de composición cuali-cuantitativa
representativa para todas las plantas para las que se solicita el
registro en la que debe figurar la razón social y dirección real de
cada uno de los establecimientos fabricantes.
c. - Estudio de UN (1) lote
Se debe presentar el análisis de una muestra representativa de UN (1)
lote de formulación para la cuantificación de la(s) sustancia(s)
activa(s), proveniente de una de las plantas para la que se solicita el
registro o del Laboratorio de desarrollo. Los valores de concentración
informados para la(s) sustancia(s) activa(s) deberán cumplir con los
límites establecidos en la Norma IRAM 12054, en función del contenido
nominal declarado.
En caso de que el
sponsor del
estudio no coincida con la empresa registrante se deberá remitir una
autorización del sponsor para la utilización de la información.
Deberá presentarse el estudio completo, de acuerdo con los principios
de Buenas Prácticas de Laboratorio, convenientemente firmado y fechado.
Se establecen los siguientes contenidos mínimos para el reporte del estudio de 1 lote:
Índice de contenidos
Nombre y domicilio real del establecimiento elaborador Cuadro de resumen de resultados
Métodos de análisis, que incluya todas las ecuaciones necesarias para reproducir los cálculos realizados
Resultados
En caso de usar curvas de calibración incluir los gráficos
identificando título y ejes (con magnitud y unidades). Además debe
incluir la ecuación de la recta. Cuando corresponda incluir los
cálculos de densidad. Se deben incluir en formato de cuadro los datos
necesarios para poder reproducir los cálculos realizados.
Los cromatogramas representativos del lote y del patrón analítico, con
encabezado (con fecha, hora, descripción) y reporte (áreas y tiempo de
retención). Certificados de análisis de todos los patrones utilizados.
Cuando sean generados por el fabricante o el laboratorio deben incluir
el reporte de cuantificación e identificación. En caso de patrones
secundarios incluir la cuantificación contra el patrón primario junto a
su certificado de análisis. Certificado de análisis del lote analizado
emitido y firmado por el formulador que incluya nombre y dirección del
establecimiento formulador y fecha de elaboración y vencimiento del
lote. De no disponer en el certificado de análisis la dirección del
establecimiento elaborador, se debe presentar una declaración jurada
indicando dicha información acompañando el certificado. Constancia BPL
OECD del Laboratorio
Acreditación BPL del estudio.
b.- Proceso de formulación
Para cada proceso de formulación debe proveerse la siguiente
información emitida y firmada por el fabricante o la empresa
registrante:
Nombre y domicilio real de los establecimientos formuladores que
interviene en el proceso. Caracterización general del proceso: deberá
consistir en una descripción completa y detallada de cada una de las
etapas que constituyen el proceso, especificando qué componentes son
agregados en cada una y qué operación se realiza.
Identificación de los ingredientes usados para formular el producto.
Descripción de los equipos usados, con sus especificaciones.
Descripción de las condiciones que se controlan en cada etapa del
proceso y los parámetros de control de calidad del producto terminado.
III - CUERPO TÉCNICO
Este cuerpo técnico se presentará con la documentación dispuesta por temas, a saber:
a- COMPOSICIÓN
Contenido de sustancia(s) activa(s), grado técnico, expresado en % p/p
o % p/v según corresponda Métodos de análisis para la determinación del
contenido de la(s) sustancia(s) activa(s).
Para el caso de preservadores de la madera: deberá expresarse en óxidos
cualesquiera fueran las sustancias que los integran, (como lo establece
la norma IRAM). Y adicionalmente mencionar el método de aplicación:
pincelado, aspersión, inmersión, prolongada, momentánea, breve,
inyección, baño caliente-frío.
b - PROPIEDADES DEL PRODUCTO FORMULADO
Propiedades Físicas y Químicas.
Aspecto: Tipo de Formulación Armonizada; Color
Estabilidad en el almacenamiento a baja temperatura y acelerada a alta temperatura
Densidad relativa Inflamabilidad
Acidez/Alcalinidad y potencial de hidrógeno (pH).
Propiedades físicas relacionadas con su uso.
Humectabilidad: Para polvos dispersables o mojables.
Persistencia de la espuma: Para formulados que se aplican con agua.
Suspensibilidad: Para gránulos dispersables (WG), polvos mojables:
(WP), suspensiones concentradas: (SC), Suspensión de encapsulado (CS)
Análisis granulométrico en húmedo: Para los polvos mojables, las
suspensiones concentradas (SC, FS), Suspoemulsión (SE).
Análisis granulométrico en seco: Para gránulos y polvos. Estabilidad de
la emulsión: Para concentrados emulsionables. Corrosividad.
Incompatibilidad con otros productos: Con otro fitosanitario y/o fertilizante. Densidad: Para sólidos y líquidos.
Punto de inflamación: Para líquidos.
Viscosidad: Para aceites, suspensiones y concentrados emulsionables.
Índice de sulfonación: (Residuo no Sulfonable) Para aceites y aceites
emulsionables destinados a
frutales u ornamentales).
Dispersión: Para gránulos dispersables.
Desprendimiento de gases: Para gránulos generadores de gas. Soltura o fluidez: Para polvos secos.
Índice de iodo: Índice de Iodo y de Saponificación. Sólo para aceites vegetales, no para losaceites minerales.
Velocidad de liberación. Para suspensiones acuosas encapsuladas (CS) y
para la formulación mixta (ZC), mezcla de suspensiones encapsuladas y
suspensiones concentradas (CS
+ SC).
Presión de vapor, si corresponde en función de la volatilidad.
IV. ENSAYOS DE EFICACIA AGRONÓMICA Y FITOTOXICIDAD
Aquellas recomendaciones de usos que no tengan antecedentes en
Argentina o las modificaciones de los usos críticos ya autorizados,
deberán respaldar la solicitud mediante informes de los ensayos de
eficacia agronómica y fitotoxicidad.
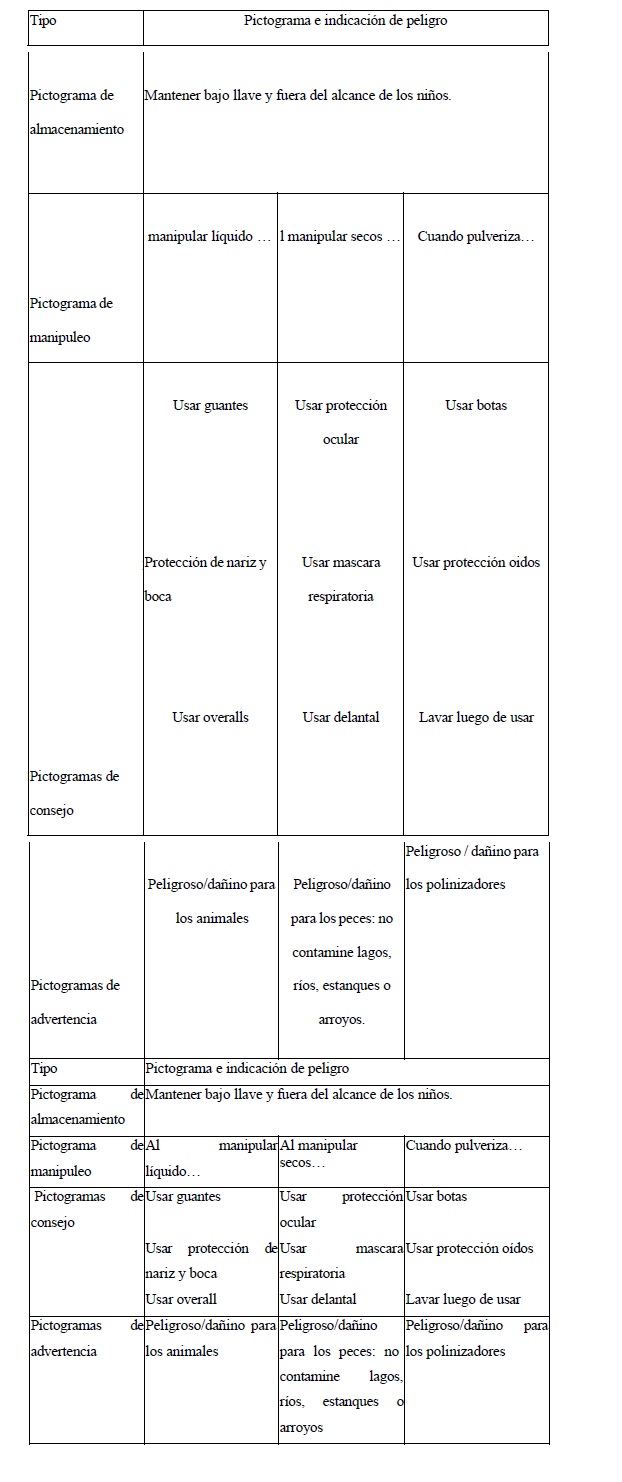
V ETIQUETADO
El etiquetado deberá ajustarse a la normativa vigente, y conforme a la
versión del Manual de las Naciones Unidas del Sistema Globalmente
Armonizado de Clasificación y Etiquetado de Productos Químicos (SGA)
adoptada por la Autoridad Competente del Registro Nacional.
VI. ENVASES Y EMBALAJES PROPUESTOS.
a.- Envases.
Tipo(s)
Material(es)
Capacidad(es)
b.-Embalajes.
Tipo
Material
Procedimientos para la descontaminación y destino final de los embalajes.
VII - EFECTOS TÓXICOS EN ESPECIES MAMÍFERAS
En el caso que la empresa registrante no disponga de estudios
toxicológicos in vivo, como alternativa de reemplazo, reducción o
refinamiento de las pruebas con animales requeridas en este apartado,
podrán presentarse estudios in vitro, siempre y cuando, dichos
protocolos y ensayos hayan sido reconocidos por autoridades
regulatorias internacionales para el Registro Nacional de Productos
Fitosanitarios. En tales casos, el registrante deberá solicitar
mediante una nota la aceptación de dichos estudios, mediante
una justificación
técnico-científica de su uso.
Se aplicarán los criterios de las directrices de la OCDE para justificar la no conducción de estudios in vivo.
a.- Toxicidad aguda.
Oral. Toxicidad oral aguda (DL50 oral)
Este estudio se requerirá en todos los casos excepto si el producto
formulado es un gas o es altamente
volátil.
Dérmica. Toxicidad cutánea aguda (DL50 cutánea)
Este estudio se requerirá a menos que:
El producto formulado es un gas o es altamente volátil. El producto
formulado es corrosivo para la piel o presenta un pH menor a DOS (2) o
mayor a ONCE
COMA CINCO (11,5).
Inhalatoria. Toxicidad aguda por inhalación (LC50 inhalación) Este
estudio se requerirá cuando el producto formulado es un gas o es
altamente volátil; o consiste en, o en las condiciones de uso darán
como resultado, un material respirable (por
ejemplo, gas,
vapor, aerosol o
partículas).
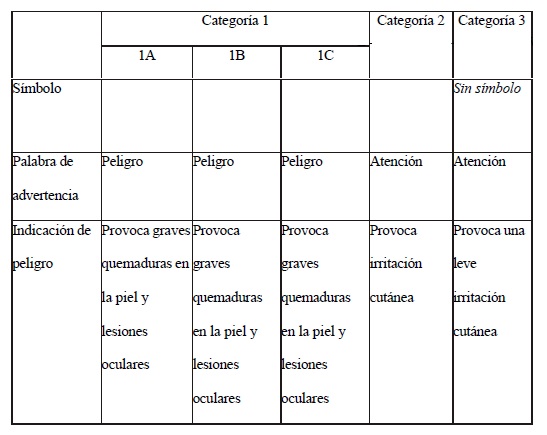
b.- Irritación cutánea y ocular.
Irritación cutánea.
El estudio in vivo no debería realizarse si: El producto formulado es
un gas o es altamente volátil. El producto formulado es corrosivo para
la piel o presenta un pH menor a DOS (2) o mayor a ONCE COMA CINCO
(11,5)
Existe información disponible que indica que satisface los criterios
para ser clasificada como corrosiva para la piel o irritante ocular La
sustancia es clasificada como muy tóxica por vía dermal
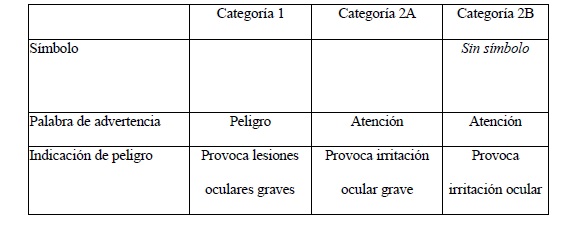
Irritación ocular.
Este estudio se requerirá a menos que:
El producto formulado sea corrosivo o severo irritante para la piel,
Presente un pH menor a DOS (2) o mayor a ONCE COMA CINCO (11,5)
La sustancia es clasificada como muy tóxica por vía dermal.
c.- Sensibilización cutánea.
Este estudio se requerirá a menos que el principio activo sea un sensibilizante conocido.
VIII - INFORMACIÓN MÉDICA OBLIGATORIA
Diagnóstico y síntomas de intoxicación
Tratamientos propuestos
Primeros auxilios. Antídotos
Tratamiento médico.
IX - DATOS DE LOS EFECTOS SOBRE EL AMBIENTE
a.- Toxicidad aguda en aves Estos estudios serán requeridos para todos
los productos cuyos usos propuestos son en lugares abiertos. Toxicidad
oral aguda (en faisán, codorniz, pato silvestre y otra especie
validada).
b.- Toxicidad aguda sobre organismos acuáticos Estos estudios serán
requeridos para todos los productos cuyos usos propuestos son en
lugares abiertos. Concentración letal media de NOVENTA Y SEIS HORAS (96
h) en peces (en trucha arco iris, carpa y otras especies validadas).
d.- Efectos tóxicos en polinizadores e invertebrados no blanco
Este estudio será requerido si por el uso propuesto pudiere resultar una exposición de las abejas.
Toxicidad oral aguda para las abejas adultas (DL50 oral adultas).
Toxicidad por contacto agudo para las abejas adultas (DL50 contacto adulto).
X EVALUACIÓN TOXICOLÓGICA Y ECOTOXICOLÓGICA
Clasificación toxicológica y ecotoxicológica para el etiquetado del
producto fitosanitario formulado y la Hoja de Datos de Seguridad, de
acuerdo a la versión del Manual de las Naciones Unidas del Sistema
Globalmente Armonizado de Clasificación y Etiquetado de Productos
Químicos (SGA), adoptada por la Autoridad Competente del Registro
Nacional.
Se considerarán como excepción las clasificaciones de peligro de aves y
abejas, las cuales adoptarán las clasificaciones de la USEPA.
XI - INFORMACIÓN SOBRE EL MANEJO DE DESECHOS DEL PRODUCTO FORMULADO
a.- Métodos de disposición final de los desechos Se debe incluir el o
los procedimientos más adecuados para eliminación de remanentes o
residuos de las aplicaciones, así como de los envases.
b.- Procedimientos para la destrucción del producto formulado y para la descontaminación.
Se deben presentar los procedimientos y métodos a seguir para la destrucción o inactivación del producto formulado.
Incineración controlada (condiciones).
Posibilidades de neutralización.
c.-Procedimientos de recuperación en caso de derrame Detallar el o los
procedimientos para la recuperación del producto formulado.
d.- Depuración de las aguas Detallar el o los procedimientos a seguir
para la depuración de fuentes de agua contaminadas con el producto
formulado.
e.- En caso
de incendio Identificar los productos de reacción y
gases de combustión poniendo énfasis en aquellas sustancias que
presentan riesgo toxicológico humano o ambiental y con base en lo
anterior establecer y presentar un protocolo de respuesta ante una
emergencia específica.
XII - EVALUACIÓN DE RIESGO
La Autoridad Competente establecerá qué categoría de productos deberán
presentar una evaluación de riesgo en cumplimiento con lo establecido
en el Anexo VII en el que se detalla el análisis de riesgos.
DECLARACIÓN DE NUEVOS ESTABLECIMIENTOS ELABORADORES DE PRODUCTO FORMULADO REGISTRADO
Se presentará una sola declaración de composición cuali-cuantitativa
representativa para todas las plantas para las que se solicita el
registro, si el producto a registrar no presenta diferencias entre las
mismas, lo que deberá indicarse bajo declaración jurada.
A tal efecto, debe presentar para cada nuevo establecimiento:
1) Declaración jurada
Formulario de declaración jurada indicando la razón social y dirección
real del establecimiento o planta a través de la plataforma SIGTrámites
del Senasa o por aquellos medios que el Senasa disponga a tal fin,
firmada por el Apoderado o Representante Legal.
* En virtud que por declaración jurada del responsable titular del registro, no existen diferencias significativas entre los productos obtenidos en los diferentes establecimientos o plantas de un mismo productos formulado, de observarse incumplimiento por acciones de control sobre el productos formulado de un establecimiento o planta, las medidas que la Autoridad Competente adopte serán aplicadas a todos los establecimientos o plantas declaradas para el registro involucrado.
2) Certificado de Origen del producto formulado.
El Certificado de Origen debe ser original y emitido por el fabricante
y estar debidamente legalizado por las autoridades del país de origen.
Debe incluir:
• identificación de la sustancia activa.
• contenido mínimo declarado en % p/p.
• Denominación/razón social y domicilio real del establecimiento elaborador.
• (*)Nombre y dirección de la empresa que registrará el producto ante SENASA.
En caso de que no figure esta
información se deberá remitir una nota emitida por el establecimiento
elaborador donde conste la autorización para realizar el registro del
producto en el país.
NUEVA MARCA COMERCIAL PARA UN PRODUCTO FORMULADO YA REGISTRADO
Si un registrante solicita un registro de un producto ya registrado por
el mismo solamente se debe mencionar expediente aprobado.
Si el registro corresponde a otra persona física o jurídica, deberá presentarse la autorización de uso correspondiente.
I.
Información legal y administrativa.
• Proyecto de marbete según normativa vigente.
• Hoja de Datos de Seguridad, de acuerdo a la versión del manual de las Naciones de las Naciones Unidas del “
Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos”, adoptada por la Autoridad Competente del Registro Nacional de Terapéutica Vegetal..
Formulario II (condicionalmente requerido). Autorización a terceros de
hacer uso del registro de un principio activo grado técnico para el
registro de un producto formulado.
Requisitos y procedimientos DE COADYUVANTES DE APLICACIÓN.
I. Información legal y administrativa.
• Formulario de solicitud del producto formulado con aptitud COADYUVANTE,
• Proyecto de marbete según normativa vigente.
• Hoja de Datos de Seguridad, de acuerdo a la versión del manual de las Naciones Unidas del “
Sistema Globalmente Armonizado de Etiquetado de Productos Químicos”, adoptada por la Autoridad Registro Nacional de Terapéutica Vegetal.
• Sistema de gestión de envases vacíos aplicado en de la Ley vigente.
II. Cuerpo técnico
1. Certificado de Origen del producto formulado.
El Certificado de Origen emitido por el fabricante (*) para cada uno de los orígenes a registrar, debe incluir:
• identificación de la sustancia principal que se pretende registrar como coadyuvante.
• contenido mínimo declarado.
• tipo de formulación
• Denominación/razón social y domicilio real del establecimiento fabricante.
(**)Nombre y dirección de la empresa que registrará el producto ante SENASA.
(*) Plantas del extranjero debidamente legalizado por las autoridades del país de origen.
(**)
En caso de que no figure esta
información se deberá remitir una nota emitida por el establecimiento
fabricante donde conste la autorización para realizar el registro del
producto en el país
2.
Declaración de composición cuali-cuantitativa del producto formulado
La misma debe estar firmada por el establecimiento fabricante o por la empresa registrante con carácter de declaración jurada:
• Nombre químico según criterios internacionales (IUPAC o CAS) y número
CAS (cuando esté disponible) de la/s sustancia/s activa/s y demás
componentes.
• Contenido nominal de la(s) sustancia(s) a registrar con clase de uso
coadyuvante, en base 100 % de pureza, expresado en porcentaje en masa
(% p/p) para los formulados sólidos o gaseosos, y en porcentaje
masa/volumen (% p/v) para los formulados líquidos.
• Contenido nominal, naturaleza química y función específica de cada
uno de los componentes restantes incluidos en la formulación.
• Tipo de formulación armonizada de acuerdo con la Norma IRAM 12074.
• Método de análisis.
Se presentará una sola declaración de composición cuali-cuantitativa
representativa para todas las plantas para las que se solicita el
registro en la que debe figurar la razón social y dirección real de
cada uno de los establecimientos fabricantes.
3.
Información toxicológica y ecotoxicológica
El
Dossier debe contener
información científica respaldatoria con la caracterización
toxicológica y/o ecotoxicológica para la clasificación de los productos
formulados en función de la información disponibles para clasificar los
peligros de los componentes principales y los co-formulantes, siendo
posible aplicar los principios de extrapolación y estimación de la
toxicidad aguda (ETA), según el manual de las Naciones Unidas del “
Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos’’.
Requisitos y procedimiento DE SEMIOQUÍMICOS EN BASE A SUSTANCIAS ACTIVAS SINTÉTICAS.
Requisitos generales de registro de productos formulados que entre sus
componentes contengan productos sintéticos, solos o mezcla con
sustancias de origen biológico, que por su forma de uso se espera
generen una respuesta en la conducta o en la fisiología de organismo
plaga que se pretende controlar o monitorear. Comprenden a:
• Dispositivos de captura, cuando el uso del semioquímico tenga como
objetivo la atracción sexual o alimentaria de plagas, con el objetivo
de monitorear poblaciones de una especie.
• Atracticidas, cuando mediante el uso de cebos o de dispositivos de
captura masivos, se combina el uso de semioquímicos (como atrayente
sexual o alimentario), con el empleo de insecticidas o mecanismos de
captura física para disminuir la abundancia y daños de las plagas en
los cultivos.
• Confusión Sexual, cuando mediante el asperjado o el uso masivo
de emisores de semioquímicos se busca la saturación del medioambiente
con una feromona sexual con el fin de interferir en comportamiento de
apareamiento de la plaga, para disminuir la abundancia y daños de las
plagas en los cultivos.
• Repelentes, cuando mediante el asperjado o el uso masivo de emisores
se busca la repelencia de plagas a fin de disminuir los daños de las
mismas en los cultivos.
I.
Información legal y administrativa.
• Formulario de solicitud del producto formulado con aptitud SEMIOQUÍMICO,
• Patrones: en caso de que la autoridad de aplicación así lo requiera,
a los fines de control y vigilancia, la empresa registrante deberá
aportar los patrones y metodología analítica de la/s sustancia/s
activa/s, en las condiciones que establezca la Dirección General de
Laboratorios y Control Técnico (DGLCyT) del SENASA.
• Proyecto de marbete según normativa vigente
• Hoja de Datos de Seguridad, de acuerdo a la versión del manual de las Naciones Unidas del “
Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos’”, adoptada por la Autoridad Competente del Registro Nacional de Terapéutica Vegetal.
• Sistema de gestión de envases vacíos aplicado en cumplimiento de la Ley vigente, si corresponde.
II.
INFORMACIÓN TÉCNICA.
NOTA: los
productos formulados utilizados exclusivamente para Monitoreo de Plagas
Agrícolas se encuentran exentos de presentación de información técnica
respaldatoria
•
Certificado de Origen de la Sustancia activa grado técnico.
El Certificado de Origen emitido por el fabricante (4), debe incluir:
• identificación de la sustancia activa.
• contenido mínimo declarado.
• Denominación/razón social y domicilio real del establecimiento fabricante.
(**) Nombre y dirección de la empresa que registrará el producto ante SENASA.
(*)
Establecimiento del extranjero debidamente legalizado por las autoridades del país de origen.
(**)
En caso de que no figure esta
información se deberá remitir una nota emitida por el establecimiento
fabricante donde conste la autorización para realizar el registro del
producto en el país.
•
Certificado de Origen del producto formulado.
El Certificado de Origen emitido por el fabricante (*) para cada uno de los orígenes a registrar, debe incluir:
• identificación de la/s sustancia/s activa/s.
• contenido mínimo de SUSTANCIA ACTIVA declarado.
• tipo de formulación
• Denominación/razón social y domicilio real del establecimiento fabricante.
• (**) Nombre y dirección de la empresa que registrará el producto ante SENASA.
(*)
Establecimiento del extranjero debidamente legalizado por las autoridades del país de origen.
(**)
En caso de que no figure esta
información se deberá remitir una nota emitida por el establecimiento
fabricante donde conste la autorización para realizar el registro del
producto en el país.
•
Declaración de composición cuali-cuantitativa del producto formulado
La misma debe estar firmada por el responsable del establecimiento
fabricante o de la empresa registrante con carácter de declaración
jurada:
• Nombre químico según criterios internacionales (IUPAC o CAS) y número
CAS (cuando esté disponible) de la/s sustancia/s activa/s y demás
componentes.
• Contenido nominal de la(s) sustancia(s) activa(s), en base 100 % de
pureza, expresado en porcentaje en masa (% p/p) para los formulados
sólidos o gaseosos, y en porcentaje masa/volumen (% p/v) para los
formulados líquidos.
• Contenido nominal, naturaleza química y función específica de cada
uno de los componentes restantes incluidos en la formulación.
• Tipo de formulación armonizada de acuerdo con la Norma IRAM 12074.
Se presentará una sola declaración de composición cuali-cuantitativa
representativa para todas las plantas para las que se solicita el
registro en la que debe figurar la razón social y dirección real de
cada uno de los establecimientos fabricantes.
•
Certificado de Análisis cuali-cuantitativo (condicionalmente requerido*)
Certificado de Análisis cuali-cuantitativo de una muestra
representativa de UN (1) lote de formulación del producto formulado a
registrar con nombre y firma del Responsable técnico del laboratorio
que realizó el análisis.
• P
ropiedades físicas y químicas del producto formulado
Se requerirá la presentación de estudios para aquellos
semioquímicos para los que se espera exposición
(i.e. pulverizables), para los restantes se podrá presentar dossier
sobre la base de la información técnica disponible para la/a
sustancia/a activa/s y los coformulantes.
• Aspecto (estado físico y color):
• Densidad.
• pH.
• Estabilidad en el almacenamiento
• Tensión superficial (cuando corresponda)
• Solubilidad (cuando corresponda)
• Suspensibilidad (cuando corresponda)
•
Ensayos de eficacia agronómica y fitotoxicidad (cuando corresponda).
En caso de no existir antecedentes de uso autorizado en Argentina, en
relación a la naturaleza química del semioquímico (dosis, tipo de
formulación/dispositivo o técnica de aplicación, etc), deben
presentarse informes de los ensayos de eficacia agronómica, de acuerdo
con lo establecido en el presente Manual según lo establecido en el
Cap. 20 del presente manual.
•
Información toxicológica y ecotoxicológica
Debe presentar un Dossier con información científica respaldatoria con
la caracterización toxicológica para la clasificación de los productos
formulados en función de la información disponible para clasificar los
peligros de los ingredientes activos y los co-formulantes, siendo
posible aplicar los principios de extrapolación y estimación de la
toxicidad aguda (ETA), según el manual de las Naciones Unidas del “
Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos”.
PRODUCTOS FORMULADOS A BASE DE AGENTES MICROBIANOS,
SUSTANCIAS BIOQUÍMICAS O INVERTEBRADOS
REQUISITOS GENERALES
a) Los Ensayos de eficacia agronómica deben ser
realizados localmente, por especie plaga que se pretenda registrar, y
cumplir con requisitos establecidos en la normativa vigente. Los
ensayos de eficacia agronómica de un bioinsumo sin antecedentes de
registro en el país, deben llevarse a cabo en al menos TRES (3) zonas
agroecológicas distintas de la REPÚBLICA ARGENTINA, durante al menos
DOS (2) campañas agrícolas. Podrán ser admitidos ensayos en una misma
campaña siempre que la DAYB cerciore que los ensayos reflejen
variabilidad climática, se realicen en al menos tres zonas
agroecológicas y respeten el mínimo número de ensayos, SEIS (6).
b) Para bioinsumos a base de organismos modificados genéticamente, en
todos casos deberá contar previamente al registro con la evaluación
favorable realizada por la Coordinación de Innovación y Biotecnología
perteneciente a la Dirección Nacional de Bioeconomía de SAGYP y la
Comisión Nacional Asesora de Biotecnología Agropecuaria (CONABIA),
conforme a lo establecido en las normativas vigentes. C) Cuando el
producto a registrar proceda de la extracción de recursos natural
nativo, la empresa registrante debe contar con el correspondiente
permiso de colecta/acceso a los recursos genéticos.
INFORMACIÓN LEGAL Y ADMINISTRATIVA GENERAL.
Presentar de acuerdo con B - PRODUCTOS FORMULADOS - I. INFORMACION ADMINISTRATIVA.
Consideración para productos bioinsumos: Certificado de Origen firmado
por personal responsable de la planta de producción / Establecimiento
elaborador del Bioinsumo. En caso de provenir de una planta extranjera,
deben estar debidamente autenticados y/o apostillados por las
autoridades del país de origen.
INVERTEBRADOS PARA EL CONTROL BIOLÓGICO
I. Información legal y administrativa
• Acreditación del Registro de planta de cría.
• Certificado de origen del hospedero/presa que acompaña al invertebrado (cuando corresponda)
• Permiso de importación del invertebrado y del hospedero/presa que acompaña al invertebrado (cuando corresponda)
• Certificado de la Cuarentena emitido por el Laboratorio oficial (cuando corresponda)
• Autorización de colecta emitida por la autoridad de aplicación ambiental (cuando corresponda).
• Muestra de referencia para ser conservada en el laboratorio del SENASA.
II. Información técnica
A. Identidad y proceso de fabricación
• Nombre científico e identificación taxonómica (indique sinonimia, subespecie, variedad o raza si corresponde).
• Descripción morfológica.
• Método utilizado para identificar el invertebrado (taxonomía clásica,
técnicas moleculares, etc.). Incluir claves de identificación
morfológica cuando corresponda
• Estado de desarrollo biológico del invertebrado.
• Descripción detallada de los sustratos orgánicos e inorgánicos incluidos en el
• producto comercial.
• Nombre científico, características y función del hospedero/presa que acompaña al
• invertebrado (cuando corresponda).
• Libro de procedimiento y control de calidad para las etapas de crianza de los invertebrados.
B. Propiedades biológicas y utilización agronómica.
• Rango de hospederos/presas conocidos.
• Pruebas de especificidad, que indiquen cualquier riesgo potencial
sobre especies no objetivos o para la salud de las personas y animales.
• Antecedentes de los resultados, de la introducción y/o liberación del organismo en otros países (para organismo exóticos).
• Estabilidad frente a diferentes condiciones climáticas
• Tipo de organismo (depredador, parasitoide o parásito), y estado o fase de desarrollo en el que será comercializado.
• Condiciones de liberación
• Método de liberación
• Dosis
• Intervalo entre liberaciones
• Periodo en que deben suspenderse las aplicaciones de otros productos fitosanitarios
• (antes y después de la liberación)
• Vida útil del producto
• Condiciones de almacenamiento, transporte y seguridad
• Informes de los ensayos de eficacia agronómica para los usos propuestos.
C. Envases y Embalajes según B - PRODUCTOS FORMULADOS - V. ENVASES Y EMBALAJES PROPUESTOS.
D. Medidas de Seguridad:
• Métodos recomendados y precauciones durante la multiplicación,
fraccionamiento, almacenamiento, liberación y manipuleo general del
producto. Indicar procedimientos de actuación en caso de accidentes.
Requisitos y procedimientos para SUSTANCIAS BIOQUIMICAS FORMULADAS A
BASE DE EXTRACTOS DE ORIGEN VEGETAL, ANIMAL O MICROBIOLÓGICO.
I. Información legal y administrativa específica
a) Certificado de Composición original firmado por el Responsable Técnico de la empresa formuladora.
b) Informe de Análisis cuali-cuantitativo del producto formulado a registrar firmado por el Responsable técnico del laboratorio.
c) Autorización de colecta emitida por la autoridad de aplicación ambiental (cuando corresponda)
d) Acreditación del Registro de planta formuladora / establecimiento.
e) Sistema de gestión de envases vacíos aplicado en cumplimiento de la Ley vigente, si corresponde.
I. Información técnica
A. Información de la sustancia activa
a) Productor de la sustancia activa
b) Nombre común: Aceptado o propuesto por ISO y Sinónimo (si lo tiene).
c) Nomenclatura química (aceptado o propuesto por IUPAC), si corresponde.
d) Fórmula empírica, si corresponde.
e) Fórmula estructural (incluyendo estereoquímica de isómeros activos si corresponde), si corresponde.
f) Masa molecular, si corresponde.
g) Grupo químico al que pertenece.
h) Grado de pureza (contenido mínimo de sustancia activa en g/kg).
i) Caracterización de los otros componentes presentes en el extracto.
j) Caracterización de otros componentes agregados (ej. estabilizantes). Identificación y concentración.
B. Método de obtención de la sustancia activa
Esta información deberá venir respaldada por un Certificado emitido por
el fabricante con el método de obtención, especificando los reactivos y
solventes empleados en el proceso. Indicar los equipos utilizados y las
condiciones de operación, especificando los parámetros controlados
durante el proceso.
C. Métodos analíticos para la cuantificación y la identificación de la sustancia activa:
• El contenido mínimo declarado de la sustancia activa debe estar sustentado en el
• análisis de 5 lotes del grado técnico. Se deberá adjuntar la
documentación de identificación y trazabilidad de los 5 lotes
presentados
• Deberá presentarse el estudio completo de cuantificación de los 5
lotes, de acuerdo con los lineamientos de Buenas Prácticas de
Laboratorio que defina la DGLyCT del Senasa, convenientemente firmado y
fechado. El informe del laboratorio deberá incluir la descripción del
método de ensayo, los registros cromatográficos, las tablas de
cuantificación (incluyendo los datos crudos) y los Certificados de
Análisis de los Patrones y la Muestra referidos en el estudio que
deberán cumplir con protocolos internacionalmente reconocidos.
• Deberán facilitarse descripciones completas de la metodología que deberá estar convenientemente validada.
Deberán presentarse los parámetros de validación obtenidos:
• Linealidad.
• Límite de detección y cuantificación.
• Especificidad.
• Exactitud y repetibilidad.
Deberá realizarse la identificación de la sustancia activa en los 5 lotes por un método espectrométrico (MS, RMN, IR).
D. Propiedades físicas y químicas de la sustancia activa
a) Aspecto:
• Estado físico
• Color
b) Densidad
c) pH.
d) Estabilidad en el almacenamiento
B. Información del producto formulado
Identidad y proceso de fabricación del producto formulado
a) Declaración de la composición cuali-cuantitativa del producto
formulado firmada por el Representante Legal con carácter de
Declaración Jurada, que deberá incluir:
• Contenido de la(s) sustancia(s) activa(s), en base 100 % de pureza,
expresado en porcentaje en masa (% p/p) para los formulados sólidos o
gaseosos, y en porcentaje masa/volumen (% p/v) para los formulados
líquidos.
• Contenido, naturaleza química y función específica de cada uno de los componentes restantes incluidos en la formulación.
• Tipo de formulación armonizada de acuerdo con la Norma IRAM 12074.
b) Análisis de una muestra representativa de UN (1) lote de formulación
para la cuantificación de la(s) sustancia(s) activa(s). Deberá
presentarse el estudio completo, de acuerdo con los lineamientos de
Buenas Prácticas de Laboratorio que defina la DGLyCT del Senasa,
convenientemente firmado y fechado,. El informe del laboratorio deberá
incluir la descripción del método de ensayo, los registros
cromatográficos, las tablas de cuantificación (incluyendo los datos
crudos) y los Certificados de Análisis de los Patrones y la Muestra
referidos en el estudio que deberán cumplir con protocolos
internacionalmente reconocidos. Asimismo, se deberá adjuntar la
documentación de identificación y trazabilidad de la muestra analizada.
Los valores de concentración informados para la(s) sustancia(s)
activa(s) deberán cumplir con los límites establecidos en la Norma IRAM
12054, en función del contenido respectivo declarado.
c) Certificado de Origen del producto formulado, donde conste la
identificación de la(s) sustancia(s) activa(s), su concentración
declarada, el tipo de formulación armonizada y el nombre y la
localización de la planta formuladora. El Certificado de Origen deberá
estar debidamente legalizado por las autoridades del país de origen.
F. Descripción del proceso de formulación, que deberá contener la siguiente información:
a) Nombre y localización de la planta formuladora que interviene en el proceso.
b) Caracterización general del proceso: deberá consistir en una
descripción completa y detallada de cada una de las etapas que
constituyen el proceso, especificando qué componentes son agregados en
cada una y qué operaciones se realizan.
c) Identificación de los ingredientes usados para formular el producto.
d) Descripción de los equipos usados, con sus especificaciones.
e) Descripción de las condiciones que se controlan en cada etapa
del proceso y los parámetros de control de calidad del producto
terminado.
f) Descripción de posibles reacciones posteriores al proceso de
formulación que ocurran entre los ingredientes activos, o entre éstos y
cualquier otro componente de la formulación o el envase; posible
migración de materiales del envase al producto.
G. Propiedades físicas y químicas del producto formulado.
a) Aspecto:
• Estado físico.
• Color.
b) Densidad.
c) pH.
d) Estabilidad en el almacenamiento
e) Tensión superficial (cuando corresponda)
f) Suspensibilidad (cuando corresponda)
g) Solubilidad (cuando corresponda)
H. Información toxicológica, ecotoxicológica y ambiental
H.1. Toxicidad aguda en mamíferos.
a) Toxicidad oral aguda (DL50 oral)
b) Toxicidad cutánea aguda (DL50 cutánea)
c) Toxicidad aguda por inhalación (LC50 inhalación). Condicionalmente requerido
d) Irritación cutánea. Se deberá seguir un enfoque escalonado:
d.1. evaluación de la corrosividad dérmica utilizando un método de prueba in vitro validado;
d.2. un estudio de irritación dérmica inicial in vivo con un animal, y donde no se observan efectos adversos;
d.3. pruebas confirmatorias in vivo con uno o dos animales adicionales.
e) Irritación ocular. Se deberá seguir un enfoque escalonado:
e.1. el uso de una prueba de irritación / corrosión cutánea in vitro para predecir irritación / corrosión ocular;
e.2. un estudio inicial de irritación ocular in vivo con un animal, y donde no se observan efectos adversos;
e.3. pruebas confirmatorias in vivo con uno o dos animales adicionales.
f) Sensibilización cutánea.
Este estudio se requerirá a menos que el principio activo sea un
sensibilizante conocido. Por ende, la no presentación de estudios de
sensibilidad dermal debe ser documentada con un estudio puente donde se
haya determinado que la sustancia es un sensibilizante dermal conocido.
g) Mutagenicidad:
Un estudio inicial de mutagenicidad es requerido mínimamente. Estudios
subsiguientes pueden o no ser requeridos de acuerdo con los resultados
obtenidos en los ensayos interiores.
Para cumplimentar este requisito se recomienda un enfoque por etapas: (IN VITRO)
g.1. Estudio de mutación genética en bacterias (por ej. Test de Ames)
g.2. Estudio de citogenética en células de mamíferos o test de
micronúcleo. Este estudio no tiene que realizarse si hay datos
negativos de estudios de citogenética in vivo.
g.3. Estudio de mutación genética en células de mamíferos, si se obtuvo
un resultado negativo en g.1 y g.2., este estudio no será requerido.
g.4. Serán requeridos estudios de mutagenicidad in vivo en el caso de
haber obtenido resultados positivos en los estudios in vitro.
H.2. Estudios subcrónicos y crónicos
Para nuevas sustancias sin antecedentes de registro en Argentina. Debe
presentar un Dossier conteniendo información científica respaldatoria
sobre la caracterización toxicológica, ecotoxicológica y destino
ambiental. Esta información puede provenir de estudios toxicológicos y
ecotoxicológicos realizados en laboratorio, mediante protocolos
reconocidos internacionalmente, o de referencias bibliográficas
completas procedentes de revistas indexadas. La evaluación de peligros
se utilizará para cuantificar o desestimar los efectos potencialmente
dañinos de la sustancia a ser comunicados en la etiqueta del producto y
en la Hoja de datos de seguridad.
En aquellos casos, que por su forma de uso se espere exposición hacia
el aplicador y el consumidor, debe presentar una Evaluación de la
exposición y caracterización del riesgo dietario al consumidor, y una
Evaluación de la exposición y caracterización del riesgo laboral
I. Ensayos de eficacia agronómica y fitotoxicidad.
Informes de los ensayos de eficacia agronómica de los usos propuestos.
J. Envases y embalajes propuestos según B -
PRODUCTOS FORMULADOS - V. ENVASES Y EMBALAJES PROPUESTOS.
AGENTES MICROBIANOS DE CONTROL BIOLÓGICO
Cada nuevo aislado se considerará como un nuevo ingrediente activo y
debe registrarse independientemente de cualquier ingrediente activo
registrado de manera similar. El nuevo aislamiento debe tener un
identificador único después del nombre taxonómico del microorganismo.
Esto no excluye la posibilidad de utilizar datos de otra cepa con
antecedentes de registro, como estudios puente, para iniciar el proceso
de registro.
Los productos elaborados en base a microorganismos sin antecedentes de
registro en el país deberán realizar una solicitud de autorización de
muestra y someterse a la evaluación de riesgo por parte autoridad
competente en lo referente a los aspectos cuarentenarios y de impacto a
nivel de los recursos naturales y/o de la salud. En caso de ser un
microorganismo nativo, debe presentar la autorización de permiso de
colecta de la provincia originaria.
Se considera como criterio excluyente de la presentación a registro los
microorganismos que son patógenos primarios de animales, plantas y el
ambiente. Aquellos que puedan presentar proximidad taxonómica con los
microorganismos que son patógenos, deberán garantizar la inocuidad para
la salud y el ambiente mediante los estudios que la avalen.
I. Información legal y administrativa
a) Certificado de Composición original con nombre y firmado por el Responsable Técnico de la empresa formuladora.
b) Informe de Análisis cuali-cuantitativo del producto formulado a registrar firmado por el Responsable técnico del laboratorio.
d) Acreditación del Registro de planta biológica / establecimiento elaborador.
e) Certificado de la Cuarentena emitido por el Laboratorio oficial (cuando corresponda)
II. Información técnica
A. Identidad y proceso de fabricación
a) Solicitante del registro.
b) Productor /proveedor de materia prima.
c) Nombre y descripción de la especie, caracterización de la cepa
y origen. Taxonomía: la identificación deberá realizarse al menor nivel
taxonómico en que se produzcan diferencias en el accionar del
microorganismo o sus productos metabólicos (especie, subespecie, cepa,
serotipo, patovar según corresponda al microorganismo), nivel de
seguridad en la identificación por encima del 98%. Origen (nativo,
exótico, OGM, etc).
d) Metodología de identificación y caracterización del
microorganismo: Señalar la metodología y criterios utilizados para la
identificación (morfología, bioquímica, serología, identificación
molecular, etc.).
e) Datos de depósito de microorganismo: identidad de la colección y número de código de aislamiento.
f) Método de producción y control de calidad. Esta información
deberá venir respaldada por una monografía, que contenga la descripción
o flujograma del proceso productivo, especificando las condiciones,
medios de cultivo, aditivos y otros empleados. Señalar las técnicas
para garantizar la uniformidad y estandarización de la producción, y
los procedimientos o metodología para el control de calidad.
g) Concentración del microorganismo (ingrediente activo) expresado en
unidades infectivas conocidas. Declarar mínimo garantizado a la
elaboración y al vencimiento, expresado en unidad de medida que
corresponda.
h) Contenido e identidad de otros componentes. (Como condensados, medio
de cultivo, promotores de la alimentación, entre otros). Señalar
identidad y contenido máximo de microorganismos contaminantes,
expresados en la unidad de medida que corresponda (CR).
i) Señalar identidad y caracterización de toxinas y metabolitos que
forma el microorganismo, indicando, cuando corresponda, si tales
toxinas o metabolitos ejercen o no la acción a la que está destinado al
uso.
j) Estabilidad genética del agente de control biológico microbiano.
B. Métodos analíticos.
Indicar los métodos de análisis o técnicas, adjuntando su descripción, para:
a) Identificación del microorganismo al nivel establecido de especificidad (especie, subespecie, biotipo, cepa, etc.)
b) Determinación del contenido y viabilidad del microorganismo en el producto formulado.
C. Identidad del producto formulado.
a) Contenido del microorganismo: Indicar el contenido del o de los
microorganismos en el producto formulado, indicando el contenido mínimo
y nominal del material viable e inviable.
b) Co-formulantes: Indicar identidad, función y contenido máximo de
aditivos, cuando corresponda; como los subproductos, condensados,
medios de cultivo. Para la identificación de las sustancias químicas
señalar nombre químico, nombre común, (si existe) y número CAS (si
existe).
c) Certificado de origen y composición cuali-cuantitativo, emitido por el productor.
d) Propiedades físico químicas del producto formulado
• Color
• Estado físico
• pH
e) Estabilidad en diferentes condiciones ambientales (luz solar, pH, aire, temperatura, metales y sus iones).
f) Actividad acuosa (miscibilidad)
g) Estabilidad en el almacenamiento
h) Suspensibilidad (cuando corresponda)
C. Propiedades biológicas y utilización agronómica.
Informes de los ensayos de eficacia agronómica de los usos propuestos.
D. Evaluación tóxico-patológica. Efectos sobre la salud humana Debe
presentar un Dossier con información científica respaldatoria con la
caracterización toxico-patológica para la clasificación de los
productos formulados en función de la información disponible para
clasificar los peligros de los ingredientes activos y los
co-formulantes. Mínimamente debe considerar información de toxicidad
aguda/patogenicidad Oral aguda, Pulmonar aguda, Indicación de
alergia/hipersensibilidad. Será condicionalmente exigido el cultivo de
células (solo para virus). Para microorganismos sin antecedentes de uso
en Argentina debe presentar información sobre la
toxicidad/patogenicidad subcrónica
E. Evaluación tóxico-patológica. Efectos sobre otros organismos no objetivo
Debe presentar un Dossier con información científica respaldatoria con
la caracterización ecotoxico-patológica para la clasificación de los
productos formulados en función de la información disponible para
clasificar los peligros de los ingredientes activos y los coformulantes
en aves, peces de agua dulce y abejas.
F. Información respecto a la seguridad
Procedimientos para la destrucción del agente microbiológico, producto
de su metabolismo, producto formulado, agentes biológicos mutantes,
indicando las condiciones físicas o químicas específicas para obtener
la desactivación o descomposición del material biológico/producto.
Métodos recomendados y precauciones de manejo durante la fabricación,
formulación, almacenamiento, transporte, uso y manipuleo general del
agente / producto. Información sobre equipos de protección personal (si
corresponde). Procedimientos de limpieza y descontaminación de equipos
de aplicación y áreas contaminadas.
G. Envases y embalajes propuestos según B - PRODUCTOS FORMULADOS - V. ENVASES Y EMBALAJES PROPUESTOS.
Consideraciones para preservadores de la madera: Los biocidas gaseosos
para la fumigación de viviendas y artículos de madera como así de los
destinados a reimpregnación de postes y los destinados a usos
domisanitarios quedan excluidos de la obligatoriedad de inscribirse en
el Registro Nacional.
PROCEDIMIENTO PARA LA EXTENSIÓN DEL VENCIMIENTO DE UN LOTE DE PRODUCTO FITOSANITARIO
Para los productos fitosanitarios vencidos o próximos a vencer, se
podrá solicitar la extensión de la fecha de vencimiento de un lote dado
de producto según el siguiente procedimiento:
1) Mediante la presentación de una solicitud, la firma
registrante deberá identificar claramente el producto y el/los lote/s
respectivo/s próximo/s a vencer o vencido/s.
2) SENASA procederá a realizar la toma de la/s muestra/s; O gestionar las mismas con la firma titular del producto.
3) La firma remitirá la/s muestra/s tomada/s a un laboratorio
reconocido por SENASA para realizar los análisis pertinentes para
comprobar que el lote del producto fitosanitario vencido o próximo a
vencer se halla en condiciones para la extensión de su vida útil
(cumple con la especificación).
4) Si corresponde extender la vida útil por un (1) año desde la fecha
de vencimiento del lote, deberán obtenerse resultados conformes para la
cuantificación de la/s sustancia/s activa/s de acuerdo con los límites
establecidos en la Norma IRAM 12054.
5) Si corresponde extender la vida útil por dos (2) años desde la fecha
de vencimiento del lote, deberán obtenerse resultados conformes para la
cuantificación de la/s sustancia/s activa/s de acuerdo con los límites
establecidos en la Norma IRAM 12054, y para el ensayo de estabilidad
acelerada en almacenamiento.
6) La firma remitirá a SENASA el informe de los análisis efectuados
junto con una nota, especificando: a. Marca comercial del producto b.
Número de registro c. Lote d. Cantidad de unidades e. Tipo de
presentación
7) En caso de poder extenderse la vida útil del lote en cuestión, el
registrante deberá modificar la fecha de vencimiento (el resto de la
información deberá mantenerse). Esto implica ubicar el nuevo
vencimiento en el envase primario (y en el empaque secundario, si es
que el producto lleva su vencimiento en la caja).
8) La firma registrante informará al Sistema Nacional de Trazabilidad
la nueva fecha de vencimiento para el lote en cuestión, si así
correspondiera.
REQUISITOS Y PROCEDIMIENTOS PARA PRODUCTOS DE TRATO DIFERENCIADO (PTD).
Se considera Producto de Trato Diferenciado a todo aquel que por sus
características físicas y químicas, toxicológicas, ecotoxicológicas,
modo de uso u otra cuestión técnica, no es alcanzado por la totalidad
de los requisitos, o por su naturaleza o estado de avance técnico al
momento de la presentación de la solicitud de registro.
Las personas físicas o jurídicas que inician un procedimiento de
registro, podrán solicitar el tratamiento diferenciado de un principio
activo o producto formulado, si corresponde, mediante la presentación
de la información y documentación que fundamente dicho trato (Waiver),
como anexo a cada tipo de categoría solicitada, a ser:
SUSTANCIAS ACTIVAS GRADO TÉCNICO NUEVAS.
SUSTANCIAS ACTIVAS GRADO TÉCNICO EQUIVALENTES.
PRODUCTOS FORMULADOS EN BASE A SUSTANCIAS ACTIVAS GRADO
TÉCNICO NUEVAS O
EQUIVALENTES.
COADYUVANTES DE APLICACIÓN, SEMIOQUÍMICOS Y FORMULADOS MISCELÁNEOS.
AUTORIZACIÓN DE PREDIOS EXPERIMENTALES Y DE USO EXPERIMENTAL
DE SUSTANCIAS
ACTIVAS SINTÉTICAS.
PRODUCTOS FORMULADOS EN BASE A SUSTANCIAS ACTIVAS BIOQUÍMICAS.
PRODUCTOS FORMULADOS MICROBIANOS DESTINADOS A LA
PROTECCIÓN VEGETAL
FISCALIZACIÓN
Fiscalización post autorización de la sustancia activa grado técnico
nueva o equivalente o del producto formulado. El SENASA podrá efectuar
fiscalizaciones post autorización de la sustancia activa grado técnico
o del producto formulado mediante análisis de muestras del producto
autorizado, estando el costo de envío de muestras y análisis a cargo
del titular del registro o del importador. En caso de que la
fiscalización demuestre inconsistencias entre la información declarada
y los análisis efectuados sobre las muestras oficiales, el mencionado
Servicio Nacional dará de baja la autorización de conformidad con los
procedimientos establecidos en la normativa vigente, sin perjuicio de
las sanciones que pudieran corresponder de acuerdo con lo dispuesto en
el Capítulo V de la Ley N° 27.233 y su Decreto Reglamentario N°
DECTO-2019-776-APN-PTE del 19 de noviembre de 2019, y la eventual
aplicación de las medidas preventivas pertinentes.
Fiscalización documental post autorización de la sustancia activa grado
técnico y/o del producto formulado. El SENASA podrá efectuar
fiscalizaciones documentales post autorización de la sustancia activa
grado técnico y/o del producto formulado. En caso de que la
fiscalización demuestre inconsistencias entre la información declarada
y la presentada al solicitar la autorización de la sustancia activa o
del formulado para la planta en cuestión, el citado Servicio Nacional
dependiendo del grado de inconsistencia dará de baja la autorización de
conformidad con los procedimientos establecidos en la normativa vigente
o solicitará la subsanación correspondiente, sin perjuicio de las
sanciones que pudieran corresponder de conformidad con lo establecido
en el Capítulo V de la mentada Ley N° 27.233 y su referido decreto
reglamentario.
Las muestras oficiales de fiscalización y control serán remitidas a
laboratorios que cuenten, al menos, con certificación de Buenas
Prácticas de Laboratorio (BPL), es decir, que cumplan con las mismas
exigencias de laboratorios que realicen estudios y análisis con objeto
de evaluación para solicitud de registro.
En caso de detectarse alguna irregularidad relacionada con la calidad
del producto o con la documentación declarada en productos con
certificaciones de registro emitidas por las autoridades competentes de
los países o grupos de países individualizados en el Anexo IV
(IF-2025-68648006-APN-DNPV#SENASA), la autoridad competente podrá
adoptará serán las siguientes acciones:
a) Suspender preventivamente el registro.
b) Dependiendo de la gravedad de lo hallado, se podrá solicitar la
subsanación de la documentación presentada (bajo régimen de caducidad y
pausado) y en caso de no ser posible la subsanación se procederá a la
cancelación del registro.
c) dar de baja en el fitosanitarios en el VADEMECUM de acuerdo con la evaluación de las subsanaciones o cancelación.
d) De reiterarse TRES (3) irregularidades en las DDJJ del mismo o de
distintos productos de una determinada firma registrantes, la Clave
Única de Identificación Tributaria (C.U.I.T.) de la firma involucrada
ingresará al régimen de vigilancia intensiva de monitoreo durante un
año y dependiendo de la gravedad del incumplimiento se procederá a
restringir por SEIS (6) meses la posibilidad de realizar cualquier
actividad vinculada al comercio de fitosanitarios,
e) Estas medidas son tomadas sin perjuicio de aquellas otras medidas
legales que pudieran adoptarse de acuerdo con la gravedad o el tipo de
falta y las competencias intervinientes que correspondan.
IF-2025-121541245-APN-DNPV#SENASA
ANEXO IV
(Anexo sustituido por art. 9° de la Resolución N° 843/2025
del Servicio Nacional de Sanidad y Calidad Agroalimentaria B.O.
4/11/2025. Vigencia: a partir del día de su publicación en el Boletín
Oficial.)
LISTADO DE PAÍSES/GRUPO DE PAÍSES CON CONVERGENCIA NORMATIVA
A continuación, se establece el listado de países/grupo de países con convergencia normativa con la REPÚBLICA ARGENTINA:
MANCOMUNIDAD DE AUSTRALIA,
CANADÁ,
CONFEDERACIÓN SUIZA,
UNIÓN EUROPEA,
ESTADOS UNIDOS DE AMÉRICA,
ESTADO DEL JAPÓN,
ISLANDIA,
PRINCIPADO DE LIECHTENSTEIN,
REINO DE NORUEGA,
NUEVA ZELANDA,
REINO UNIDO DE GRAN BRETAÑA E IRLANDA DEL NORTE,
REPÚBLICA FEDERATIVA DE BRASIL.
IF-2025-121541330-APN-DNPV#SENASA